Похожие презентации:
Гетероциклические соединения
1.
Гетероциклические соединения.Шестичленные гетероциклы
2. Содержание лекции
1. Электронное строение пиридина2. Получение пиридина
3. Химические свойства
3.
Электронное строение пиридинаN
N
H
По своей конфигурации атом азота в пиридине существенно отличается от атома азота в пирроле
p-орбитали
Пиридин относится к ароматическим соединениям: он не подвергается реакциям
присоединения и вступает в реакции электрофильного замещения.
Теплота сгорания указывает на существенную энергию резонанса 23 ккал/моль
4. Получение пиридина
45
6
3
N
1
2
N
2-пиколин
N
3-пиколин
N
4-пиколин
Основной источник пиридина и ряда
метилпиридинов - каменноугольная
смола
5.
• В лабораторныхусловиях пиридин
можно
синтезировать из
синильной
кислоты и
ацетилена
6. Физические свойства
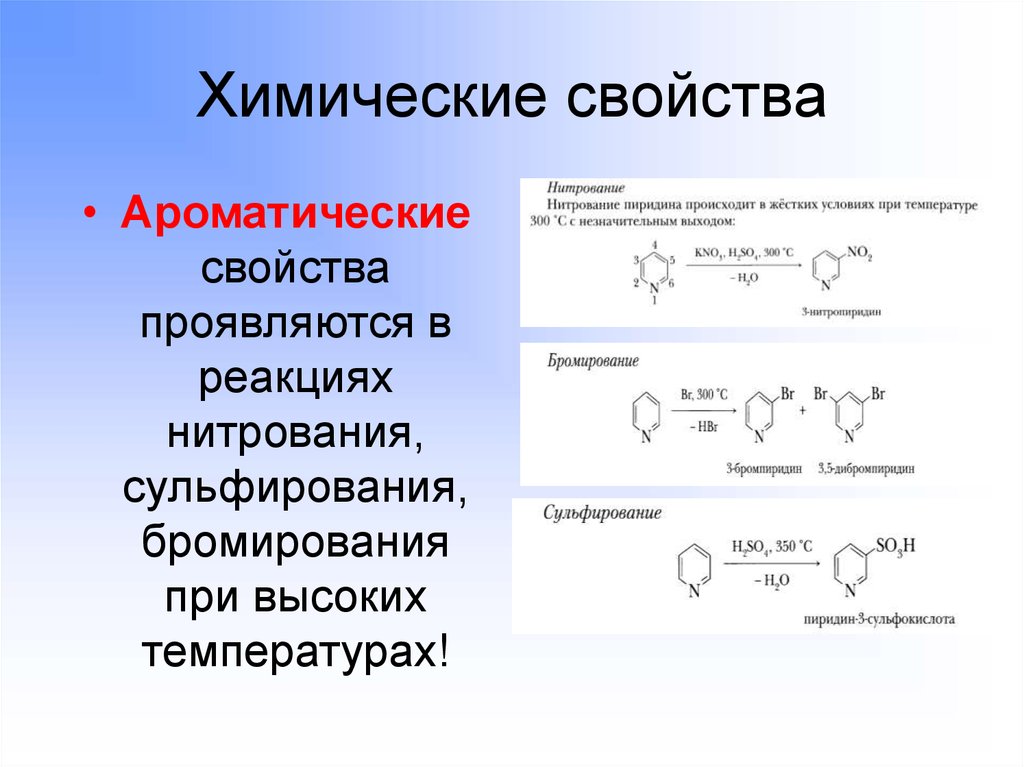
7. Химические свойства
• Ароматическиесвойства
проявляются в
реакциях
нитрования,
сульфирования,
бромирования
при высоких
температурах!
8.
NO2H2SO4 конц., HNO3 конц.
3000C, 1 день
N
H2SO4 конц.
HgSO4 ,2200C
N
SO3H
N
70%
Br
Br2, 66% олеум
N
86%
Cl
Cl2, AlCl3
1000C
6%
N
30%
Менее активен, чем бензол в 106 раз
9.
10. Основные свойства
• В отличие от пирролапиридин проявляет
основные свойства, хорошо
растворим в воде и
окрашивает лакмус в синий
цвет. Это связано с тем, что в
пиридине неподеленная
электронная пара атома
азота не принимает участие
в образовании единого 6-пи
электронного облака и
находится снаружи цикла.
11.
Восстановление пиридинаПиридины восстанавливаются гораздо легче, чем бензол и его
производные
H2/Pt
N
AcOH/1 атм/ 200C
Na/EtOH
N
кипячение
N
H
N
H
пиперидин
1,2,5,6- тетрагидропиридин
(основной продукт)











 Химия
Химия








