Похожие презентации:
Расстановка коэффициентов способом сравнения левой и правой частей уравнения
1.
Расстановкакоэффициентов
способом сравнения левой
и правой частей уравнения.
Учитель химии МОУ СОШ
пгт Новокручининский Читинского
района Забайкальского края
2.
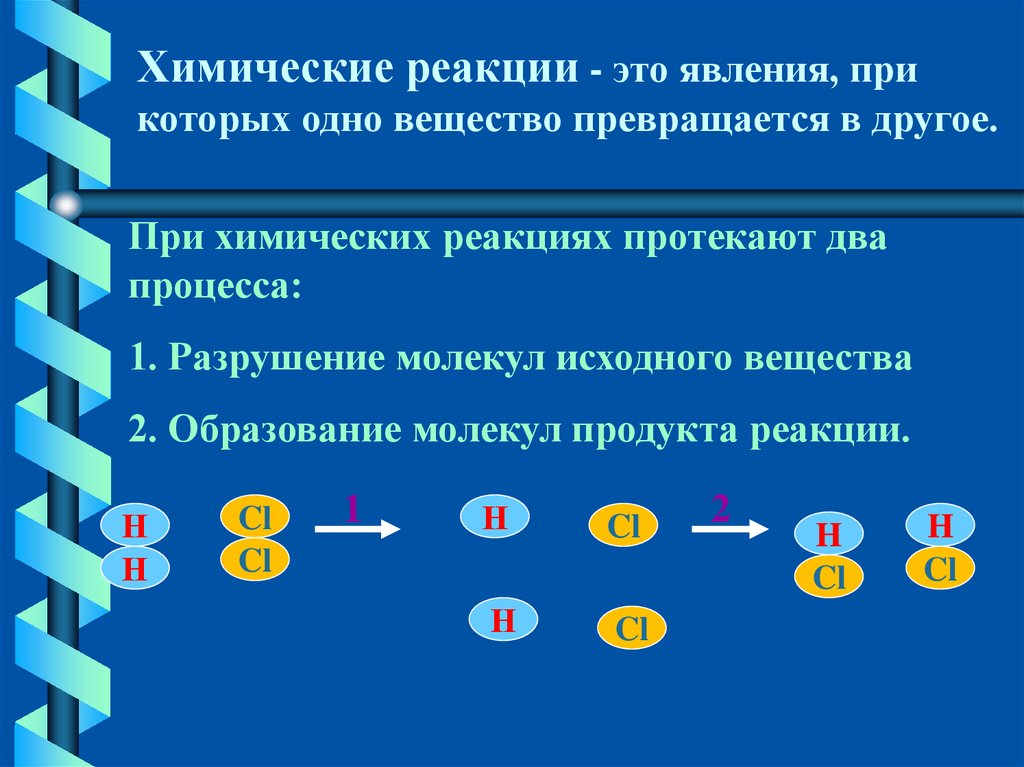
Химические реакции - это явления, прикоторых одно вещество превращается в другое.
При химических реакциях протекают два
процесса:
1. Разрушение молекул исходного вещества
2. Образование молекул продукта реакции.
Н
Н
Cl
Cl
1
Н
Cl
Н
Cl
2
H
Cl
H
Cl
3.
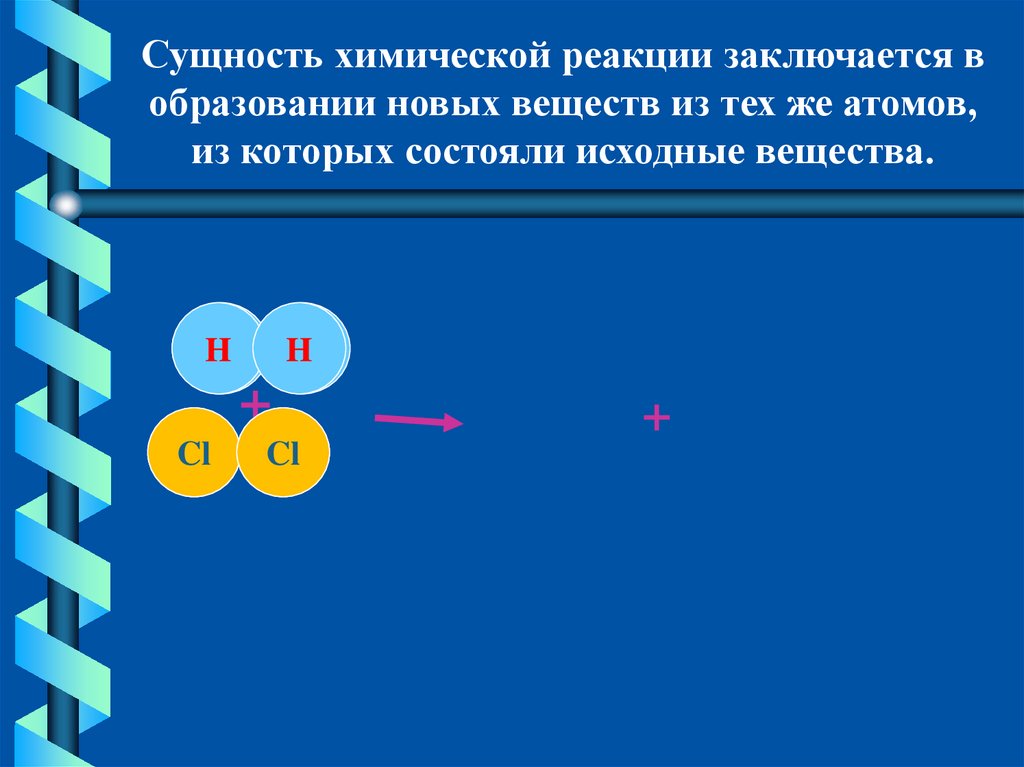
Сущность химической реакции заключается вобразовании новых веществ из тех же атомов,
из которых состояли исходные вещества.
H
Н
H
Н
+
Cl
Cl
+
4.
Закон сохранения массы веществ5.
Количество атомов в ходе химической реакциине изменяется, поэтому масса исходных
веществ равна массе продуктов реакции
m (H2) + m (Cl2) = m (HCL)
H
H
1х2=2
Cl
H
H
35,5 х 2 = 71
Cl
Cl
Cl
2 + 71 = 73
( 1 + 35,5 ) Х 2
= 73
6.
Согласно закону сохранениямассы веществ количество
атомов одного и того же
элемента должно быть
одинаковым в левой и правой
части уравнения.
7.
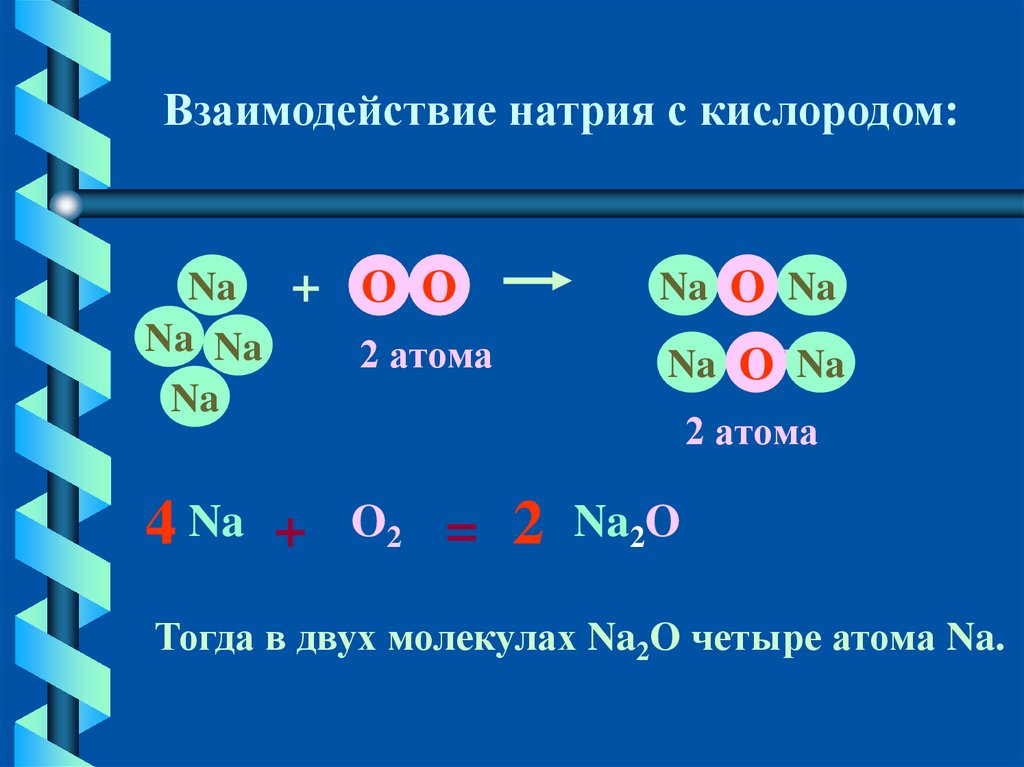
Взаимодействие натрия с кислородом:Na
Na Na
+ O O
2 атома
Na
4 Na +
Na O Na
1 атом
Na
O Na
2 атома
O2
= 2 Na2O
Тогда в двух молекулах Na2O четыре атома Na.
8.
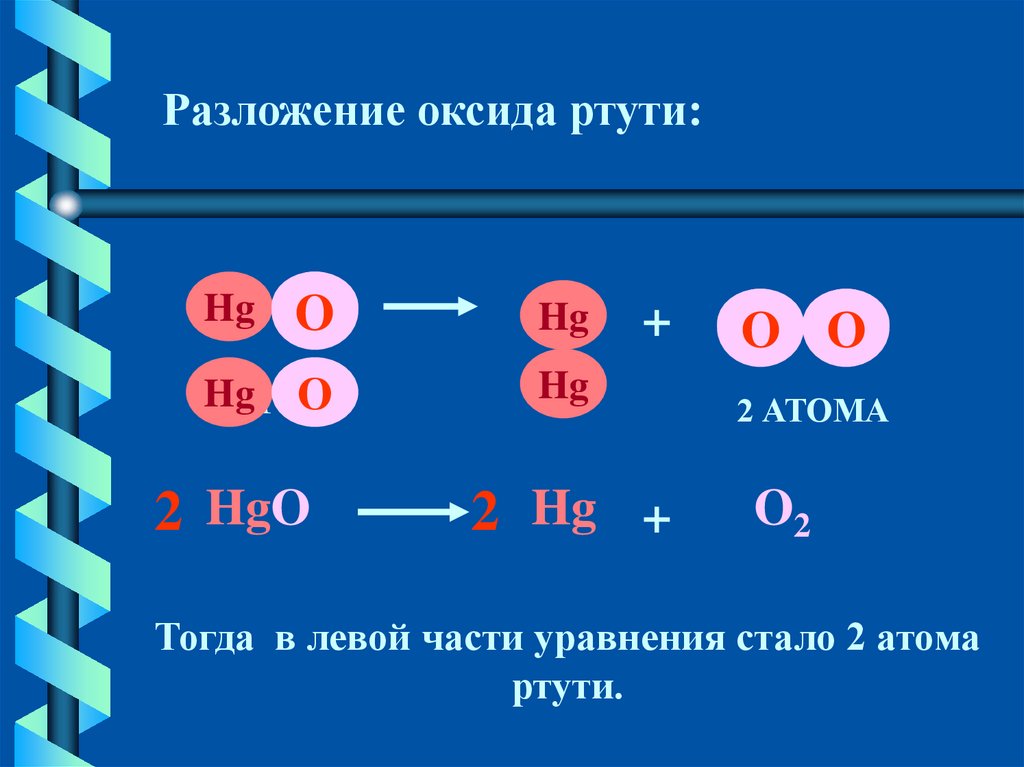
Разложение оксида ртути:О
O
Hg
Hg
О
1 АТОМ
Hg
Hg
2 HgO
+
2 Hg +
О O
О
O
2 АТОМА
O2
Тогда в левой части уравнения стало 2 атома
ртути.
9.
Алюминий взаимодействует с кислородомс образованием оксида алюминия.
6
4 Al + 3 O2
2 атома
+3
-2
2 Al 2 O 3
3 атома
Наименьшее общее кратное
между числами 2 и 3 - число 6.
Атомов Al в правой части уравнения 2х2=4
10.
Расставьте коэффициенты в уравнениях:1. Al + S = Al2S3
2. Na + Cl2 = Na Cl
3. Mg + N2 = Mg3N2
4. Fe + Cl2 = Fe Cl3
5. H2 + O2 = H2O
11.
Проверьте расстановку коэффициенты вуравнениях:
1. 2Al + 3 S = Al2S3
2. 2Na + Cl2 = 2Na Cl
3. 3Mg + N2 = Mg3N2
4. 2Fe + 3Cl2 = 2Fe Cl3
5. 2H2 + O2 = 2H2O







 Химия
Химия








