Похожие презентации:
Кислоты
1.
Тема: Кислоты• Класс: 8
Учитель химии
Голосеева Татьяна Анатольевна
2.
Проверка знаний, умений, навыков.Распределите эти формулы
по классам в таблицу
оксиды
основания
HCl, HNO3, H2SO4,
Ca(OH)2, K2O, Na2O,
Al2O3, Zn(OH)2, Fe(OH)3
ответ
3.
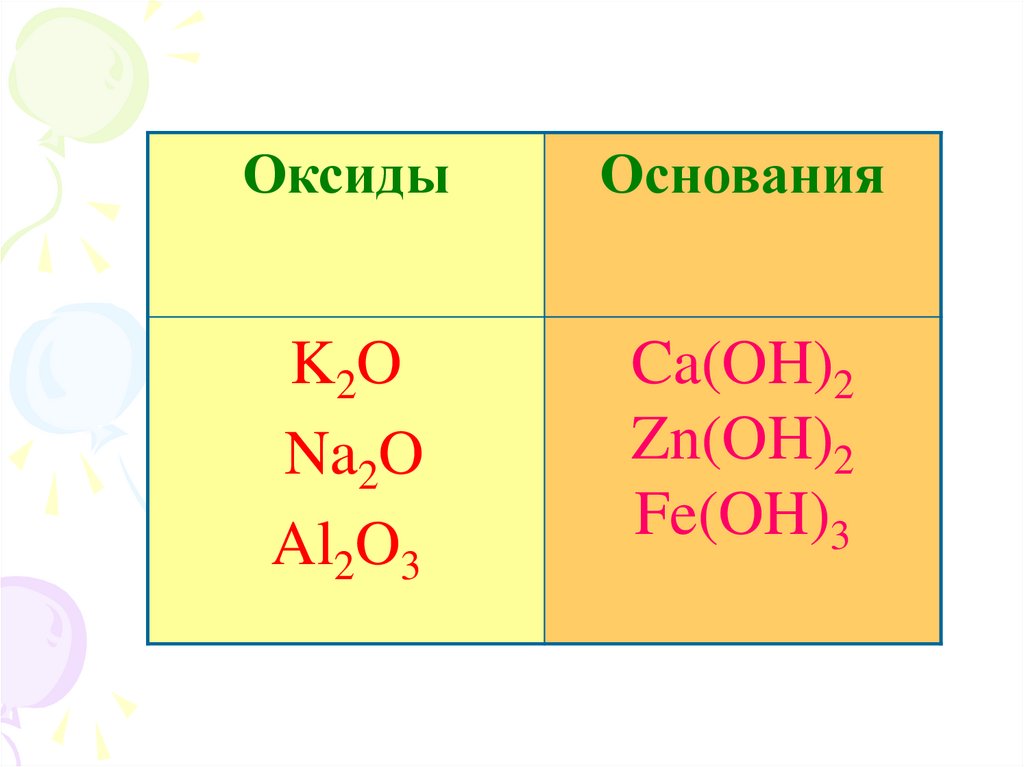
ОксидыОснования
K2 O
Na2O
Al2O3
Ca(OH)2
Zn(OH)2
Fe(OH)3
4.
Что должны узнать на уроке:какие бывают кислоты по происхождению
применение кислот
как их классифицируют
как составляют название
умение распознавать кислоты среди других
соединений
• знать правила техники безопасности при
работе с кислотами.
5.
По происхождению кислоты бываютОРГАНИЧЕСКИЕ –
ЛИМОННАЯ, ЯБЛОЧНАЯ, УКСУСНАЯ,
ЩАВЕЛЕВАЯ, МУРАВЬИНАЯ.
6.
НЕОРГАНИЧЕСКИЕСЕРНАЯ, СОЛЯНАЯ,ПЛАВИКОВАЯ,
ФОСФОРНАЯ, АЗОТНАЯ.
7.
КИСЛОТЫ СОДЕРЖАТСЯ ВОРГАНИЗМАХ ЖИВОТНЫХ
Молочная кислота
образуется в мышцах при
физической нагрузке.
Соляная кислота, находящаяся
в желудке, помогает
переваривать пищу.
8.
КИСЛОТЫПРИМЕНЯЮТСЯ В МЕДИЦИНЕ.
Аскорбиновая,
фолиевая,
липоевая,
ацетилсалициловая
и другие
9.
КИСЛОТЫ ПРИМЕНЯЮТСЯ ВКУЛИНАРИИ .
Уксусная и
лимонная кислоты.
10.
Что произойдет, если ксахару добавить
концентрированную
серную кислоту?
11.
Концентрированнаясерная кислота
обугливает
органические вещества.
Правила техники безопасности:
Внимание!
Работать с кислотами необходимо аккуратно, так как
можно получить ожог или отравление. При попадании
кислоты на кожу надо смыть ее струей воды.
12.
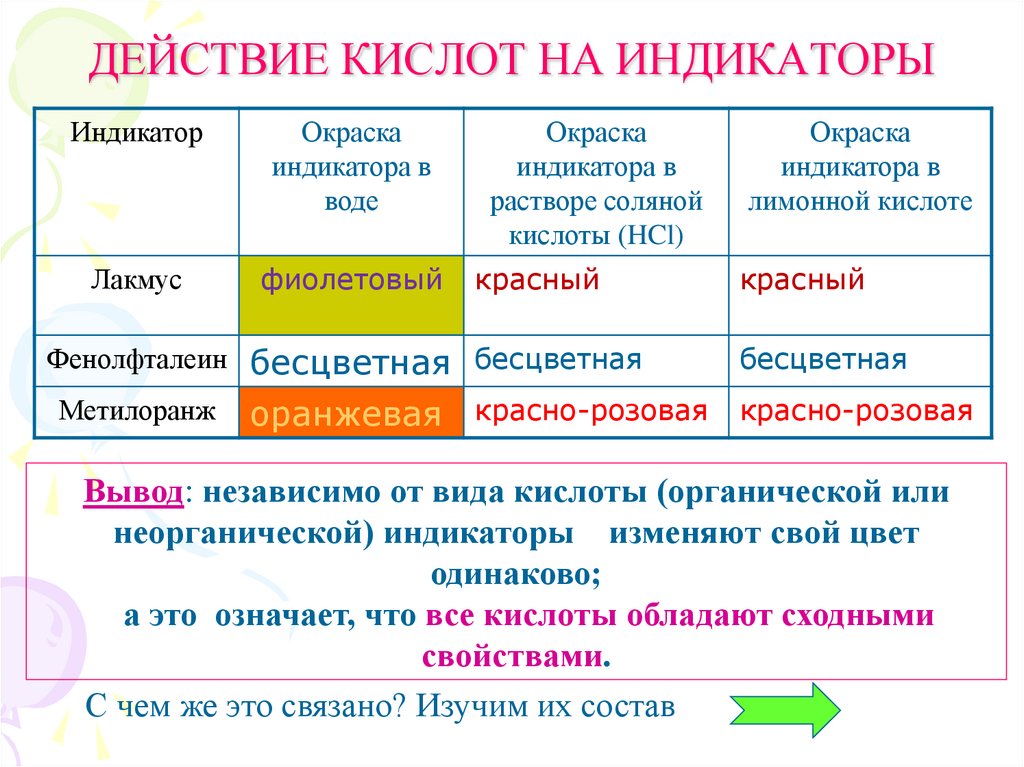
ДЕЙСТВИЕ КИСЛОТ НА ИНДИКАТОРЫИндикатор
Окраска
индикатора в
воде
Лакмус
фиолетовый
Окраска
индикатора в
растворе соляной
кислоты (HCl)
красный
Фенолфталеин бесцветная бесцветная
Метилоранж
Окраска
индикатора в
лимонной кислоте
красный
бесцветная
оранжевая красно-розовая красно-розовая
Вывод: независимо от вида кислоты (органической или
неорганической) индикаторы изменяют свой цвет
одинаково;
а это означает, что все кислоты обладают сходными
свойствами.
С чем же это связано? Изучим их состав
13.
Прочитайте формулы кислот.HCl, H2SO4, H3PO4
Что общего во всех этих формулах?
все общие свойства кислот,
в том числе изменение окраски индикаторов,
связаны с элементом водородом.
Остальная часть молекулы называется кислотным остатком.
Кислоты
– это сложные вещества, состоящие
из ионов водорода и кислотного
остатка.
А чем ещё кроме разных кислотных остатков
отличаются формулы кислот?
Н
О
14.
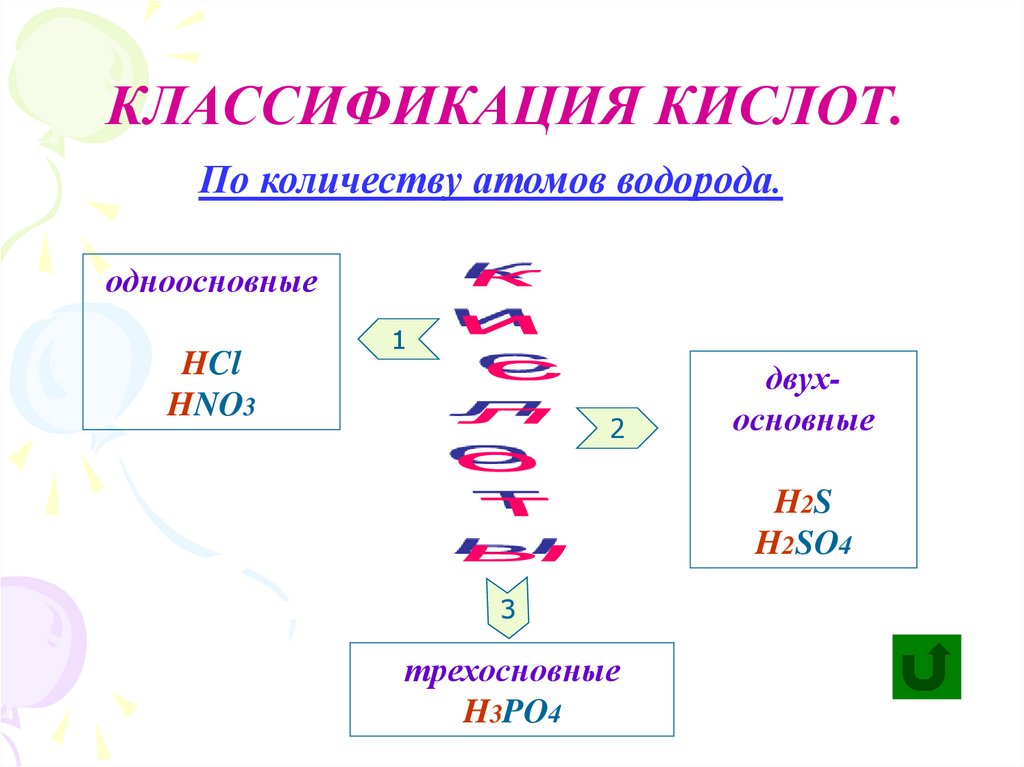
КЛАССИФИКАЦИЯ КИСЛОТ.По количеству атомов водорода.
одноосновные
HCl
HNO3
1
2
двухосновные
H2S
H2SO4
трехосновные
H3PO4
15.
По содержаниюкислорода.
Бескислородные
HF
HCl
HBr
HI
H2S
номенклатура
проверка
Кислородсодержащие
HNO3
HNO2
H2SO4
H2SO3
HClO4
H2SiO3
H3PO4
номенклатура
проверка
16.
НОМЕНКЛАТУРА КИСЛОТБескислородные кислоты:
К названию кислотообразующего
элемента добавляют гласную «о»
и слова «водородная кислота»
HCl – хлороводородная кислота
17.
Кислородсодержащиекислоты:
К русскому названию кислотообразующего
элемента добавляют суффикс:
Если элемент проявляет высшую СО (равную № группы)
+6
– «-ная»: H2SO4
серная кислота
Если СО элемента ниже высшей
+4
– «-истая»: H2SO3
сернистая кислота
18.
Кислоты бескислородныеФормула
HF
Название
Фтороводородная (плавиковая)
HCL
Хлороводородная (соляная)
HBr
HI
H2 S
Бромоводородная
Йодоводородная
Сероводородная
19.
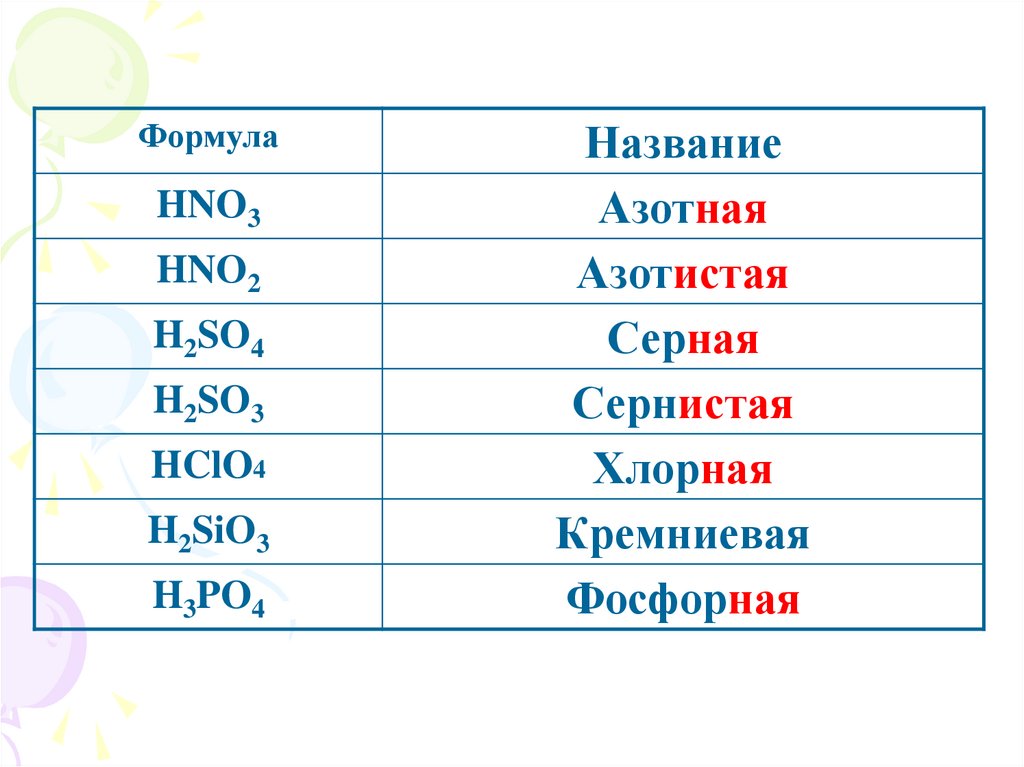
ФормулаHNO3
HNO2
H2SO4
H2SO3
HClO4
H2SiO3
H3PO4
Название
Азотная
Азотистая
Серная
Сернистая
Хлорная
Кремниевая
Фосфорная
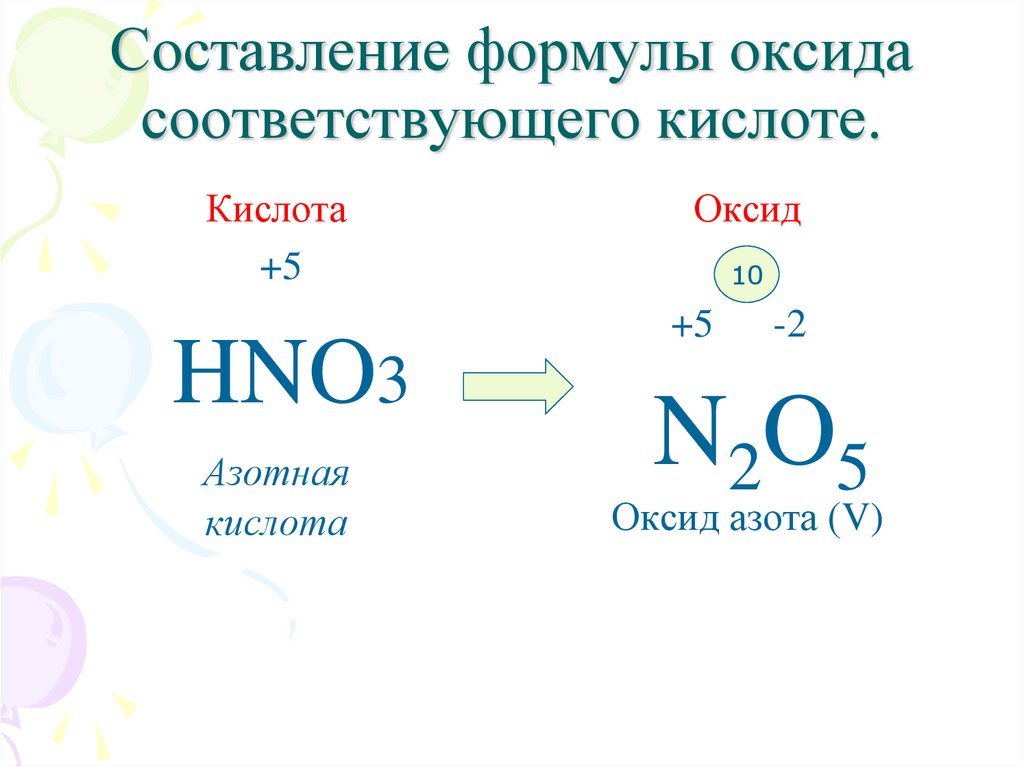
20.
Составление формулы оксидасоответствующего кислоте.
Кислота
+5
HNO3
Азотная
кислота
Оксид
10
+5
-2
N2O 5
Оксид азота (V)
21.
Д/З:О.С.Габриелян Химия 8 &20,
упр.1,3,4 стр.107.
















 Химия
Химия








