Похожие презентации:
Иммунология
1.
Иммунология как определенное направлениеисследований
возникла
из
практической
необходимости
борьбы
с
инфекционными
заболеваниями.
Имеются свидетельства тому, что первые прививки
оспы проводили в Китае за тысячу лет до Рождества
Христова. Инокуляция содержимого оспенных
пустул здоровым людям с целью их защиты от
острой формы заболевания распространилась затем
в Индию, Малую Азию, Европу, на Кавказ. Однако
прием искусственного заражения натуральной
(человеческой) оспой не во всех случаях давал
положительные
результаты.
Иногда
после
инокуляции отмечалась острая форма заболевания
и даже смерть.
2.
E.JennerНа смену инокуляции пришел метод
вакцинации (от лат. vacca - корова),
разработанный в конце XVIIIв.
английским врачом Э.Дженнером
(E.Jenner). Он обратил внимание на
тот
факт,
что
молочницы,
ухаживавшие
за
больными
животными, иногда заболевали в
крайне слабой форме оспой коров, но
при этом никогда не болели
натуральной
оспой.
Подобное
наблюдение
давало
в
руки
исследователя реальную возможность
борьбы с болезнью людей. В 1796г.,
через 30 лет после начала своих
изысканий,
Э.Дженнер
решился
апробировать
метод
вакцинации
коровьей оспой. Эксперимент прошел
успешно, и с тех пор способ
вакцинации по Э.Дженнеру нашел
широкое применение во всем мире.
3.
Рождениеинфекционной
иммунологии связывают с именем
выдающегося
французского
ученого Луи Пастера (Louis
Paster).
Первый
шаг
к
целенаправленному
поиску
вакцинных
препаратов,
создающих устойчивый иммунитет
к инфекции, был сделан после
хорошо известного наблюдения
Пастера
над
патогенностью
возбудителя
куриной
холеры.
Было показано, что заражение кур
ослабленной
(аттенуированной)
культурой возбудителя создает
невосприимчивость к патогенному
микробу (1880г). В 1881г. Пастер
продемонстрировал эффективный
подход к иммунизации коров
против сибирской язвы, а в 1885г.
ему удалось показать возможность
защиты людей от бешенства.
4.
К 40-50-м годам нашего столетия принципы вакцинации,заложенные Пастером, нашли свое проявление в создании
целого арсенала вакцин против самого широкого набора
инфекционных заболеваний.
Хотя
Пастер
считается
основателем
инфекционной
иммунологии, он ничего не знал о факторах, включенных в
процесс защиты от инфекции. Первыми, кто пролил свет на
один из механизмов невосприимчивости к инфекции, были
Беринг
(Behring)
и
Китазато
(Kitasato).
Они
продемонстрировали,
что
сыворотка
от
мышей,
предварительно иммунизированных столбнячным токсином,
введенная интактным животным, защищает последних от
смертельной дозы токсина. Образовавшийся в результате
иммунизации сывороточный фактор - антитоксин представлял собой первое обнаруженное специфическое
антитело. Работы этих ученых положили начало изучению
механизмов гуморального иммунитета.
5.
У истоков познания вопросовклеточного иммунитета стоял
русский
биолог-эволюционист
Илья Мечников.
В 1883 году он сделал первое сообщение по фагоцитарной
(клеточной)
теории
иммунитета
на
съезде
врачей
и
естествоиспытателей в Одессе. Мечников утверждал тогда, что
способность подвижных клеток беспозвоночных животных
поглощать пищевые частицы, т.е. участвовать в пищеварении,
есть фактически их способность поглощать вообще все "чужое", не
свойственное организму: различных микробов, инертных частиц,
отмирающих частей тела. У человека также есть амебоидные
подвижные клетки - макрофаги и нейтрофилы. Но "едят" они
пищу особого рода - патогенных микробов. Эволюция сохранила
поглотительную способность амебоидных клеток от одноклеточных
животных до высших позвоночных, включая человека. Однако
функция этих клеток у высокоорганизованных многоклеточных
стала иной - это борьба с микробной агрессией.
6.
Параллельно с Мечниковым разрабатывал своютеорию иммунной защиты от инфекции немецкий
фармаколог Пауль Эрлих. Он знал о том факте,
что в сыворотке крови животных, зараженных
бактериями, появляются белковые вещества,
способные убивать патогенные микроорганизмы.
Эти вещества впоследствии были названы им "
антителами ". Самое характерное свойство антител
- это их ярко выраженная специфичность.
Образовавшись как защитное средство против
одного микроорганизма, они нейтрализуют и
разрушают только его, оставаясь безразличными к
другим.
Пытаясь
понять
это
явление
специфичности, Эрлих выдвинул теорию "боковых
цепей", по которой антитела в виде рецепторов
предсуществуют на поверхности клеток. При этом
антиген микроорганизмов выступает в качестве
селективного фактора. Вступив в контакт со
специфическим рецептором, он обеспечивает
усиленную продукцию и выход в циркуляцию
только этого конкретного рецептора (антитела).
7.
Пауль Эрлих. Портрет набанкноте в 200 марок
1996 г.
Прозорливость Эрлиха поражает,
поскольку
с
некоторыми
изменениями
эта
в
целом
умозрительная
теория
подтвердилась в настоящее время.
Две
теории
клеточная
(фагоцитарная) и гуморальная - в
период
своего
возникновения
стояли
на
антагонистических
позициях. Школы Мечникова и
Эрлиха боролись за научную
истину, не подозревая, что каждый
удар и каждое его парирование
сближало противников. В 1908г.
обоим ученым одновременно была
присуждена Нобелевская премия.
8.
Новый этап развитияиммунологии связан
в первую очередь с
именем
выдающегося
австралийского
ученого
М.Бернета
(Macfarlane
Burnet;
1899-1985).
Именно он в значительной степени
определил лицо современной иммунологии.
Рассматривая иммунитет как реакцию,
направленную на дифференциацию всего
"своего" от всего "чужого", он поднял вопрос
о значении иммунных механизмов в
поддержании генетической целостности
организма в период индивидуального
(онтогенетического)
развития.
Именно
Бернет обратил внимание на лимфоцит, как
на основного участника специфического
иммунного реагирования, дав ему название
" иммуноцит ". Именно Бернет предсказал, а
англичанин Питер Медавар и чех Милан
Гашек
экспериментально
подтвердили
состояние,
противоположное
иммунной
реактивности - толерантности. Именно
Бернет указал на особую роль тимуса в
формировании
иммунного
ответа.
И
наконец,
Бернет
остался
в
истории
иммунологии как создатель клональноселекционной теории иммунитета. Формула
такой теории проста: один клон лимфоцитов
способен реагировать только на одну
конкретную антигенную специфическую
детерминанту.
9.
ПитерБрайан
Медавар (англ. Sir
Peter Brian Medawar)
(р. 28 февраля 1915,
Рио-де-Жанейро — у.
2 октября 1987) —
английский биолог.
Особого
внимания
заслуживают
взгляды
Бернета на иммунитет как на такую реакцию
организма, которая отличает все "свое" от всего
"чужого".
После
доказательств
Питером
Медаваром иммунной природы отторжения
чужеродного трансплантата и накопления
фактов по иммунологии злокачественных
новообразований
стало
очевидным,
что
иммунная реакция развивается не только на
микробные антигены, но и тогда, когда имеются
любые, пусть незначительные антигенные
различия
между
организмом
и
тем
биологическим материалом (трансплантатом,
злокачественной
опухолью),
с
которым
встречается организм. Строго говоря, ученые
прошлого, включая Мечникова, понимали, что
предназначение иммунитета - не только борьба
с инфекционными агентами. Однако интересы
иммунологов первой половины нашего столетия
концентрировались в основном на разработке
проблем инфекционной патологии. Необходимо
было время, чтобы естественный ход научного
познания позволил выдвинуть концепцию роли
иммунитета в индивидуальном развитии. И
автором нового обобщения был Бернет.
10.
Роберт КохБольшой вклад в становление современной
иммунологии внесли также Роберт Кох
(Robert
Koch;
1843-1910),
открывший
возбудитель туберкулеза и описавший
кожную туберкулиновую реакцию; Жюль
Борде (Jules Bordet; 1870-1961), сделавший
важный вклад в понимание комплемент зависимого
лизиса
бактерий;
Карл
Ландштейнер (Karl Landsteiner; 1868-1943),
получивший
Нобелевскую
премию
за
открытие групп крови и разработавший
подходы к изучению тонкой специфичности
антител с помощью гаптенов; Родни Портер
(Rodney Porter; 1917-1985) и Джеральд
Эдельман
(Gerald
Edelman;
1929),
изучившие структуру антител; Джордж
Снелл (George Snell), Барух Венацерраф
(Baruj Benacerraf) и Жан Доссе (Jean
Dausset), описавшие главный комплекс
гистосовместимости у животных и человека
и открывшие гены иммунного ответа.
11. Иммунитет и иммунная система.
ИММУНИТЕТ И ИММУННАЯСИСТЕМА.
Иммунитет - защита организма от генетически чужеродных
агентов экзогенного и эндогенного происхождения,
направленная на сохранение и поддержание генетического
гомеостаза организма, его структурной, функциональной,
биохимической целостности и антигенной
индивидуальности.
12. Особенности иммунной системы:
ОСОБЕННОСТИ ИММУННОЙ СИСТЕМЫ:1. Иммунная система многокомпонентна, она
генерализована по всему телу, но функционально
выступает как единое целое.
2. Ее клетки постоянно рециркулируют по всему
организму через кровоток.
3. Иммунная система имеет мультивариантную
регуляцию, многократное дублирование функций
компонентами, ее составляющими.
4. Иммунная система – открытая система
функционирования.
5. Она обладает уникальной способностью
вырабатывать строго специфические молекулы
антител, различные в своей специфике в отношении
каждого антигена.
13. Главные задачи иммунной системы:
ГЛАВНЫЕ ЗАДАЧИ ИММУННОЙ СИСТЕМЫ:1. Быстрое распознавание чужеродного
агента.
2. Нейтрализация веществ и уничтожение
клеток, генетически отличных от
собственных структур организма.
3. Элиминация чужеродного агента из
организма.
14. Органы и ткани иммунной системы
ОРГАНЫ И ТКАНИ ИММУННОЙ СИСТЕМЫЦентральные органы:
Кольцо
Пирогов
а
Тимус
Костный
мозг
Лимфатические
узлы
Печень
Селезенка
Пейеровы
бляшки
•костный мозг;
•вилочковая железа (тимус);
•сумка Фабрициуса у птиц.
Периферические лимфоидные
органы:
•селезенка;
•лимфатические узлы;
•неинкапсулированная
лимфоидная ткань слизистых
оболочек и кожи;
•печень;
•периферическая кровь.
15. Центральные органы иммунной системы
ЦЕНТРАЛЬНЫЕ ОРГАНЫ ИММУННОЙСИСТЕМЫ
Сумка (бурса) Фабрициуса (bursa Fabricii) – орган лимфопоэза
птиц, где В-лимфоциты получают иммунокомпетентность, т.е.
происходит их созревание.
Наподобие тимуса, сумка Фабрициуса состоит из многочисленных
фолликулов, в которых можно различить корковый и мозговой
слои.
У млекопитающих его функции
выполняют костный мозг и пейеровы
бляшки тонкого кишечника.
16. Органы и ткани иммунной системы
ОРГАНЫ И ТКАНИ ИММУННОЙ СИСТЕМЫЦентральными органами иммунной системы называют
органы, где происходит дифференцировка лимфоцитов из
стволовой кроветворной клетки.
Лимфопоэз – это дифференцировка лимфоцитов от
стволовой кроветворной клетки до зрелого неиммунного
лимфоцита.
Зрелые неиммунные лимфоциты называют наивными
(naive) или девственными (virgine).
В центральных органах созревание лимфоцитов происходит
без влияния антигенов (антигеннезависимая
дифференцировка).
17. Органы и ткани иммунной системы
ОРГАНЫ И ТКАНИ ИММУННОЙ СИСТЕМЫНа территории периферических
лимфоидных органов зрелые
неиммунные лимфоциты вступают в
контакт с антигенпредставляющими
клетками.
Т.о., в периферических органах иммунной системы
происходит антигензависимая пролифирация и
дифференцировка лимфоцитов.
Дифференциацию лимфоцитов на периферии после
распознавания антигена называют иммуногенезом.
В результате иммуногенеза развиваются клоны иммунных
или эффекторных лимфоцитов, которые распознают антиген
и организуют его деструкцию.
18. Периферические лимфоидные органы
ПЕРИФЕРИЧЕСКИЕ ЛИМФОИДНЫЕ ОРГАНЫСелезенка – относительно большой
непарный орган, с массой в
среднем 150 г у взрослого
человека. Лимфоидную ткань
селезенки называют белой
пульпой. В белой пульпе имеются
тимусзависимые и
тимуснезависимые зоны, которые
заселяются Т- и В-лимфоцитами
соответственно.
Селезенка – лимфоцитарная «таможня» для антигенов, попавших в
системную циркуляцию в кровь.
19. Периферические лимфоидные органы
ПЕРИФЕРИЧЕСКИЕ ЛИМФОИДНЫЕ ОРГАНЫЛимфатические узлы – множественные,
симметрично расположенные по телу,
инкапсулированные периферические
лимфоидные органы бобовидной формы,
размером от 0,5 до 1,5 см в длину (вне
воспаления). Они состоят из заключенной в
капсулу паренхимы, содержащей лимфоциты.
Лимфатические узлы расположены
регионарно и называются в соответствии с
частью тела, которую они «обслуживают»:
околоушные, заднешейные, подчелюстные,
подмышечные, подколенные, паховые,
брыжеечные и т.д.
Лимфатические узлы через афферентные
лимфатические сосуды (которых несколько
на один узел) дренируют тканевую жидкость
из всех барьерных тканей.
Лимфатические узлы – это «таможня» всех веществ (антигенов),
попадающих во внутреннюю среду организма через покровные ткани.
20. Периферические лимфоидные органы
ПЕРИФЕРИЧЕСКИЕ ЛИМФОИДНЫЕ ОРГАНЫНеинкапсулированная лимфоидная ткань
слизистых оболочек и кожи:
1. Лимфоидная ткань, ассоциированная с ЖКТ (GALT –
gut-associated lymphoid tissue). Это глоточное
лимфоидное кольцо Пирогова, пейеровы бляшки
тонкой кишки, лимфоидные фолликулы аппендикса.
Особой субпопуляцией являются
внутриэпителиальные лимфоциты слизистой
оболочки кишки (IEL – intra-epitelial lymphocytes).
2. Лимфоидная ткань, ассоциированная с бронхами и
бронхиолами (BALT - bronchial-associated lymphoid
tissue). IEL слизистой оболочки дыхательной системы.
3. Лимфоидная ткань других слизистых оболочек (MALT
– mucosal-associated lymphoid tissue).
4. Лимфоидная ткань, ассоциированная с кожей (SALT – skin- associated
lymphoid tissue) и субпопуляция диссеминированных внутриэпителиальных
лимфоцитов кожи (IEL).
Основная функция лимфоидной ткани слизистых оболочек и кожи –
поддержание иммуногенеза В-лимфоцитов и их дифференцировка в
плазмоциты, продуцирующие антитела – иммуноглобулины секреторных
классов А и Е.
21. Периферические лимфоидные органы
ПЕРИФЕРИЧЕСКИЕ ЛИМФОИДНЫЕ ОРГАНЫПечень.
Печень
В печени у человека локализована
большая часть особых лимфоидных
клеток – нормальных киллеров (NK).
Субпопуляции лимфоцитов в печени
«обслуживают» кровь воротной вены,
несущей все внешние, всосавшиеся в
кишечнике вещества.
Лимфоциты печени обеспечивают
постоянное поддержание
иммунологической толерантности к
пищевым веществам.
В печени находится половина массы всех
тканевых макрофагов организма.
Периферическая кровь – транспортно-коммуникационный
компонент иммунной системы. В ней циркулируют кроветворные
и иммунокомпетентные клетки.
22.
Иммунологическая защита осуществляется спомощью ряда различных механизмов,
которые можно разделить на две большие
группы:
1. Неспецифические механизмы иммунитета,
наиболее филогенетически древние, которые
направлены против любого чужеродного
агента.
2. Факторы специфической иммунной защиты,
активация которых происходит при
проникновении в организм возбудителей или
веществ, имеющих определенные
(специфические) антигенные свойства.
23.
24.
Факторы и механизмынеспецифической
противоинфекционной защиты
организма
25.
К врожденным факторам неспецифической противоинфекционной защитыорганизма относятся:
•кожные и слизистые покровы
•лимфатические узлы
•лизоцим и другие ферменты полости рта и желудочно-кишечного тракта,
•нормальная микрофлора,
• интерферон,
• натуральные киллеры (NK) и фагоцитирующие клетки
•система комплемента
26.
Кожные и слизистые покровыГлавной линией "обороны" служит кожа, которая, оставаясь неповрежденной,
непроницаема для большинства инфекционных агентов. Кроме того,
вырабатываемые потовыми и сальными железами молочная и жирные кислоты
обладают бактерицидным действием, поэтому различные микроорганизмы, не
входящие в число постоянных обитателей кожных покровов, быстро исчезают
с ее поверхности.
27.
Лимфатические узлыЛимфатические
узлы
являются
«своеобразным
биологическим фильтром для возбудителей, переносимых
с лимфой». У человека имеется около 1000 лимфатических
узлов, размер которых варьирует от булавочной головки до
зерна фасоли. лимфатические узлы не просто «фильтруют»
лимфу, но и активно удаляют из нее микробов, выполняя
важнейшую
неспецифическую
защитную
функцию.Лимфатические узлы не только захватывают
чужеродный материал, они являются местом, где
происходит избирательное накопление активированных
данным чужеродным веществом клеток, которые
участвуют в иммунных реакциях против него.
28.
Лизоцим и другие ферменты полости ртаи желудочно-кишечного тракта.
Лизоцим - антибактериальный агент, фермент класса гидролаз,
разрушающий клеточные оболочки бактерий путём гидролиза
мурамилглюкозамина клеточной стенки грам-положительных
бактерий. Лизоцим содержится в в слизистой оболочке
желудочно-кишечного тракта, слёзной жидкости, слюне, слизи
носоглотки и т. д. В больших количествах лизоцим содержится
в слюне, чем объясняются ее антибактериальные свойства.
Ферменты пищеварения - включают в себя ферменты пищеварительного тракта,
расщепляющие сложные компоненты пищи до более простых веществ, которые затем
всасываются в организм. Основные места действия пищеварительных ферментов - это
ротовая полость, желудок, двенадцатипёрстная кишка и тонкий кишечник. Эти ферменты
вырабатываются такими железами, как слюнные железы, железы желудка, поджелудочная
железа и железы тонкого кишечника.
29.
Нормальная микрофлораНормальная микрофлора способствует созреванию иммунной системы и
поддержанию ее в состоянии высокой функциональной активности.
30.
ИнтерфероныИнтерферон является низкомолекулярным белком,
обладающим противовирусными свойствами. Впервые
открыт в 1957 г. А. Айзексом и Д. Линденманном
Действие интерферона основано на блокаде трансляции
мРНК и активации латентной эндонуклеазы, приводящей к
деградации мРНК как вируса, так и хозяина.
Интерфероны подразделяют на три класса: a, b и g.
Интерферон a (лейкоцитарный) обладает выраженной
противовирусной активностью, g-Интерферон — главным
образом противоопухолевой.
31.
Натуральные киллеры (НК) представляют собой популяциюлимфоидных клеток, которые не несут на своей поверхности ни
маркёров Т-, ни маркёров В- лимфоцитов и относятся к группе так
называемых 0- клеток. Морфологически сходны с лимфоцитами.
Однако крупнее их и содержат множество цитоплазматических
вакуолей. Естественные киллеры составляют 5-10% от общего
количества лимфоцитов в крови человека.
32. Механизм реализации внеклеточного киллинга
МЕХАНИЗМ РЕАЛИЗАЦИИ ВНЕКЛЕТОЧНОГО КИЛЛИНГАПредполагается, что нормальные киллеры способны узнавать структуры из
ненормальных высокомолекулярных гликопротеинов, экспрессируемых на
мембранах зараженных вирусами клеток. Сближение с клеткой-мишенью и
ее распознавание возможно благодаря рецепторам NK. Происходит
активизация нормальных киллеров, при которой в пространство вне клеток
выбрасывается содержимое гранул.
Главную роль в уничтожении принадлежит секретируемым белкам –
перфорину и цитолизину, которые образуют трансмембранную пору на
мембране атакуемой клетки, что приводит к её лизису.
33.
34.
Распознают мишени по главному комплексу тканевойсовместимости . В случае, если клетка не повреждена и на её
поверхности экпрессированы молекулы МНС класса 1 (они
присутствуют у всех нормальных клеток организма), развиваются
реакции «запрета», обусловленные сигналами от рецепторов KIR
(рецепторы подавления цитотоксичности).
35. Основные мембранные маркёры и рецепторы
ОСНОВНЫЕ МЕМБРАННЫЕ МАРКЁРЫ ИРЕЦЕПТОРЫ
Основными маркёрами NK- клеток считаются CD56 и CD57, причастные к адгезии с мишенью и цитолизу.
Кроме того, на поверхности ЕК-клеток есть специальный киллинг-активирующий рецептор (КАР), с
помощью которого ЕК-клетка распознает клетку-мишень.
Кроме того, на NK- клетках экпрессировано большое число адгезивных молекул, в том числе интегринов
CD11/CD18 (бетта 2-интегрины),VLA2 («очень поздний антиген 2») (бетта 1интегрин),CD2,CD7,CD8,CD44,CD54,CD58 и других.
Существует субфракция NK- клеток, это К-клетки. Они выполняют лизис мишеней (антителозависимый
цитолиз), связываясь с ними через молекулу иммуноглобулина G (IgG1, IgG3).
На поверхности NK- клеток ещё экспрессируется группа ингибиторных рецепторов – KIR, которые распознают
собственные продукты МНС класса 1 и отменяют цитолиз собственных, нормальных клеток.
36.
Фагоцитирующие клеткиФагоцитирующие клетки - гранулоциты и макрофаги.
Гранулоциты - подгруппа белых клеток крови, характеризующихся наличием крупного сегментированного ядра и
присутствием в цитоплазме специфических гранул (лизосомы и пероксисомы), выявляемых в световой микроскоп
при обычном окрашивании.
Макрофаги - полибласты, клетки мезенхимальной природы в животном организме, способные к активному захвату
и перевариванию бактерий, остатков погибших клеток и других чужеродных или токсичных для организма частиц. К
макрофагам относят моноциты крови, гистиоциты соединительной ткани, эндотелиальные клетки капилляров
кроветворных органов, купферовские клетки печени, клетки стенки альвеол лёгкого (лёгочные макрофаги) и стенки
брюшины (перитонеальные макрофаги).
37.
38.
Система комплемента.Первые данные о существовании системы, дополняющей иммунологическую реакцию антиген
— антитело, были получены в конце XIX в. Бухнером, Ж. Борде и др. Было установлено, что в
сыворотке крови всех позвоночных имеется термолабильный фактор, который вызывает лизис
мембран паразитов в присутствии специфических антител. Это вещество получило название
комплемента (лат. comple — дополнение). В отсутствие комплемента (прогревание при t° 56°)
специфические антитела способны вызывать агглютинацию чужеродных клеток, в том числе и
бактериальных, однако их гибель не происходит. Добавление же свежей сыворотки, не
содержащей антител, но содержащей комплемент, сопровождается лизисом клеток. В
последующем были установлены и другие биологические функции комплемента, в частности,
активация фагоцитоза, освобождение биологически активных аминов из гранул тучных клеток
(гистамин, серотонин, брадикинин), повышение проницаемости клеточных мембран и снижение
сосудистого тонуса, положительный хемотаксис, иммунное прилипание
39.
В настоящее время известно, что комплементпредставляет собой систему сывороточных белков,
состоящую из 11 компонентов и 3 ингибиторов.
Компоненты, входящие в состав системы
комплемента, обозначаются буквой С с порядковыми
номерами от 1 до 9. Дефект любых компонентов СК
проявляется рецидивом бактериальной или
грибковой инфекции. Дефект С1-С4 –
иммунодефициты.
Активация системы комплемента может
осуществляться иммуноглобулинами класса М и G,
которые входят в состав иммунного комплекса или же
без участия иммуноглобулинов, но при участии
пропердиновой системы (лат. perder — разрушать).
Исходя из этого, существует два пути активации
системы комплемента. Первый носит название
классического, или антителозависимого, а второй –
альтернативного, или пропердинового.
40.
41. ПРОПЕРДИН
Пропердин — белок с молекулярным весом 220000, обнаруженный в сыворотке крови
Пиллемером с сотр. в 1954 — 1956 гг. Свою
активность пропердин проявляет только в
присутствии в сыворотке крови ионов Мд+2 и
компонентов комплемента. Комплекс
пропердин-коминт Мд2+ получил название
системы пропердина.
42. Илья Ильич Мечников-русский и французский биолог. Дата жизни: 1845-1916г.
ИЛЬЯ ИЛЬИЧМЕЧНИКОВ-РУССКИЙ И
ФРАНЦУЗСКИЙ БИОЛОГ.
ДАТА ЖИЗНИ:
1845-1916Г.
43.
44.
Условно факторы неспецифическойзащиты можно разбить на четыре
типа:
1. физические (анатомические);
2. физиологические;
3. клеточные, осуществляющие
эндоцитоз или прямой лизис
чужеродных клеток;
4. молекулярные (факторы
воспаления).
45. Физические барьеры: 1. кожа 2. слизистая оболочка 3. микрофлора
ФИЗИЧЕСКИЕБАРЬЕРЫ:
1. КОЖА
2. СЛИЗИСТАЯ
ОБОЛОЧКА
3. МИКРОФЛОРА
46.
Физиологическийтип
защиты включает
температуру тела, рН и
напряженность кислорода в
районе колонизации
микроорганизмами, а также
различные растворимые
факторы, воспаление.
47. Клеточные факторы
КЛЕТОЧНЫЕ ФАКТОРЫК клеточным факторам неспецифической защиты относятся
фагоцитирующие клетки и натуральные киллеры.
Натуральные киллеры (НК или NK) или естественные
киллеры (ЕК) представляют собой популяцию лимфоидных
клеток, лишенных признаков Т- и В-лимфоцитов. Их участие
в неспецифическом иммунном ответе состоит в способности
оказывать прямое цитотоксическое действие на
злокачественнотрансформированные и вирусинфицированные
клетки, а также клетки, поглотившие некоторые
внутриклеточные бактериальные патогены. В процессе
цитолиза различают три основных стадии: распознавание,
выделение цитотоксинов («летальный удар») и лизис клеткимишени.
48. Гуморальные (молекулярные) факторы неспецифической защиты
ГУМОРАЛЬНЫЕ (МОЛЕКУЛЯРНЫЕ) ФАКТОРЫ НЕСПЕЦИФИЧЕСКОЙЗАЩИТЫ
В неспецифическом иммунитете
против микробов участвуют белки
острой фазы воспаления: Среактивный протеин (белок),
сывороточный амилоид, альфа2макроглобулин, фибриноген, bлизины, интерфероны, система
комплемента, лизоцим и др.
49.
Фагоцитоз - это процесс распознавания, поглощения ипереваривания фагоцитами различных чужеродных
корпускулярных объектов.
Со времени И.И. Мечникова все клетки, обладающие
способностью к фагоцитозу, делятся на 2 группы:
50. Нейтрофилы (нейтрофильные гранулоциты)
НЕЙТРОФИЛЫ(НЕЙТРОФИЛЬНЫЕ ГРАНУЛОЦИТЫ)
Обладают наибольшей фагоцитарной
активностью.
Продолжительность жизни – 8 суток
Находятся в кровяном русле – 8-12
часов
Количество нейтрофилов в норме: 45%
- 70% от общего количества лейкоцитов
В мазке крови: цитоплазма
слобооксифильна, имеется мелкая
зернистость.
51. Эозинофилы
ЭОЗИНОФИЛЫМенее активны, чем нейтрофилы
Фагоцитируют бактерии, грибы,
реагируют на чужеродные белки,
участвуют в аллергических реакциях.
В крови находятся 7-8 часов
Норма в крови: 120—350 эозинофилов на
микролитр
В мазке крови: ядро из двух частей,
соединённых нитью, мелкие и крупные
гранулы в цитоплазме
52. Базофилы
БАЗОФИЛЫСлабая фагоцитарная активность
В мазке крови: в цитоплазме крупные гранулы, Sобразное ядро
Норма: 0,5 - 1% всех лейкоцитов крови
53.
Моноциты (CD14) – основные клеткимоноцитарно-макрофагальной системы.
Моноциты являются предшественниками
тканевых макрофагов. Моноциты
образуются в костном мозге, затем
поступают в кровь, но быстро покидают ее
и в тканях под названием макрофаги
выполняют свою эффекторную функцию.
Поверхностные рецепторы макрофагов:
1. К Fc-фрагменту иммуноглобулинов.
2. К С3-фракции комплемента.
3. К антигенам главного комплекса гистосовместимости
(МНС) II класса.
54. Макрофаги
МАКРОФАГИИмеют
-
особенности строения в различных
тканях.
соед. тк. – гистиоциты
печень – ретикулоэндотелиоциты
лёгкие – альвеолярные макрофаги
лимф. узлы и селезёнка – свободные и
частично фиксированные макрофаги
серозные оболочки – перитонеальные и
плевральные макрофаги
костная тк. – остеокласты
НС – микроглиальные клетки
55. Процесс фагоцитоза, т. е. поглощение инородного вещества клетками-фагоцитами, протекает в 4 стадии: 1) активация фагоцита и его
ПРОЦЕСС ФАГОЦИТОЗА, Т. Е. ПОГЛОЩЕНИЕИНОРОДНОГО ВЕЩЕСТВА КЛЕТКАМИФАГОЦИТАМИ, ПРОТЕКАЕТ В 4 СТАДИИ:
1) АКТИВАЦИЯ ФАГОЦИТА И ЕГО
ПРИБЛИЖЕНИЕ К ОБЪЕКТУ (ХЕМОТАКСИС);
2) СТАДИЯ АДГЕЗИИ — ПРИЛИПАНИЕ
ФАГОЦИТА К ОБЪЕКТУ;
3) ПОГЛОЩЕНИЕ ОБЪЕКТА С
ОБРАЗОВАНИЕМ ФАГОСОМЫ;
4) ОБРАЗОВАНИЕ ФАГОЛИЗОСОМЫ И
ПЕРЕВАРИВАНИЕ ОБЪЕКТА С ПОМОЩЬЮ
ФЕРМЕНТОВ.
56. Стадия приближения фагоцита к объекту фагоцитоза
СТАДИЯ ПРИБЛИЖЕНИЯ ФАГОЦИТА КОБЪЕКТУ ФАГОЦИТОЗА
Стадия осуществляется за счёт
хемотаксиса – движение по
направлению к градиенту
хемоатрктанта. На поверхности
фагоцита имеются рецепторы для
хемоатрактантов, в результате чего
клетка чувствует градиент
хемотаксического сигнала. Благодаря
хемотаксису, фагоцит целенаправленно
движется в сторону повреждающего
агента. Чем выше концентрация
хемоаттрактанта, тем большее число
фагоцитов устремляется в зону
повреждения. Движение фагоцитов
осуществляется в результате
взаимодействия актина и миозина и
сопровождается выдвижением
псевдоподий, которые служат точкой
опоры при перемещении фагоцита.
57. Стадия аттракции
СТАДИЯ АТТРАКЦИИВ эту стадию происходит
опсонизация, распознавание и
прикрепление фагоцита к объекту
фагоцитоза
В сыворотке крови находятся
опсонины, соединения, которые
способствуют активации
фагоцитоза, а именно процесс
узнавания чужеродного объекта и
прилипание фагоцита к нему.
К опсонинам относят иммунные
комплексы, некоторые фрагменты
системы комплемента, Среактивный белок,
агрегированные белки,
фибронектины и др.
58. Стадия поглощения
СТАДИЯ ПОГЛОЩЕНИЯВ эту стадию начинается
взаимодействие опсонинов и
поверхностных рецепторов
фагоцита. Затем происходит
обхват псевдоподиями
чужеродной частицы и
погружение её в цитоплазму
фагоцита.
Поглощение – это
энергозависимый процесс.
Происходит дызательный «взрыв»
- увеличение в потребности
кислорода и окислении глюкозы,
усиление метаболизма углеводов,
липидов, синтеза РНК,
повышение уровня цГМФ,
снижение синтеза белка и
59. Стадия киллинга или переваривания
СТАДИЯ КИЛЛИНГА ИЛИПЕРЕВАРИВАНИЯ
Формируется фаголизосома,
состоящая из поглощённой
частицы и инвагинированной в
цитоплазму ЦПМ. Фагосома
сближается с лизосомами и
первичными азрофильными и
вторичными специфическими
гранулами фагоцита.
Происходит излияние
ферментов из гранул в
фагосому – дегрануляция.
Чужеродный объект
переваривается.
60. Завершённый и незавершённый фагоцитоз
ЗАВЕРШЁННЫЙ И НЕЗАВЕРШЁННЫЙ ФАГОЦИТОЗЕсли чужеродный агент проникает в фагоцит и
образуется фагосома, в которой в дальнейшем
происходит убиение это агента, то такой
фагоцитоз называют завершённым.
Если стадия киллинга не произошла, то такой
фагоцитоз – незавершённый.
Некоторые чужеродные объекты, которые
подверглись незавершённому фагоцитозу,
способны в дальнейшем размножаться в
фагоците. Например, так могут делать
различные бактериальные клетки.
61. Последствия
ПОСЛЕДСТВИЯПатология фагоцитоза сопровождается
выраженными изменениями в полости
рта. Развитие острых и хронических
воспалительных процессов в полости рта
(стоматита, гингивита, глоссита)
характерно для синдромов ЧедиакаХигаси, Лази. При агранулоцитозе
отмечаются обширные язвеннонекротические поражения слизистой
полости рта. В особо тяжелых случаях
гнойно-некротические зменения могут
наблюдаться в челюстных костях.
62.
ФАКТОРЫ И МЕХАНИЗМЫСПЕЦИФИЧЕСКОЙ ЗАЩИТЫ
Специфический иммунитет обеспечивают
специальные иммунокомпетеитиые
клетки — Т- и В- лимфоциты, которые
участвуют в распознавании чужеродных
антигенов, синтезе специфических
антител (иммуноглобулинов) и других
формах иммунного ответа.
63.
Иммунная система – объединяет органы и ткани, вкоторых происходит образование, созревание и
взаимодействие иммунокомпетентных клеток,
выполняющих функции распознавания Аг и
осуществляющих специфические реакции их
уничтожения.
Иммунокомпетентные клетки – клетки несущие
на своей мембране рецепторы к определенному Аг, и
способные его узнать:
Т- и В- лимфоциты, Аг-представляющие клетки
64.
В Костном мозге образуются:В-лимфоциты (10-15%), гуморальный иммунитет
Моноциты – предшественники макрофагов и другие Агпредставляющие клетки
В Тимусе образуются Т-лимфоциты
клеточный иммунитет:
Тк- лимфоциты киллеры CD8
Тх- лимфоциты хелперы CD4
Тс- лимфоциты супрессоры CD8
Т-индукторы
Нулевые клетки – остальные лимфоциты
(70-80%)
65. Центральные органы иммунной системы
ЦЕНТРАЛЬНЫЕКостный
мозг
ОРГАНЫ ИММУННОЙ СИСТЕМЫ
Костный мозг (medulla ossea rubra) –
центральный орган всего кроветворения,
место обитания пула стволовых
кроветворных клеток, которые являются
родоначальницами всех форменных
элементов крови и соответственно
иммунокомпетентных клеток.
Костный мозг локализуется в губчатом
веществе костей (эпифизы трубчатых
костей, грудина).
Главная функция – продукция иммунокомпетентных
клеток из полипотентной стволовой.
66. Центральные органы иммунной системы
ЦЕНТРАЛЬНЫЕОРГАНЫ ИММУННОЙ СИСТЕМЫ
Все клетки крови происходят из общей
клетки-предшествественницы – стволовой
кроветворной клетки (СКК).
На территории костного мозга проходит
полный «курс» :
•эритропоэза (заканчивается
эритроцитами);
•миэлопоэза (заканчивается лейкоцитами –
нейтрофилами, моноцитами, эозинофилами,
базофилами);
•мегакариоцитопоэза (заканчивается
тромбоцитами);
•образуется общая клетка –
предшественник всех лимфоцитов.
67. Иммунокомпетентные клетки.
ИММУНОКОМПЕТЕНТНЫЕ КЛЕТКИ.Центральной клеткой
иммунной системы является
лимфоцит (1-4×109/л)
В 1969 году И. Ройт ввел в иммунологию
понятие Т- и и В-лимфоцитов:
•Т-лимфоциты – тимус (thymus)
•В-лимфоциты (bursa Fabricii у птиц)
68. В-лимфоциты (15-20 %) – отвечают за развитие гуморального иммунитета и представлении антигена Т-лимфацитам.
В-ЛИМФОЦИТЫ (15-20 %) – ОТВЕЧАЮТЗА РАЗВИТИЕ
ГУМОРАЛЬНОГО ИММУНИТЕТА И ПРЕДСТАВЛЕНИИ АНТИГЕНА
Т-
ЛИМФАЦИТАМ.
Поверхност ные рецепт оры В-лимфоцит ов:
1.
2.
3.
4.
К эритроцитам мышей.
К компонентам комплемента C3b и C3d.
Ig-рецепторы (к антигенам).
К антигенам главного комплекса гистосовместимости (МНС) I
и II классов.
5. К Fc-фрагменту иммуноглобулинов.
69.
B-лимфоциты (CD19)B-лимфоциты являются основными клетками, участвующими в
гуморальном иммунитете. У человека они образуются из СК
красного костного мозга, затем поступают в кровь и далее заселяют
В-зоны периферических лимфоидных органов.
Для В-лимфоцитов характерно наличие на плазмолемме
поверхностных иммуноглобулиновых рецепторов (SIg или mlg) для
Аг
При действии антигена В-лимфоциты в периферических
лимфоидных органах активизируются, пролиферируют,
дифференцируются в плазмоциты, активно синтезирующие
антитела различных классов, которые поступают в кровь, лимфу и
тканевую жидкость.
70. Эволюция В-лимфоцита после контакта с антигеном
ЭВОЛЮЦИЯ В-ЛИМФОЦИТА ПОСЛЕ КОНТАКТА С АНТИГЕНОМТ-зависимый путь – характерен для ответа на
большинство антигенов, осуществляется с помощью
цитокинов, продуцируемых Т-хелперами.
Т-независимый путь формирования иммунного ответа
В-лимфоцита осуществляется без помощи Тлимфоцитов и индуцируется некоторыми
небелковыми, в том числе, микробными, антигенами.
71. Субпопуляции В-лимфоцитов
СУБПОПУЛЯЦИИ В-ЛИМФОЦИТОВВ-1 субпопуляция (CD5) локализуется в брюшной и
плевральной полостях, сальнике, миндалинах, это клетки
естественного иммунитета, а образуемые ими
иммуноглобулины – естественные антитела.
В-2 субпопуляция (CD19, CD20, CD22) – обычные Влимфоциты, имеющие на поверхности Ig-рецепторы для
распознавания антигена. При стимуляции антигенами они
созревают в плазмоциты, секретирующие антитела –
иммуноглобулины.
Плазматические клетки – результат конечной
дифференцировки В-лимфоцитов, не имеют на наружной
мембране рецепторов для антигенов, направлены на
интенсивный синтез иммуноглобулинов.
После завершения фазы активной продукции антител
плазмоциты прекращают свое существование.
В-лимфоциты памяти – эффекторы вторичных иммунных
реакций.
72. Нулевые клетки (0-клеки, ни В-, ни Т-лимфоциты) составляют 5-10 % лейкоцитов периферической крови.
НУЛЕВЫЕ КЛЕТКИ (0-КЛЕКИ, НИ В-, НИ Т-ЛИМФОЦИТЫ)СОСТАВЛЯЮТ 5-10 % ЛЕЙКОЦИТОВ ПЕРИФЕРИЧЕСКОЙ КРОВИ.
Среди нулевых клеток по функциональной характеристикам
выделяют:
•естественные киллеры (NK-клетки);
•эффекторы антителозависимой клеточной цитотоксичности
(К- и L-клетки).
Осуществляют главнейшую функцию иммунной системы –
сохранение генетического гомеостаза организма путем
киллинга всех клеток, несущую генетическую чужеродность:
мутанты (в основном опухолевые клетки), клетки, зараженные
вирусом, или клетки трансплантанта.
73. Антитела являются сывороточными белками – глобулинами, которые вырабатываются в ответ на поступление в организм антигена и
АНТИТЕЛА ЯВЛЯЮТСЯ СЫВОРОТОЧНЫМИ БЕЛКАМИ – ГЛОБУЛИНАМИ,КОТОРЫЕ ВЫРАБАТЫВАЮТСЯ В ОТВЕТ НА ПОСТУПЛЕНИЕ В ОРГАНИЗМ
АНТИГЕНА И СПОСОБНЫ С НИМ СПЕЦИФИЧЕСКИ ВЗАИМОДЕЙСТВОВАТЬ.
74.
антитела играют важную роль в формированииприобретенного постинфекционного,
поствакцинального и пассивного иммунитета.
Связываясь с токсинами, они нейтрализуют их
действие и обеспечивают формирование
антитоксического иммунитета
Связываясь с вирусами, антитела создают иммунитет
против вирусов.
75. Строение IgG
СТРОЕНИЕ IGG76. Иммуноглобулин IgЕ
ИММУНОГЛОБУЛИН IGЕКонцентрация IgE в сыворотке крови невелика – менее
0,001% от всех иммуноглобулинов сыворотки крови ( 0 –
100 кЕ/л). Основная физиологическая функция IgE,
очевидно, защита внешних слизистых оболочек
организма путем локальной активации факторов
плазмы и эффекторных клеток благодаря индукции
острой воспалительной реакции. Определение
содержания общего IgE в сыворотке используют для
диагностики атопических аллергических заболеваний.
Определение IgE имеет важное значение для
диагностики редкого заболевания – гипер IgE-синдрома.
Этот синдром характеризуется повышением IgE в крови
до 2000-50000 кЕ/л, эозинофилией, резко выраженной
крапивницей и гиперемией на вдыхаемые аллергены,
пыльцу, пищу, бактериальные и грибковые аллергены.
Астма не является характерной для данного синдрома.
Снижение содержания IgE выявляют при атаксии –
телеангиэктазии вследствие дефекта Т-клеток.
77. Иммуноглобулин IgG
ИММУНОГЛОБУЛИН IGGСоставляют основную массу
иммуноглобулинов сыворотки крови, на их долю
приходится 70 – 80 % всех сывороточных
иммуноглобулинов.
IgG – мономер, имеет два антигенсвязывающих
центра, т.е может связать две молекулы антигена.
В отличие от других классов иммуноглобулинов эти
антитела легко проходят через плаценту и
обеспечивают естественный пассивный иммунитет
у новорожденного.
Границы концентрации IgG в сыворотке крови
здоровых людей, начиная с 12 лет, составляют 5,3–
16,5 мг/мл.
78. Иммуноглобулин IgM
ИММУНОГЛОБУЛИН IGMНа долю IgМ приходится 5 – 10 %
всех сывороточных
иммуноглобулинов.
IgМ – пентамер, имеющий 10
антигенсвязывающих участков.
Границы концентрации IgM в
сыворотке крови здоровых людей,
начиная с 12 лет, составляют 0,5–
2,0 мг/мл
Антитела класса IgМ в своей
первоначальной
мембраносвязанной форме служа
т рецепторами В-клеток, при
первичном иммунном ответе они
первыми появляются в крови
(ранние антитела). Действие их
направлено прежде всего против
микроорганизмов.
79. Иммуноглобулин IgA
ИММУНОГЛОБУЛИН IGAНа долю сывороточного IgA приходится около 10 –
15 % всех иммуноглобулинов.
Секреторный IgA представлен главным образом
димерной формой.
Границы концентрации IgА в сыворотке крови
здоровых людей, начиная с 15 лет, составляют 0,8–
4,0 мг/мл
IgA содержится преимущественно в выделениях
слизистых оболочек — в слюне, слезной жидкости,
носовых выделениях, поте, молозиве и в секретах
легких, мочеполовых путей и желудочнокишечного тракта, где обеспечивает защиту
поверхностей, сообщающихся с внешней средой, от
микроорганизмов.
80. Иммуноглобулин IgD
ИММУНОГЛОБУЛИН IGDIgD содержатся в сыворотке крови и
составляют около 0,2 % общего количества
циркулирующих иммуноглобулинов.
обильно представлен на мембране многих Bклеток совместно с мономерным IgM. Вопрос о
конкретной форме участия IgD в иммунных
процессах остается открытым.
Предположительно он участвует в антигензависимой дифференцировке лимфоцитов.
81.
IgG — наиболее распространенныйиммуноглобулин, в сыворотке крови его около
75% от всего количества иммуноглобулинов,
что составляет от 6,9 до 22 г/л.
IgM - в сыворотке крови матери составляет
0,48 — 2 г/л, а наличие его у плода указывает
на внутриутробное инфицирование.
IgA составляет лишь 10 — 15% всех
иммуноглобулинов сыворотки
IgE содержится в сыворотке крови в небольшом
количестве.
IgD обнаруживается в сыворотке в очень
небольших количествах и его роль как
сывороточного иммуноглобулина не совсем
ясна.
82. Центральные органы иммунной системы
ЦЕНТРАЛЬНЫЕ ОРГАНЫ ИММУННОЙСИСТЕМЫ
Тимус (вилочковая железа)(thymus) –
Тимус
специализированный лимфоидный орган, в котором
проходит лимфопоэз большая часть Т-лимфоцитов
организма.
Тимус расположен в переднем верхнем средостении,
за грудиной, над сердцем.
Строение тимуса:
Тимус состоит из двух больших долей, которые
фрагментированы на множество долек,
разделенных фиброзными перегородками.
Структурная единица тимуса - долька.
В каждой дольке четко различимы две
гистологические зоны: по периферии – корковая, в
центре – медуллярная.
Строма тимуса эпителиальная.
Основным элементом коры являются фолликулы Кларка, в которых
концентрируются эпителиальные и дендритные клетки, макрофаги и
лимфоциты (тимоциты).
83.
Т-лимфоцит ы (50-75%) – клетки, отвечающие за клеточныйиммунитет.
Поверхност ные рецепт оры Т-лимфоцит ов:
1.
2.
3.
4.
5.
CD2 (рецептор к эритроцитам барана).
CD3 (рецепторы к антигенам).
К Fc-фрагменту иммуноглобулинов.
К белкам системы комлемента (но не имеют рецепторов к C3b).
К интерлейкинам.
Субпопуляции Т-лимфоцит ов:
нулевые Т-лимфоциты;
Т-хелперы;
эффекторы ГЗТ (ТГЗТ);
цитотоксические Т-лимфоциты (Т-киллеры);
Т-супрессоры;
Т-клетки памяти.
84.
Нулевые Т-лимфоцит ы (Т0) (CD2, CD3) – это тимические, незрелые, «наивные» Тлимфоциты.Т-хелперы (CD4) распознают антиген в комплексе с локализованными на мембране клетокмишеней антигенами МНС II класса.
Т-хелперы стимулируют пролиферацию и
дифференцировку Т- и В-лимфоцитов,
выделяя интерлейкины.
Среди них различают:
Т-хелперы первого типа (Th1), выделяющие ИЛ-2, ИЛ-12, ИФН-γ,
ФНО-α – обеспечивают реакции Т-клеточного иммунитета.
Т-хелперы второго типа (Th2), секретирующие ИЛ-4, ИЛ-5, ИЛ-10,
ИЛ-13 – стимулируют синтез антител, т.е. гуморальное звено
иммунной системы.
ТГЗТ – эффект оры реакций гиперчувствительности замедленного типа.
85. Центральные органы иммунной системы
ЦЕНТРАЛЬНЫЕ ОРГАНЫ ИММУННОЙСИСТЕМЫ
Созреванию и дифференцировке Т-лимфоцитов в тимусе
способствуют гормоны (тимулин, α- и β-тимозин, тимопоэтин),
синтезируемые эпителиальными клетками. Незрелые лимфоциты,
поступившие в кору тимуса, в процессе деления созревают. При
этом в клетках формируются рецепторы как к чужеродным, так и
собственным антигенам.
Селекция Т-лимфоцитов в тимусе:
•селективная селекция – обор клеток, обладающими рецепторами
для молекул главного комплекса тканевой совместимости (МНС),
обеспечивающих возможность последующих контактов Тлимфоцитов с клетками, представляющими им чужеродный
антиген.
•негативная селекция – клетки с рецепторами для собственных
антигенов погибают.
86. Центральные органы иммунной системы
ЦЕНТРАЛЬНЫЕ ОРГАНЫ ИММУННОЙСИСТЕМЫ
Онтогенез тимуса
1. появляется в период внутриутробного развития и начинает
функционировать у шестинедельног эмбриона;
2. к моменту рождения тимус человека весит всего 10-15 г;
3. окончательно созревает к 5-летнему возрасту;
4. к 9-12 годам достигает максимального развития и веса (3040 г);
5. после периода полового созревания начинается инволюция
органа – замещение лимфоидной ткани жировой и
соединительной с утратой до 3 % активной ткани ежегодно.
87.
Т-лимфоциты (50-75%) – клетки, отвечающие за клеточныйиммунитет.
Поверхностные рецепторы Т-лимфоцитов:
1.
2.
3.
4.
5.
CD2 (рецептор к эритроцитам барана).
CD3 (рецепторы к антигенам).
К Fc-фрагменту иммуноглобулинов.
К белкам системы комлемента (но не имеют рецепторов к C3b).
К интерлейкинам.
Субпопуляции Т-лимфоцитов:
нулевые Т-лимфоциты;
Т-хелперы;
эффекторы ГЗТ (ТГЗТ);
цитотоксические Т-лимфоциты (Т-киллеры);
Т-супрессоры;
Т-клетки памяти.
88.
Цитотоксические Т-лимфоциты (Ткиллеры)Несут на своей поверхности антиген CD8,
который служит рецептором для
антигенов к молекулам главного
комплекса гистосовместимости (МНС) I
класса.
После активации антигеном Т-киллеры
связываются с антигенами на
поверхности клеток и, выделяя
цитотоксин (белок перфорин), разрушают
их.
Т-киллеры уничтожают различные
опухолевые клетки, клетки чужеродных
трансплантантов, патологически
мутированные клетки, клетки,
инфицированные вирусами.
89.
Т-супрессоры регулируют интенсивностьиммунного ответа, подавляя активность
CD4-лимфоцитов.
Т-супрессоры:
•предотвращают развитие аутоиммунных реакций;
•защищают организм от нежелательных последствий иммунных
реакций;
•обеспечивают толерантность матери к чужеродным антигенам,
представленных на клетках вынашиваемого плода.
Т-клетки иммунологической памяти (CD45RO) – это долго
живущие Т-хелперы и Т-киллеры, потомки клеток,
встречавшихся с антигенами и сохранившие к ним
рецепторы.
90. Т-лимфоциты (CD3)
Т-ЛИМФОЦИТЫ (CD3)Тимус (вилочковая
железа) — лимфоидный
орган человека и многих
видов животных, в
котором происходит
созревание,
дифференцировка и
иммунологическое
«обучение» T-клеток
иммунной системы.
Т-хелперы - CD4, узнав антиген, стимулируют
основные компоненты иммунной системы, т. е. Вклетки и другие Т-клетки, специфичные к
данному антигену. Th синтезируют большое
число биологически активных веществ лимфокинов, которые необходимы для
иммунологических реакций.
Т-супрессоры – CD8 - Их биологическая роль
заключается в торможении иммунного ответа и
формировании естественной и индуцированной
антигеном иммунологической толерантности
(лат. tolerantia — терпение).
Т-индукторы - играют важную роль в
антигензависимой дифференцировке хелперных
и супрессорных клеток и не оказывают эффекта
на В-лимфоциты.
Т-киллеры - (цитотоксичные лимфоциты),
несущие CD8 – маркеры. Основная функция этих
клеток — выявлять мутантные, опухолевые
клетки или клетки организма. зараженные
вирусами.
91.
Нулевые Т-лимфоциты (Т0) (CD2, CD3) – это тимические, незрелые, «наивные» Тлимфоциты.Т-хелперы (CD4) распознают антиген в комплексе с локализованными на мембране
клеток-мишеней антигенами МНС II класса.
Т-хелперы стимулируют пролиферацию и
дифференцировку Т- и В-лимфоцитов,
выделяя интерлейкины.
Среди них различают:
Т-хелперы первого типа (Th1), выделяющие ИЛ-2, ИЛ-12, ИФН-γ,
ФНО-α – обеспечивают реакции Т-клеточного иммунитета.
Т-хелперы второго типа (Th2), секретирующие ИЛ-4, ИЛ-5, ИЛ-10,
ИЛ-13 – стимулируют синтез антител, т.е. гуморальное звено
иммунной системы.
ТГЗТ – эффекторы реакций гиперчувствительности замедленного
типа.
92. Иммунокомпетентные клетки.
ИММУНОКОМПЕТЕНТНЫЕ КЛЕТКИ.1. Регуляторные ИКК «управляют» функцией иммунной
системы путем выработки медиаторов – цитокинов. Эти
клетки обуславливают направление развития иммунной
реакции, ее интенсивность и продолжительность.
2. Эффекторные клетки являются непосредственными
исполнителями иммунного реагирования. Они
действуют на объект либо непосредственно, либо путем
биосинтеза биологически активных веществ со
спецефическим эффектом (иммуноглобулины).
93. По функциональной активности иммунокомпетентные клетки (ИКК) подразделяют на:
ПО ФУНКЦИОНАЛЬНОЙАКТИВНОСТИ
ИММУНОКОМПЕТЕНТНЫЕ КЛЕТКИ
ПОДРАЗДЕЛЯЮТ НА:
АГ-презентирующие – Т-хелперы
Регуляторные – Т-супрессоры
Эффекторные клетки – Т-киллеры
(ИКК)
94.
Cluster of differentiation (CD) – это показательдифференцировки, маркер, определяющий
особенности клеток иммунной системы и
обладающий антигенными свойствами.
95. Самое сложное в иммунном ответе – распознать «свой» или «чужой»
САМОЕ СЛОЖНОЕ В ИММУННОМОТВЕТЕ – РАСПОЗНАТЬ «СВОЙ» ИЛИ
«ЧУЖОЙ»
96. АНТИГЕНЫ
Антигенами (anti — против, genos - род)называют вещества любого происхождения, в
том числе микробного, которые распознаются
клетками иммунной системы организма
реципиента как генетически чужеродные и
которые вызывают специфические
гуморальные или клеточные
иммунологические реакции (продукция
специфических иммуноглобулинов (антител) и
образование специфических Т-клеток
эффекторов (исполнителей).
97. Основные функции антигенов:
ОСНОВНЫЕ ФУНКЦИИ АНТИГЕНОВ:1.
2.
3.
4.
Индуцируют иммунологический ответ (синтез
антител и запуск реакций клеточного
иммунитета).
Специфически взаимодействуют с
образовавшимися антителами как in vivo, так
и in vitro.
Обеспечивают иммунологическую память –
способность организма отвечать на повторное
введение антигена иммунологической
реакцией, характеризующейся большей силой
и более быстрым развитием.
Обуславливают развитие иммунологической
толерантности – арреактивности к
последующему иммуногенному воздействию
антигена.
98. Основные свойства антигенов:
ОСНОВНЫЕ СВОЙСТВА АНТИГЕНОВ:1.
Иммуногенность – способность вызывать
иммунитет, невосприимчивость к
инфекции.
2.
Антигенность – способность вызывать
образование специфических антител.
3.
Специфичность – способность
избирательно реагировать со
специфическими антителами или
сенсибилизированными лимфоцитами.
99.
Адъюванты (от лат.- adjuvans,помогать) – вещества, введение
которых одновременно с
антигенами (или гаптеном)
усиливает иммунный ответ.
Механизм действия адъювантов заключается в
депонировании (запасании) антигена,
стимуляции фагоцитоза и мутагенном действии
на лимфоциты, способствуют продукции
цитокинов.
100. Различают антигены:
РАЗЛИЧАЮТ АНТИГЕНЫ:1.
2.
3.
Гаптены (неполноценные антигены) – это
чистая детерминантная группа. Гаптены
имеют небольшую молекулярную массу и не
распознаются иммунокомпетентными
клетками. Гаптены обладают только
специфичностью.
Полноценные (конъюгированные) антигены –
образуются при связывании гаптена с
высокомолекулярным носителем,
обладающим собственной иммуногенностью.
Связь должна быть ковалентной.
Полугаптены – это неорганические радикалы
(J-, Cr-, Br-, N+), присоединение которых к
молекулам белка меняет его иммуногенные
свойства.
101. По способности специфично взаимодействовать с антителами выделяют несколько типов антигенов:
ПО СПОСОБНОСТИСПЕЦИФИЧНО ВЗАИМОДЕЙСТВОВАТЬ С
АНТИТЕЛАМИ ВЫДЕЛЯЮТ НЕСКОЛЬКО ТИПОВ АНТИГЕНОВ:
1.
2.
3.
4.
Видовые антигены представлены
антигенными детерминантами,
присутствующими у особей разных видов.
Групповые антигены (аллоантигены)
представлены антигенными детерминантами,
обусловливающими внутривидовые различия
у особей одного вида, разделяющие их на
группы.
Индивидуальные антигены (изоантигены) –
антигены конкретного индивидуума,
обладающие иммуногенностью по отношению
к другим представителям этого вида.
Гетерогенные антигены представлены
антигенными детерминантами, общими для
организмов разных таксономических групп
(антигенная мимикрия,
перекрестнореагирующие антигены).
102. В зависимости от систематического положения антигены микроорганизмов делят на:
В ЗАВИСИМОСТИ ОТ СИСТЕМАТИЧЕСКОГОПОЛОЖЕНИЯ АНТИГЕНЫ МИКРООРГАНИЗМОВ ДЕЛЯТ
НА:
1.
Группоспецифические – у разных групп
одного и того же семейства.
2.
Видоспецифические – у разных видов
одного и того же семейства.
3.
Типоспецифические – у разных типов
(вариантов) в пределах вида. По этим
антигенам микроорганизмы подразделяют
на серовары или серотипы.
103.
Основные антигены бактерий:К-Aг
(капсульный
)
Vi-Aг
(вирулентности)
Н-Aг
(жгутиковый)
О-Aг
(соматический)
104. Основные антигены бактерий:
ОСНОВНЫЕ АНТИГЕНЫ БАКТЕРИЙ:Название
антигена
Химическая
природа
Н-антиген
(жгутиковый)
Белок флагеллин
О-антиген
(соматически
й)
Липополисахарид Термостабильный
клеточной стенки (выдерживает кипячение в
течение 1 часа)
К-антиген
(капсульный)
Кислый
А – термостабильный
липополисахарид (выдерживает кипячение в
течение 2-х часов);
В – (промежуточный,
выдерживает нагревание до
600С, но при кипячении
разрушается);
L – термолабильный
(разрушается при нагревании
Отношение к температурным
воздействиям
Термолабильный
(разрушается при 56-600С)
105.
Протективные антигены – активные веществапатогенных микроорганизмов, способные
вызывать продукцию защитных антител,
предохраняющих организм от развития
патологического процесса, т.е развивается
эффект приобретенного иммунитета.
106. Антигены вирусов
АНТИГЕНЫ ВИРУСОВS -антигены
1.
2.
гемагглютинин
нейраминидаза
У простоустроенных
вирусов антигены
связаны с
нуклеокапсидом. По
химическому составу это
рибонуклеопротеиды и
обозначаются как
S- антигены.
У сложноустроенных
вирусов кроме Sантигенов есть
поверхностные
V-антигены, которые
представлены
гемагглютининами и
ферментом
нейраминидазой,
расположенными на
суперкапсиде.
107. Антигены человека и животных
АНТИГЕНЫ ЧЕЛОВЕКА И ЖИВОТНЫХ1. Изоантигены
(аллоантигены) –
антигены
организма
человека,
видоспецифичны
а) антигены
гистосовместимости (HLA);
б) антигены
эритроцитов
человека (АВ, Rh).
108. Антигены человека и животных
АНТИГЕНЫ ЧЕЛОВЕКА И ЖИВОТНЫХАНТИГЕНЫ ГИСТОСОВМЕСТИМОСТИ H L A
I класс
HLA – A,B,C
Экспрессия на любых
ядерных клетках
Взаимодействуют
преимущественно с вирусными,
опухолевыми и
трансплантационными
антигенами
II класс
HLA – D
Экспрессия на лимфоцитах,
макрофагах, нефагоцитирующих
клетках моноцитарного
происхождения, дендритных клетках
Взаимодействуют
преимущественно с антигенами
бактерий и прочими
молекулярными антигенами и
гаптенами
109. Антигены человека и животных
АНТИГЕНЫ ЧЕЛОВЕКА И ЖИВОТНЫХ2. Аутоантигены – собственные антигены
организма, которые при определенных
условиях распознаются антителами
как чужеродные и вызывают
выработку иммунного ответа.
а) врожденные антигены (головной мозг,
передняя камера глаза, роговица,
хрусталик, сетчатка, стекловидное
тело, семенные канальца яичек,
фолликулы щитовидной железы,
подкожная жировая клетчатка,
волосяные луковицы, рубцовая ткань,
эмбриональные белки);
б) приобретенные антигены (ожоговые,
лучевые и др.).
3. Перекрестнореагирующие антигены
(гетероантигены) – общие для
человека и микроорганизмов.
110. Основные формы иммунного ответа в соответствии с ведущим механизмом элиминации антигена
ОСНОВНЫЕ ФОРМЫ ИММУННОГО ОТВЕТАВ СООТВЕТСТВИИ С ВЕДУЩИМ МЕХАНИЗМОМ
ЭЛИМИНАЦИИ АНТИГЕНА
ГУМОРАЛЬНЫЙ ИММУННЫЙ ОТВЕТ → элиминация антигена
происходит при посредстве антител
- первичный иммунный от вет ;
- вт оричный иммунный от вет ;
- секрет орный иммунный от вет ;
- гиперчувст вит ельност ь немедленного т ипа.
КЛЕТОЧНЫЙ ИММУННЫЙ ОТВЕТ → элиминация антигена
происходит при участии лимфоцитов с цитотоксическими
свойствами
- гиперчувст вит ельност ь замедленного т ипа;
- ант игениндуцированная цит от оксичност ь;
- ест ест венная цит от оксичност ь.
ИММУНОЛОГИЧЕСКАЯ ТОЛЕРАНТНОСТЬ → элиминация антигена
не происходит
- ест ест венная (врожденная) т олерант ност ь;
- приобрет енная т олерант ност ь.
ИММУНОЛОГИЧЕСКАЯ ПАМЯТЬ → элиминация антигена происходит
при участии Т- и В-лимфоцитов памяти
111. Иммунологическая память
ИММУНОЛОГИЧЕСКАЯ ПАМЯТЬИммунологическая память - одна из форм
иммунного ответа, означает способность
организма человека или животного
реагировать на повторное введение того
антигена, которым он был иммунизирован
ранее, быстрее и с большей силой.
112. Иммунологическая толерантность
ИММУНОЛОГИЧЕСКАЯТОЛЕРАНТНОСТЬ
особая форма иммунного ответа,
характеризующуюся запретом, налагаемым Ти В-супрессорами на образование клетокэффекторов против данного, в том числе
собственного, антигена
113. Гиперчувствительность немедленного типа
ГИПЕРЧУВСТВИТЕЛЬНОСТЬНЕМЕДЛЕННОГО ТИПА
К реакциям чувствительности немедленного
типа относятся:
сывороточная анафилаксия;
лекарственная анафилаксия;
сывороточная болезнь;
сенная лихорадка;
бронхиальная астма;
крапивница и другие аллергические реакции.
В их основе лежат общие механизмы, которые
лучше всего изучены при анафилаксии
114. Гиперчувствительность замедленного типа
ГИПЕРЧУВСТВИТЕЛЬНОСТЬЗАМЕДЛЕННОГО ТИПА
местные и общие реакции, выявляющие
гиперчувствительность замедленного типа,
развиваются спустя значительно больший срок
после введения антигена
реакций гиперчувствительности замедленного
типа опосредуются не антителами, а
сенсибилизированными клетками - Тлимфоцитами
115. Иммунные реакции традиционно разделяют на гуморальные (реализуются циркулирующими в организме антителами) и клеточные
ИММУННЫЕ РЕАКЦИИ ТРАДИЦИОННО РАЗДЕЛЯЮТ НА ГУМОРАЛЬНЫЕ(РЕАЛИЗУЮТСЯ ЦИРКУЛИРУЮЩИМИ В ОРГАНИЗМЕ АНТИТЕЛАМИ) И
КЛЕТОЧНЫЕ (РЕАЛИЗУЮТСЯ ПРИ НЕПОСРЕДСТВЕННОМ КОНТАКТЕ
ИММУНОКОМПЕТЕНТНЫХ КЛЕТОК).
Гуморальный иммунный ответ
Распознавание антигена
Первичный
иммунный ответ
IgM
Вторичный
IgG, A,
иммунный ответ E
Секреторный
иммунный ответ
IgD
IgA
Гиперчувствительность
немедленного типа (ГНТ)
Реагиновый тип
IgE
Цитотоксический
IgG
тип
Иммунокомплексный
тип
IgG
Элиминация антигена, препятствие для его распространения в
организме (фиксация на клетках), запоминание антигена
116. Клеточный иммунный ответ.
КЛЕТОЧНЫЙ ИММУННЫЙ ОТВЕТ.Эффект оры клет очных иммунных реакций –
цитотоксические Т-лимфоциты, ТГЗТ-эффекторы и NK.
Различие в функциональной активности состоит в том, что
цитотоксические Т-лимфоциты и NK обладают прямой
цитотоксичностью, в то время как ТГЗТ-эффекторы
преимущественно вовлекают в ответ клетки других типов.
117. Иммунологическую память – способность организма отвечать на повторное введение антигена иммунологической реакцией,
ИММУНОЛОГИЧЕСКУЮ ПАМЯТЬ – СПОСОБНОСТЬ ОРГАНИЗМА ОТВЕЧАТЬ НАПОВТОРНОЕ ВВЕДЕНИЕ АНТИГЕНА ИММУНОЛОГИЧЕСКОЙ РЕАКЦИЕЙ,
ХАРАКТЕРИЗУЮЩЕЙСЯ БОЛЬШЕЙ СИЛОЙ И БОЛЕЕ БЫСТРЫМ РАЗВИТИЕМ.
Носителями иммунологической памяти становятся Т- и В-лимфоциты
после взаимодействия с соответствующим антигеном, или так
называемые ант игенст имулированные лимфоцит ы.
Клет ки памят и представляют ту часть Т- и В-антигенстимулированных
лимфоцитов, которые после 2-3 делений переходят в покоящееся
состояние и длительное время рециркулируют в организме. Они служат
своеобразным резервом иммунокомпетентных клеток, способных при
повторной встрече с тем же антигеном быстро превращаться в клеткиэффекторы иммунного ответа. В-лимфоцит ы быстро
трансформируются в антителообразующие клетки, а выроботка антител
происходит по вторичному типу.
Ант игенст имулированные Т-лимфоцит ы, циркулируя в организме,
готовы в любой момент распознать антиген, который их
сенсибилизировал, и немедленно включится в иммунный ответ.
Возникновение и поддержание популяции клет ок иммунной памят и –
одно из главных условий длит ельного сохранения приобрет енного
иммунит ет а.
118.
«Буст ер-эффект » (от англ. boost – усиливать) – это феноменинтенсивного развития иммунного ответа на вторичное
введение антигена.
Его используют на практике для получения лечебнопрофилактических и диагностических сывороток с высокими
титрами антител от иммунизированных животных.
119. Иммунологическая толерантность – арреактивность к последующему иммуногенному воздействию антигена (отсутствие иммунного ответа
ИММУНОЛОГИЧЕСКАЯ ТОЛЕРАНТНОСТЬ – АРРЕАКТИВНОСТЬ КПОСЛЕДУЮЩЕМУ ИММУНОГЕННОМУ ВОЗДЕЙСТВИЮ АНТИГЕНА
(ОТСУТСТВИЕ ИММУННОГО ОТВЕТА НА КОНКРЕТНЫЙ АНТИГЕН ПРИ
СОХРАНЕНИИ СПОСОБНОСТИ К ИММУННОМУ ОТВЕТУ НА ДРУГИЕ
АНТИГЕНЫ).
Иммунная сист ема т олерант на к собственным антигенам и не
толерантна к чужеродным.
Механизмы т олерант ност и:
1. Супрессорный (Т-супрессоры действуют на В-лимфоциты
или подавляют функции Т-хелперов).
2. Уничтожение аутореактивных клонов Т- и В-лимфоцитов.
3. Ограничение взаимодействия антигенпредставляющих клеток
и лимфоцитов (блокада антигенсвязывающих рецепторов).
120. Виды толерантности:
ВИДЫ ТОЛЕРАНТНОСТИ:Ест ест венная (врожденная) т олерант ност ь развивается по отношению к
аутоантигенам и сохраняется годами. Ее состояние развивается до
рождения ребенка.
Искусст венная (приобрет енная) т олерант ност ь может индуцироваться
различными веществами, попавшими в организм в начальном периоде
постнатального развития. Такие вещества называют толерогенами.
Приобретенная толерантность сохраняется всего лишь несколько
месяцев.
Поливалент ная т олерант ност ь возникает одновременно на все
антигенные детерминанты, входящие в состав конкретного антигена.
Моновалент ная (расщепленная) т олерант ност ь – избирательная
невосприимчивость каких-то отдельных антигенных детерминант, т.е.
гаптенов. При введение гаптенов развивается расщепленная
толерантность: антитела не образуются, но сохраняются клеточные
реакции иммунитета, или наоборот, имеются антитела при отсутствии
клеточных реакций.
Иммунный паралич – близкое к толерантности состояние,
развивающееся после введения больших доз антигена.
121. Основные формы иммунного ответа
ОСНОВНЫЕ ФОРМЫ ИММУННОГО ОТВЕТАФормы
иммунного
ответа
Основные эффекторы
Значение для организма
Гуморальный
Зрелые В-лимфоциты
1.Защита от АГ (синтез АТ).
2.Презентация АГ.
3.ГНТ.
4.Иммунологическая память.
Клеточный
Цитотоксические Тлимфоциты, ТГЗТ, NK
1.Цитотоксический эффект.
2.Синтез цитокинов.
3.ГЗТ.
4.Отторжение трансплантанта.
5.Иммунологическая память.
Иммунологическая
память
Т- и В-лимфоциты памяти
Устойчивость к повторному
внедрению АГ.
Иммунологическая
толерантность
Т-супрессоры
Отсутствие иммунного ответа к
аутоантигенам.
122. Основные субпопуляции клеток, участвующих в иммунных реакциях
ОСНОВНЫЕ СУБПОПУЛЯЦИИКЛЕТОК,
УЧАСТВУЮЩИХ В ИММУННЫХ РЕАКЦИЯХ
Типы клеток
Поверхностные
маркеры
Свойства
Т-лимфоциты
CD2, СD3
Участие в клеточных и гуморальных иммунных реакциях,
регуляции иммунного ответа
Т-хелперы
СD4
Распознавание антигена в комплексе с HLA-D; стимуляция
дифференцировки В-лимфоцитов и цитотоксических Тлимфоцитов; активация макрофагов
Цитотоксические
Т-лимфоциты (ЦТЛ)
СD8
Распознавание антигена в комплексе с HLA-A,B,C; уничтожение
клеток, экспрессирующих антигены
В-лимфоциты
CD19, CD20,
CD22, Ig, C3R
Распознавание антигена; дифференцировка в плазматические
клетки, секретирующие антитела; презентация антигена
Естественные
киллеры (ЕК)
CD16, CD56
Распознавание антигена; уничтожение клеток,
экспрессирующих антигены; антителозависимая
цитотоксичность; регуляция иммунного ответа
Макрофаги
(фагоцитирующие
клетки моноцитарного ряда)
CD16, HLA-D,
FcγR, C3R
Фагоцитоз, уничтожение микроорганизмов и опухолевых
клеток; презентация антигена; регуляция иммунного ответа
Нефагоцитирующие
клетки моноцитарного ряда,
дендритные клетки
HLA-D,
FcγR, C3R
Презентация антигена
123. Основные дифференцировочные маркеры клеток, участвующие в иммунном ответе
ОСНОВНЫЕ ДИФФЕРЕНЦИРОВОЧНЫЕ МАРКЕРЫКЛЕТОК, УЧАСТВУЮЩИЕ В ИММУННОМ ОТВЕТЕ
CD
маркер
Тип клетки
несущей
маркер
Функция
l
2
3
CD1
Т-лимфоцит
Участвует в представлении антигена
CD 2
Т-лимфоцит
Осуществляет
адгезию
(прилипание)
цитотоксических Т-лимфоцитов к клеткам мишеням,
Т-лимфоцитов
к
эндотелию,
тимоцитов к тимическим эпителиальным
клеткам
CD3
Т-лимфоцит
Проведение сигнала активации Т-клетки,
маркер абсолютного большинства всех зрелых
Т-лимфоцитов
124.
CD 4Т-лимфоцит
Ко-рецептор для ТКР при ГКС П распознавании, маркер Тхелперов
CD 8
T лимфоцит
Созревание и позитивная селекция ГКС I
рестриктированных лимфоцитов в тимусе, маркер
цитотоксических Т-лимфоцитов
CD 25
T -, В -, NKклетки,
тимоциты,
макрофаги
Индуцирует активацию и пролиферацию Т-, В-лимфоцитов,
естественных киллеров (NK), тимоцитов и макрофагов αсубъединица рецептора для ИЛ-2
CD 28
Т-лимфоцит
Ко-стимуляторная сигнальная молекула, независимая от ТКР
CD 30
Т-лимфоцит
Проведение сигнала для запуска апоптоза Т-лимфоцитов
CD 5
Т- и В- лимфоциты
CD 9
В лимфоцит
Представлен на пре - В клетках, ответственен за агрегацию и
активацию тромбоцитов
CD19, 20, 21
В-лимфоцит
Регуляция активации и пролиферации В-лимфоцитов
CD 22
В-лимфоцит
Ответственен за адгезию к эритроцитам, Т-клеткам, Влимфоцитам, моноцитам и нейтрофилам
CD 40
В-лимфоцит
Участвует в В-клеточной активации, пролиферации и
дифференцировке
Выражен при аутоиммунных заболеваниях, костимуляторный сигнал активации Т- лимфоцитов и
тимоцитов
125.
CD 16Естественный
киллер
Активация антиген-зависимой комплементопосредованной цито-токсичности и цитокиновой
продукции
CD 56
Естественный
киллер
Активация цитотоксичности и цитокиновой
продукции
CD 94
Естественный
киллер
Ингибиция/активация цитотоксичности
естественных киллеров
CD lla/
CD18
Моноциты,
гранулоциты
Адгезия (прилипание) лейкоцитов к эндотелию,
адгезия лейкоцита к лейкоциту
CD lib/
CD18
Моноциты,
гранулоциты
Адгезия (прилипание) моноцитов и нейтрофилов к
эндотелию сосудов, опсонизация комплемент
связанных частиц
CD lie/
CD18tob
Моноциты,
гранулоциты
Адгезия моноцитов и гранулоцитов к эндотелию при
воспалении: фагоцитарный рецептор
CD 45
Гранулоциты
Рецептор для тирозинфосфатазы
CD64
Макрофаги
Активация макрофагов
CD 34
Стволовая клетка,
комитированный
колоние-образующий
предшественник
Прикрепление L-селектин лимфоцитов к эндотелию
сосудов, прикрепление стволовых гемопоэтических
клеток к строме костного мозга
126. Фазы иммунного ответа
ФАЗЫ ИММУННОГО ОТВЕТАНазвание фазы
Характеристика
Афферентная
Фагоцитоз и процессинг АГ макрофагом,
выставление на поверхности мембраны
макрофага фрагментов АГ
Центральная
Распознавание антигена Т- и Влимфоцитами
Эффекторная
Реализация иммунного ответа по
клеточному (цитотоксические Т-лимфоциты)
или гуморальному (синтез антител) типу
127.
Межклеточная кооперация иммунокомпетентныхклеток при иммунном ответе
Т-хелперы
ИЛ1
ИЛ2
Аг-представляющая
клетка
Клеточный иммунный
ответ
Активаци
я
ТТ-хелпер
хелпера
ИЛ2
В-лимфоцит
Гуморальный иммунный
ответ
ИЛ-2
ИЛ-4
ИЛ-5
ИЛ-6
γИФ
Н
Цитокины
А
Т
Вклетка
памяти
Плазматическая
клетка
Активац
ия
Цитотоксический
Т-лимфоцит
Клетка - мишень
Уничтожени
е
Цитолиз
128.
Иммунный ответАГ + Тцл → клеточная реакция
Клеточный иммунитет
АГ
+ МФ
Т-цитотоксический
лимфоцит
Т-цитотоксический
лимфоцит
Т-хелперы
(Т4)
Т-цитотоксический
лимфоцит
В-лимфоциты
АГ + АТ → серологическая
реакция
Гуморальный иммунитет
Плазматически
е клетки
IgM
IgA
IgG
Т8 (Тцитотоксический
лимфоцит)
IgE
IgD
С помощью серологической и клеточных реакций иммунитета АГ
нейтрализован и выведен из организма, а Т- и В-клетки памяти запоминают
антигены и при повторном его проникновении нейтрализуют антиген
(постинфекционный и поствакционный иммунитеты)!!!
129. Компоненты иммунной системы:
КОМПОНЕНТЫ ИММУННОЙ СИСТЕМЫ:1. Органы иммунной системы:
a) Центральные (костный мозг, тимус).
b) Перифирические (селезенка, лимфатические узлы,
лимфоидная ткань слизистых оболочек).
2. Иммунокомпетентные клетки (Т- и В-лимфоциты, NК,
макрофаги, нейтрофилы, дендритные клетки и др.).
3. Биологически активные макромолекулы:
a) Медиаторы иммунных реакций (интерлейкины).
b) Ростовые факторы (интерфероны, ФНО, КСФ и др.)
c) Гормоны (тимопептиды, миелопептиды).
130.
Цит окины (от греческих корней cyto – клетка, kinos –движение) – это молекулы, секретируемые клетками во
внеклеточную среду с целью воздействовать на другие
клетки или на себя же, подать сигнал к запуску тех или
иных процессов в клетках-мишенях (интерлейкины,
факторы роста, ФНО, КСФ, интерфероны).
Цит окины – молекулярный язык межклеточного общения.
131.
Нарушение функционирования иммуннойсистемы.
132.
Р. Брутон (1957 г.) – первая форма врождённогоиммунодефицита (агаммаглобулинемия
брутоновского типа).
Иммунная система не только
защищает организм от болезней, но и
сама имеет болезни.
133. ИММУННЫЕ НАРУШЕНИЯ
Все иммунологическиенарушения подразделяют на
3 группы:
1.
1.
2.
Иммунодефициты
Аутоиммунные процессы
(заболевания)
Аллергия
134.
Иммунодефициты —самостоятельные заболевания
(нозологические формы) и
сопутствующие синдромы,
характеризующиеся
недостаточностью иммунной
системы.
135.
136. ФОРМЫ ВРОЖДЕННЫХ ИММУНОДЕФИЦИТОВ
ТКИН:А. Синдром Ди-Джорджи
Б. Синдром Незелофа (нарушается синтез спец.антител)
2. Синдром Луи-БАРА (атаксия, телеангиоэктазия,
1.
пневмония)
3. Синдром Брутона
4. Дисиммуноглобулинемия
-селективный дефицит IgA
-селективный дефицит IgG, IgM
-селективный гипер- IgE
5. Синдром Вискотта-Олдрича (экзема,
тромбоцитопения)
6. Недостаточность фагоцитоза
7. Недостаточность в системе комплемента
8. Общий вариабельный иммунодефицит
137. ПРИЧИНЫ ПРИОБРЕТЁННЫХ ИММУНОДЕФИЦИТОВ
Ожоговаяболезнь
Уремия
Опухоли
Старение
Инфекционные
и паразитарные
болезни
Стресс
Химио- и радиотерапия
Терапия гормонами и другими
цитостатиками
138. Аутоиммунные заболевания Аутоиммунные заболевания – это группа болезней, при которых происходит разрушение органов и тканей
АУТОИММУННЫЕЗАБОЛЕВАНИЯ
АУТОИММУННЫЕ ЗАБОЛЕВАНИЯ – ЭТО ГРУППА
БОЛЕЗНЕЙ, ПРИ КОТОРЫХ ПРОИСХОДИТ
РАЗРУШЕНИЕ ОРГАНОВ И ТКАНЕЙ ОРГАНИЗМА ПОД
ДЕЙСТВИЕМ СОБСТВЕННОЙ ИММУННОЙ СИСТЕМЫ.
139.
К наиболее распространеннымотносятся склеродермия, системная
красная волчанка, аутоиммунный
тиреоидит Хасимото, диффузный
токсический зоб и пр. Кроме того,
развитие многих заболеваний
(инфаркт миокарда, вирусный
гепатит, стрептококковые,
герпесные, цитомегаловирусные
инфекции) может осложняться
появлением аутоиммунной реакции.
140. Факторы, приводящие к развитию аутоиммунного заболевания:
ФАКТОРЫ, ПРИВОДЯЩИЕ КРАЗВИТИЮ АУТОИММУННОГО
ЗАБОЛЕВАНИЯ:
генетические факторы
перекрестная сенсибилизация
повреждение собственных тканей
организма
141.
Внешние причины — это в основномвозбудители инфекционных
заболеваний или физическое
воздействие, например,
ультрафиолетовое излучение или
радиация. При поражении
определенной ткани человеческого
организма, они изменяют собственные
молекулы таким образом, что
иммунная система воспринимает
их как чужие.
142.
Внутренние причины — этогенные мутации, передающиеся
по наследству.
Мутации изменяют антигенную
структуру определенного органа
или ткани, мешая лимфоцитам
распознавать их как «своих».
143. Пусковым моментом развития аутоиммунных реакций является образование в организме аутоантигенов (собственных антигенов). Их
ПУСКОВЫМ МОМЕНТОМ РАЗВИТИЯАУТОИММУННЫХ РЕАКЦИЙ ЯВЛЯЕТСЯ
ОБРАЗОВАНИЕ В ОРГАНИЗМЕ АУТОАНТИГЕНОВ
(СОБСТВЕННЫХ АНТИГЕНОВ). ИХ РАЗДЕЛЯЮТ
НА ДВЕ ГРУППЫ.
1. Первичные, или истинные
2. Вторичные аутоантигены не
аутоантигены — это нормальные, так
называемые забарьерные ткани,
которые в процессе формирования
иммунной системы в эмбриогенезе не
имели, а во взрослом состоянии не
имеют контакта с
иммунокомпетентными клетками, так
как определены гистогематическим
барьером.
являются истинными. Они
образуются из компонентов клеток
и тканей организма под влиянием
различных факторов среды
внешней и внутренней, например,
при инфекционном и
неинфекционном воспалениях, при
употреблении лекарственных
препаратов.
144. АЛЛЕРГИЯ
-типоваяформа измененной
иммуногенной реактивности
организма, основу которой
составляет специфическое
избирательное повышение его
чувствительности к повторным
воздействиям аллергенов,
антигенов и гаптенов
145.
ИММУННЫЙ СТАТУС– это есть состояние
здоровья иммунной системы.
Для оценки иммунного
статуса производят забор
крови
из вены.
146.
Оцениваютобщее количество лимфоцитов
количество Т-лимфоцитов
общее количество В-лимфоцитов
Т-хелперы (Т4) – 600-1600
клеток - NВ!!!
Т-супрессоры (Т8) – 300-800
клеток
иммунорегуляторный индекс
(Т4/Т8) – не меньше 1 и не
больше 3 – 3,5
иммуноглобулины (IgG, IgM, IgA, IgE,
IgD)










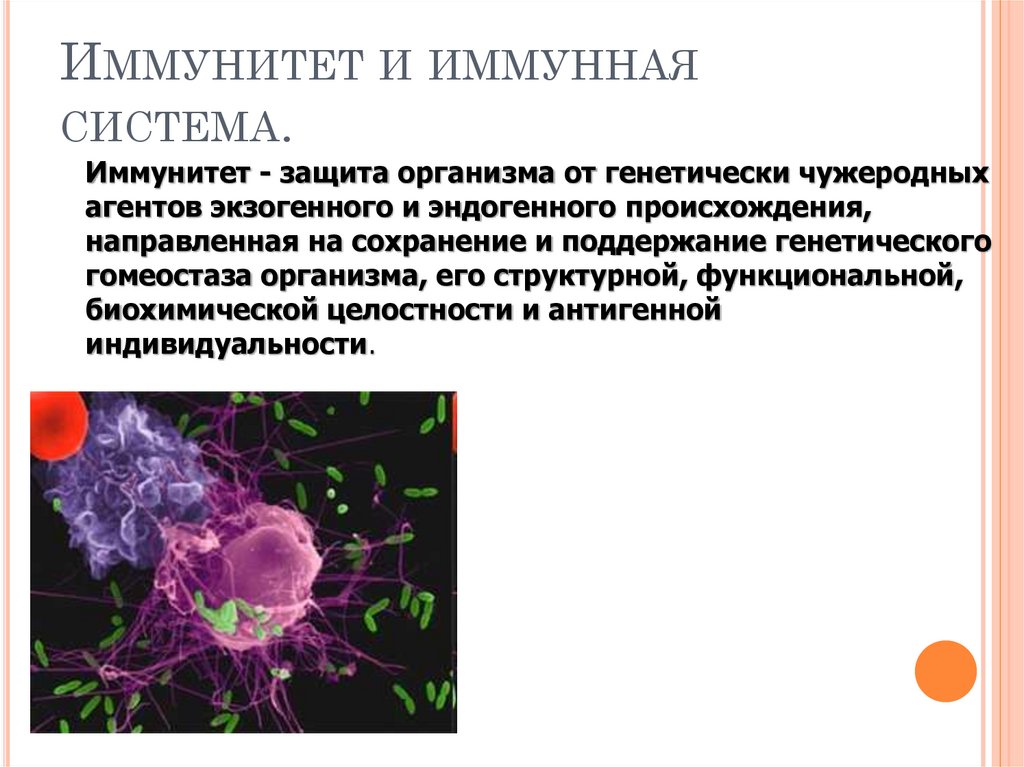


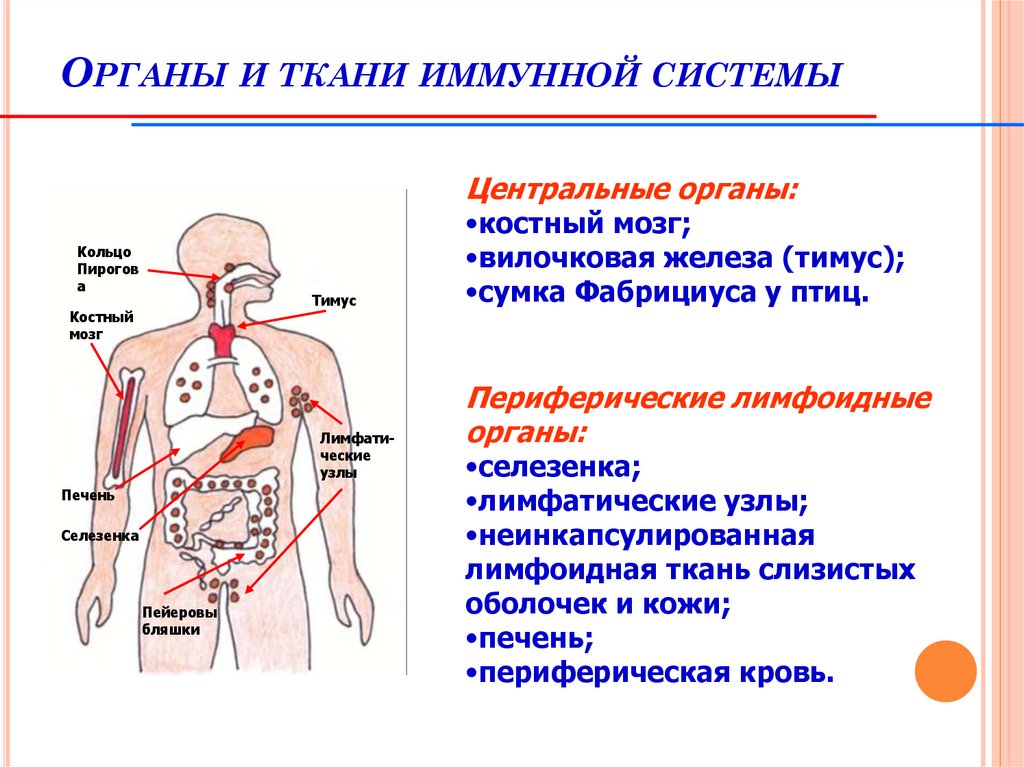



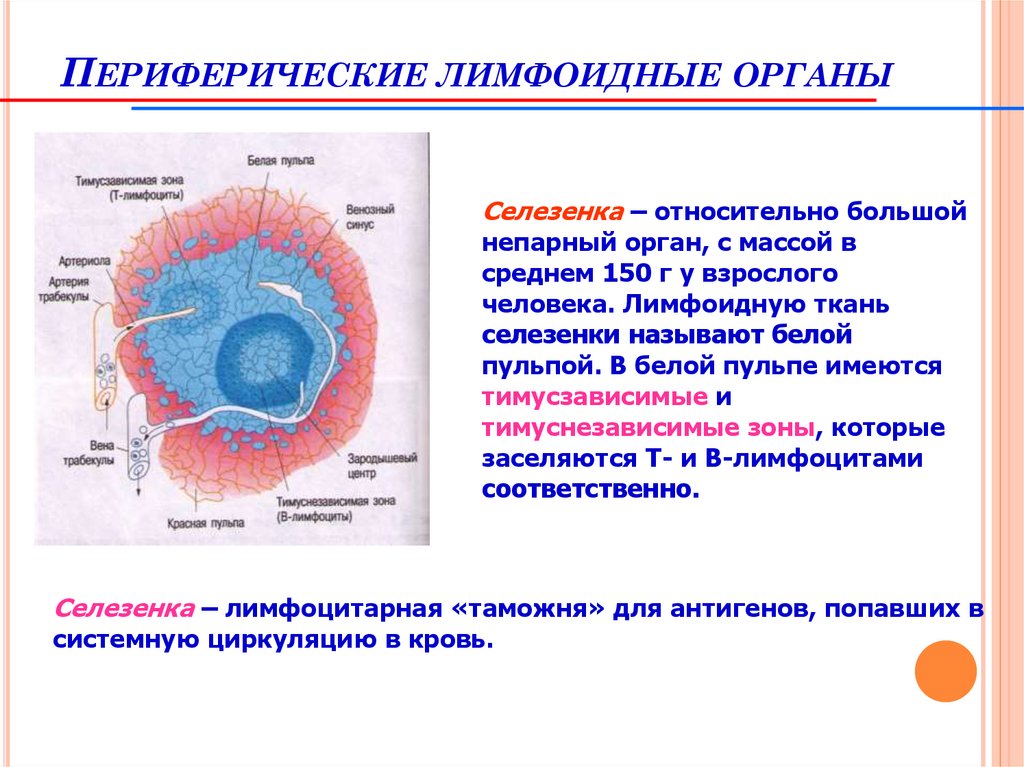


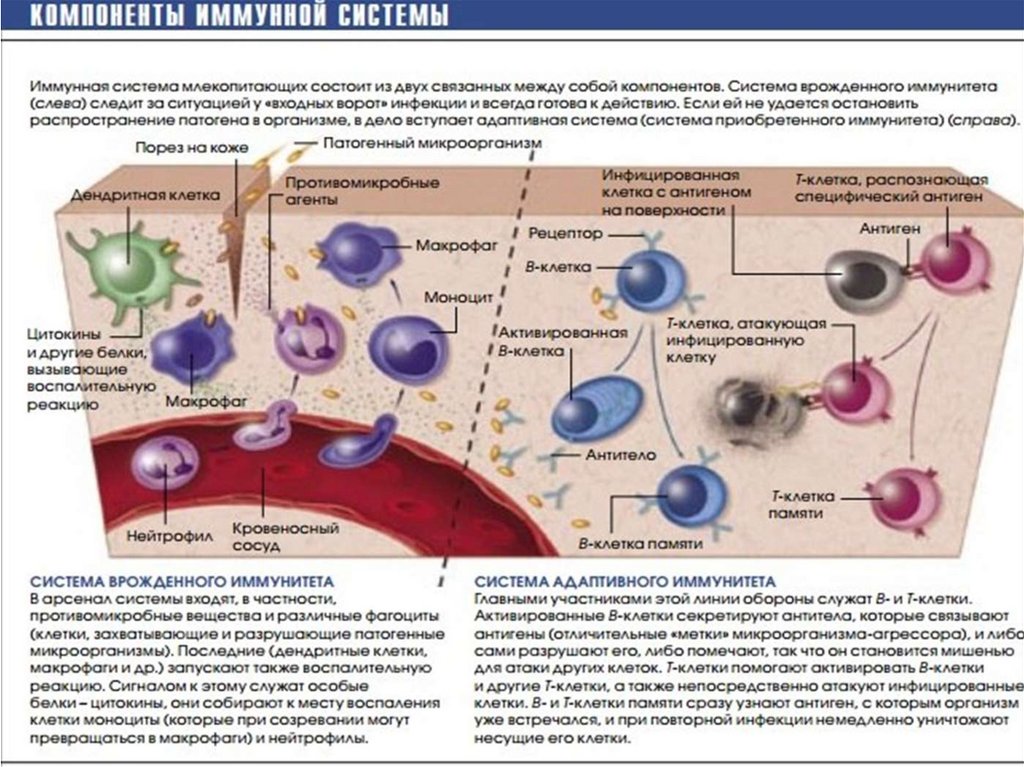



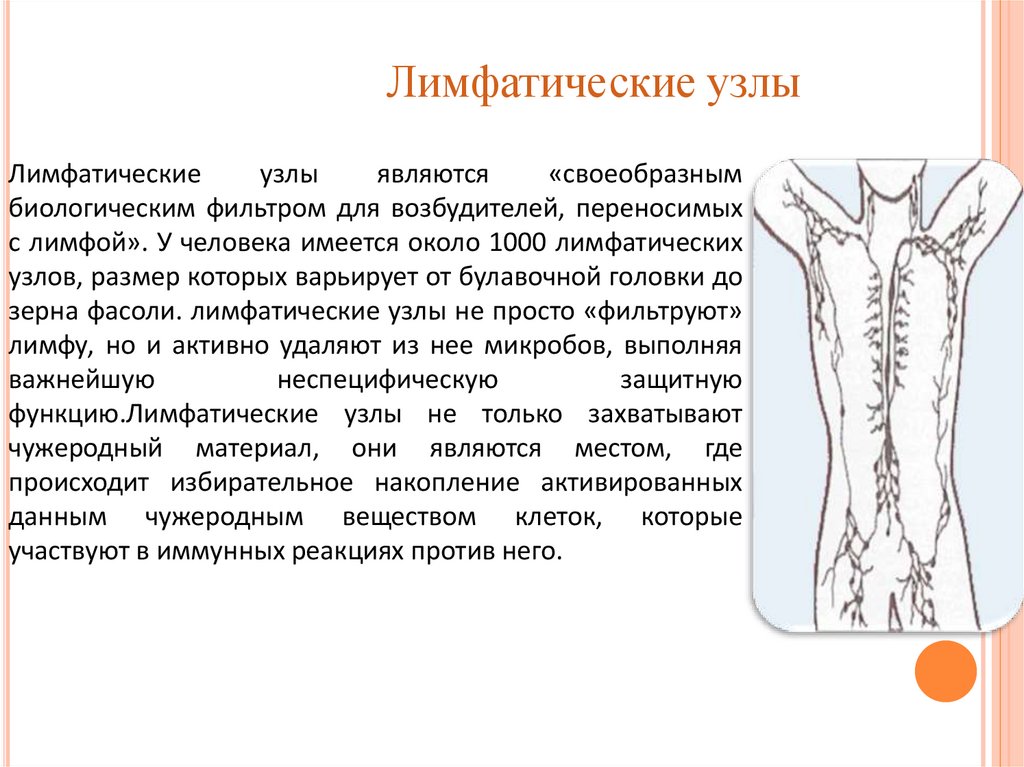




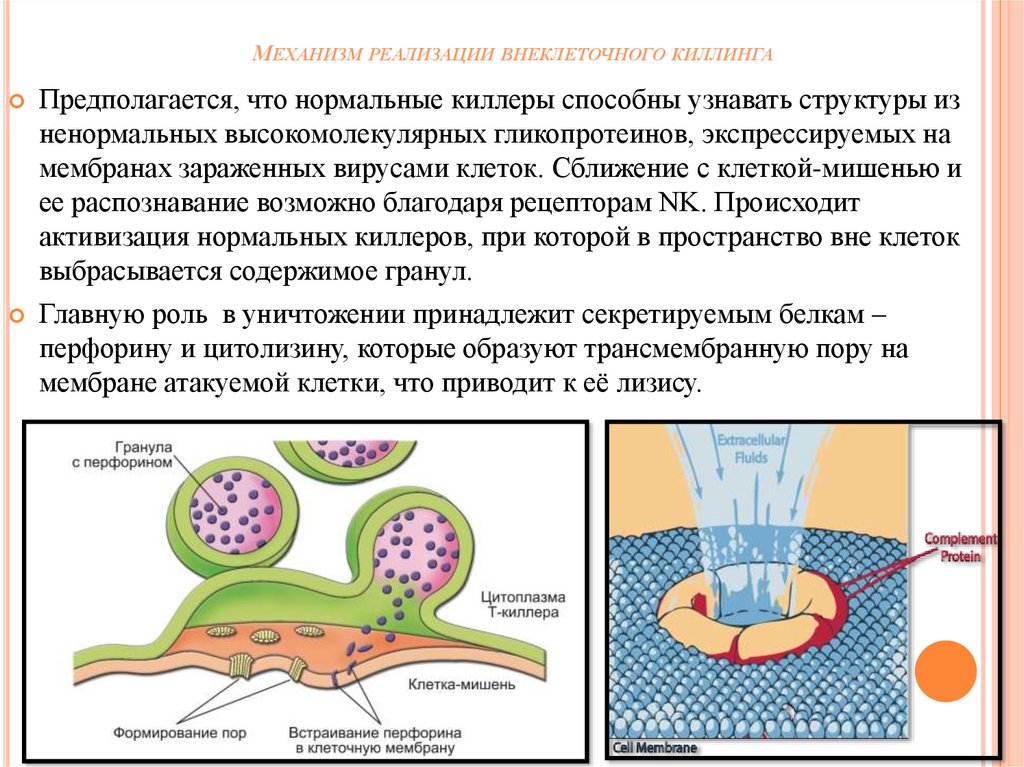
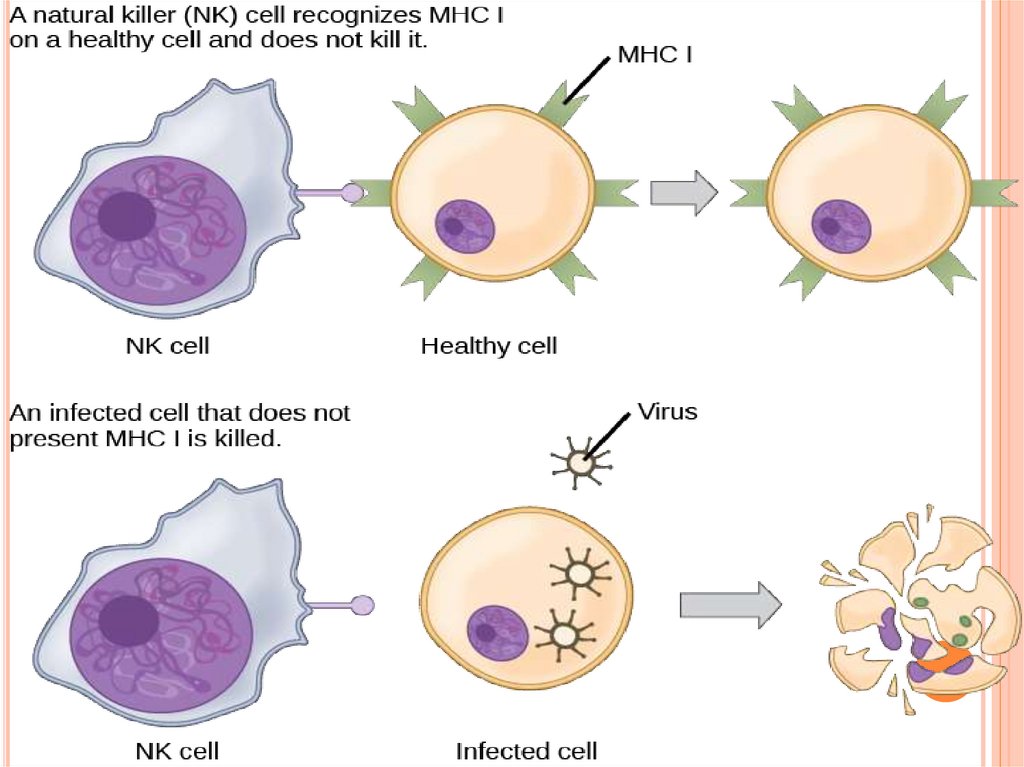
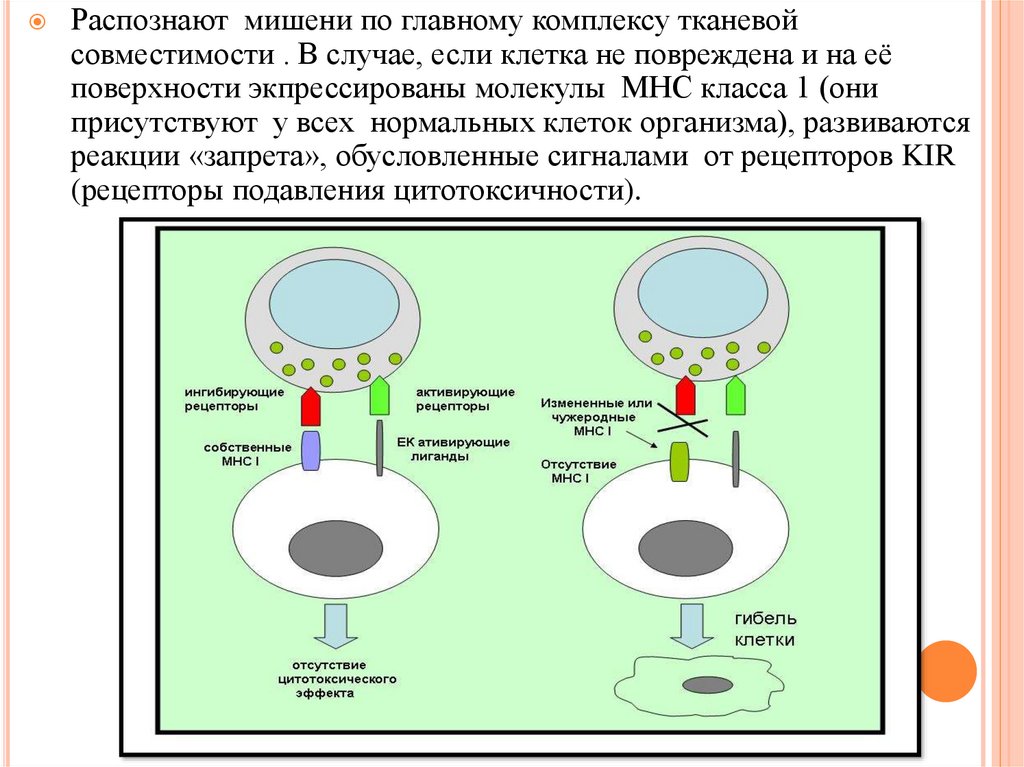
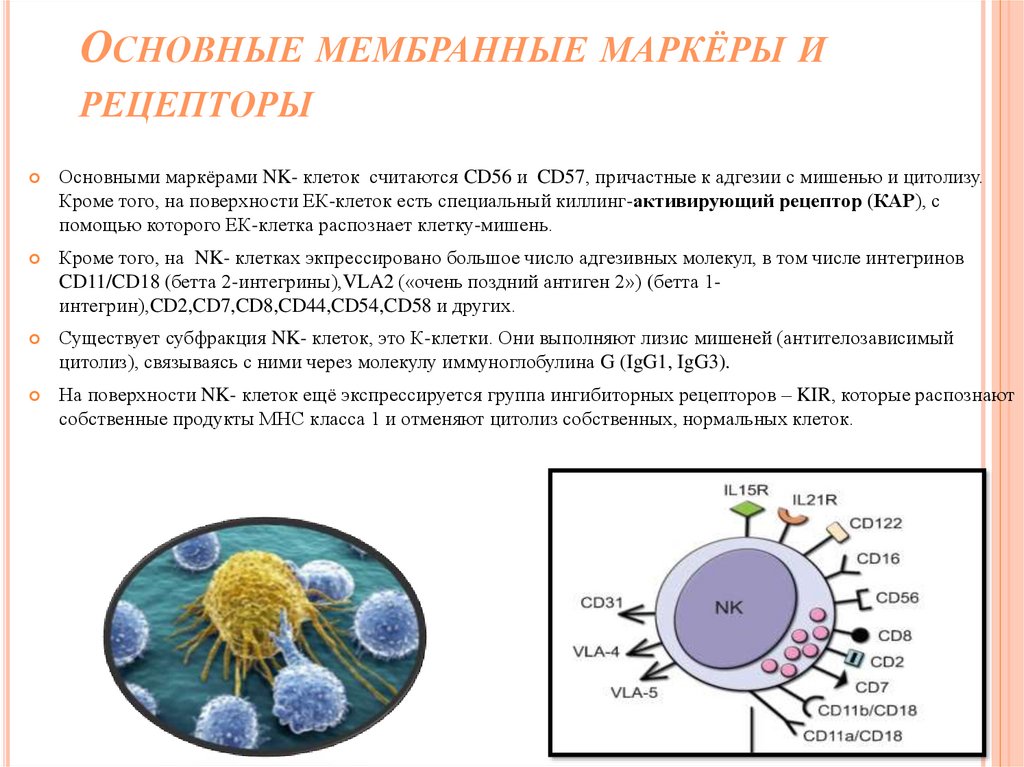

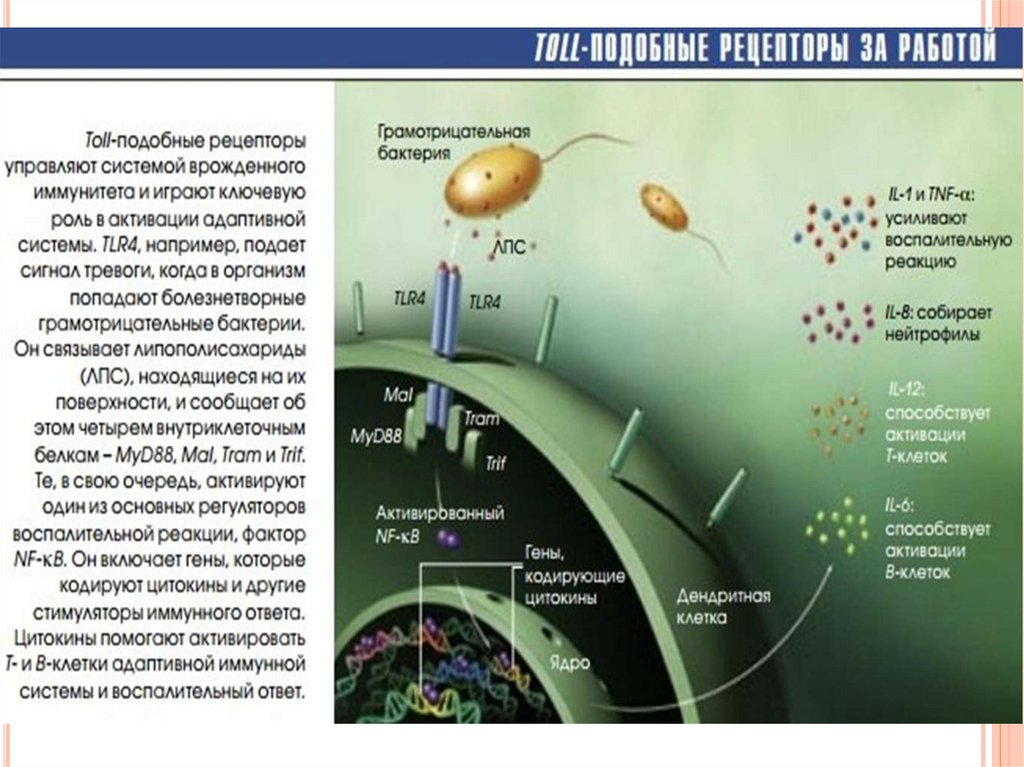


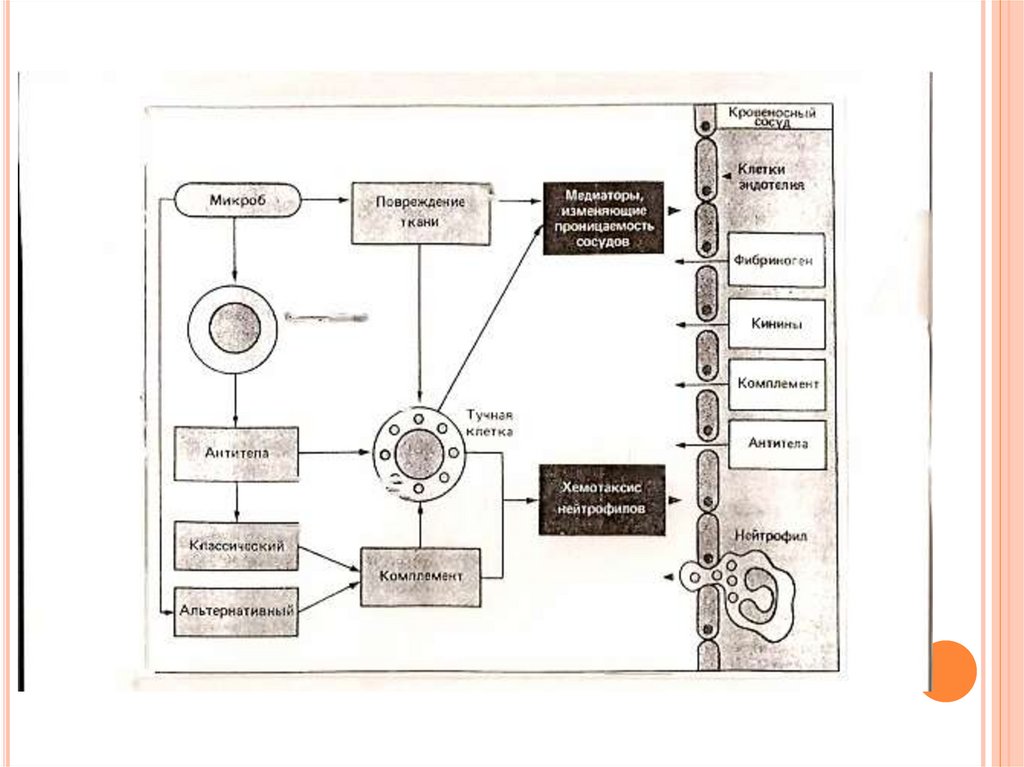







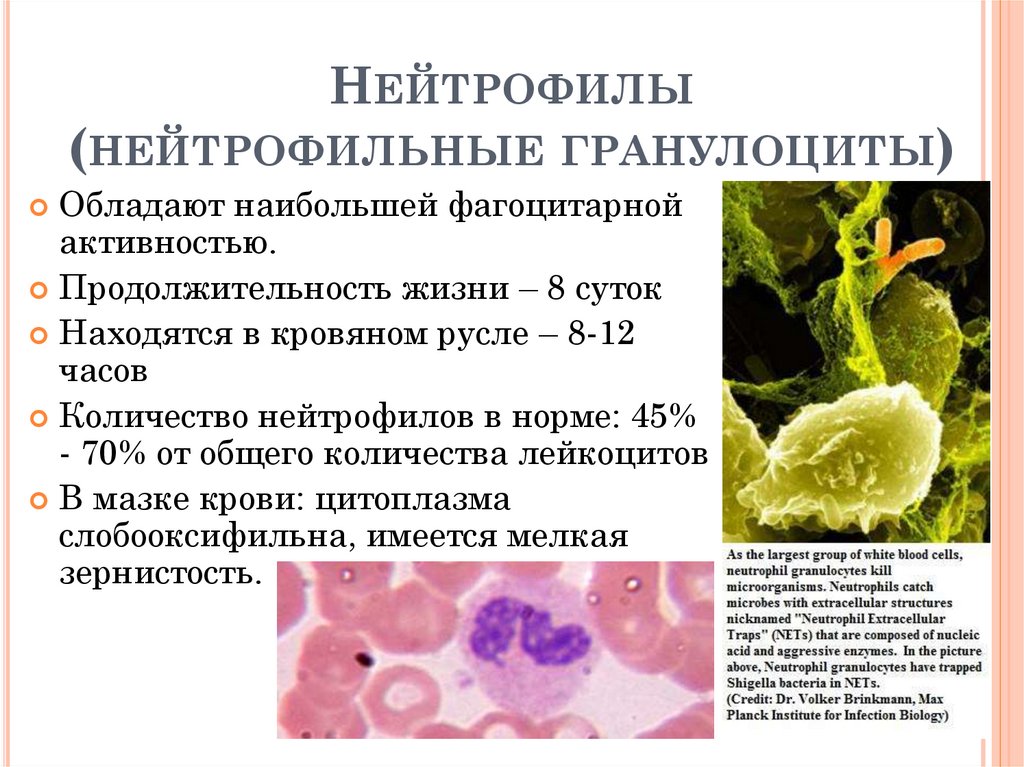
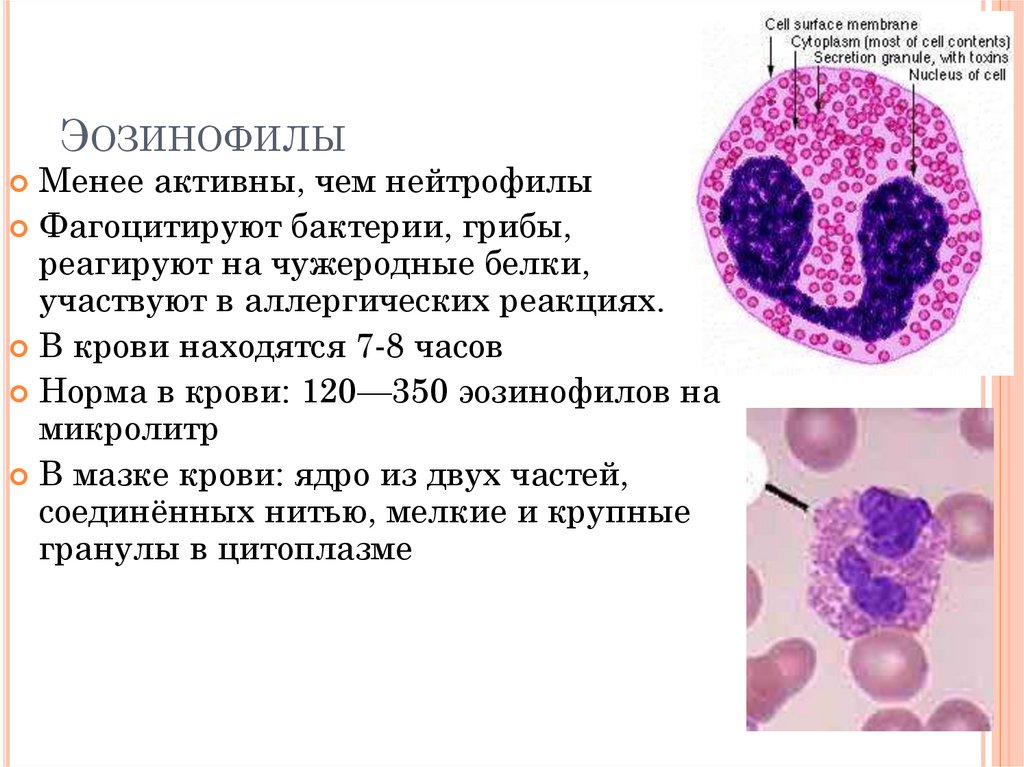
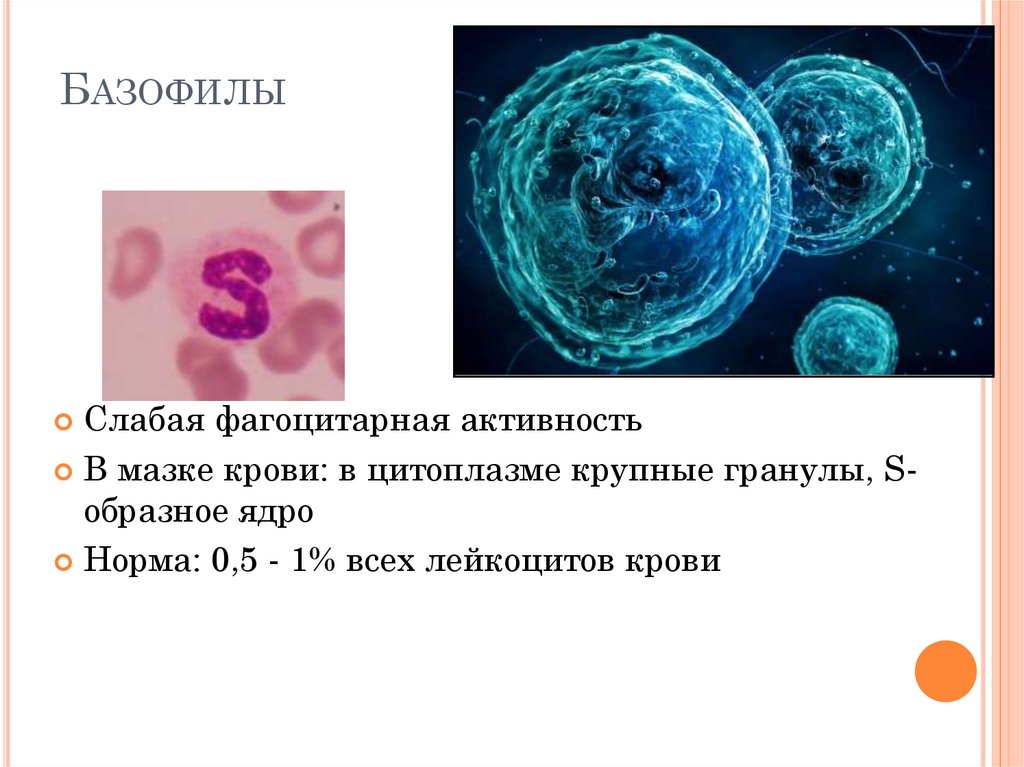




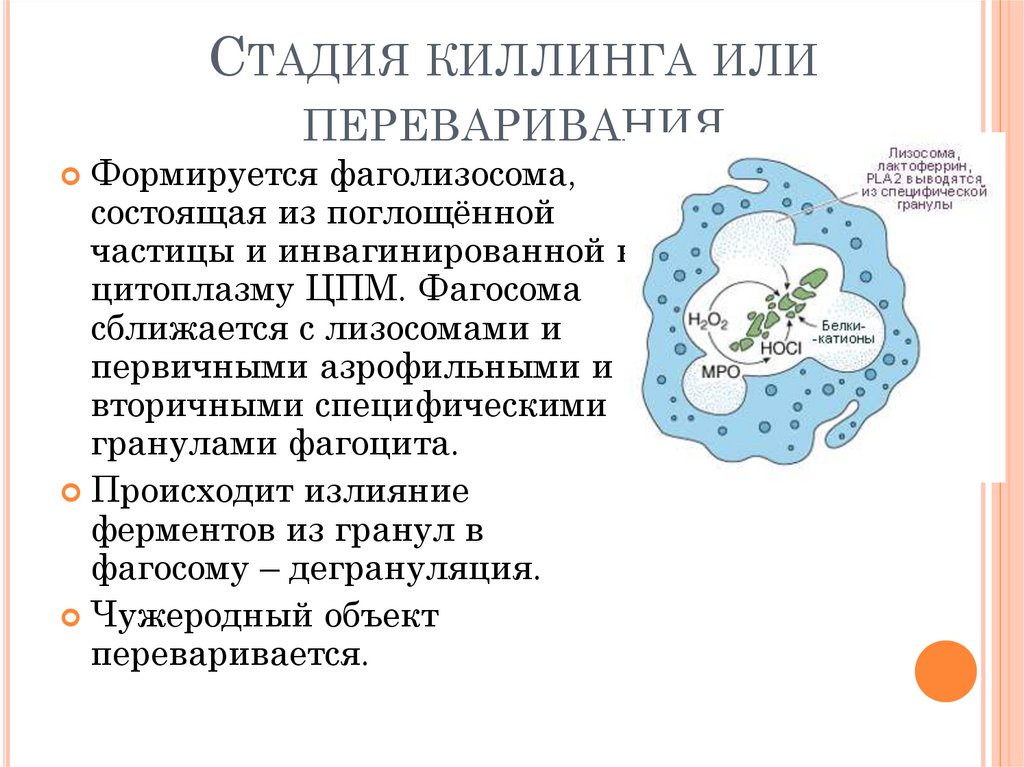





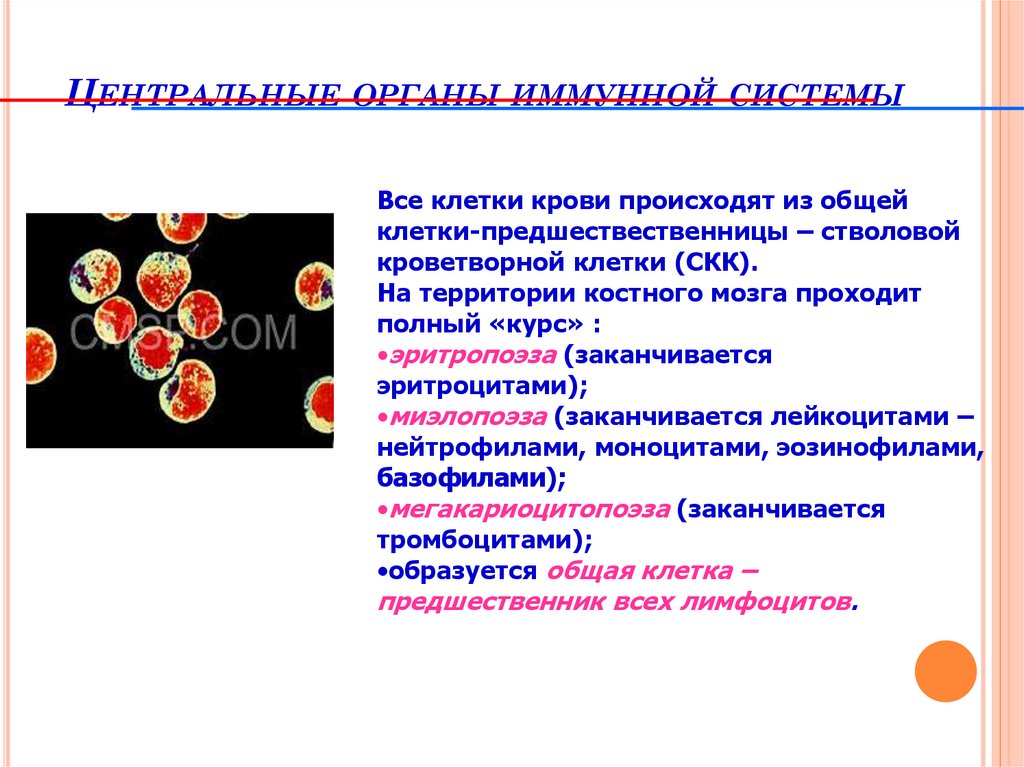






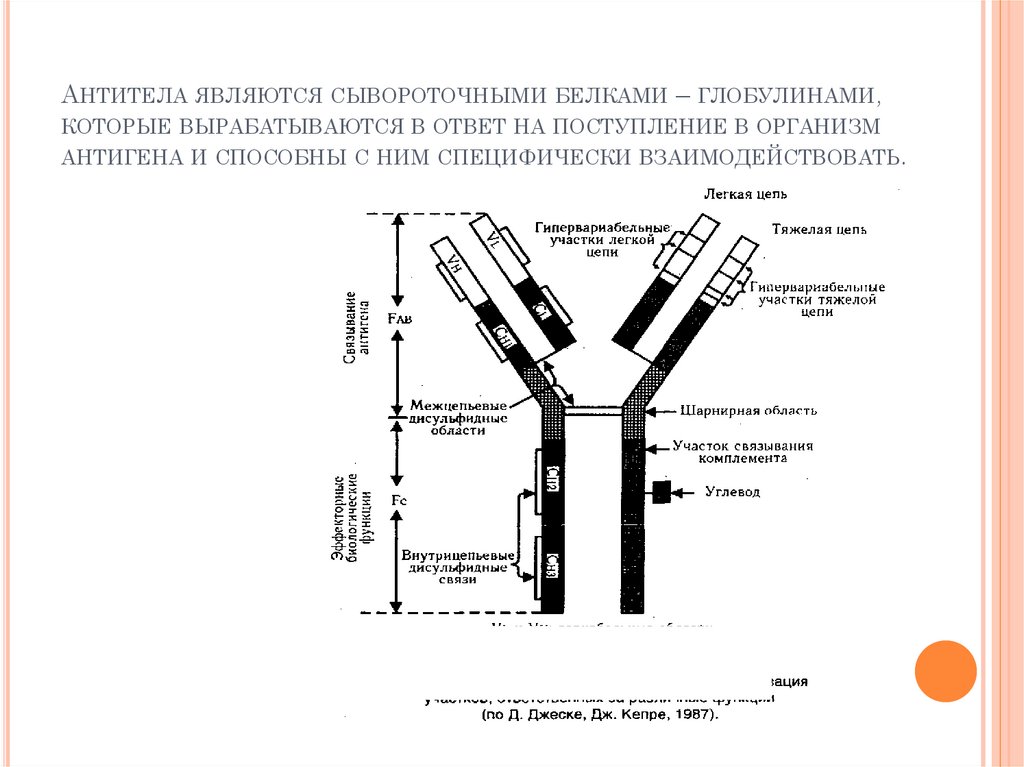

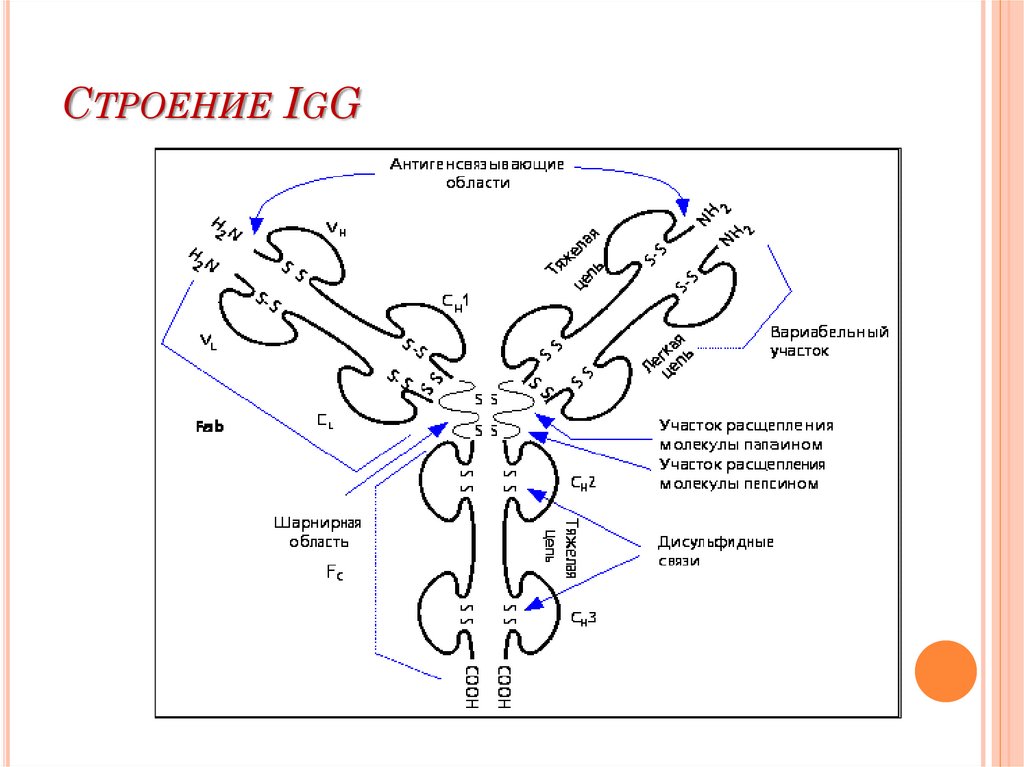


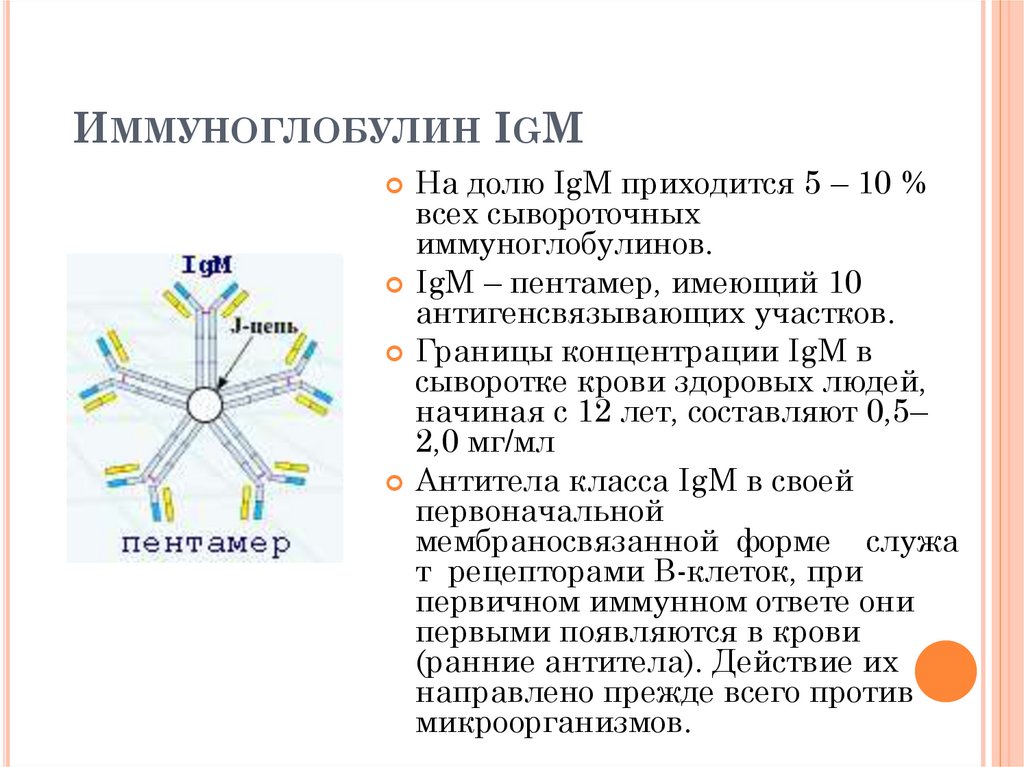






















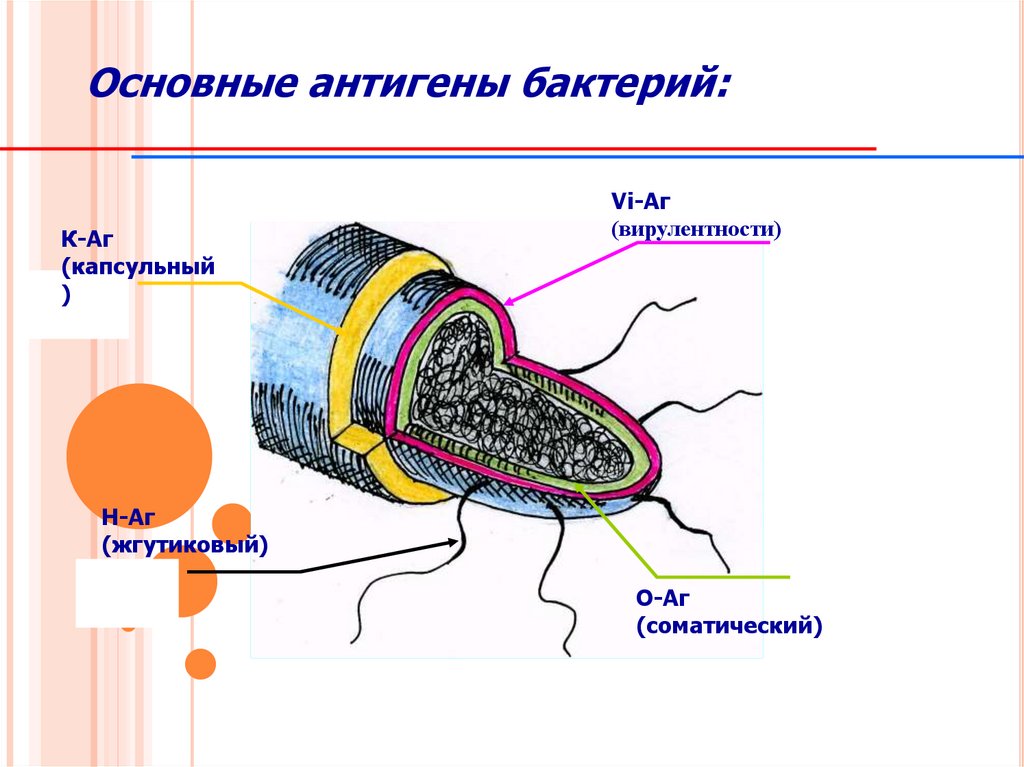
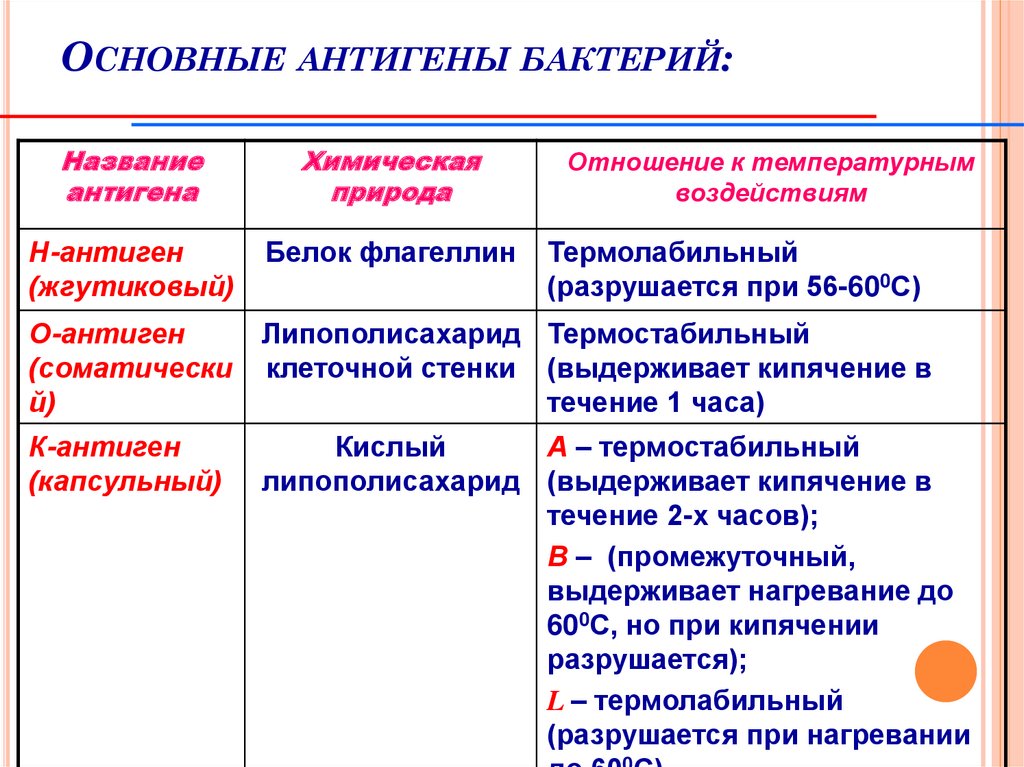

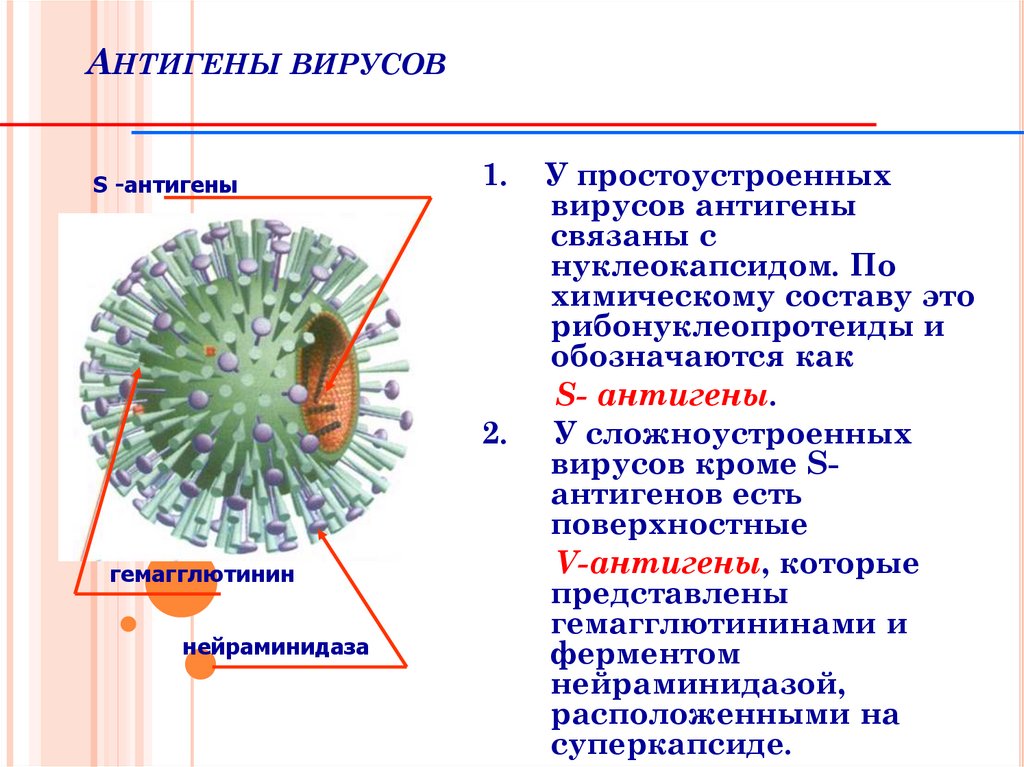
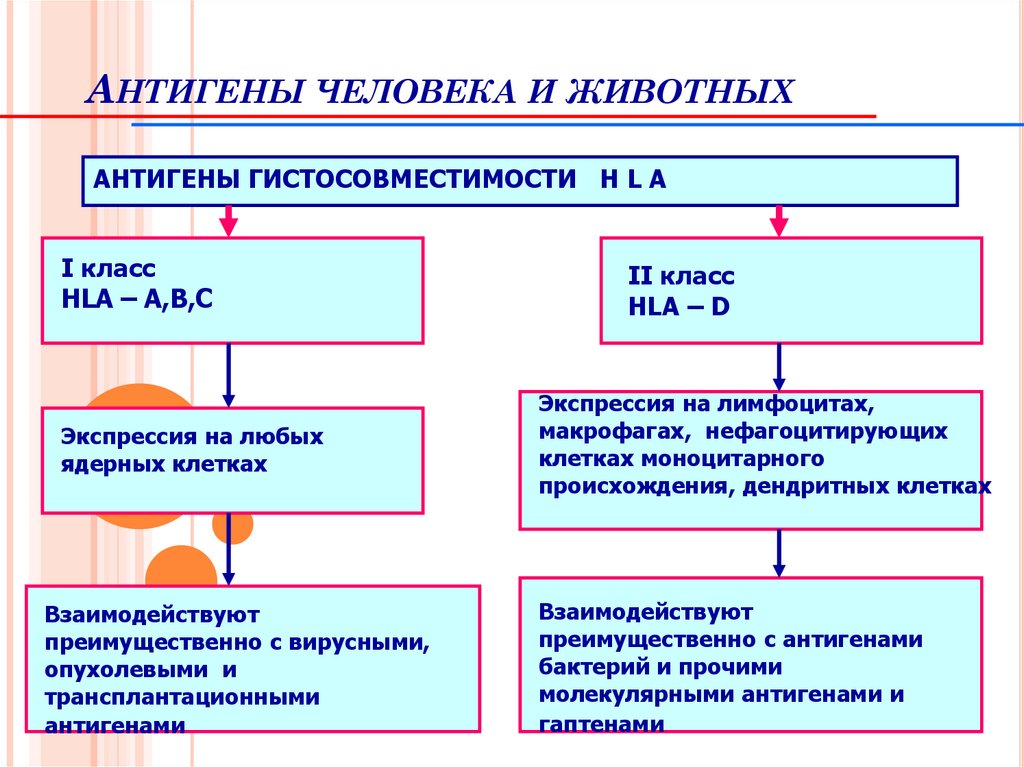






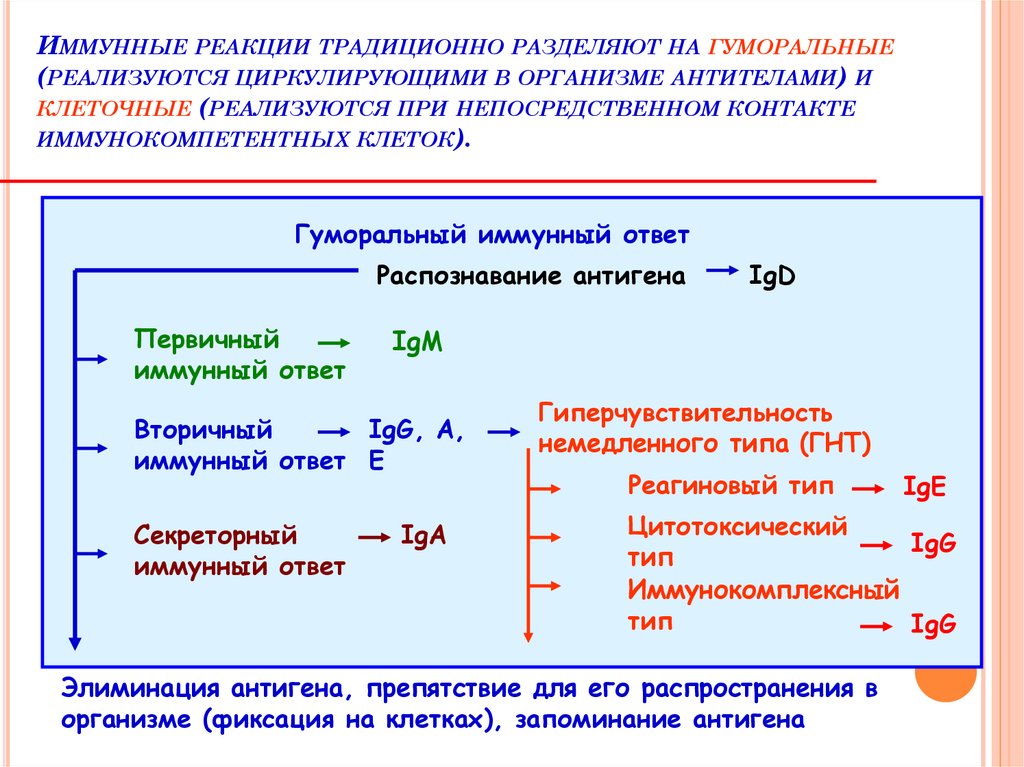






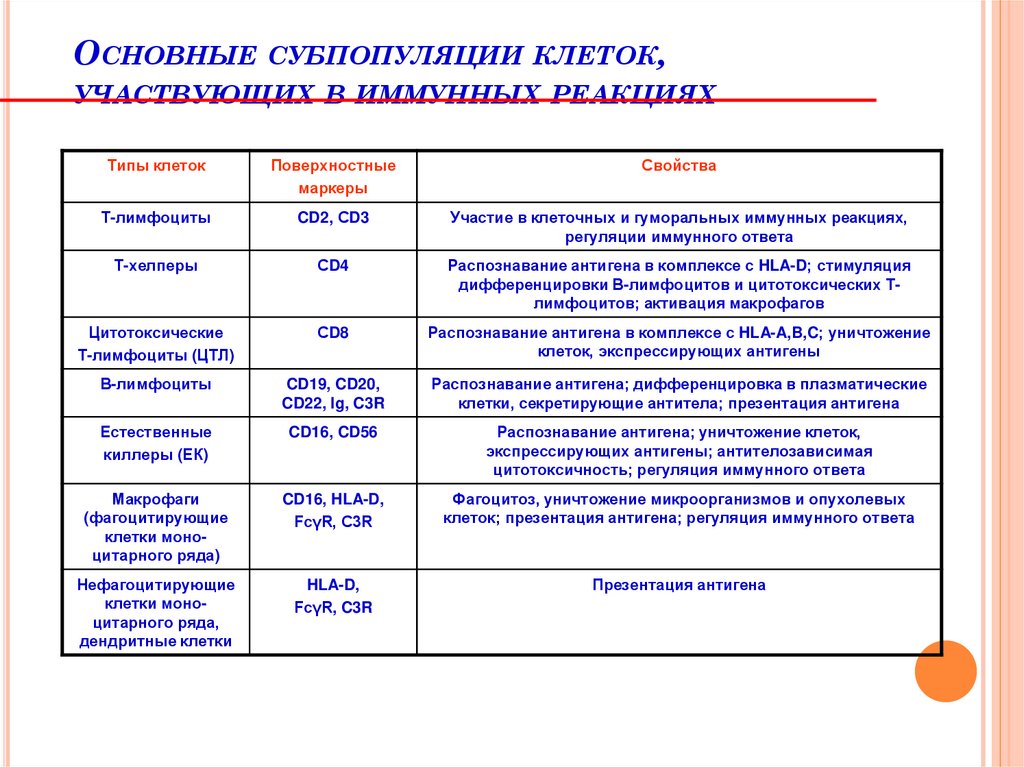

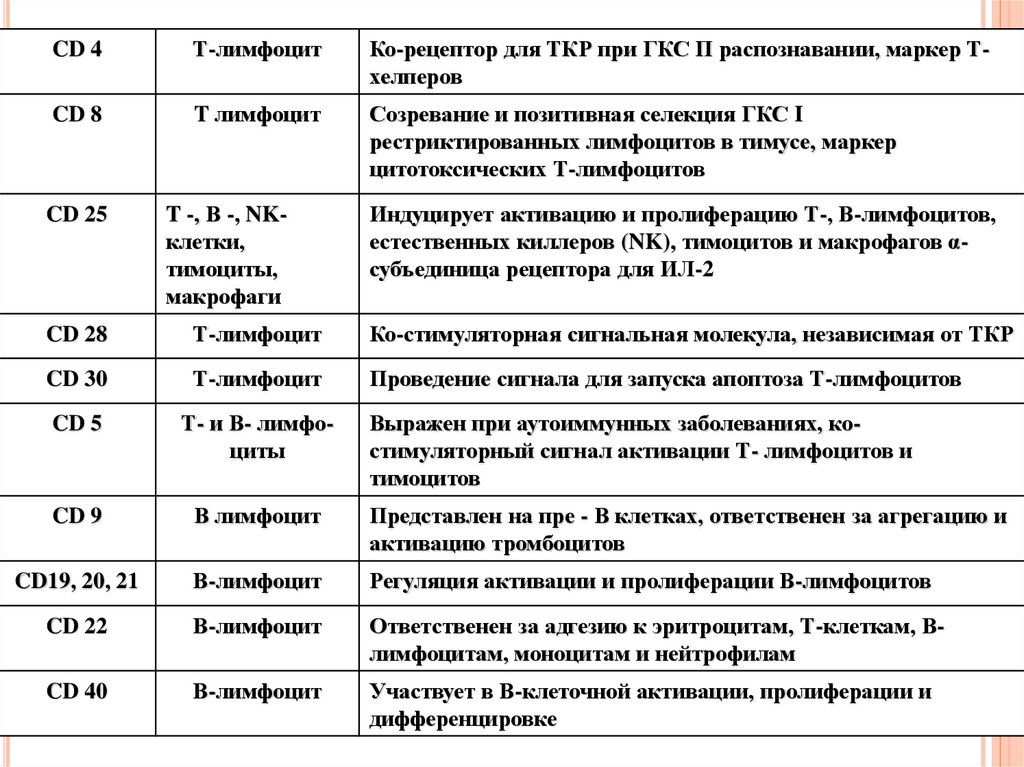
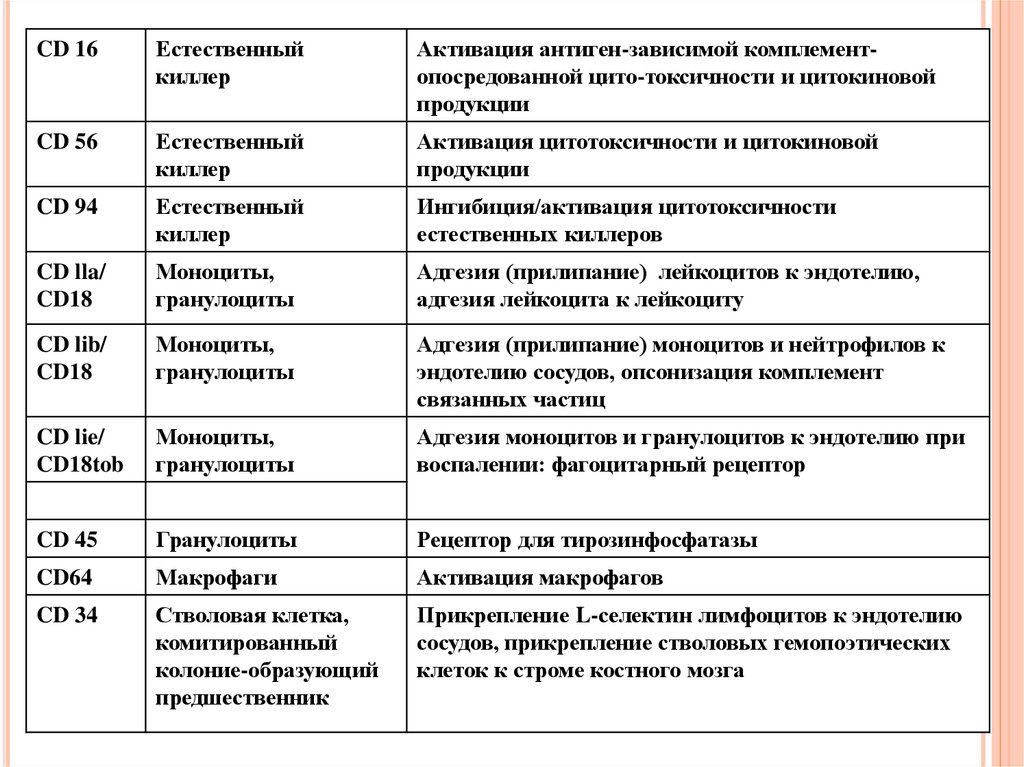
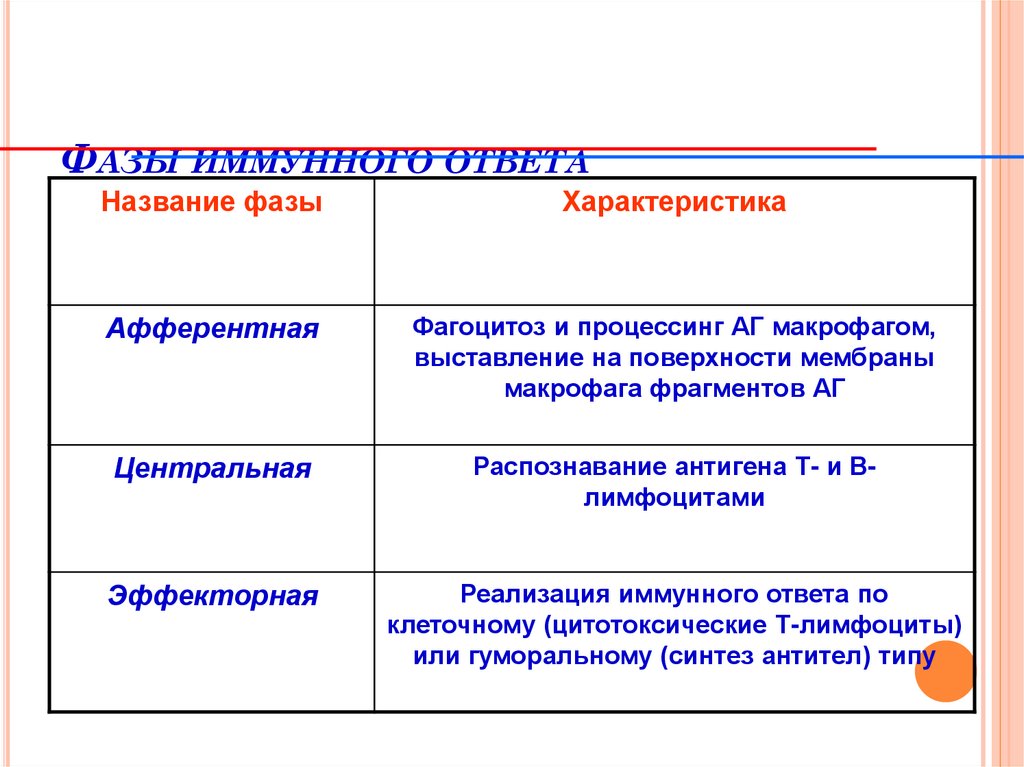
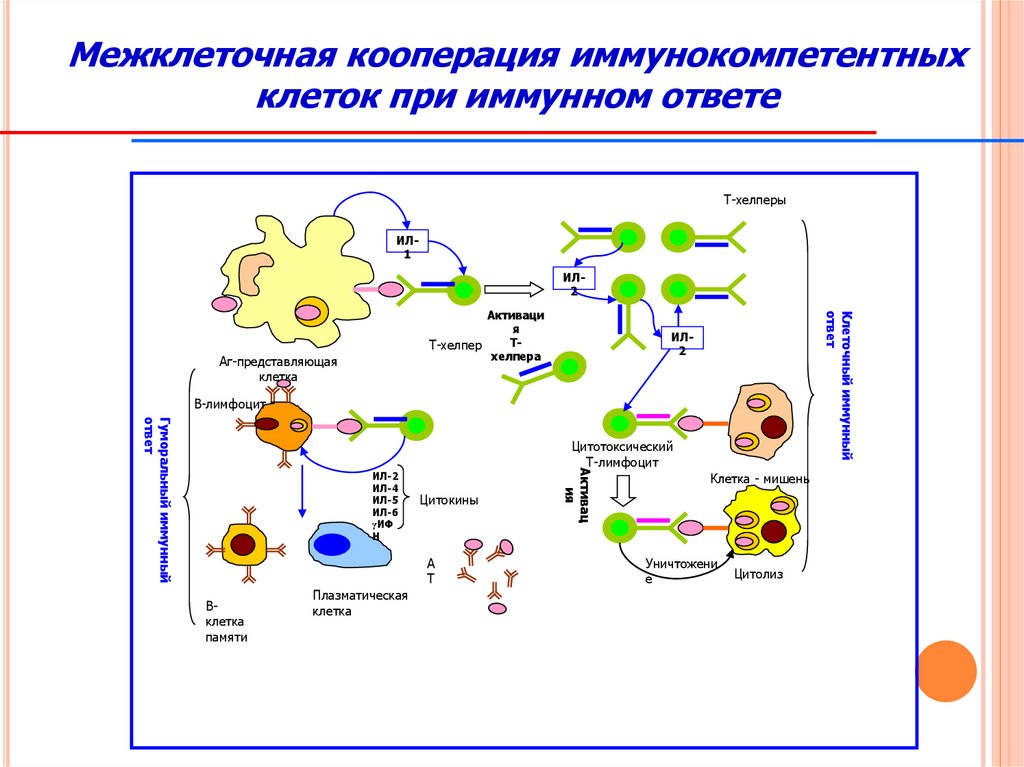
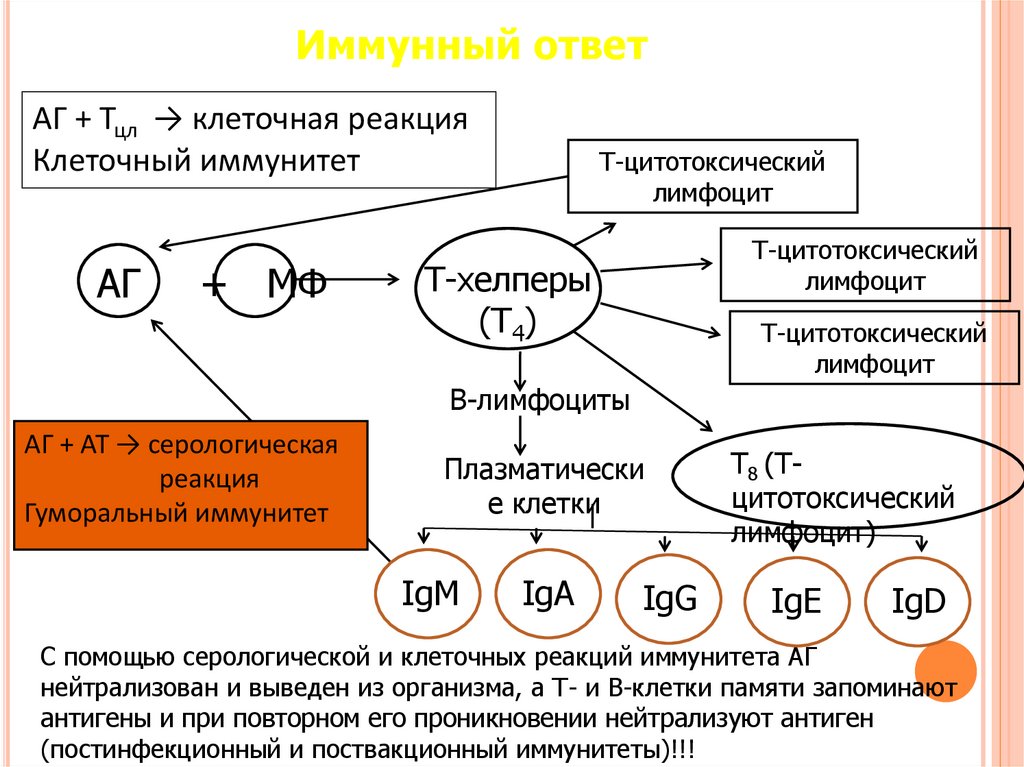






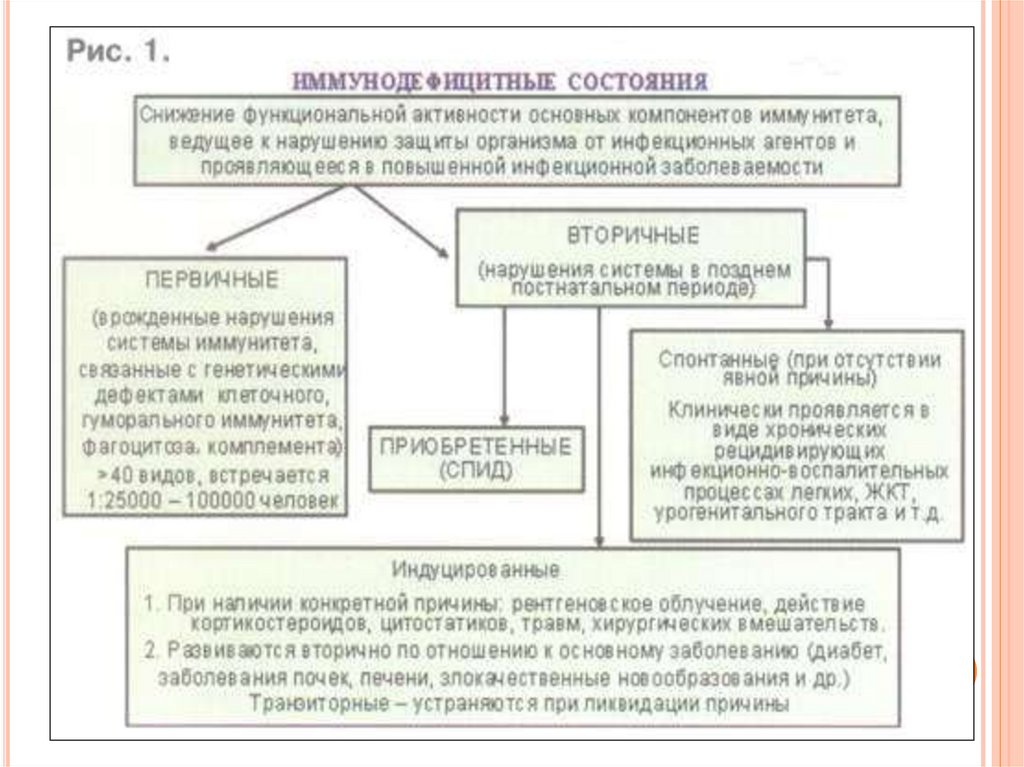











 Медицина
Медицина Биология
Биология