Похожие презентации:
Галогены и их соединения в ОВР
1.
ГАЛОГЕНЫ И ИХСОЕДИНЕНИЯ в ОВР
11 класс
2.
3.
1. Простые вещества (F2 , Cl2 , Br2 , I2)• Хлор – сильный
окислитель,
окисляет металлы,
неметаллы и
другие вещества,
превращаясь в
устойчивый анион
Cl(-) :
4.
1. Простые вещества (F2 , Cl2 , Br2 , I2)• Фтор –
сильнейший
окислитель.
5.
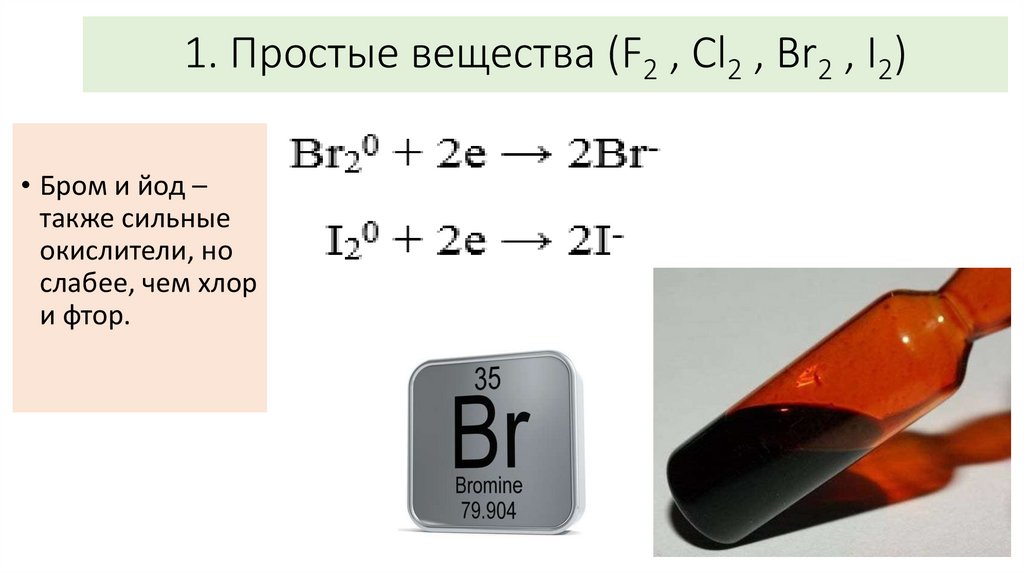
1. Простые вещества (F2 , Cl2 , Br2 , I2)• Бром и йод –
также сильные
окислители, но
слабее, чем хлор
и фтор.
6.
1. Простые вещества (F2 , Cl2 , Br2 , I2)• Йод быть и
восстановителем
с более сильными
окислителями,
преимущественно
переходя в
степень
окисления +5:
7.
1. Простые вещества (F2 , Cl2 , Br2 , I2)• Йод быть и
восстановителем
с более сильными
окислителями,
преимущественно
переходя в
степень
окисления +5:
8.
9.
10.
11.
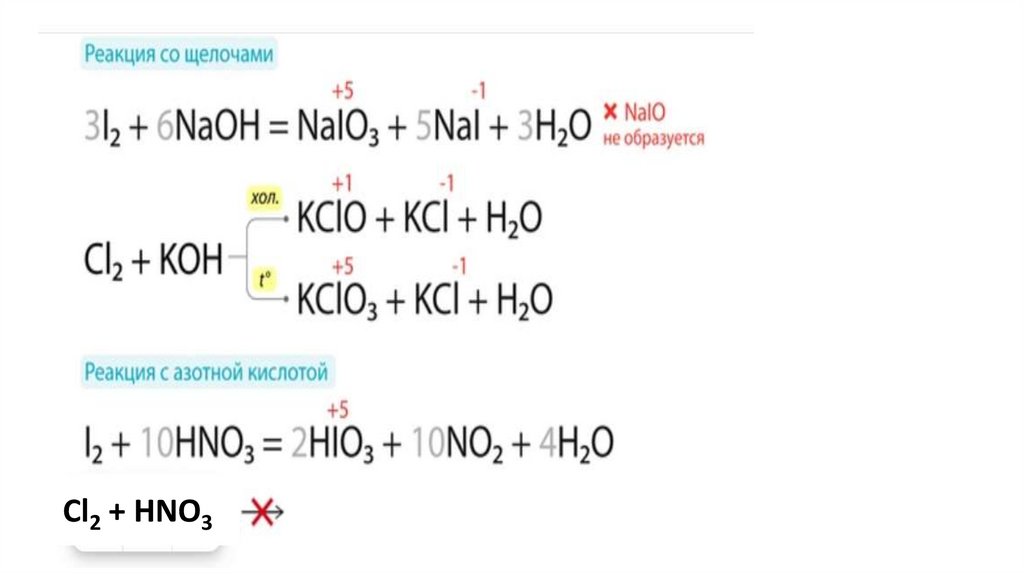
Cl2 + HNO3C12.
13.
2. Галогеноводороды (HCl, HBr, HI)• HCl
проявляет
свойства
восстановителя
за счет Cl(-) :
14.
2. Галогеноводороды (HCl, HBr, HI)• HBr и HI
• Br(-) и I(-) - более
сильные
восстановители, чем
Cl(-). Помимо
взаимодействия с
KMnO4 , MnO2 ,
K2Cr2O7 и другими
окислителями,
бромоводород и
иодоводород
окисляются серной
кислотой
15.
3. Кислородсодержащие соединения на примерехлора
• Все
кислородсодержащие
соединения являются
сильными
окислителями,
переходя в степень
окисления (-1):














 Химия
Химия








