Похожие презентации:
Оксиды
1.
2Х3недели=6
уроков
2Х5 недель=10 уроков
3-4 уроков
2.
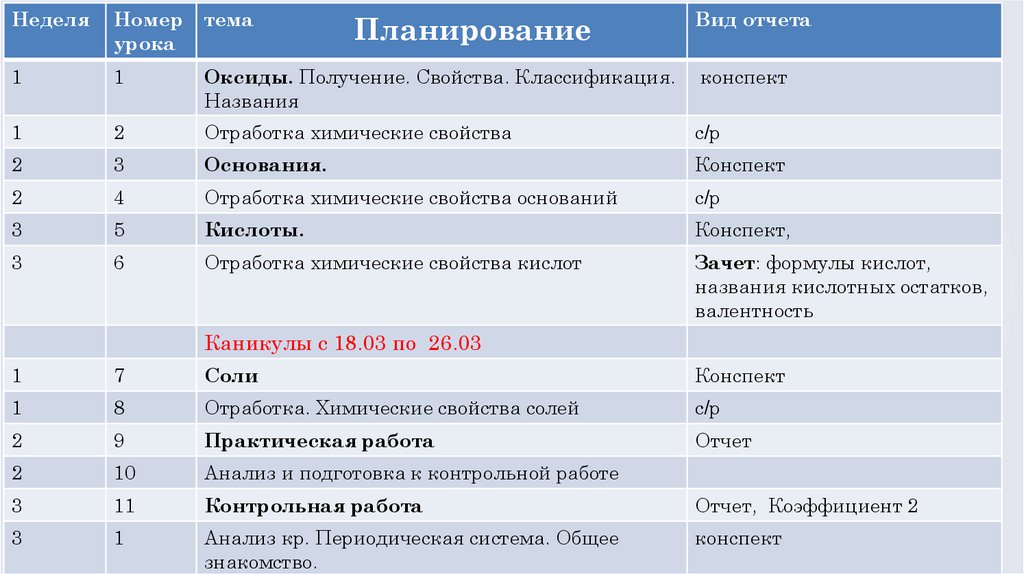
НеделяНомер
урока
тема
1
1
Оксиды. Получение. Свойства. Классификация.
Названия
конспект
1
2
Отработка химические свойства
с/р
2
3
Основания.
Конспект
2
4
Отработка химические свойства оснований
с/р
3
5
Кислоты.
Конспект,
3
6
Отработка химические свойства кислот
Зачет: формулы кислот,
названия кислотных остатков,
валентность
Планирование
Вид отчета
Каникулы с 18.03 по 26.03
1
7
Соли
Конспект
1
8
Отработка. Химические свойства солей
с/р
2
9
Практическая работа
Отчет
2
10
Анализ и подготовка к контрольной работе
3
11
Контрольная работа
Отчет, Коэффициент 2
3
1
Анализ кр. Периодическая система. Общее
знакомство.
конспект
3.
Цель:• Знать что такое оксид и классификацию
оксидов
• Уметь различать типы оксидов
Отработка умений
• Составлять формулу по валентности
• Определять валентность неизвестного
элемента в бинарном соединении
4.
Оксиды — это сложные вещества,состоящие из двух химических
элементов, один из которых кислород
в степени окисления –2.
5.
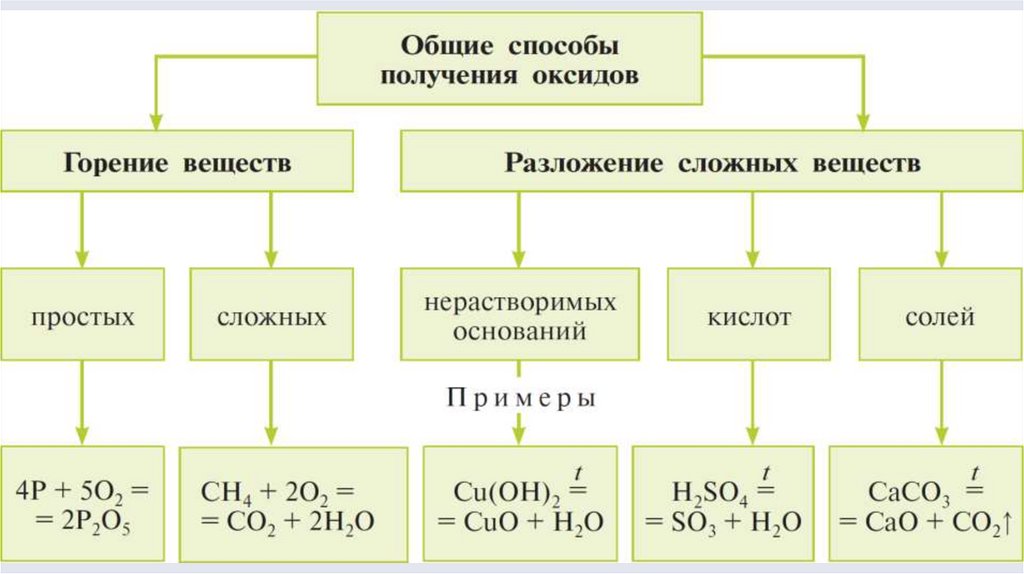
1. Получение оксидовПростое вещество + О2 = оксид
Соединения
Горения
Окисления
Экзотермическая
Запишите реакции получения оксидов,
укажите тип реакции
• оксида кальция
6.
2. Получение оксидовСложное органическое вещество
+ О2 = СО2 + Н2О
Запишите реакцию горения метана
7.
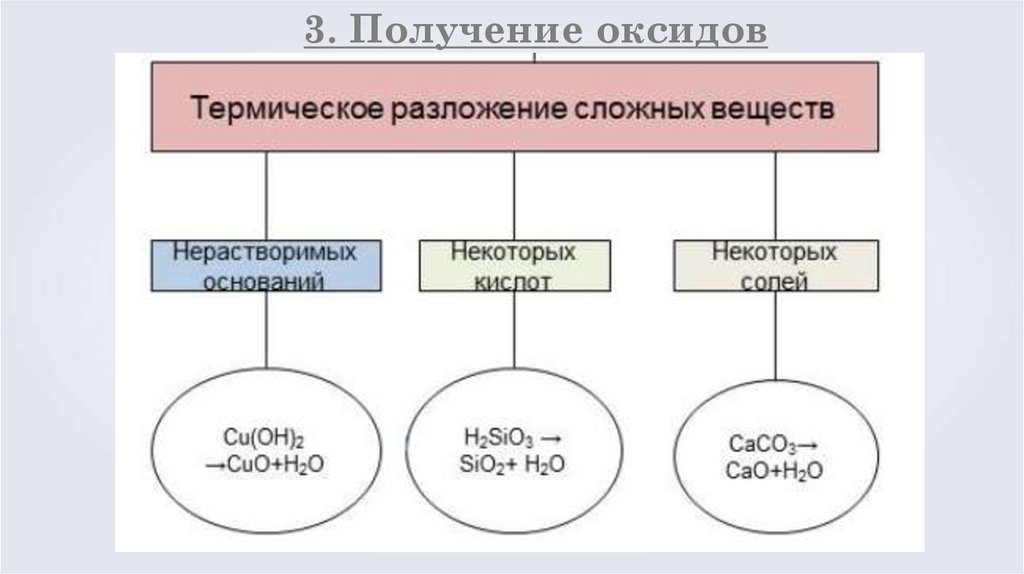
3. Получение оксидов8.
9.
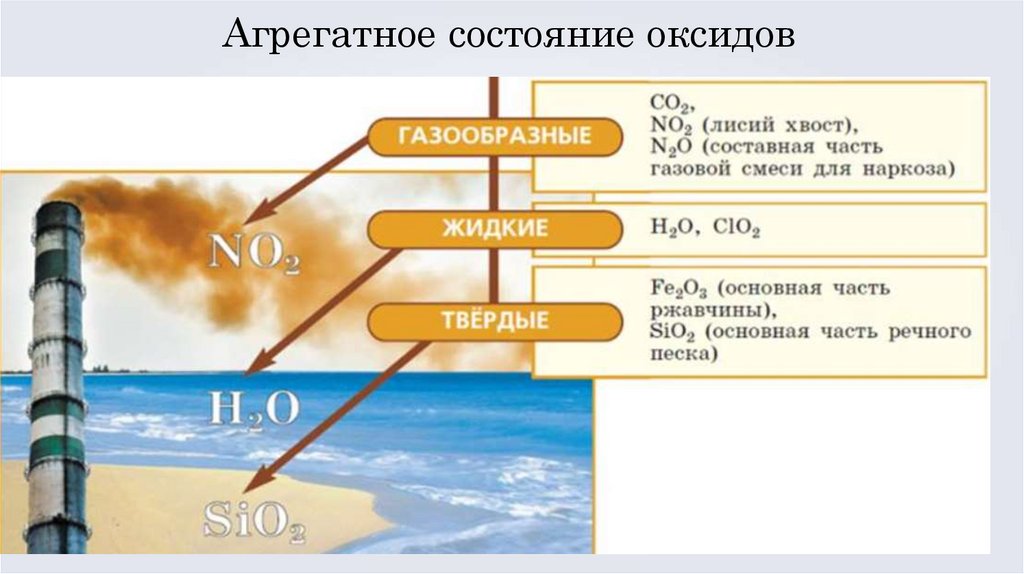
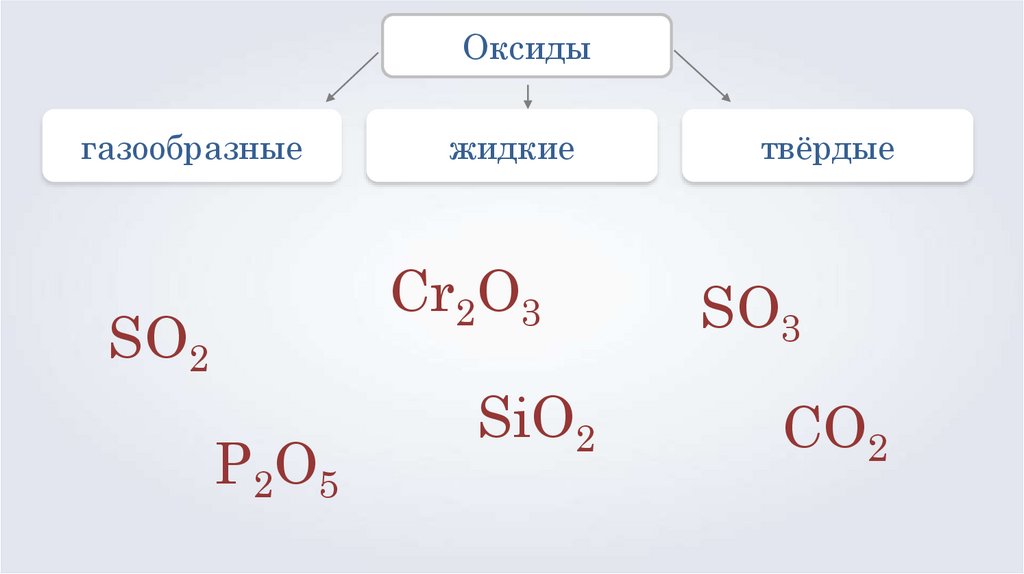
Агрегатное состояние оксидов10.
Оксидыгазообразные
жидкие
Cr2O3
SO2
P2O5
SiO2
твёрдые
SO3
CO2
11.
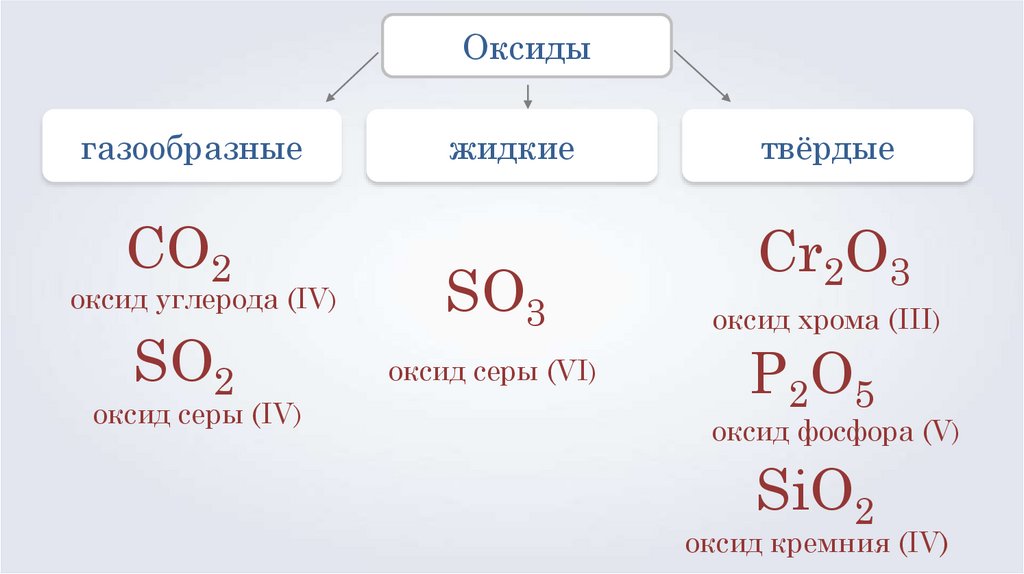
Оксидыгазообразные
CO2
оксид углерода (IV)
SO2
оксид серы (IV)
жидкие
SO3
оксид серы (VI)
твёрдые
Cr2O3
оксид хрома (III)
P2O5
оксид фосфора (V)
SiO2
оксид кремния (IV)
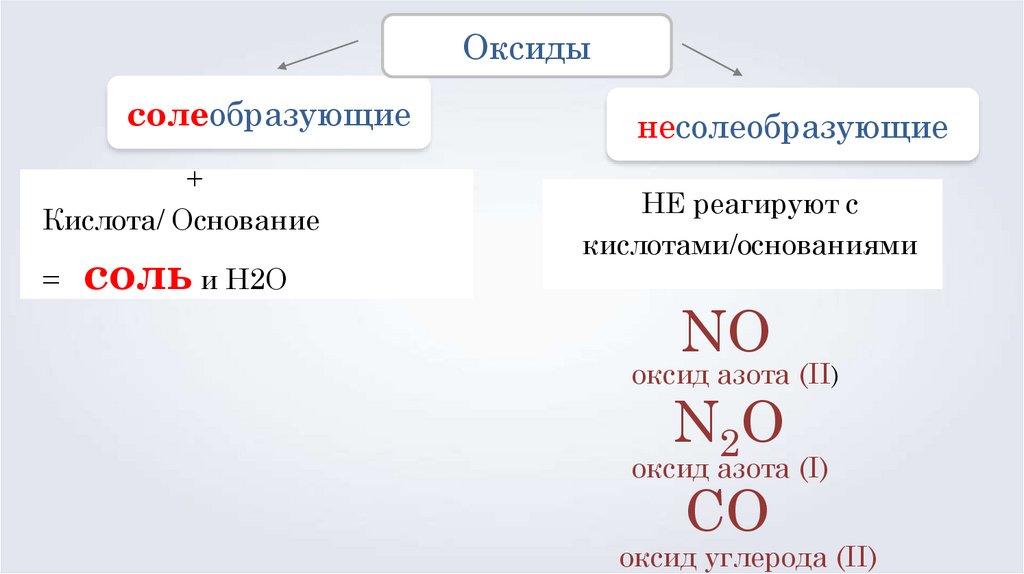
12.
Оксидысолеобразующие
+
Кислота/ Основание
=
соль и Н2О
несолеобразующие
НЕ реагируют с
кислотами/основаниями
NO
оксид азота (II)
N2O
оксид азота (I)
CO
оксид углерода (II)
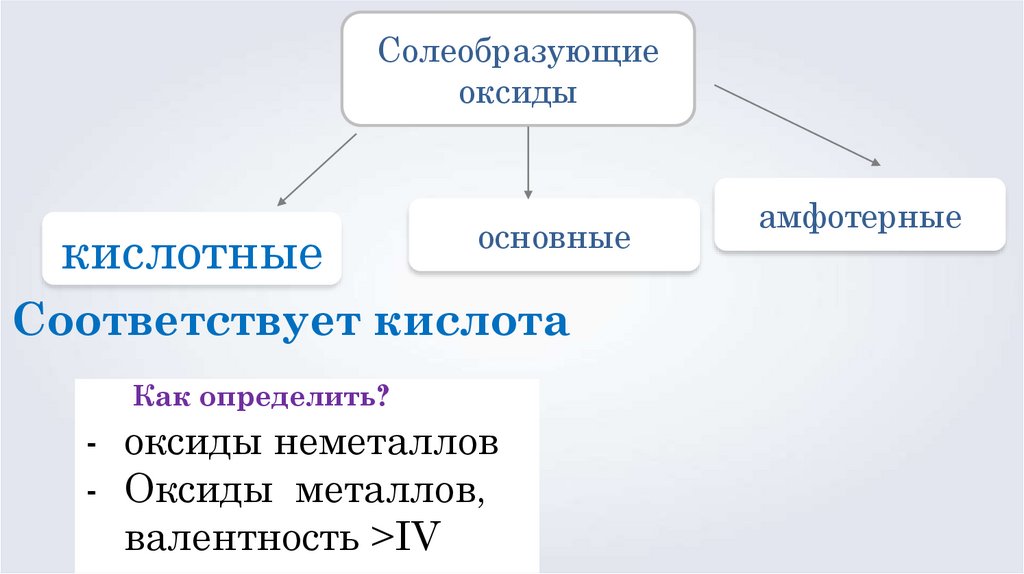
13.
Солеобразующиеоксиды
кислотные
основные
Соответствует кислота
Как определить?
- оксиды неметаллов
- Оксиды металлов,
валентность >IV
амфотерные
14.
Найти кислотный оксид1. AI2O3
2. CO2
3. CI2O7
4. MgO
5. CaO
6. N2O5
Алгоритм
1.Смотрю на первый ХЭ :Нем/Ме
-Если Неметалл –кислотный
-Если МЕ, определяю его валентность
Если валентность >IV – кислотный окcид
- оксиды неметаллов
- Оксиды металлов,
валентность >IV
15.
Кислотные оксиды - кислотаCO2 оксид углерода (IV) — H2CO3 угольная кислота
SiO2 оксид кремния (IV) — H2SiO3 кремниевая кислота
SO3
оксид серы (VI)
—
H2SO4 серная кислота
N2O3 оксид азота (III) — HNO2 азотистая кислота
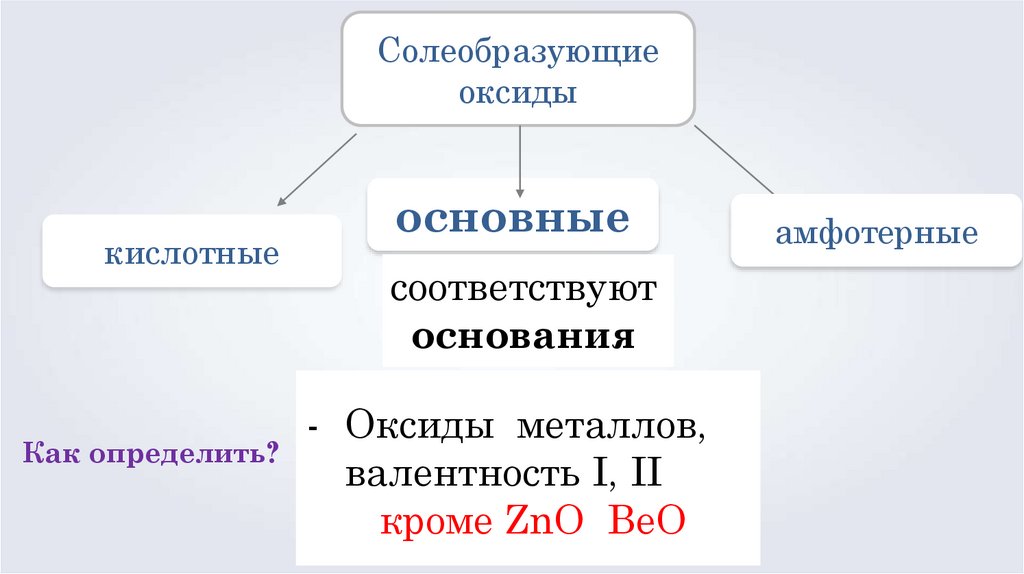
16.
Солеобразующиеоксиды
кислотные
основные
соответствуют
основания
- Оксиды металлов,
Как определить?
валентность I, II
кроме ZnO BeO
амфотерные
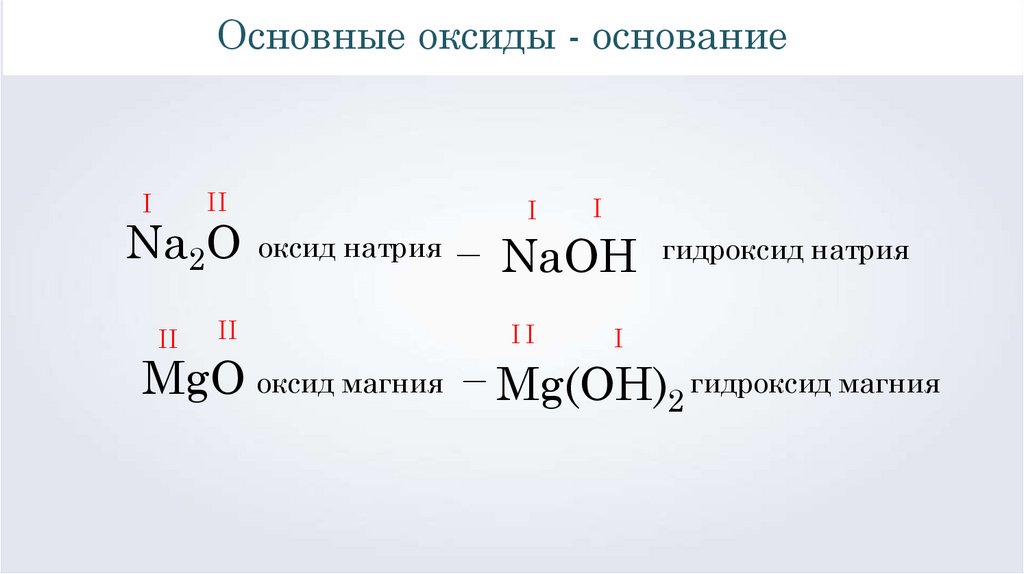
17.
Основные оксиды - основаниеI
II
I
II
II
I
Na2O оксид натрия — NaOH гидроксид натрия
II
I
MgO оксид магния — Mg(OH)2 гидроксид магния
18.
Найти основный оксид1. AI2O3
2. CO2
3. CI2O7
4. MgO
5. CaO
6. ZnO
Алгоритм
1.Смотрю на первый ХЭ :Нем/Ме
-Если Неметалл –кислотный
-Если МЕ, определяю его валентность
Если валентность = I, II – основный окcид
Кроме ZnO BeO
- Оксиды металлов,
валентность I, II
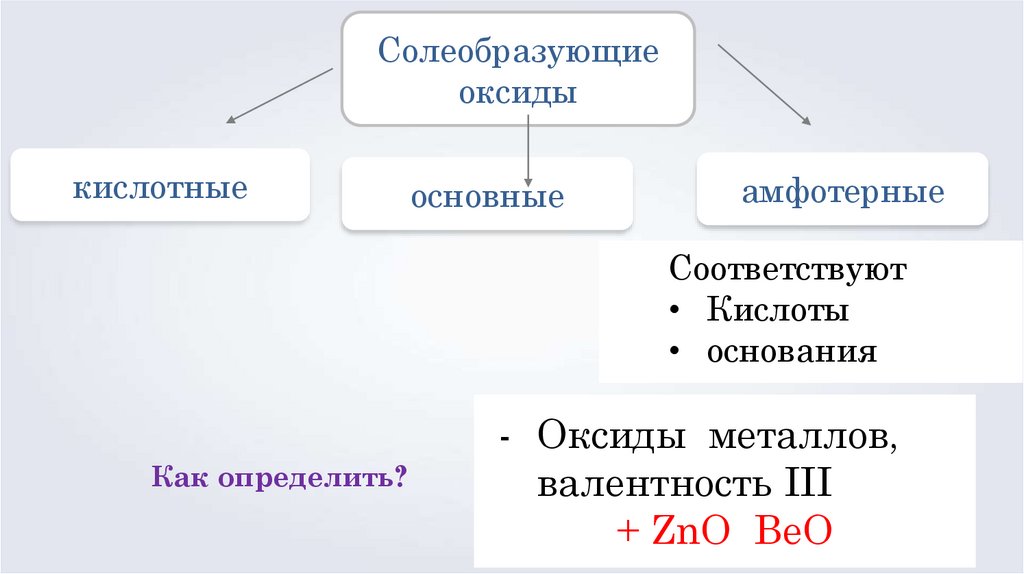
19.
Солеобразующиеоксиды
кислотные
основные
амфотерные
Соответствуют
• Кислоты
• основания
Как определить?
- Оксиды металлов,
валентность III
+ ZnO BeO
20.
Найти амфотерный оксид1. AI2O3
2. CO2
3. CI2O7
4. MgO
5. CaO
6. ZnO
Алгоритм
1.Смотрю на первый ХЭ :Нем/Ме
-Если Неметалл –кислотный
-Если МЕ, определяю его валентность
Если валентность = III –амфотерный окcид
+ ZnO BeO
- Оксиды металлов,
валентность III
21.
Цель:Что такое оксиды
Различать кислотные оксиды от основных
Выучить формулы кислот
Продолжение умений:
• Составлять формулу по валентности
• Определять валентность неизвестного
элемента в бинарном соединении
22.
Цель:• Знать что такое оксид и классификацию
оксидов
• Уметь различать типы оксидов
Отработка умений
• Составлять формулу по валентности
• Определять валентность неизвестного
элемента в бинарном соединении
23.
Определить характер оксида1.FeO
2.Fe2O3
3.MnO
4.MnO3
5.СrO
6.Cr2O3
7.CrO3
1.Смотрю на первый ХЭ – это МЕ
2.Определяю его валентность: 2
3.Правило если Ме валентность 1, 2
– основный оксид ( знать
исключения)
24.
Записать формулу оксидов и определить характер1. Оксид кремния
2. Оксид серы (IV)
3. Оксид серы(VI)
4. Оксид цинка
5. Оксид бария
6. Оксид железа ( II)
7. Оксид железа (Ш)
8. Оксид азота (II)
9. Оксид азота (Ш)
10. Оксид азота (V)
11. Оксид лития
12. Оксид Алюминия
13. Оксид углерода (II)
14. Оксид углерода (IV)
Алгоритм
1. Записываем символы элементов
2. Записываем валентность «О»=II
3.Валентность Ме = номеру
группы для А п/гр для Б п/гр = II
*Валентность неметаллов может
быть разной)
4. Находим НОК
5. Находим индекс: делим НОК на
валентность
25.
ДЗ страница 136 все тестовые заданияКонспект учить наизусть
26.
Химические свойства оксидовКислотный оксид + вода= кислота
Основный оксид + вода = основание
Кислотный оксид + Основание= соль и вода
Основный оксид + кислота= соль и вода
Кислотный оксид + основный оксид= соль
Сu O… + H2SO4 → CuSO4 + H2O;
Кислота
соль
вода
Валентность кислотного остатка определяется числом
атомов водорода в кислоте
27.
СаО28.
Ср включает 3 элемента1. Выбрать формулу оксида, основания, кислоты, соли.
Применить классификацию.
1. Дать название оксиду (установить валентность элемента)
гидроксиду, соли (знать названия кислотных остатков)
2. Написать уравнения реакции согласно схеме
(составить формулы продуктов, дать название, указать тип
реакции, уравнять)
Зачет «кислоты» ( по 3 кислоты на вариант)
1. Знать формулы кислот и название
2. Названия кислотных остатков
3. Валентность кислотных остатков

















 Химия
Химия








