Похожие презентации:
Коллоид системаларнинг тайёрлаш ва тозалаш усуллари. 5 - маъруза
1. Ўзбекистон Республикаси Олий ва Ўрта махсус таълим вазирлиги
ТОШКЕНТ КИМЁ ТЕХНОЛОГИЯ ИНСТИТУТИ«Ноорганик, аналитик, физикавий ва коллоид кимё
кафедраси»
Маърузачи:
Доцент - Х.С. Талипова
Тошкент - 2022
2.
КОЛЛОИД СИСТЕМАЛАРНИНГТАЙЁРЛАШ ВА ТОЗАЛАШ УСУЛЛАРИ
5 - маъруза
РЕЖА:
Коллоид системалар олишнинг
диспергация усули.
Физикавий ва кимёвий конденсация
усуллари.
Коллоид эритмаларни тозалаш йўллари.
3.
TAYANCH SO‘Z VA IBORALARDispergatsiya –
yirik zarrachalarni maydalash.
Kondensatsiya – kichik zarrachalarni yiriklashtirish.
Peptizatsiya – yangi tushgan cho‘kmani qaytadan kolloid eritma xolatiga
o‘tkazish.
Fizik kondensatsiya – dispersion muxitga qattiq jism bug‘ini yuborib kolloid
eritma xosil qilish.
Kimyoviy kondensatsiya – kimyoviy reaksiyalar yordamida kolloid eritmalar
olish.
Stabilizator – zarracha sirtiga adsorbsiyalanib, ularning turg‘unligini oshiruvchi
modda.
Dializ – kolloid eritmalarni yarim o‘tkazgich membrana yordamida tozalash.
Elektrodializ – dializni elektr maydonida o‘tkazish.
Ultrafiltratsiya – dispers sistemalarni bosim ostida tozalash.
Ultratsentrafuga – kolloid eritmalarni markazdan qochma kuch yordamida
tozalash(ajratib olish).
4.
Коллоид системаларнинг олиниш усуллариДисперс системаларни заррачаларининг ўлчамига
қараб синфларга ажратилганда маълум бўлдики, коллоид
системалар дағал дисперс системалар билан чин эритмалар
орасидаги оралиқ ҳолатни эгаллайди. Уларда энг юқори
майдаланиш даражасига эришилади. Бу системаларда
“фаза”, “гетерогенлик” терминлари сақланади.
Коллоид эритмалар ҳосил қилиш усуллари бир-бирига
қарама-қарши икки принципга асосланади:
•йирикроқ заррачаларни майдалаш (дисперслаш)
•молекула ва ионлардан йирикроқ заррачалар ҳосил
қилиш (конденсация)
5.
чинэритмалар
r< 10-9 м
a< 1 нм
Конденсация усулида
Коллоид дисперс системалар
(золлар)
r= 10-7 - 10-9 м
a=1-100 нм
Диспергация
усулида
Дағал дисперс системалар
r= 10-4 - 10-7 м
a>100 нм
6.
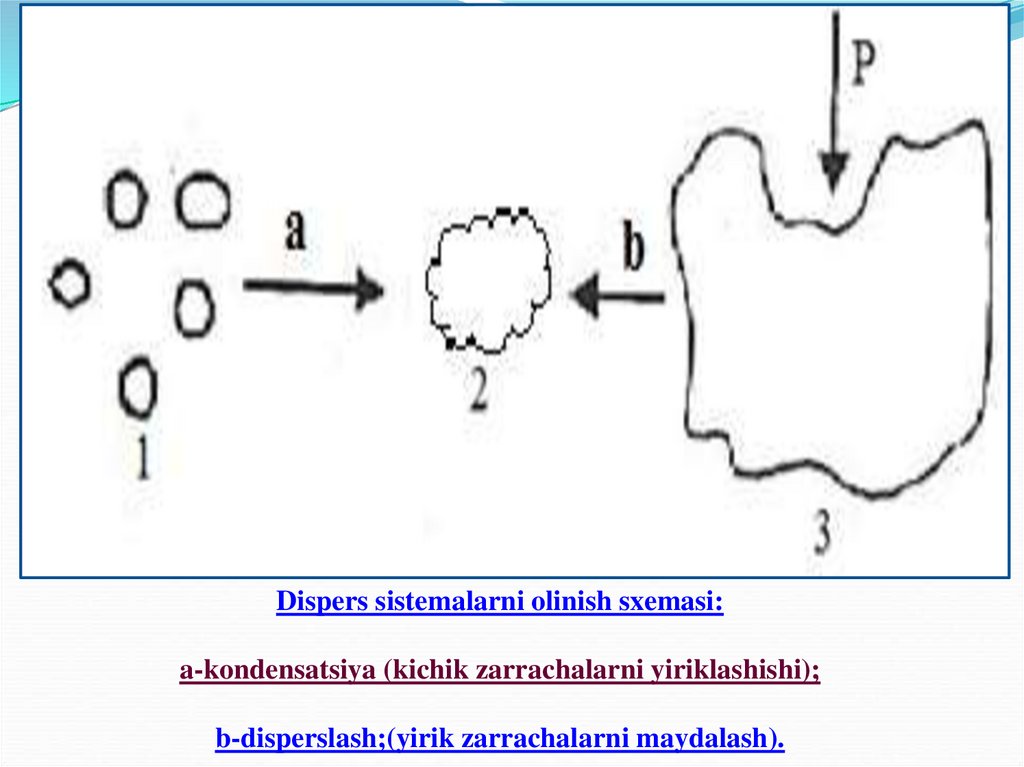
Dispers sistemalarni olinish sxemasi:a-kondensatsiya (kichik zarrachalarni yiriklashishi);
b-disperslash;(yirik zarrachalarni maydalash).
7.
Коллоид эритмаларда дисперс фазазаррачалари ўлчами 1нм – 100 нм гача
(10-7-10-9м) бўлиши керак.
Бундай коллоид эритмалар олишнинг иккита
муҳим шарти бор:
1. дисперс фаза дисперс муҳитда мумкин
қадар кам эрувчан бўлиши керак;
2. системада дисперс фаза ва дисперс
муҳитдан ташқари учинчи модда – яъни
стабилизатор бўлиши керак.
8.
Диспергация усулида коллоид эритмаолишнинг бир неча усуллари мавжуд:
1. Коллоид тегирмонлар ёки вибротегирмонлар ёрдамида майдалаш
2. Металларни электр токи ёрдамида
чанглатиш
3. Ультратовуш ёрдамида майдалаш
4. Пептизация
9.
1. Коллоид тегирмонлар ёрдамидамайдалашда:
тез-тез енгил зарбалар берилади
зарбалар бевосита эмас, балки суюқлик орқали берилади.
Коллоид эритмаси тайёрланадиган модда - муҳит ва
стабилизатор билан аралаштирилиб, тешик орқали
тегирмонга солинади. Ўққа ўрнатилган куракча ёрдамида
аралаштирилади. Куракча минутига 10.000 – 15.000 марта
айланади. Суюқлик ва қаттиқ модда заррачалари жуда тез
ҳаракатланади ва ҳаракатсиз тешикларга келиб урилади ва
майдаланилади.
Тайёр бўлган коллоид эритма пастки тешикдан қуйиб
олинади. Бу усулда бўёқ, олтингугурт, графит, кварц ва
бошқа
моддаларнинг
тайёрланади.
коллоид
эритмалари
10.
Коллоид тегирмон11.
Obtaining disperse systemsDispersion methods
-grinding large sample
disperse particles sizes;
substance
to
11
12.
Colloid millsAllow to reach more subtle grinding
12
13.
Диспергация жараённини осонлаштириш учун жисм хўлланиб, қўшимчамоддалар иштирокида кукун қилиб майдаланади. Қўшимча модда сифатида
ишлатиладиган хар хил тузлар (NaCI, CaCI2, MgCI2, AICI3, Na2CO3, Na2SiO3)
ишқорлар -NaOH, Ca(OH)2, совун ва баъзи сирт-фаол моддалар диспергация
жараёнини осонлаштириш билан бирга, олинаётган коллоид системанинг
барқарорлигини таъминлашда стабилизатор вазифасини ўтайди.
Академик Ребиндер таълимотига кўра қаттиқ жисмнинг кристаллик
панжарасида дефектлар (заиф ва дарз кетган жойлар) мавжуд бўлиб,
механик куч таъсирида микротирқишлар хосил қилади. Қўшимча моддалар эса
дастлаб жисм юзасида ютилиб, сўнгра унинг микротирқишларига киради.
Натижада, қарама-қарши турган адсорбцион қатламлар орасида электростатик
итарилиш
кучи
энергиясини
осонлаштиради
таъсирида
ёрувчи
камайтириб,
эффект
қаттиқ
хосил
улар сирт
емирилишини
бўлиб,
жисмнинг
F S
бу ерда:
F - сиртнинг эркин энергияси,
- сирт таранглик коэффициенти,
S - фазалараро сирт катталигининг ўзгариши.
Бу усулда “асл металл”ларнинг золлари олинади.
14.
Расм.Жисм мустаҳкамлигининг адсорбцион равишда камайиши.
(Ребиндер эффекти)
Механик диспергация жараёнида қаттиқ жисм
мустаҳкамлигини қўшимча моддалар ёрдамида
камайиши
“Ребиндер
эффекти”
ёки
мустаҳкамликнинг
адсорбцион
камайиши
дейилади.
15.
2. Металларни электр токи ёрдамида чанглатиш(Вольта ёйи ёрдамида)
+
_
Бу усулни 1898 йилда Бредиг таклиф этган. Коллоид эритмаси олиниши керак бўлган
металлдан ясалган сим дисперсион муҳитга туширилади.
Муҳитга озгина ишқор қўшиб қўйилади. Бу усулда нодир металларнинг золлари
олинади.
16.
3. Ультратовуш ёрдамида чанглатишКоллоид эритма олиш учун ультратовуш тўлқини
майдонига бир-бири билан аралашмайдиган иккита
суюқлик солинган идиш қўйилади. Эмульсиялар шу усулда
олинади. Бу усул билан Ag, Pd, Bi ларнинг коллоид эритмалари ҳосил
қилинади.
4. Пептизация
Золни коагуляция маҳсулотини қайтадан коллоид эритмага
ўтказиш – пептизация дейилади. Уни амалга ошириш учун янги
чўккан аморф чўкмага бирор электролит қўшиб, эритувчи билан
аралаштирилади. Бу қўшилган электролит пептизатор дейилади.
Пептизация тезлигига – электролит концентрацияси,
чўкма ҳолати ва миқдори, ҳарорат, аралаштириш тезлиги,
рН, ультратовуш, радиактив нурлар ва ҳ.к. таъсир этади.
17.
1. Агар заррача сиртига пептизаторнинг ўзи ютилиб, коллоид эритма ҳосилбўлса – бевосита пептизация дейилади.
FeCl3 3NH 4OH Fe(OH )3 3NH 4Cl
FeCl3
- пептизатор
m Fe(OH ) n Fe 3(n x)Cl 3xCl
3
3
x
3
2. Агар заррача сиртига пептизаторнинг ўзи эмас, унинг чўкма билан
ҳосил қилган оралиқ маҳсулоти шимилса – билвосита пептизация
дейилади.
Fe(OH ) 3 HCl FeOCl 2 H 2O
аморф чўкма
FeOCl
- пептизатор
m Fe(OH ) n FeO (n x)Cl xCl
3
x
18.
Пептизация механизмиПептизация коагуляцияга тескари жараёндир. Унда
чўкмага тушган заррачалар дезагрегацияга учраб, қайтадан
алоҳида коллоид заррачаларга ўтиши руй беради.
пептизатор
19.
!!!Маълумки, қаттиқ жисм ёки суюқликни коллоидўлчамигача (1-100 нм) майдалаш жараёни иш ёки энергия
сарфлашни талаб этади. Бу иш
А К S
формула билан ифодаланади. Формуладаги
К - дисперация усулига ва майдаланаётган модда
табиатига боғлиқ бўлган катталик;
S - янги ҳосил бўлаётган юза.
Одатда
моддалар
юқори
дисперслик
даражасигача
майдаланганда кўп ғаройиб хоссаларга эга бўлиб қоладилар.
Масалан, бўёқлар чиройли жилвага, ярқироқлик, барқарорлик,
енгил қопланувчанлик хоссаларига эришадилар.
Катализаторлар кимёвий реакцияларда юқори активликка
эришадилар, озиқ-овқат махсулотларини таъм-мазаси яхшиланади,
крахмал ва оқсил моддаларнинг сувда эрувчанлиги ортади ва х.к.
20.
Конденсация усуллариМолекуляр ёки ион ўлчамидаги заррачаларни
Ван-дер-Ваальс тортилиш кучи хисобига
коллоид
заррача
ўлчамигача
йириклаштириш усули конденсацион усули
дейилади.
21.
Физикавий конденсация1. Дисперсион муҳитга қаттиқ жисм
буғини юбориш
(З.С. Рогинский ва А.И. Шальников
усули)
2. Эритувчини алмаштириш усули
Кимёвий конденсация
Бу
усул - бирор кимёвий
реакция натижасида қийин
эрийдиган
чўкмалар
ҳосил
бўлишига
асосланган(оксидланиш, қайтарилиш, гидролиз, алмашиниш
ва б.)
22.
З.С. Рогинский ва А.И. Шальников асбоби23.
Кимёвий конденсация усулларининг асоси шундаки:1. Реакция учун олинган дастлабки моддалар суюлтирилган
ҳолда ишлатилиши керак, чунки бу шароитда ҳосил
бўладиган маҳсулотнинг кристалл заррачаларининг ўсиш
тезлиги катта бўлмайди. Шу сабабли системанинг
седиментацион барқарорлиги (яъни, дисперс фаза
заррачалари чўкмайди) таъминланади.
2. Реагентлардан бири юқори концентрацияда олиниши ҳам
мумкин, бу шароитда ҳосил бўлган маҳсулотнинг
кристаллари сиртида қўш электр қават ҳосил бўлиб,
улар
системанинг
агрегатив
барқарорлигини
таъминлайди,
натижада
заррачалар
йириклашиб
кетмайди.
3. Стабилизатор
эса
ҳар
иккала
барқарорликни
таъминлайди.
24.
1. Қайтарилиш усули -дисперс фаза чин эритмада бирор
қайтарувчи ёрдамида қайтарилади. Мисол:
2НAuCl4 3H 2O2 2 Au 8HCl 3O2
Бу тенгламаларда золь
тарзида ҳосил бўлган
модда
квадрат
қавсларга олинади.
AgO H 2 Ag H 2O
Қайтарувчи сифатида
ишлатилади.
–
танин,
гидразин,
алкалоид
кабилар
2 AgNO3 K 2CO3 Ag2O 2KNO3 CO2
3 Ag2O С76 H 52O46 6 Ag C76 H 52O49
танин
флобафен
25.
Chemical condensation methodsMethods based on the formation of poorly soluble compounds by chemical
reactions.
1. Reduction reaction.
Recovery of sodium aurate by formaldehyde.
2NaAuO2 + 3HCOH + Na2CO3 = 2Au + 3HCOONa +NaHCO3 + H2O
Micelle structure :
m Au nAuO ( n x )Na xNa
2
x
25
26.
2. Оксидланиш усули. Молекуляр эритмани оксидлашйўли билан коллоид эритма олинади
2H 2 S O2 2 S 2H 2O
S билан бир қаторда Н2S5О6 пентатион кислота ҳам ҳосил
бўлиб, стабилизатор вазифасини бажаради
Н2S5О6 2Н+ + S5O62-
m S nS O 2(n x) H 2 xH
5
2
6
2 x
27.
3. Алмашиниш усули.Алмашиниш реакцияси коллоид эритма олишда
кимёвий конденсациянинг кенг таркалган усулидир:
Ba ( NO3 ) 2 K 2 SO4 BaSO4 2KNO3
Ba (NO3 )2
ортиқча олинса,
m BaSO nBa 2(n x) NO 2 xNO
2
4
2 x
3
3
ортиқча олинса
K 2 SO4
m BaSO nSO 2(n x)K 2xK
4
2
4
2 x
Гидролиз реакцияси асосида золни Крекке ва Грем усуллари ёрдами билан
олинади.
28.
Exchange reactionObtaining of Prussian blue sol
3K4[Fe(CN)6] + 4FeCl3 Fe4[Fe(CN)6]3 + 12KCl
Micelle structure :
{[mFe4[Fe(CN)6]3·n[Fe(CN)6]4-]4n-·4 (n-х)K+}4x-·4xK+
{[m Fe4[Fe(CN)6]3·nFe3+] 3+·3(n-х)Сl-}3x+·3xCl-
28
29.
AgNO3 + KCl→[AgCl] +KNO3KCl → K+ +
ClK+
K+
K+
ClCl-
K+
Cl-
K+
Cl-
K+ Cl-
[AgCl] Cl- K+
K+
Cl-
K+
Cl-
K+
K
K +
+
K+
K+
30.
Коллоид эритмаларни тозалашКоллоид эритмаларни кимёвий усулларда
олишда
келтирилган
мисоллардан
кўриниб
турибдики, системада золдан ташқари бошқа
аралашмалар ҳам (кислата, асос, тузлар) бўлади.
Албатта барқарор ҳолатда коллоид эритма
олиш учун бу эритмада маълум миқдорда
электролитлар ҳам бўлиши керак. Лекин, уларнинг
хоссаларини ўрганиш учун ортиқча электролитлардан тозалаш зарур. Бунинг учун -------диализ,
-электродиализ,
-ультрафильтрация каби усуллардан фойдаланилади.
31.
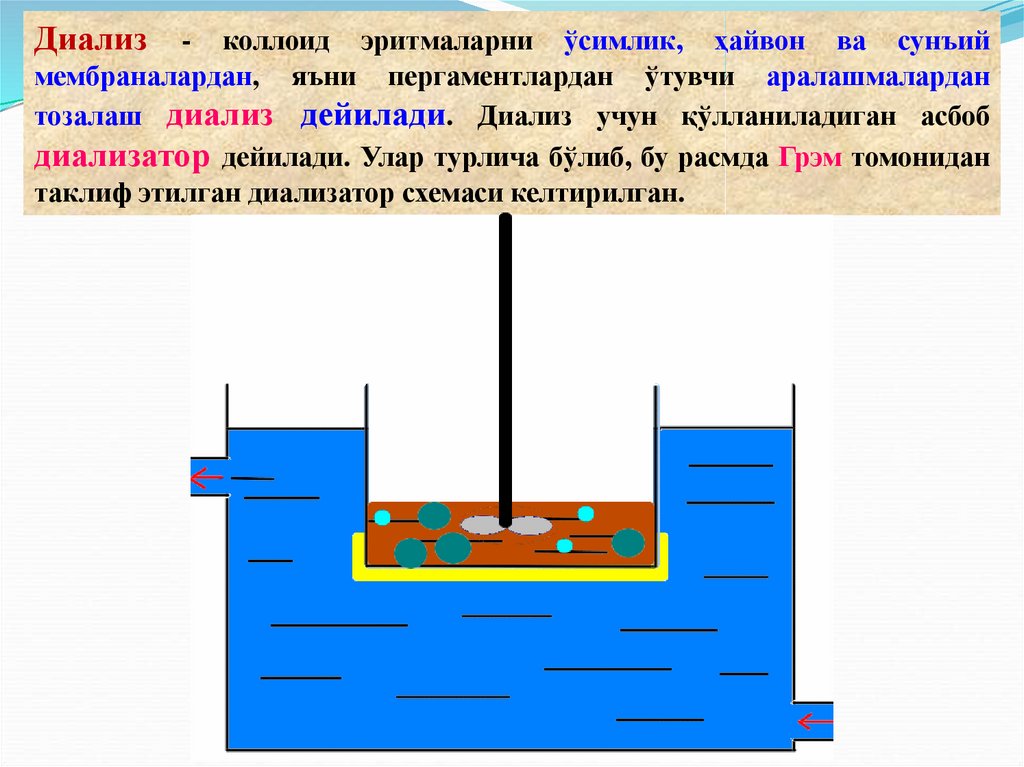
Диализ - коллоид эритмаларни ўсимлик, ҳайвон ва сунъиймембраналардан, яъни пергаментлардан ўтувчи аралашмалардан
тозалаш диализ дейилади. Диализ учун қўлланиладиган асбоб
диализатор дейилади. Улар турлича бўлиб, бу расмда Грэм томонидан
таклиф этилган диализатор схемаси келтирилган.
32.
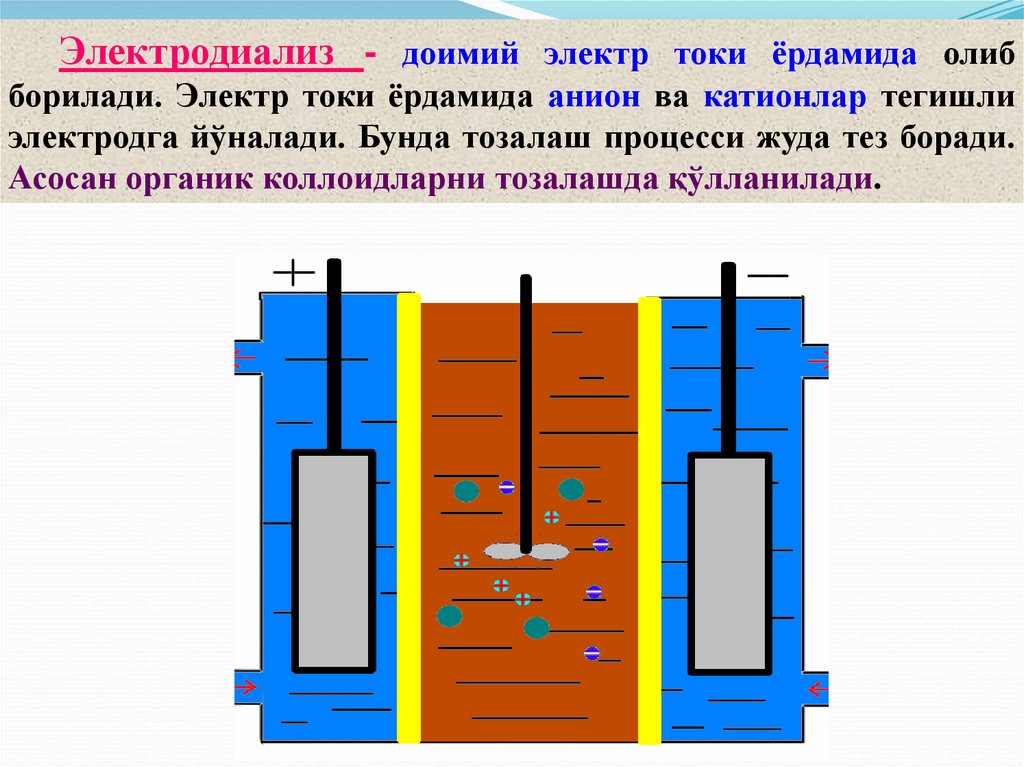
Электродиализ - доимий электр токи ёрдамида олибборилади. Электр токи ёрдамида анион ва катионлар тегишли
электродга йўналади. Бунда тозалаш процесси жуда тез боради.
Асосан органик коллоидларни тозалашда қўлланилади.
33.
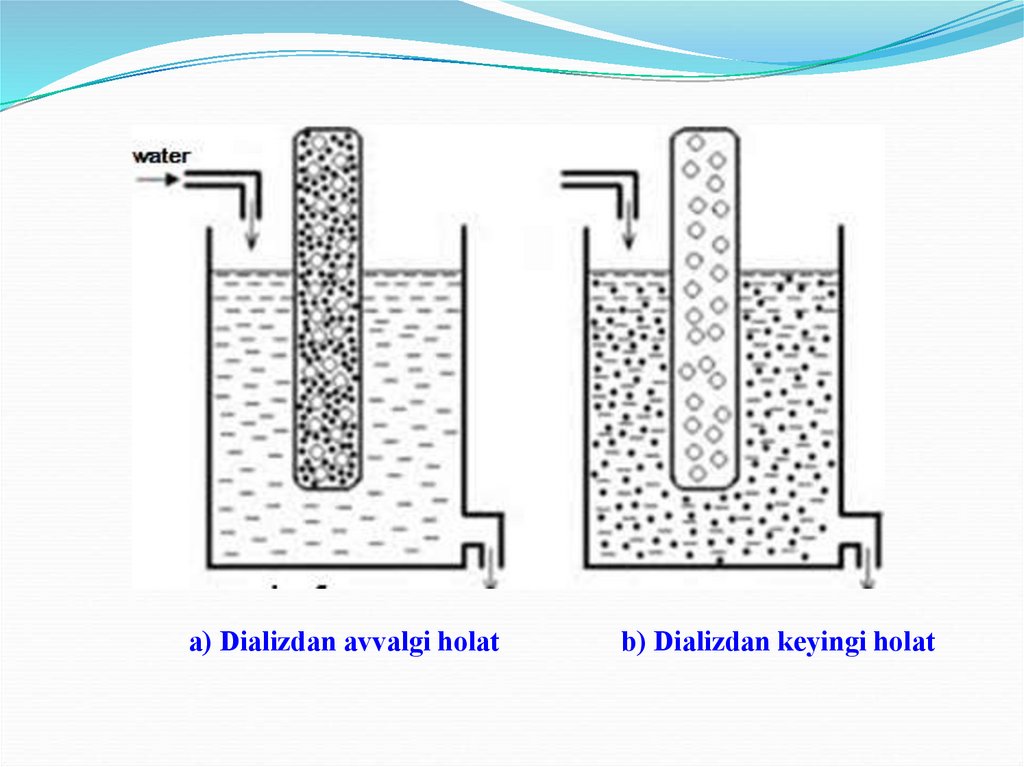
а) Diаlizdаn аvvаlgi holаtb) Diаlizdаn keyingi holаt
34.
Компенсацион диализ - бу усул Михаэлис ва Ронатомонидан таклиф этилган бўлиб, асосан биологик
суюқликларни тозалаш ва ўрганишда кенг
қўлланилади. Бу усулда диализаторда тоза эритувчи
ўрнига биологик суюқлик таркибидаги паст
молекуляр бирикманинг ҳар хил концентрацияли
эритмалари ишлатилади.
Ультрафилтрация - бу усул ҳам коллоид
эритмаларни тозалашнинг энг муҳим усулларидан
бўлиб, у дисперс фазани дисперс муҳитдан
ажратишга асосланган. Кўпинча вакуум остида
олиб борилади ва маҳсус мембраналардан
фойдаланилади. Юқори босимда ҳам олиб бориш
мумкин.
35.
Methods for cleaning of disperse systemsLow molecular weight impurities destroy colloidal systems.
Ultrafiltration - the electrodialysis under pressure
(hemodialysis).
35
36.
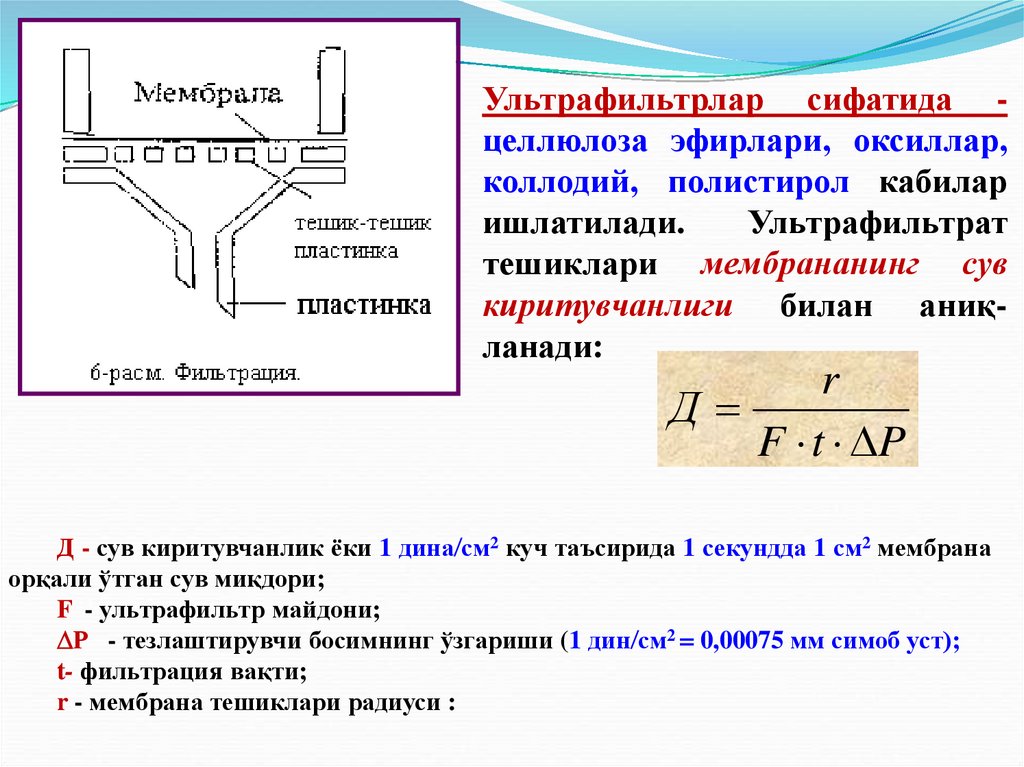
Ультрафильтрлар сифатида целлюлоза эфирлари, оксиллар,коллодий, полистирол кабилар
ишлатилади.
Ультрафильтрат
тешиклари мембрананинг сув
киритувчанлиги билан аниқланади:
r
Д
F t P
Д - сув киритувчанлик ёки 1 дина см2 куч таъсирида 1 секундда 1 см2 мембрана
орқали ўтган сув миқдори;
F - ультрафильтр майдони;
Р - тезлаштирувчи босимнинг ўзгариши (1 дин см2 0,00075 мм симоб уст);
t- фильтрация вақти;
r - мембрана тешиклари радиуси :
37.
мембрана тешикларирадиуси :
r
2
24D
бу ерда
- мембрана қалинлиги (микрометрларда ўлчанади)
- сув қовушоқлиги
- 1 см2 юзада сув билан тўлган ғоваклар ҳажми.
Тешиклар хажми
қўйидагича аниқланади:
бу ерда
Jn Jк
F d H 2O
Jn - нам мембрана оғирлиги
JК - қуруқ мембрана оғирлиги
d H 2 O - сувнинг зичлиги
F - фильтр майдони
38.
Ultratsentrifugalash. Kolloidlarni tozalashda va ularniturli fraksiyalarga ajratishda eng ko‘p ishlatiladigan usul –
ultratsentrifugalash usulidir. Kolloid eritmalarni tozalash uchun
sentrifugadan dastlab 1913 yilda A.V.Dumanskiy foydalandi.
Keyinchalik shved olimi Svedberg (va uning shogirdlari) 105-106g
ga yaqin tezlanish bilan ishlaydigan ultratsentrifugalar
yaratishga muvaffaq bo‘ldi. Zamonaviy ultratsentrifugalar
yordami bilan faqat gidrofob kolloid zarrachalarnigina emas,
balki oqsil va boshqa yuqori molekulyar moddalarni xam
cho‘kmaga tushirish mumkin bo‘ldi.
Zamonaviy ultratsentrifugalar murakkab qurilma bo’lib,
ularni markaziy rotorlari 20-60000 ayl/min tezlikdan oshadi.
Mаrkаzdаn qochmа kuch tа’siridа dispers sistemаlаr molekulа,
аtom, ionlаrdаn аjrаtilishi mumkin[1].
[1]
Slideplayer.com
39.
40.
МАЪРУЗА БЎЙИЧА ТАЯНЧ СЎЗ ВА ИБОРАЛАРДиспергация – йирик заррачаларни майдалаш.
Конденсация – кичик заррачаларни йириклаштириш.
Пептизация – чўкмани қайтадан коллоид эритма холатига ўтказиш.
Физик конденсация – дисперсион мухитга қаттиқ жисм буғини юбориб коллоид эритма олиш.
Кимёвий конденсация – кимёвий реакциялар ёрдамида коллоид эритмалар олиш.
Стабилизатор – заррача сиртига адсорбцияланиб, уларнинг турғунлигини оширувчи модда.
Диализ – коллоид эритмаларни ярим ўтказгич мембрана ёрдамида тозалаш.
Электродиализ – диализни электр майдонида ўтказиш.
Ультрафильтрация – дисперс системаларни босим остида тозалаш.
Ультрацентрафуга – коллоид эритмаларни марказдан қочма куч ёрдамида тозалаш.
ФОЙДАЛАНИЛГАН АДАБИЁТЛАР
К.С. Ахмедов, Х.Р. Рахимов. Коллоид химия. Т, 1992, 12-21 бетлар.
Ю.Т. Фролов. Курс коллоидной химии. М., 1982, с. 96-107.
С.С. Воюцкий. Курс коллоидной химии. М., 1976. с. 223-240.
Ҳ.Р. Рахмонбердиев, М.Н. Мавлонова, А.С. Сидиков, С.М.Турабжонов.
“Техника фанлари
бакалаврлари учун коллоид кимёдан услуби кўлланма”. (Коллоид системалар, уларнинг олиниши ва
тозалаш усуллари. Мицеллалар тузилиши. 1 қисм) Т, 1999, 8-14 бетлар.
Шукин Е.О, Перцов А.В, Амелина Е.А. “Коллоидная химия” - М. МГУ, 1982 - 352 с.
Евстратова К.И., Купина Н.А., Малахова Е.Е., Физическая и коллоидная химия. - М.,. Высшая
школа, 1990
41.
ЭЪТИБОРИНГИЗ УЧУНРАҲМАТ




































 Химия
Химия