Похожие презентации:
Дисперсные системы
1.
Дисперсныесистемы
2.
истинные растворыСмеси
веществ
дисперсные системы
3.
4.
Растворы- это гомогенные (однофазные)системы, состоящие из двух и более
компонентов
(составных
частей)
и
продуктов их взаимодействия.
5.
Дисперсныесистемы
–
гетерогенные (неоднородные) системы,
в которых одно вещество в виде очень
мелких
частиц
равномерно
распределено в объёме другого.
6.
Дисперсные системы состоят как минимумиз двух компонентов:
1. дисперсионной среды, которая играет роль
растворителя и, следовательно, является
непрерывной фазой;
2. дисперсной фазы, играющей роль растворённого
вещества.
7.
Дисперсная фаза - вещество, котороеприсутствует в дисперсной системе в
меньшем
количестве.
Дисперсионная среда - вещество,
которое
в
дисперсной
системе
находится в большем количестве.
Дисперсионная среда
Дисперсная фаза
8.
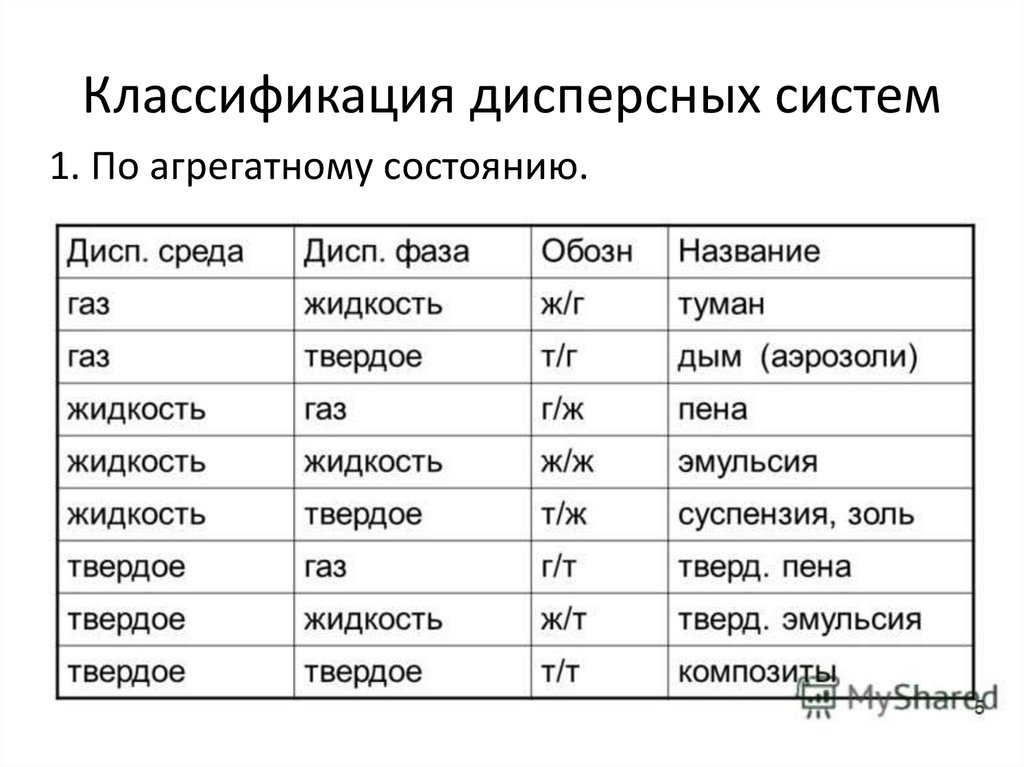
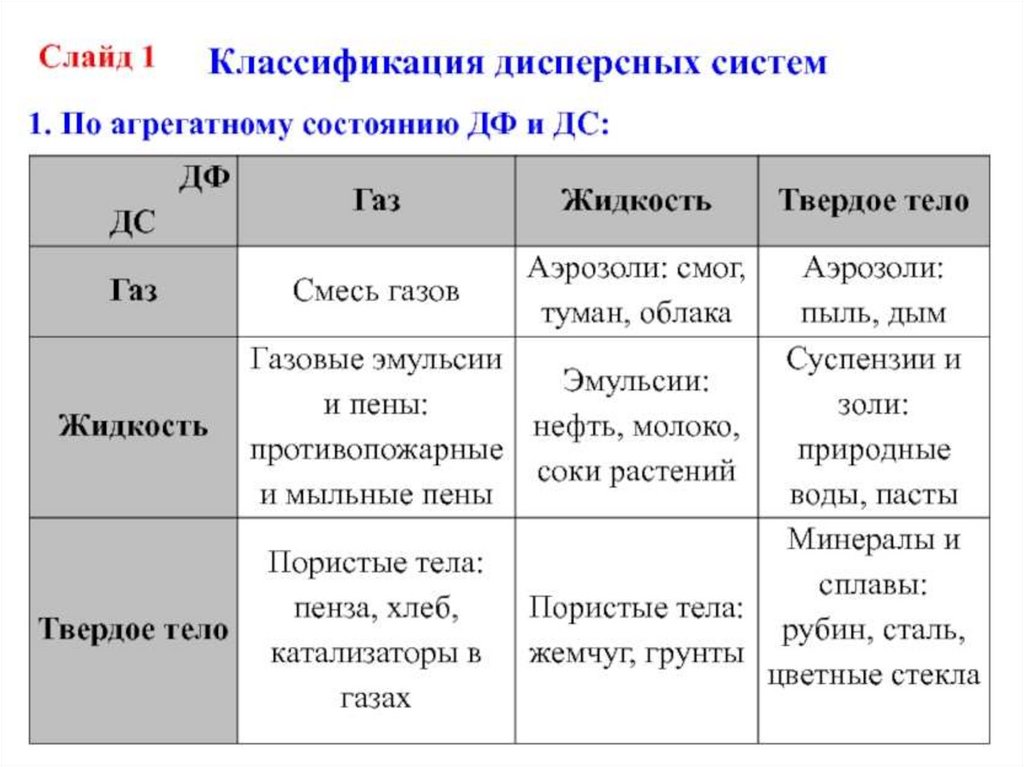
Классификация дисперсных систем1. По агрегатному состоянию.
9.
10.
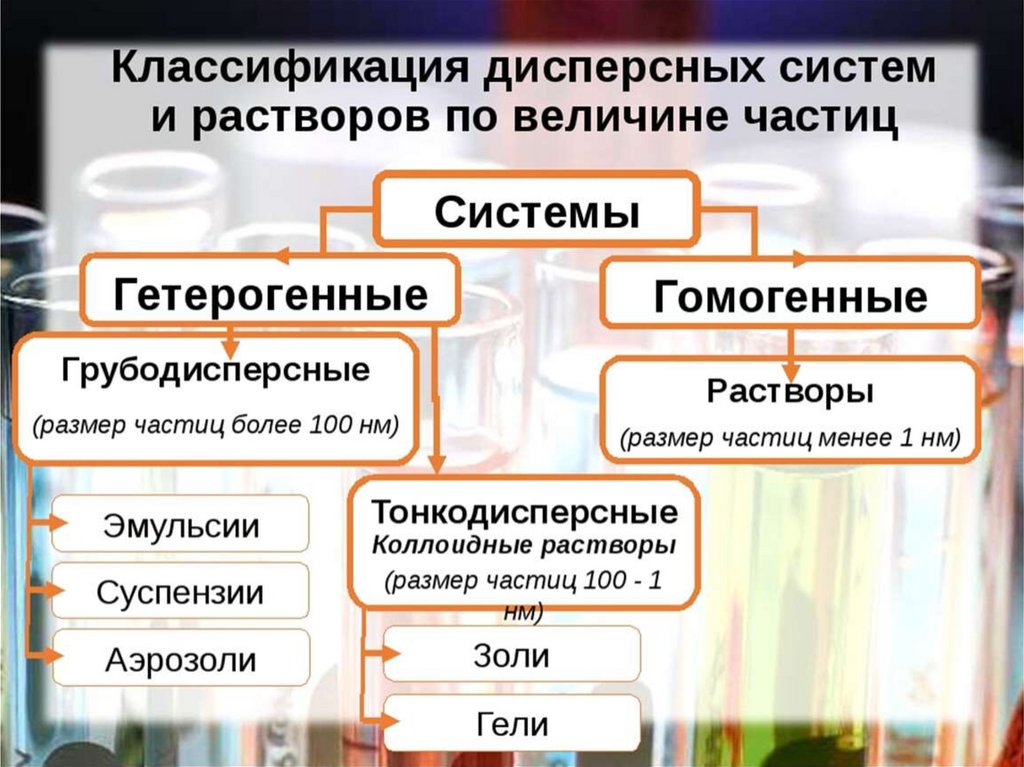
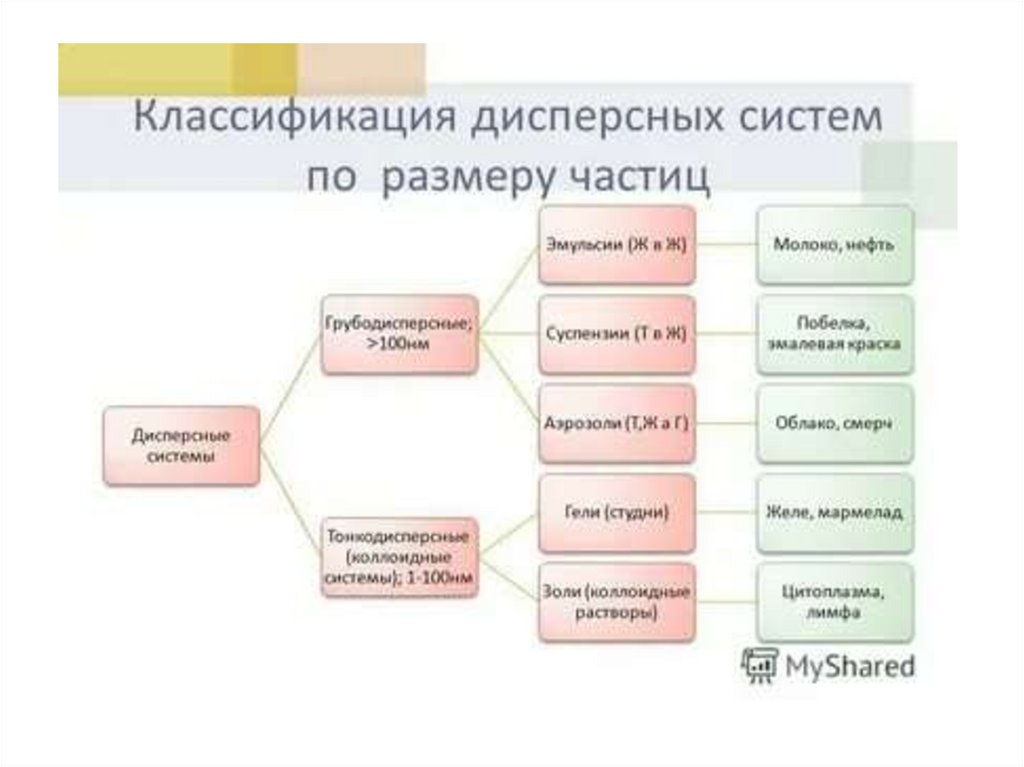
Классификация дисперсных систем:2. По величине частиц веществ,
составляющих дисперсную фазу
А) грубодисперсные (взвеси) с размерами
частиц более 100 нм
Б) тонкодисперсные (коллоидные растворы
или коллоидные системы) с размерами
частиц от 100 до 1 нм.
11.
12.
ВЗВЕСИВзвеси – это дисперсные системы, в которых
размер частицы фазы более 100 нм. Это
непрозрачные системы, отдельные частицы
которых можно заметить невооруженным
глазом.
Дисперсная фаза и дисперсная среда легко
разделяются отстаиванием,
фильтрованием.
13.
ВИДЫ ВЗВЕСЕЙЭмульсия – это дисперсная система с жидкой
дисперсионной средой и жидкой дисперсной фазой
(прямая, обратная).
Суспензия – это дисперсная система с жидкой
дисперсионной средой и твердой дисперсной фазой
(паста, взвесь).
Аэрозоли – это дисперсная система, в которой
дисперсионной средой является газ, а дисперсной
фазой – жидкость.
14.
КОЛЛОИДНЫЕ СИСТЕМЫКоллоидные системы (в переводе с
греческого “колла” – клей, “еидос” вид
клееподобные) – это такие дисперсные
системы, в которых размер частиц фазы от
100 до 1 нм.
Эти частицы не видны невооруженным
глазом, и дисперсная фаза и дисперсная
среда в таких системах отстаиванием
разделяются с трудом.
15.
Гель – это студенистый, не текучий раствор.Золь – это подвижный текучий коллоидный
раствор. К золям относят кровь, лимфу,
цитоплазму.
16.
Эффект Тиндаля-
рассеяние света при прохождении светового
пучка через оптически неоднородную среду.
Обычно наблюдается в виде светящегося конуса
(конус Тиндаля), видимого на тёмном фоне.
Назван по имени открывшего его Дж. Тиндаля..
Слева – раствор крахмала,
справа - вода
17.
КоагуляцияКоагуляция – явление слипания
коллоидных частиц и выпадения
их в осадок.
При этом раствор превращается
в суспензию или гель.
Некоторые органические коллоиды
коагулируют при нагревании
(клей, яичный белок) или при
изменении кислотно-щелочной
среды раствора.
18.
СинерезисСо временем структура гелей нарушается
(отслаивается) – из них выделяется вода.
Это явление называют синерезисом.
19.
Роль дисперсных системДля химии наибольшее значение имеют дисперсные
системы, в которых средой является вода и жидкие
растворы.
Природная вода всегда содержит растворённые
вещества. Природные водные растворы участвуют в
процессах почвообразования и снабжают растения
питательными веществами. Сложные процессы
жизнедеятельности, происходящие в организмах человека
и животных, также протекают в растворах.
Многие технологические процессы в химической и
других отраслях промышленности, например получение
кислот, металлов, бумаги, соды, удобрений протекают в
растворах.














 Химия
Химия








