Похожие презентации:
Углеводороды. Алканы
1.
ТЕМА: «УГЛЕВОДОРОДЫ»Алканы
2.
ПРИЗНАКИОбщая формула СnH2n+2
Наличие одинарных связей
Реакция горения, замещения,
разложения
3.
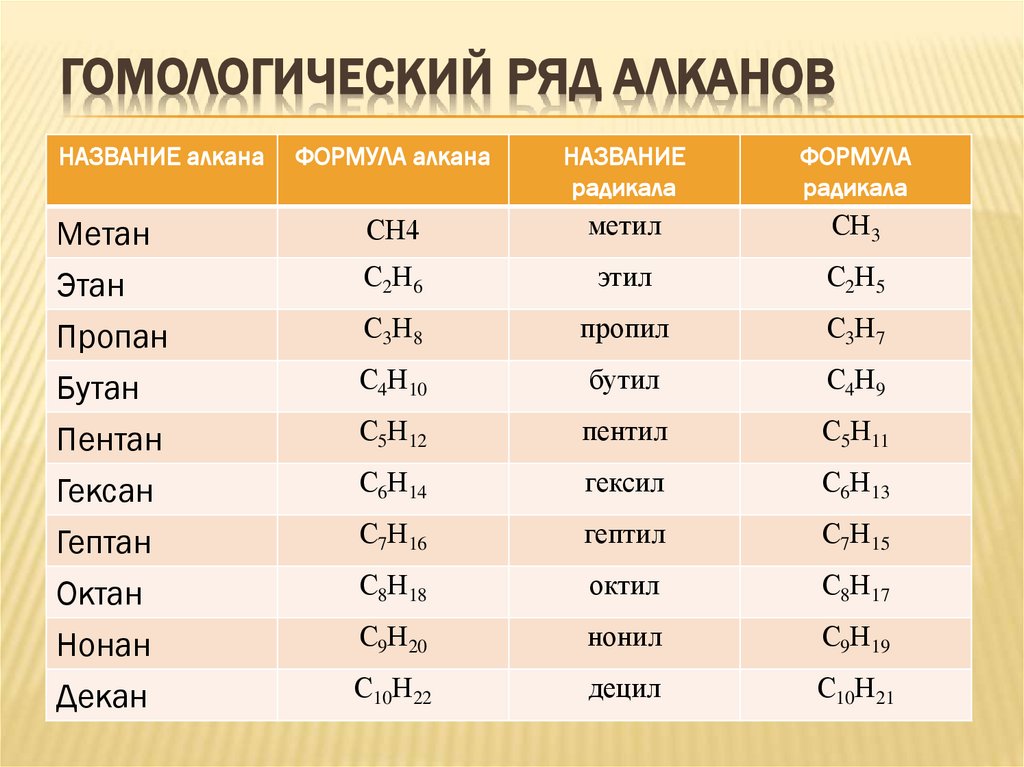
ГОМОЛОГИЧЕСКИЙ РЯД АЛКАНОВНАЗВАНИЕ алкана
ФОРМУЛА алкана
НАЗВАНИЕ
радикала
ФОРМУЛА
радикала
СН4
метил
СН3
С2Н6
этил
С2Н5
С3Н8
пропил
С3Н7
С4Н10
бутил
С4Н9
С5Н12
пентил
С5Н11
Гексан
Гептан
Октан
С6Н14
гексил
С6Н13
С7Н16
гептил
С7Н15
С8Н18
октил
С8Н17
Нонан
С9Н20
нонил
С9Н19
Декан
С10Н22
децил
С10Н21
Метан
Этан
Пропан
Бутан
Пентан
4.
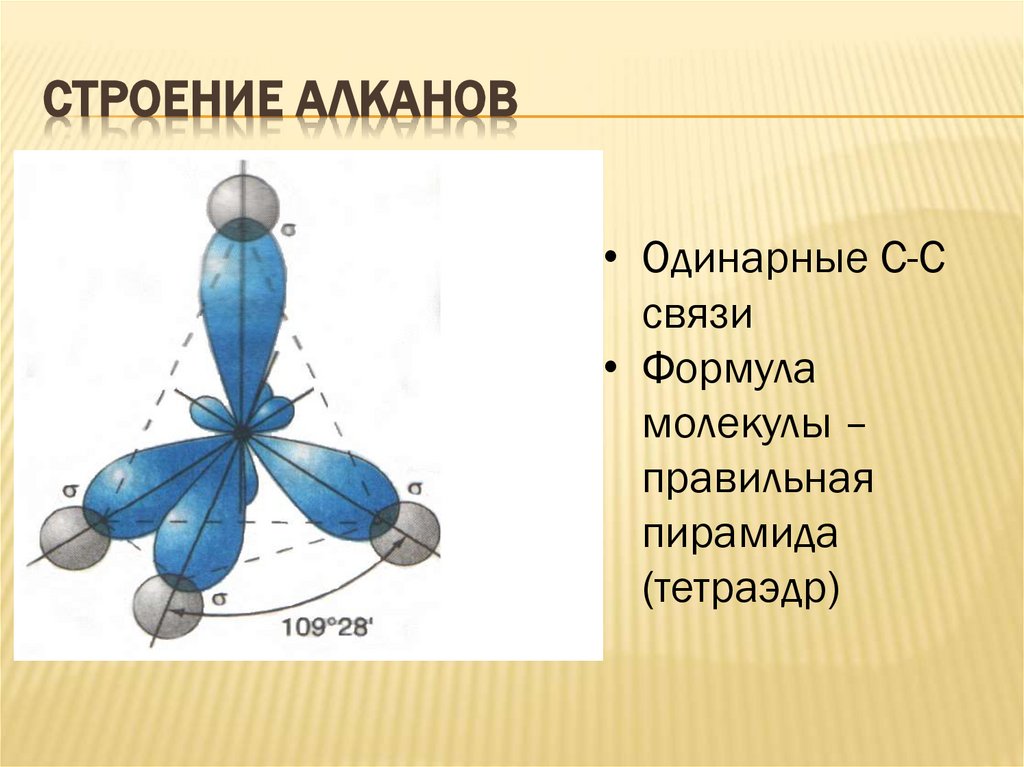
СТРОЕНИЕ АЛКАНОВ• Одинарные С-С
связи
• Формула
молекулы –
правильная
пирамида
(тетраэдр)
5.
ПРАВИЛА НОМЕНКЛАТУРЫ АЛКАНОВВыбрать самую длинную углеродную цепь
Пронумеровать ее с того конца, к которому ближе
разветвление
Указать номера атомов углерода у которых содержатся
заместители, если их несколько, то их располагают в
порядке старшинства. Если заместителей несколько, но
они одинаковые, то их число указывается греческими
числительными
(2 - ди, 3 - три, 4 - тетра, 5 - пента и
т.д.)
Назвать главную углеродную цепь
1
2
3 4
5 6
С -С -С - С- С- С
3,4-диметилгексан
|
|
СН3 СН3
6.
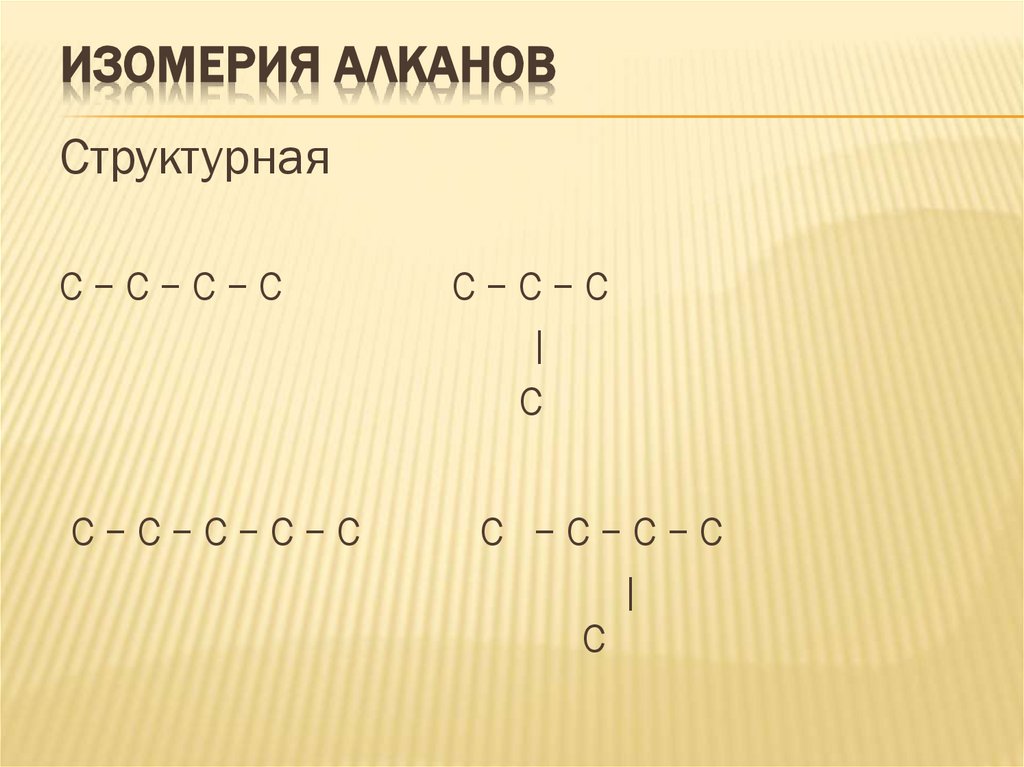
ИЗОМЕРИЯ АЛКАНОВСтруктурная
С−С−С−С
С−С−С−С−С
С−С−С
|
С
С −С−С−С
|
С
7.
ФИЗИЧЕСКИЕ СВОЙСТВАС1 - С 4 – газы
С5 – С16 – жидкости
С17 - …… - твердые вещества
Цвета нет, в воде растворимы плохо.
Жидкие алканы – легче воды.
СН4 – газ, без цвета и запаха, мало
растворим в воде, легче воздуха.
8.
Природные источникиалканов
нефть и газ
(презентация)
9.
Химические свойстваПрименение
1. Реакция горения
Топливо
СnH2n+2 + O2 → CO2 +H2O
CH4 + 2O2 → CO2+ 2H2O
10.
Химические свойстваПрименение
2. Отношение к окислителям
устойчивы, не обесцвечивают
марганцовку и бромную воду
3. Реакция замещения
hυ
СnH2n+2 + Cl2 → CnH2n+1 Cl + HCl
hυ
CH4 + Cl2 → CH3Cl + HCl
CH3Cl + Cl2 → ……
Получение
растворителей,
соляной кислоты,
полимеров
11.
Химические свойстваПрименение
4. Реакции разложения
(крекинг и дегидрирование)
Получение сажи,
резины, краски,
водорода, этилена
и ацетилена,
полимеров
?
СH4 → C + 2H2
?
2CH4 → C2H4 + 2H2
?
2CH4 → C2H2 + 3H2
t
СnH2n+2 → CnH2n + H2
крекинг
t
C20H42 → C10H22 + C10H20
Получение
нефтепродуктов
12.
Химические свойстваПрименение
5.Реакция с водой
Получение
синтез-газа
CH4 + H2O → CO +3H2
13.
ПОЛУЧЕНИЕ АЛКАНОВиз нефти
из природного газа
СО + Н2 → СnH2n+2 + H2O
(презентация)
14.
15.
16.
17.
18.
ЗАКРЕПЛЕНИЕ1. Изомерия невозможна для
а) 2-метилгексана
б) пропана
в) пентана
г) 2,3-диметилпентана
2. Верны ли следующие суждения:
А. Все алканы газообразны
В. Метан обесцвечивает раствор KMnO4
а) верно А
б) верно В
в) верно А и В
г) оба суждения не верны
19.
3. Гомологами являютсяа) пропан и пентан
б) пропан и циклопропан
в) пентан и пентен
г) циклопропан и гексан
4. Пропан реагирует с
а) металлическим натрием
б) хлором при облучении
в) водой
г) раствором KMnO4
20.
5. При взаимодействии 1 моль СН4 с 2 моль Cl2при освещении получается
а) хлорметан
б) дихлорметан
в) хлороформ
г) тетрахлорметан
6.Превращение этана в этен относится к реакции
а) полимеризации
б) дегидрирования
в) дегидратации
г) изомеризации
21.
7. Экологически чистым топливом являютсяа) водород
б) нефть
в) каменный уголь
г) природный газ
8. Для метана характерны
а) реакция гидрирования
б) тетраэдрическая форма молекулы
в) наличие π-связи в молекулах
г) sp3-гибридизация орбиталей атома углерода
в молекуле
д) реакция с галогеноводородами
е) горение на воздухе


















 Химия
Химия








