Похожие презентации:
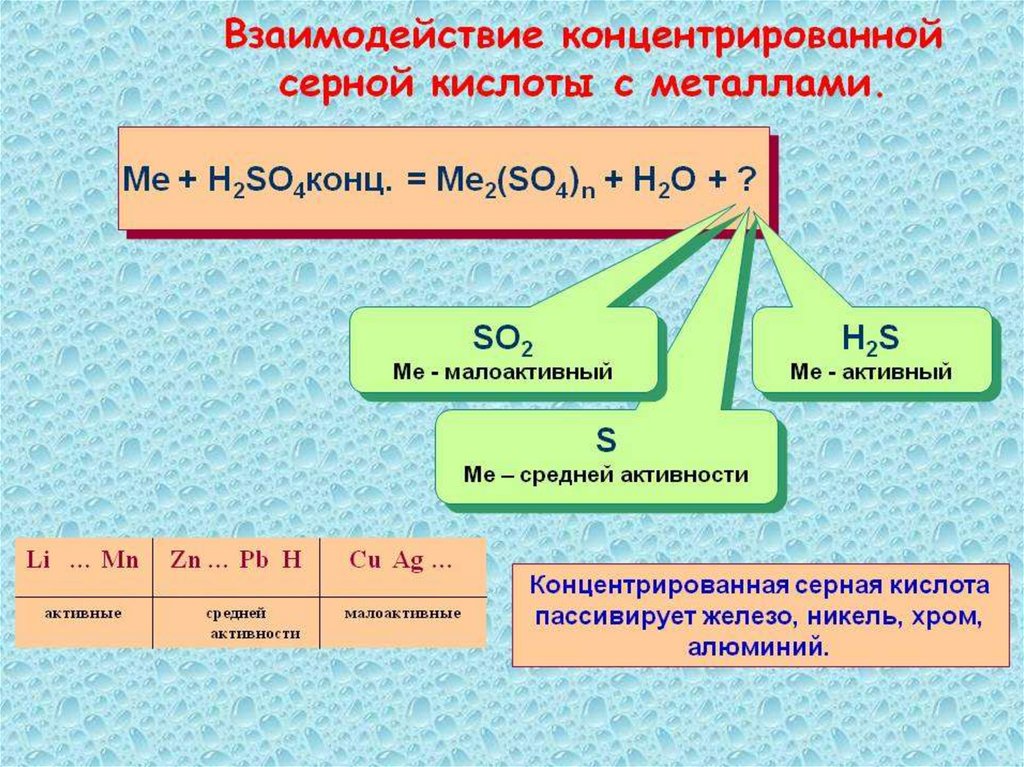
Взаимодействие концентрированной серной кислоты с металлами
1.
2.
Повторим пройденное:• Что изучили во 2 четверти?
• Что узнали нового?
• Расскажите про водород, галогены,
халькогены.
• Что такое олеум?
• Что такое «царская водка»
3.
Напишите возможные уравненияреакций:
1.
2.
3.
4.
5.
6.
7.
8.
Фтор +вода=
Сера + кислород=
Соляная кислота +магний=
Оксид серы (IV) + кислород=
Серная кислота (разб.)+ железо=
Серная кислота (конц.) + цинк=
Серная кислота (разб.)+ медь=
Серная кислота (конц.)+ медь=
4.
5.
6.
7.
Подготовка к практической работе №3«Свойства неМе и их соединений»
стр.259 учебника химии ГабриелянО.С.
• Задачи №1 : Даны две пробирки с растворами
гидроксида натрия и серной кислоты.
Определить в какой пробирке находится
серная кислота и провести качественные
реакции, подтверждающие ее состав.
Написать уравнения х.р.
• Задача №5: Определить содержит ли
поваренная соль примесь сульфатов. Написать
уравнения х.р.
8.
Интересные факты:Впервые эта болезнь возникла после изобретения воздушного насоса
и последовавшего за этим изобретения в 1841 г. кессона — камеры с
повышенным давлением, использовавшейся для строительства
туннелей под реками и закрепления в донном грунте опор мостов.
Рабочие входили в кессон через шлюз и работали в атмосфере
сжатого воздуха, что препятствовало затоплению камеры.
Практически с самого начала у тоннельных и кессонных рабочих после
возвращения в условия обычного атмосферного давления стали
появляться недомогания. Чаще всего рабочие жаловались на кожный
зуд. Реже появлялись сильные боли в суставах и мышцах, не дающие
распрямиться (поэтому рабочие прозвали эту болезнь «корчами»).
Риск и симптомы усиливались с увеличением давления и времени
пребывания, поэтому водолазы, неизбежно подвергавшиеся
воздействию высокого давления, страдали чаще, чем кессонные
рабочие. В наиболее серьезных случаях при подъеме на поверхность
человек испытывал головокружение, затем наступал паралич, потеря
сознания и смерть — и все это в считанные минуты».
Почему?*?
9.
10.
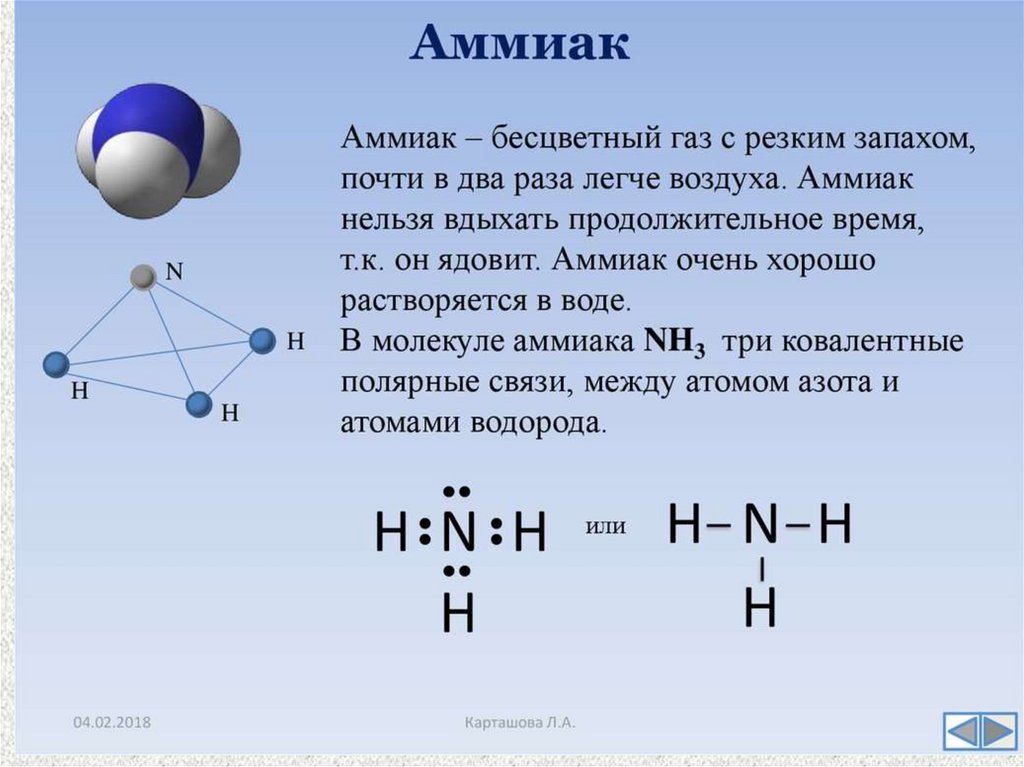
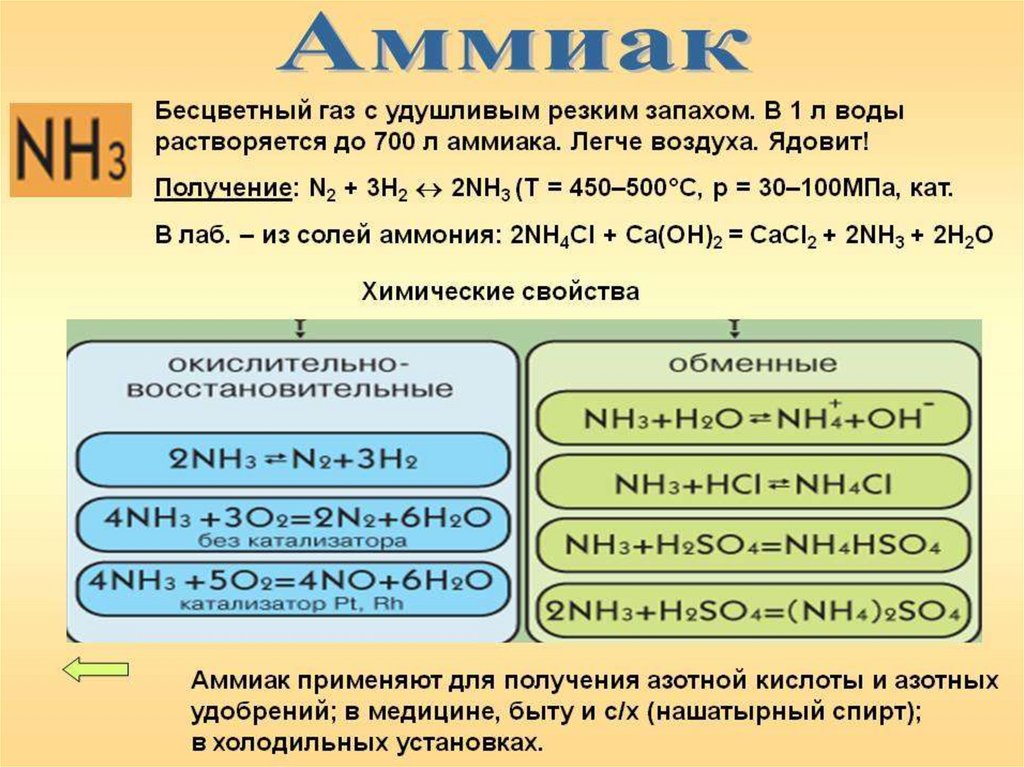
Тема урока : Азот. Соединенияазота: аммиак
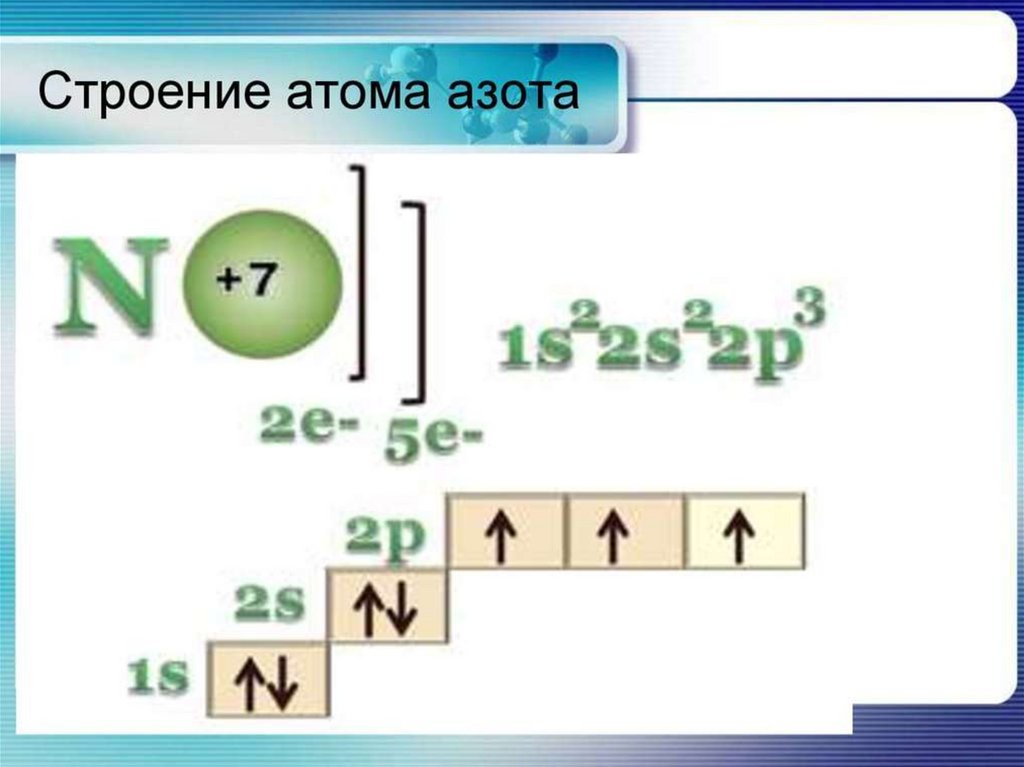
• Рассмотреть общую характеристику азота.
Строение
• Рассмотреть свойства азота как простого
вещества.
• Рассмотреть физические свойства азота
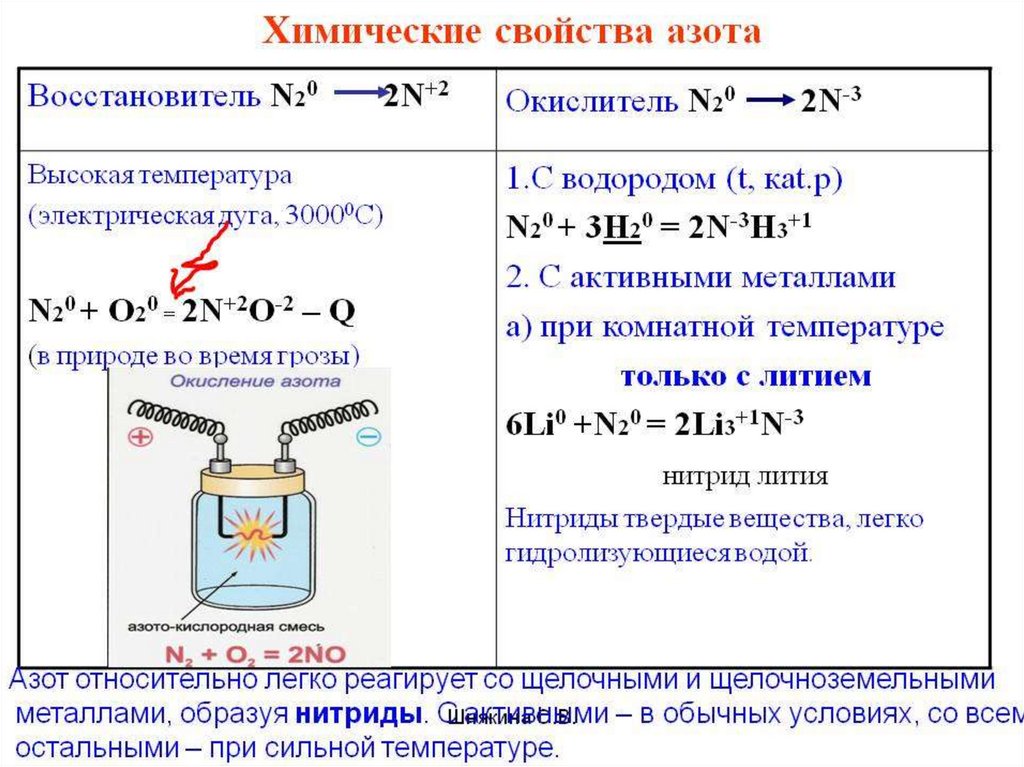
• Рассмотреть химические свойства азота
• Получение, применение, нахождение в
природе
11.
12.
13.
14.
15.
16.
Наиболее важные соединенияазота:
17.
18.
19.
20.
21.
22.
23.
24.
25.
26.
Проверь себя (параграф 29, стр.210-214)• Что такое аммиачная вода?
• Что такое нашатырный спирт?
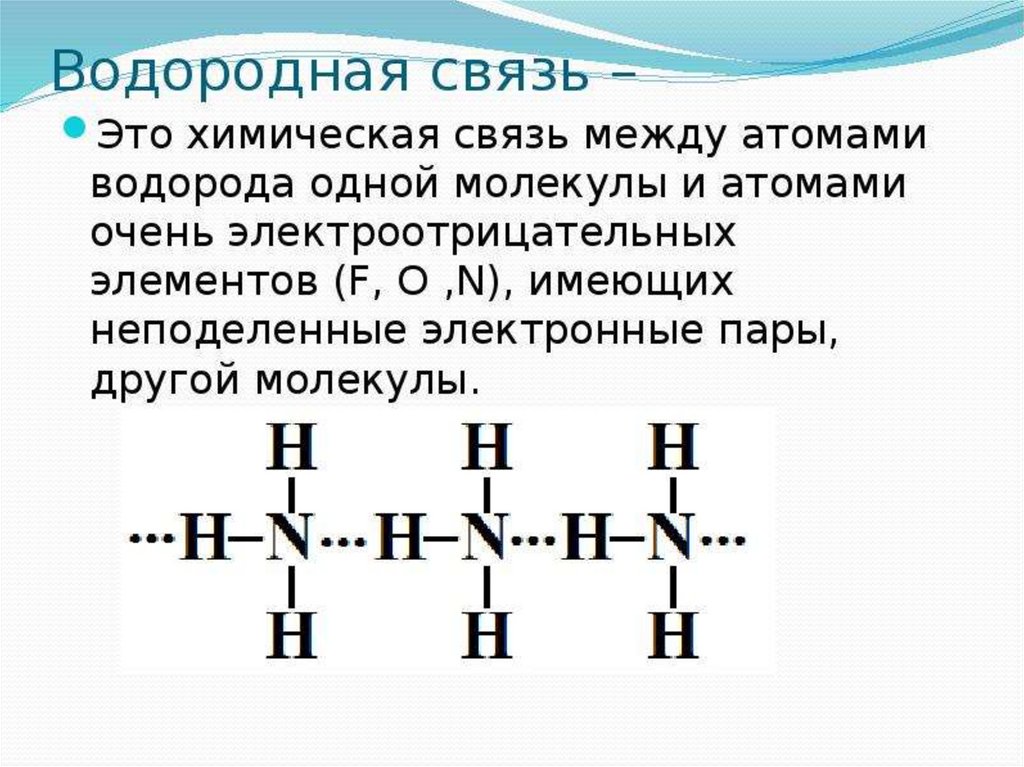
• Объясните принцип донорно-акцепторного
механизма образования ковалентной связи
на примере иона аммония
• Агрегатное состояние аммиака
27.
• Закончите предложения:- Теперь я знаю, что……….
- Я понял, что………..
- Я буду……………
• оцените результаты своей деятельности.
«!» - все понятно
«?» - остались вопросы
«???» - тема очень трудная, много неясного
• нарисуйте смайлик на полях, описывающий
ваше настроение , у кого +,-,0 (поднимите
руки)
28.
Домашнее задание:• Общее:- параграф 28 (стр.204-208)
- параграф 29 (стр.210-214)
- оформить практическую работу №3(с.259)
• Инд.:- происхождение названия х.э. «Азот»
-круговорот азота в природе
- значение азота для жизни на земле
- основные области применения аммиака
- Жидкий азот: что это?






















 Химия
Химия








