Похожие презентации:
Оптические методы. Фотометрические методы. Хроматография
1. СПб ГБОУ 3 медколледж
ОП.06 Физико-химические методы и ТЛРТема: Оптические методы. Фотометрические
методы. Хроматография
2.
3.
4.
5. Cвет представляет собой электромагнитные волны определенного диапазона (от 10 до 1,5х104нм;1нм = 10-9м). Глаз воспринимает
только свет с λ от 380 до 770 нм.• УФ-излучение с λ < 380 нм, >
770 нм - ИК-излучение ,
невидимы глазом. Свет
определенной длины волны
называется
монохроматическим.
6.
7.
8.
Фотометрические методы анализа используются вмедицинских лабораториях для исследования
состава и свойств биологических жидкостей,
лекарственных веществ, токсинов, пищевых
продуктов. Эти методы базируются на
способности жидких сред (растворов)
взаимодействовать с электромагнитным
излучением в ультрафиолетовой, видимой или
инфракрасной областях спектра.
9.
• Спектр представляет собой зависимость количества поглощенной илиизлученной системой энергии от длины волны или другого параметра.
• Молекулы взаимодействуют с излучением в широком диапазоне длин волн,
поэтому их спектры лежат в разных областях. Для измерения в каждом
спектральном диапазоне используется специальное оборудование, которые
широко используются в повседневной работе КДЛ.
• Основные законы поглощения
• При прохождении света через равномерно поглощающую среду его
интенсивность I0 уменьшается до величины I.Отношение интенсивностей
прошедшего и падающего света I/ I0 называется пропусканием – Т.
• Поглощение – А или экстинция – Е (оптическая плотность - D) – это
величина, равная lg1/T=lg I/ I0 .
• Согласно закону экстинция пропорциональна концентрации поглощающего
вещества и толщине образца.
• Пропускание (Т) измеряется в % - 0 до 100 %.
• Экстинция (Е, оптическая плотность D ) – величина безразмерная и
изменяется от 0 до .
10.
11.
12.
13.
Фотометрические методыГлавное преимущество этих методов состоит в том, что вещество в процессе
исследования не разрушается.
Оптические методы позволяют обнаруживать незначительные количества вещества.
Принципы метода
При фотометрических определениях интенсивность окраски или степень мутности
определяемого раствора сравнивают с окраской раствора, концентрация которого
известна.
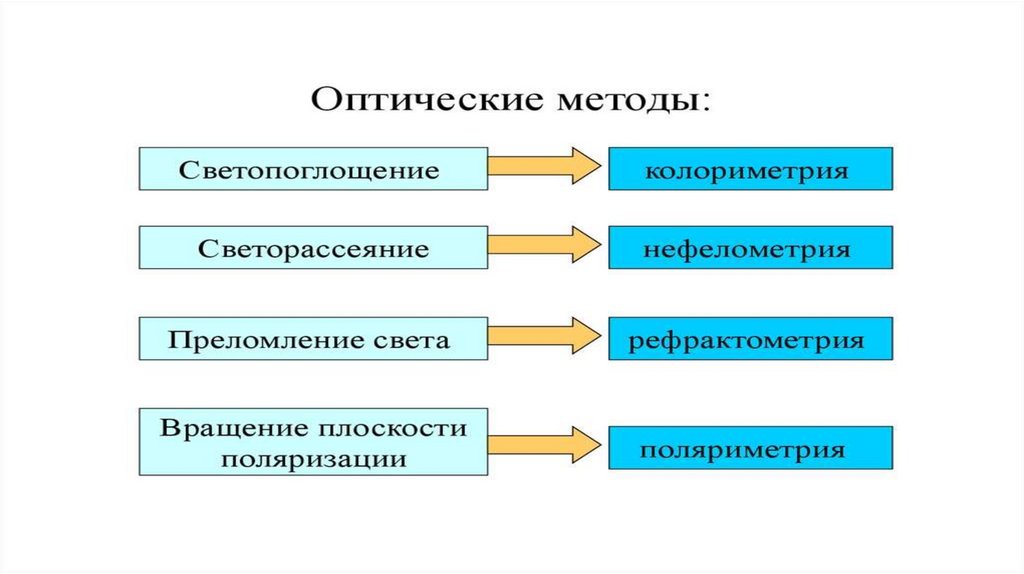
Имеются различные фотометрические методы:
• Фотоэлектроколориметрия – определение концентрации вещества в растворе по
изменению силы тока в фотоэлементе при падении на него луча света, прошедшего
через исследуемый раствор (прозрачный, окрашенный).
• Нефелометрия – определение содержания вещества в мутном растворе по
интенсивности света, рассеянного взвешенными частицами суспензии.
• Спектрофотометрия – определение содержания вещества по поглощению раствором
света определенной длины волны, характерного для поглощения данным веществом.
14.
• ФОТОЭЛЕКТРОКОЛОРИМЕТРИЯ – ОПРЕДЕЛЕНИЕ КОНЦЕНТРАЦИИВЕЩЕСТВА В РАСТВОРЕ ПО ИЗМЕНЕНИЮ СИЛЫ ТОКА В
ФОТОЭЛЕМЕНТЕ ПРИ ПОПАДЕНИИ НА НЕГО ЛУЧА СВЕТА
ПРОШЕДШЕГО ЧЕРЕЗ ИССЛЕДУЕМЫЙ РАСТВОР.
При прохождении светового потока через окрашенную прозрачную жидкость
часть света поглощается. Степень поглощения света, или коэффициент экстинции
(«тушения»), во многих случаях прямопропорциональна интенсивности окраски
раствора.
Окраска раствора зависит от концентрации в нем растворенного вещества:
чем выше концентрация и тем больше света поглощает раствор.
Степень светопоглощения определяют в приборе фотоэлектроколориметре
(ФЭК) путем уравнивания интенсивности света, прошедшего через исследуемый
окрашенный раствор (рабочий), и света, прошедшего через контрольный раствор
(растворитель, чаще дист. вода) – бесцветный растворитель исследуемого вещества.
По степени светопоглощения определяют содержание вещества в растворе.
15.
Основной элемент прибора ФЭК – фотоэлеменет (ФЭ). Фотоэлемент преобразуетсветовое излучение в электрический ток.
При попадании света на светочувствительные вещества (селен или цезий)
фотоэлемента энергия световых квантов передается электронам этого вещества, которые
начинают двигаться в одном направлении, т.е. возникает электрический ток, силу которого
можно измерить микроамперметром.
Сила тока пропорциональна световому потоку, падающему на фотоэлемент. Когда
на пути светового потока ставят кювету с раствором, поглощающим или рассеювающим
свет, на ФЭ падает меньше лучей. Сила тока в цепи уменьшается, на что указывает
отклонение стрелки амперметра.
По изменению силы тока можно судить о концентрации исследуемого вещества.
Определение концентрации прозрачных окрашенных растворов называется
колориметрический метод, а во взвесях и эмульсиях – нефелометрический метод.
Частички взвеси, помещенной на пути пучка света, отражают световые волны –
рассеивают свет.
Чем мутнее взвесь, т.е. чем больше ее концентрация, тем больше света отражается,
тем меньшей силы ток возникает в ФЭ.
16.
17.
Устройство прибора ФЭКВ корпусе прибора имеются осветитель, оптическая система, кюветодержатели,
фотоэлементы, электрическая сеть с микроамперметром.
Осветитель – лампа накаливания (ртутно-кварцевая лампа), световой пучок от
которой перекрывается шторкой, преграждающей путь света в направления ФЭ.
В оптическую часть входят светофильтры, которые пропускают световой поток
определенного спектрального диапазона.
18.
19. Спектрофотометр
20.
21.
22.
23.
24.
25. Принципы построения калибровочного графика
• Концентрации веществ в пробах при фотометрическом способеопределения находим по калибровочному грапфику.
• Указания по приготовлению шкалы стандартов для построения
калибровочного графика приведены вы каждой методике. График
строится на миллиметровой бумаге, откладывая по горизонтальной
оси (абсцисс) концентрации, а по вертикальной (ординат) – величину
оптической плотности, средне из результатов 3-5 измерений.
• Калибровочный график проверяют после смены каждого реактива, но
не реже одного раза в месяц.
• При определении концентрации вещества в пробе анализируемый
раствор наливают в ту же кювету, для которой построен
калибровочный график и при том же светофильтре определяют
оптическую плотность.
• На точность результатов измерения большое влияние оказывает
чистота рабочих граней кювет.
26.
27.
28. КФК-2
29.
КОЛОРИМЕТР ФОТОЭЛЕКТРИЧЕСКИЙ КОНЦЕНТРАЦИОННЫЙКФК-2
Назначение: измерение в отдельных участках диапазона длин волн 315-980 нм, выделяемых светофильтрами,
коэффициентов пропускания и оптической плотности жидкостных растворов, а также определения концентрации
веществ в растворах методом построения градуировочных графиков.
Правила работы
Колориметр включить в сеть за 15 мин. до начала измерений. Во время прогрева кюветное отделение должно быть
открыто!
Ввести необходимый по роду измерений цветной светофильтр (см. методику).
Установить минимальную чувствительность колориметра. Для этого ручку ЧУВСТВИТЕЛЬНОСТЬ установить в
положение «1», ручку УСТАНОВКА 100 ГРУБО – в крайнее левое положение.
Перед измерениями и при переключении фотоприемников проверить установку стрелки колориметра на «0» по шкале
коэффициентов пропускания Т при открытом кюветном отделении. При смещении стрелки от нулевого положения, ее
подводят к нулю с помощью потенциометра НУЛЬ, выведенного под шлиц.
ИЗМЕРЕНИЕ ОПТИЧЕСКОЙ ПЛОТНОСТИ
В световой пучок поместить кювету с контролем.
Закрыть крышку кюветного отделения.
Ручками ЧУВСТВИТЕЛЬНОСТЬ и УСТАНОВКА 100 ГРУБО и ТОЧНО установить отсчет 100 по шкале
колориметра. Ручка ЧУВСТВИТЕЛЬНОСТЬ может находиться в одном из трех положений: «1», «2» или «3».
Затем, поворотом 4 (переключение кювет) кювету с контролем заменить кюветой с рабочим раствором.
Снять отсчет по шкале колориметра, соответствующий оптической плотности по шкале Д в единицах оптической
плотности.
Измерение проводить 3-5 раз и окончательное значение измеренной величины определить как среднее
арифметическое из полученных значений.
30.
ВЫБОР КЮВЕТЫПредварительно кювета выбирается визуально, соответственно интенсивности
окраски раствора. Если раствор интенсивно окрашен (тёмный), следует пользоваться
кюветами с малой рабочей длиной (1 – 3 мм). В случае слабо окрашенных растворов
рекомендуется работать с кюветами с большой рабочей длиной (30 – 50 мм).
В предварительно подобранную кювету наливают раствор и измеряют его
оптическую плотность, включив в ход лучей соответствующий для данного раствора
светофильтр.
При измерении оптической плотности ряда растворов кювету заполняют раствором
средней концентрации. Если полученное значение оптической плотности составляет
примерно 0,3 – 0,5, то данную кювету выбирают для работы с этим раствором, в
противном случае следует испробовать другую кювету. Если величина измеренной
оптической плотности больше 0,5 – 0,6, берут кювету меньшей рабочей длины, если
величина оптической плотности меньше 0,3 – 0,2, следует выбрать кювету с большей
рабочей длиной.
31. ВЫБОР СВЕТОФИЛЬТРА
• Проводится выбор светофильтров следующим образом.• Налейте раствор в кювету и определите оптическую плотность для всех светофильтров.
• По полученным данным постройте кривую, откладывая по горизонтальной оси длины волн,
соответствующие максимуму коэффициента пропускания светофильтров, а по вертикальной
оси - соответствующие значения оптической плотности раствора. Отметьте тот участок
кривой, для которого выполняются следующие условия:
• оптическая плотность имеет максимальную величину;
• ход кривой примерно параллелен горизонтальной оси, т.е. оптическая плотность мало зависит
от длины волн (второе условие может для некоторых растворов не иметь места, тогда при
выборе светофильтра ограничиваются выполнением первого условия).
• Светофильтр для работы выбирается так, чтобы длина волны, соответствующая максимуму
коэффициента пропускания светофильтра, приходилась на отмеченный выше участок
спектральной кривой испытуемого раствора.
• Если эти условия выполняются для нескольких светофильтров, то выберите тот из них, для
которого чувствительность колориметра выше.
32.
33.
34.
35.
36.
37.
38. Электрофорез
• Многие важные в биологическом отношении молекулы(аминокислоты, пептиды, белки и нуклеиновые кислоты)
содержат ионизующиеся группы, поэтому в растворе они могут
существовать в заряженной форме в виде катионов (+) либо
анионов (-).
• Молекулы с зарядами, близкими по величине, но
различающимися молекулярной массой, отличаются друг от друга
отношением заряда к массе.
• На этих различиях основано разделение ионов при движении их в
растворе под действием электрического поля.








































 Физика
Физика Электроника
Электроника








