Похожие презентации:
Алканы. Предельные углеводороды
1.
«Алканы»2.
Предельные углеводороды(алканы, парафины,
насыщенные УВ)
I. Строение
С–С–С–С–…
содержат в своём составе
простую (одинарную,σ) связь
между атомами углерода
3.
Общая формулагомологического ряда алканов
СnH2n+2
4.
III. Изомерия и номенклатураалканов
5.
Изомеры – вещества, имеющиеодинаковый состав, но разное
химическое строение, а потому и
разные свойства.
У алканов – единственный вид
изомерии – изомерия углеродного
скелета
6.
Номенклатура алканов:Название нормального
(неразветвленного)
алкана =
корень основной
углеродной цепи
( мет-, проп-, бут- и далее
греч.числительные)
+ суффикс aн
7.
-R или -СnH2n+1) - этоуглеводородный радикал,
частица, образующаяся при
отрыве атома водорода от
молекулы предельного
углеводорода (алкана)
8.
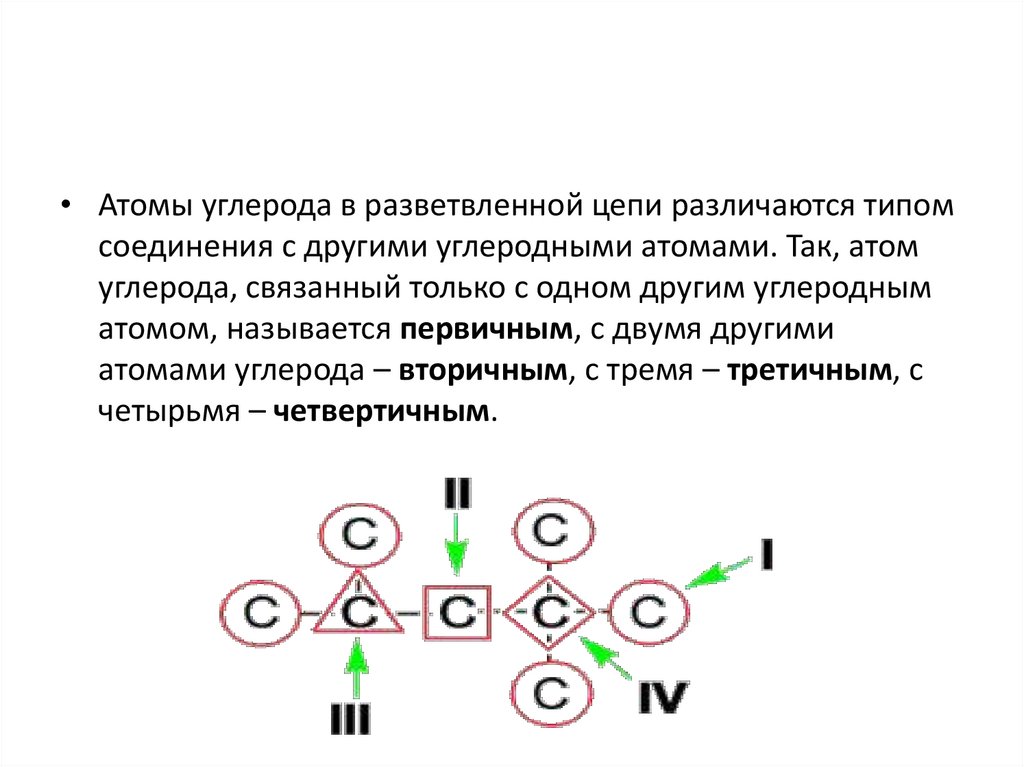
• Атомы углерода в разветвленной цепи различаются типомсоединения с другими углеродными атомами. Так, атом
углерода, связанный только с одном другим углеродным
атомом, называется первичным, с двумя другими
атомами углерода – вторичным, с тремя – третичным, с
четырьмя – четвертичным.
9.
10.
11.
12.
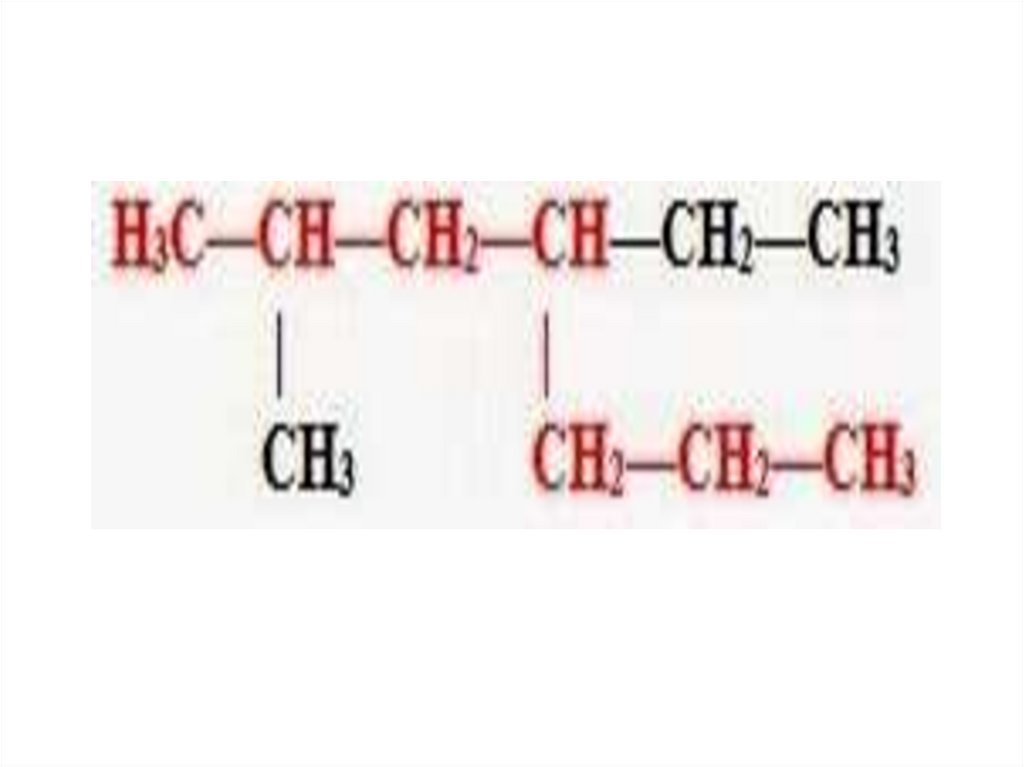
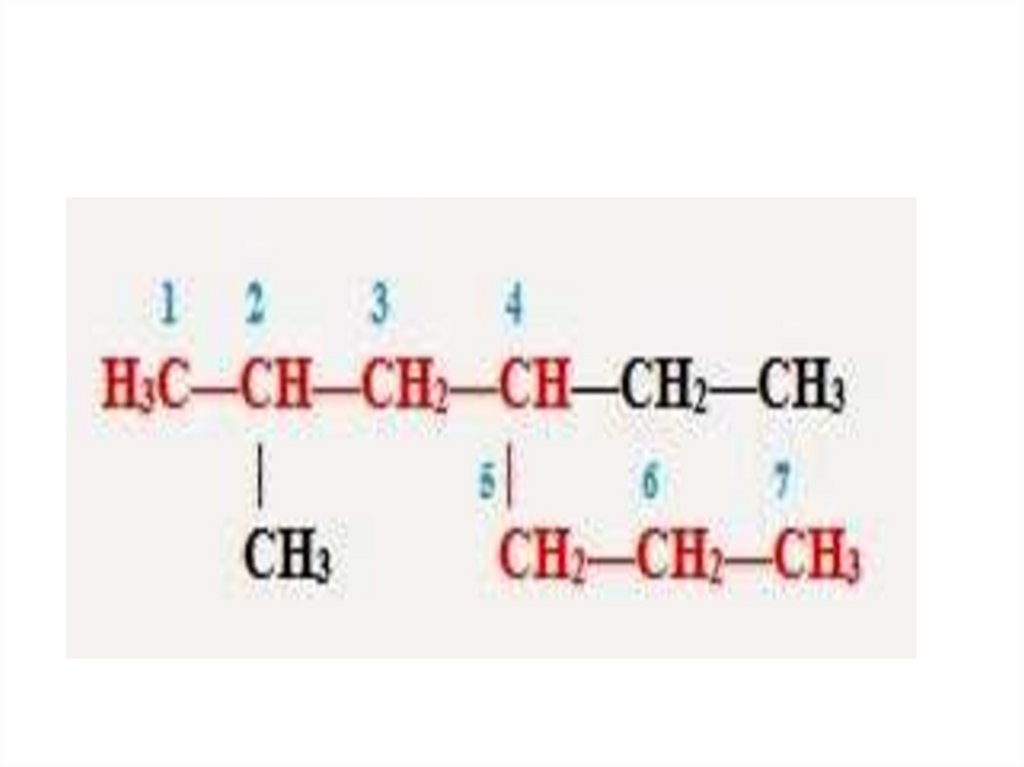
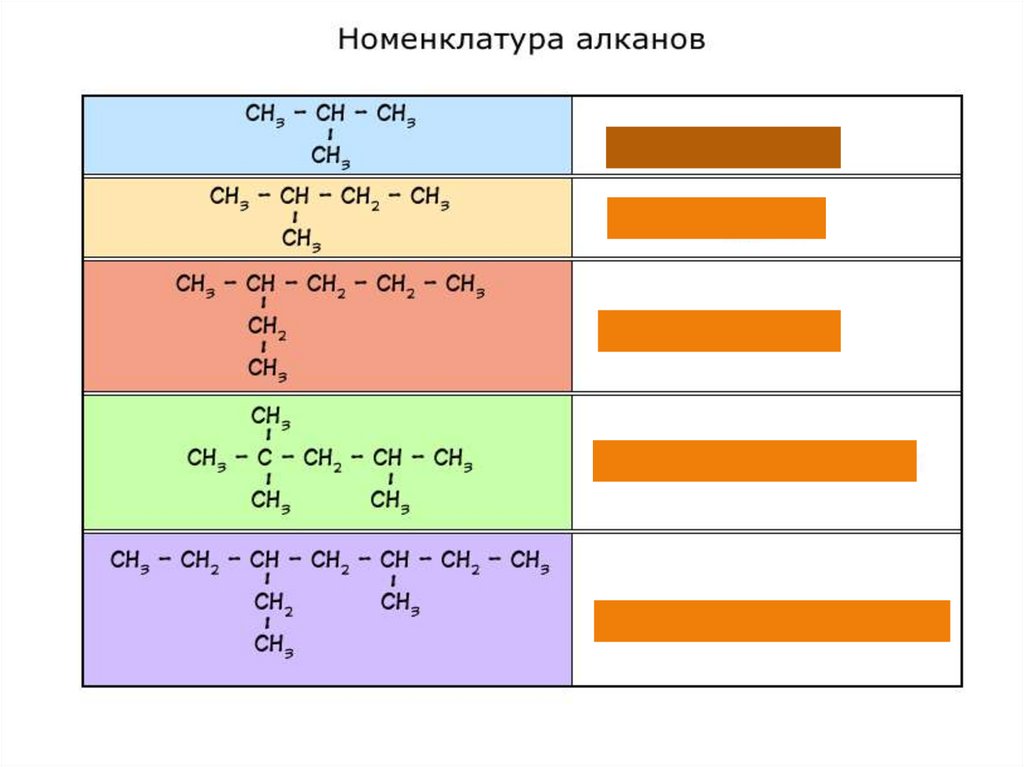
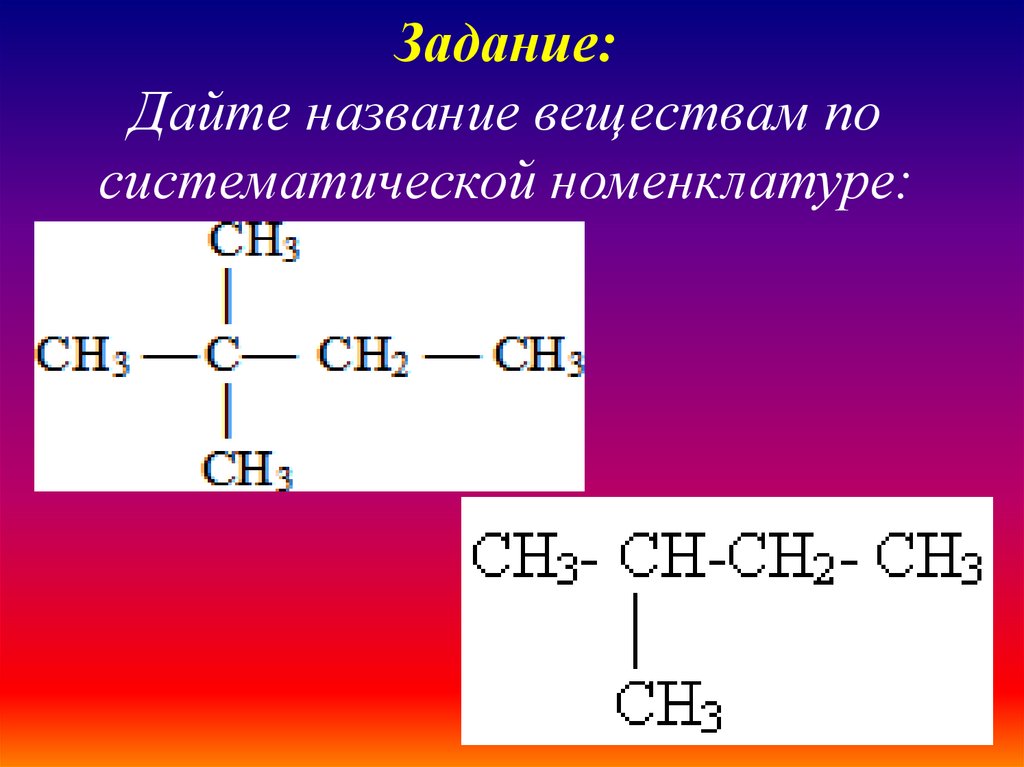
Задание:Дайте название веществам по
систематической номенклатуре:
13.
IV. Физическиесвойства
14.
Алканы плохо растворимы в воде, нохорошо растворяются в органических
растворителях.
С1– С4 - газы
С5– С15 - жидкости
С16 - … - твёрдые вещества
С увеличением молекулярной массы
алканов, в гомологическом ряду,
повышаются температуры кипения
и плавления, увеличивается плотность
веществ.
15.
V. Нахождение в природеМетан.
Пропан.
16.
VI. Химические свойства17.
Типы химических реакций,которые характерны для алканов
Реакции
замещения
Реакции разложения
(дегидрирование, крекинг)
Реакции горения
18.
Горение алкановЗАДАНИЕ:
Составьте уравнение горения метана
СН4 + 2О2
метан
СО2 + 2Н2О
Горение метана.
19.
ЗАДАНИЕ:Составьте уравнение горения бутана
С4Н10 + 13/2О2
бутан
2С4Н10 + 13О2
4СО2 + 5Н2О
8СО2 + 10Н2О
20.
Реакции замещения- главныйтип реакции для ПУВ
1) Галогенирование
CН3– СН2 – СН3 + Сl2 СН3 –СНCl – СН3 +HCl
пропан
2-хлорпропан
Реакция идёт только на свету (hν)
Замещение начинается с третичного атома углерода
(затем вторичного, затем первичного)
21.
Реакции замещения- главныйтип реакции для ПУВ
2) Нитрование
CН3– СН2 – СН3 + HNO3 СН3 –СН(NO2) – СН3 + H2O
пропан
2-нитропропан
Реакция идёт в присутствии конц. серной кислоты.
Замещение начинается с третичного атома углерода
(затем вторичного, затем первичного)
22.
Реакции разложения1) Крекинг (разрыв С-С связи)
2СН4 C2H2 + 3H2 (при 15000С)
ацетилен
СН4 C+ 2H2 (при 10000С)
2) Дегидрирование (разрыв С-Н связи)
23.
Реакции изомеризацииСН3-СН2-СН2-СН3 CH3-СН(CH3)-CH3
название?
2-метилпропан
Реакция проходит при нагревании
и в присутствии катализатора AlCl3
24.
Получениеметана
Получение
1. Оргсинтез: С+2Н2 СН4
При
повышенном
давлении, Ni
2. Реакция Вюрца:
2RCl + 2Na R-R + 2NaCl
3.
Из солей карбоновых кислот(реакция Дюма)
RCOONa + NaOH R-H + Na2CO3
3.
Гидрирование непредельных и
ароматических углеводородов:
С2Н4 + Н2 С2Н6
При нагревании и
катализаторе
С6Н6 + 4Н2 С6Н14
25.
Получение• Гидролиз
Al4C3+12H2O=CH4+Al(OH)3




















 Химия
Химия








