Похожие презентации:
α-Аминокислоты и белки
1.
ОМСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙУНИВЕРСИТЕТ
КАФЕДРА ХИМИИ
α-Аминокислоты и белки
1. α-Аминокислоты, строение,
номенклатура, изомерия.
2. Физические и химические свойства.
3. Пептиды и белки.
Лектор: Ирина Петровна Степанова, доктор биологических
наук, профессор, зав. кафедрой химии
2.
Медико-биологическоезначение темы
Из остатков аминокислот
построены такие важные
соединения как белки, которые
участвуют практически во всех
процессах in vivo: биосинтез
алкалоидов, порфиринов,
тетрапиррольных пигментов,
мочевины и т.д.
С нарушениями метаболизма
аминокислот связаны
наследственные заболевания как
фенилкетонурия и алкаптонурия.
3.
Медико-биологическое значение темыНекоторые
аминокислоты
являются
лекарственным
и препаратами.
4. Медико-биологическое значение темы
5.
-АминокислотыПептиды и белки построены из
20 аминокислот, информация о положении которых в
белковой
молекуле
записана
цифровым
трёхбуквенным кодом в ДНК и РНК.
-Аминокислоты
гетерофункциональные
соединения - производные карбоновых кислот, у
которых один атом водорода у
углеродного звена замещен на аминогруппу.
6. α-Аминокислоты, строение, номенклатура, изомерия
Общий фрагментОсновный
центр
Кислотный
центр
R
Радикал
7. α-Аминокислоты, строение, номенклатура, изомерия
I. По строению углеводородного радикалаα-аминокислоты делят на 7 групп:
I. Моноаминомонокарбоновые
II. Моноаминодикарбоновые
III. Диаминомонокарбоновые
IV. Гидроксиаминокислоты
V.Серосодержащие аминокислоты
VI. Ароматические
VII. Гетероциклические
8.
α-Аминокислоты, строение, номенклатура, изомерияI. Моноаминомонокарбоновые аминокислоты
(нейтральные )
H2N CH2 COOH
Глицин (ГЛИ)
-Аминоуксусная кислота
Боковые радикалы
-аминокислот этой
подгруппы гидрофобные.
9.
Моноаминомонокарбоновые аминокислотыH2N CH COOH
CH3
Аланин (АЛА)
-Аминопропионовая
кислота
10.
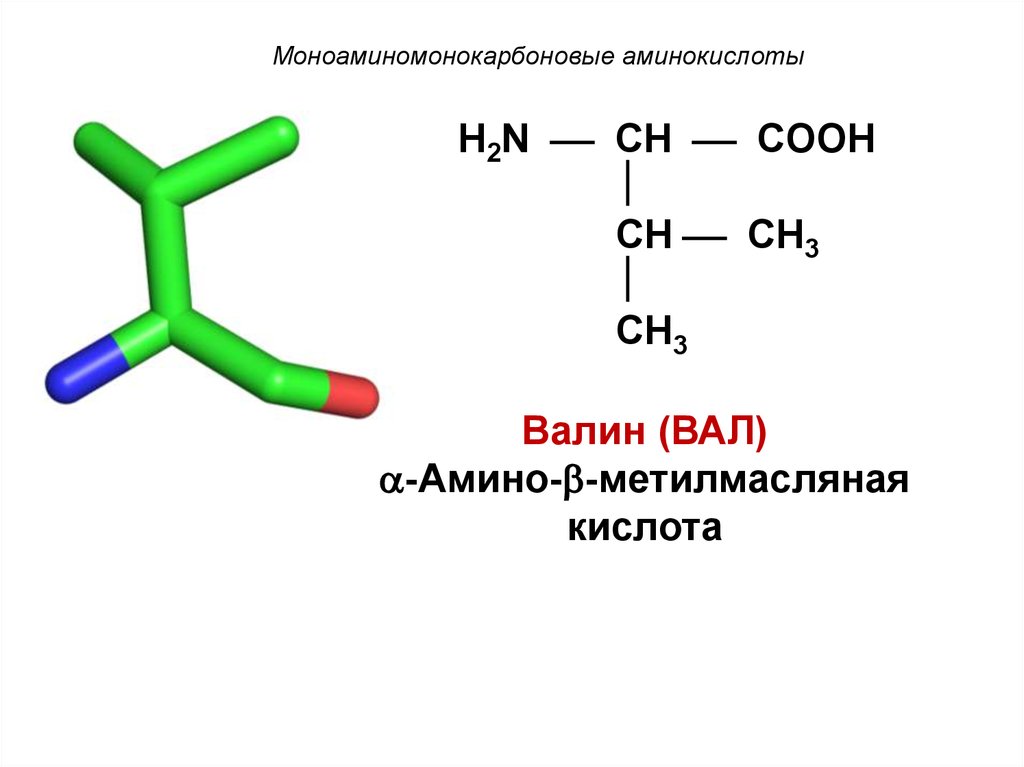
Моноаминомонокарбоновые аминокислотыH2N CH COOH
CH CH3
CH3
Валин (ВАЛ)
-Амино- -метилмасляная
кислота
11.
Моноаминомонокарбоновые аминокислотыH2N CH COOH
CH2
CH CH3
CH3
Лейцин (ЛЕЙ)
-Амино- -метилвалериановая кислота
12.
Моноаминомонокарбоновые аминокислотыH2N CH COOH
CH CH3
CH2
CH3
Изолейцин ( ИЛЕ )
-Амино- -метилвалериановая кислота
13. α-Аминокислоты, строение, номенклатура, изомерия
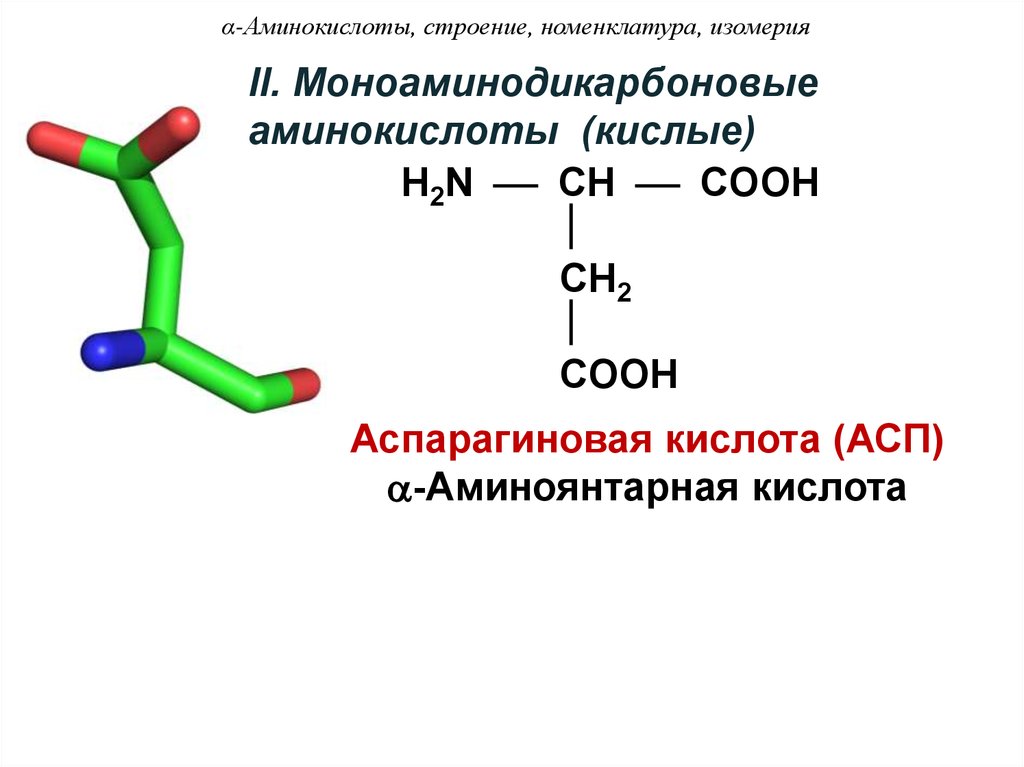
II. Моноаминодикарбоновыеаминокислоты (кислые)
H2N CH COOH
CH2
COOH
Аспарагиновая кислота (АСП)
-Аминоянтарная кислота
14.
Моноаминодикарбоновые аминокислотыH2N CH COOH
CH2
CH2
COOH
Глутаминовая кислота (ГЛУ)
-Аминоглутаровая кислота
Боковые радикалы
гидрофильные, ионогенные,
несут отрицательный заряд
(-OOC CH2 ).
15.
Моноаминодикарбоновые аминокислотыH2N CH COOH
CH2
CONH2
Аспарагин (АСН)
В состав белков
входят амиды данных
кислот.
16.
Моноаминодикарбоновые аминокислотыH2N CH COOH
CH2
CH2
CONH2
Глутамин (ГЛН)
17.
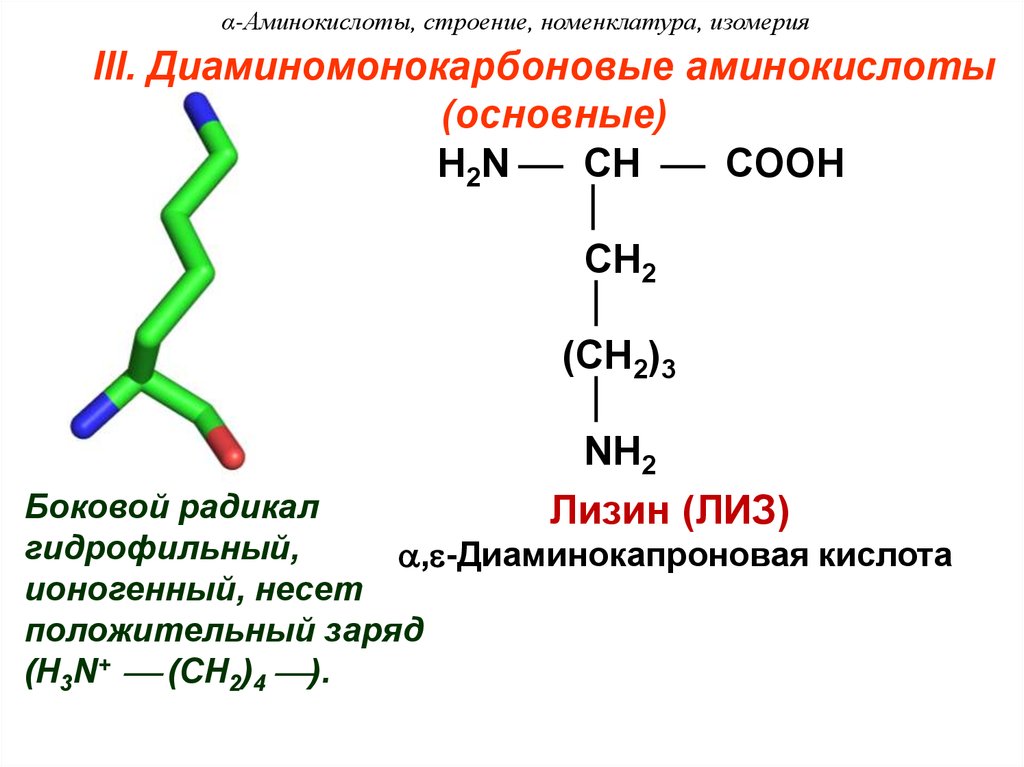
α-Аминокислоты, строение, номенклатура, изомерияIII. Диаминомонокарбоновые аминокислоты
(основные)
H2N CH COOH
CH2
(CH2)3
NH2
Боковой радикал
Лизин (ЛИЗ)
гидрофильный,
, -Диаминокапроновая кислота
ионогенный, несет
положительный заряд
(H3N+ (CH2)4 ).
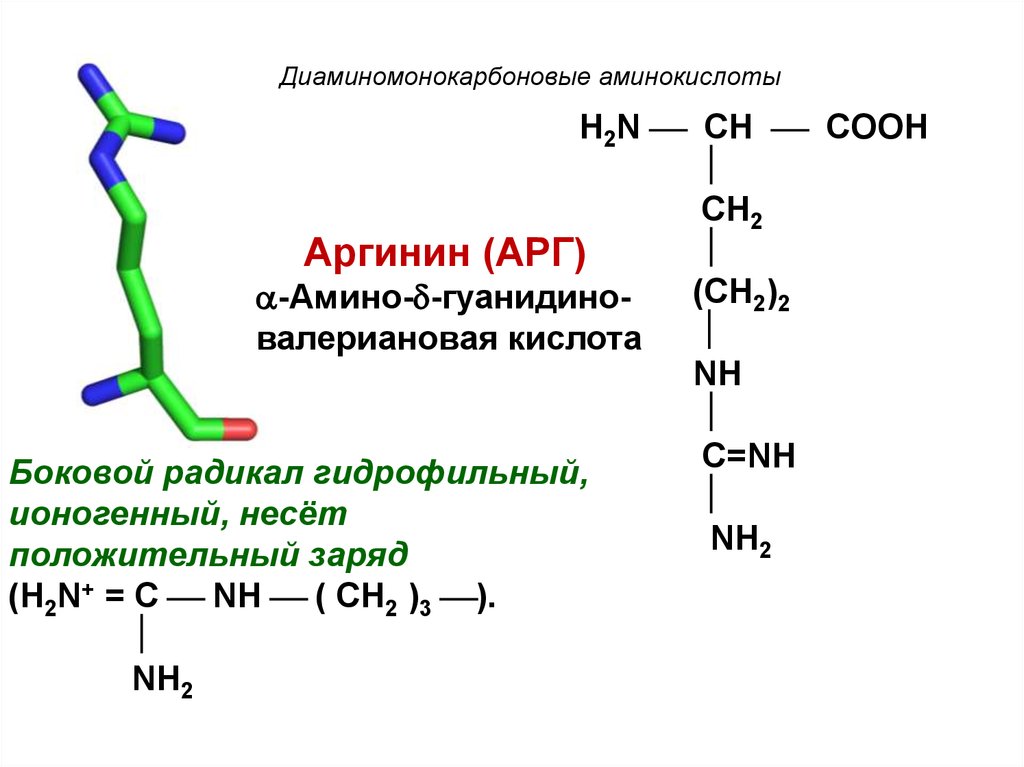
18.
Диаминомонокарбоновые аминокислотыH2N CH COOH
CH2
Аргинин (АРГ)
(CH2)2
-Амино- -гуанидино
валериановая кислота
NH
C=NH
Боковой радикал гидрофильный,
ионогенный, несёт
NH2
положительный заряд
(H2N+ = C NH ( CH2 )3 ).
NH2
19.
α-Аминокислоты, строение, номенклатура, изомерияIV. Оксиаминокислоты
H2N CH COOH
CH2 OH
Серин (СЕР)
-Амино- -оксипропионовая кислота
20.
ОксиаминокислотыH2N CH COOH
CH OH
CH3
Треонин (ТРЕ)
-Амино- -оксимасляная
кислота
Боковые радикалы
гидрофильные,
неионогенные (имеют
спиртовую природу).
21.
α-Аминокислоты, строение, номенклатура, изомерияV. Серосодержащие аминокислоты
H2N CH COOH
CH2 SH
Цистеин (ЦИС)
-Амино- -меркаптопропионовая
кислота
Боковой радикал
гидрофильный, ионогенный,
несёт отрицательный заряд
(- S CH2 ).
22.
Серосодержащие аминокислотыH2N CH COOH H2N CH COOH
CH2 S S CH2
Цистин (ЦИС-ЦИС)
, -Диамино- , -димеркаптопропионовая
кислота
Окисление
Боковой радикал гидрофобный.
23.
Серосодержащие аминокислотыH2N CH COOH
CH2
CH2 S CH3
Метионин (МЕТ)
-Амино- -метилтиомасляная
кислота
Боковой радикал гидрофобный.
24.
α-Аминокислоты, строение, номенклатура, изомерияVI. Ароматические -аминокислоты
H2N CH COOH
CH2
Фенилаланин (Фен)
-Амино- -фенилпропионовая
кислота
Боковой радикал
гидрофобный.
25.
Ароматические - аминокислоты.
H2N CH COOH
CH2
Тирозин (ТИР)
OH
-Амино- -параоксифенилпропионовая
кислота
Боковой радикал гидрофильный,
ионогенный, несёт отрицательный
заряд
26.
α-Аминокислоты, строение, номенклатура, изомерияVII. Гетероциклические -аминокислоты
H2N CH COOH
CH2
Гистидин (ГИС)
HN
N
N
NH
Боковой радикал
гидрофильный,
ионогенный несёт
положительный заряд
-Амино- -имидазолилпропионовая
кислота
H
27.
Гетероциклические - аминокислотыH2N CH COOH
CH2
Триптофан (ТРИ)
H
-Амино- -индолилпропионовая
кислота
Боковой радикал
гидрофобный, неионогенный.
28.
ИминокислотыOH
H
H
Пролин ( ПРО ) Оксипролин ( ОПР )
У пролина боковой радикал гидрофобный,
неионогенный, у оксипролина –
гидрофильный, ионогенный.
29.
α-Аминокислоты, строение, номенклатура, изомерияII. По способности синтезироваться в организме
аминокислоты делятся на заменимые и
незаменимые.
К незаменимым
аминокислотам
относят: валин,
изолейцин, лейцин,
триптофан,
фенилаланин,
метионин, лизин,
треонин.
30.
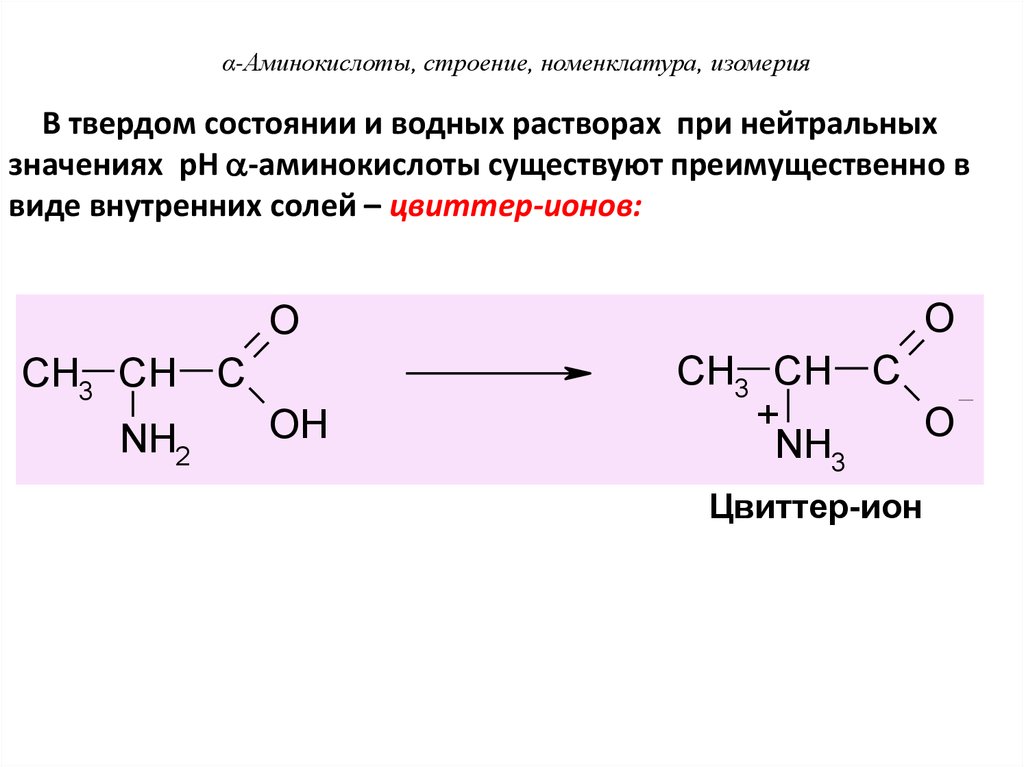
α-Аминокислоты, строение, номенклатура, изомерияВ твердом состоянии и водных растворах при нейтральных
значениях pH -аминокислоты существуют преимущественно в
виде внутренних солей – цвиттер-ионов:
O
O
CH3 CH C
NH2
OH
CH3 CH C
+
O
NH3
Цвиттер-ион
31.
α-Аминокислоты, строение, номенклатура, изомерияВ сильнокислой среде преобладает катионная форма,
в сильнощелочной - анионная.
+
CH3 CH
COOH
+
NH3
Катионная
форма
Сильнокислая
среда
-H
+
+H
CH3 CH
COO -
+
NH3
Цвиттер-ион
Нейтральная
+
-H
+
CH3 CH
+H
COO-
NH2
Анионная
форма
Сильнощелочная
среда
32. α-Аминокислоты, строение, номенклатура, изомерия
Значение pH, при котором концентрациядиполярных ионов максимальна, а минимальные
концентрации катионных и анионных форм аминокислоты равны, называется
изоэлектрической точкой (pI).
В изоэлектрической точке суммарный заряд
молекулы кислоты равен 0.
33. α-Аминокислоты, строение, номенклатура, изомерия
Для моноаминомонокарбоновых кислот pI ≈ 5-6,pI моноаминодикарбоновых кислот (Asp, Glu) ≈ 3,
pI диаминомонокарбоновых кислот (His, Lys, Arg) ≈ 8-11.
Если pH меньше pI, AK имеет положительный заряд и
движется к катоду. Если pH больше pI, AK имеет
отрицательный заряд и движется к аноду. Диполярные
ионы не перемещаются в электрическом поле.
34. α-Аминокислоты, строение, номенклатура, изомерия
На этом основано разделение-аминокислот методом
электрофореза.
35. α-Аминокислоты, строение, номенклатура, изомерия
In vivo при физиологических значения рН=7,347,36 α-аминокислоты и белки находятся в анионнойформе, отрицательный заряд которой
уравновешивается катионами натрия и калия.
36.
НоменклатураНазвания -аминокислот строятся по
рациональной и заместительной номенклатуре
ИЮПАК, но обычно используются их тривиальные
названия:
CH2 CH
OH
COOH
NH2
-амино- -гидроксипропионовая кислота
2-амино-3-гидроксипропановая кислота
серин
37.
ИзомерияСтруктурная изомерия
CH3
CH3
CH CH2 CH
CH3
COOH
NH2
лейцин
CH3 CH COOH
NH2
аланин
CH
CH3 CH2
CH
COOH
NH2
изолейцин
CH2 CH2 COOH
NH2
-аланин
38. Стереоизомерия
α - Аминокислоты - хиральные соединения,обладающие оптической активностью. Исключение
составляет глицин:
H2N CH2 COOH
Зеркало Венеры, 1898,
Edward Jones.
Все объекты на этой
картине имеют зеркальные
отображения.
39. Стереоизомерия
Относительная конфигурация аминокислот определяется поположению –NН2 группы у αуглеродного звена. Расположение
аминогруппы слева соответствует L-,
справа – D-конфигурации.
Почти все природные аминокислоты принадлежат
к L-ряду.
40.
СтереоизомерияCOOH
COOH
NH2
H
H
H2N
R
R
COOH
COOH
H
Формулы Фишера
NH2
R
D-аминокислота
Формулы с
H клиновидными
связями
H2N
R
L-аминокислота
41. Аминокислоты, строение, номенклатура, изомерия, классификация
COOHCH3
L - треонин
COOH
CH3
D - треонин
COOH
COOH
CH3
CH3
L - алло-треонин
D - алло-треонин
В состав белков входит L - треонин.
42.
Физические свойства-Аминокислоты - кристаллические вещества.
Имеют высокие температуры плавления (выше
200 С), нелетучие, растворимые в воде и
нерастворимые в неполярных органических
растворителях.
Способность -аминокислот растворятся в
воде является важным фактором обеспечения их
биологического функционирования - с нею
связаны всасываемость -аминокислот, их
транспорт в организме и т.п.
43.
Химические свойства-Аминокислоты - амфотерные соединения.
I. Реакции по группе -COOH
1. Солеобразование:
CH3 CH
NH2
аланин
COOH
+
NaOH
CH3 CH
COONa
+
H2O
NH2
2-аминопропионат натрия
44. Реакции по группе - COOH
Химические свойстваРеакции по группе - COOH
2. Реакция этерификации
R
CH
NH2
COOH
+
CH3OH
HCl газ
R
CH
COOCH3
+
H2O
NH2
Метиловый эфир аминокислоты
Используется для защиты карбоксильной группы
в синтезе пептидов
45.
Химические свойстваII. Реакции по группе –NH2:
1. Солеобразование
CH3 CH
COOH
NH2
аланин
+
HCl
CH3 CH
COOH
+
NH3
гидрохлорид
аланина
Cl
46. Взаимодействие с Cu(OH)2
Химические свойстваРеакции по группе –NH2:
Взаимодействие с Cu(OH)2
2 CH3 CH
COOH
+
Cu(OH)2
NH2
O
H3C
NH2
O
C
CH3
+
Cu
NH2
Хелатная соль меди
O
C
O
2 H2O
47. Реакции по аминогруппе 2.Ацилирование
Химические свойстваРеакции по аминогруппе
2.Ацилирование
O
R
CH
NH2
COOH
+
CH3 C
R
Cl
Хлористый ацетил
(Ацетилхлорид)
CH
COOH
+
HCl
NH
C O
CH3
ацетил
N-ацетиламинокислота
48. Химические свойства
II. Биологически важные химические реакции:1. Декарбоксилирование - путь образования биогенных
аминов из -аминокислот.
Процесс идет с участием ферментов декарбоксилаз:
N
N
CH2
H
гистидин
CH
COOH
декарбоксилаза
N
N
NH2
CO2
CH2
H
гистамин
CH2
NH2
49.
Химические свойстваДекарбоксилирование
CH2
N
CH
NH2
COOH
CH2
декарбоксилаза
N
H
CO2
триптофан
CH2
NH2
H
триптамин
50.
Химические свойства2. Дезаминирование - это реакция удаления
аминогруппы путем окислительного,
восстановительного, гидролитического или
внутримолекулярного дезаминирования.
В организме преобладает путь окислительного
дезаминирования: с участием ферментов
дегидрогеназ и кофермента - НАД+.
51. Окислительное дезаминирование in vivo
Химические свойстваОкислительное дезаминирование in vivo
R
CH
R
COOH
NH2
NAD+
NADH + H+
C
COOH
NH
H2O
иминокислота
R
C
COOH
O
кетокислота
На первой стадии процесса происходит
дегидрирование -звена с образованием иминокислоты, на второй стадии неферментативный гидролиз, приводящий к
образованию -кетокислоты.
NH3
52.
Дезаминирование53.
Химические свойства3. Трансаминирование (переаминирование) - это путь
синтеза необходимых -аминокислот из
кетонокислот.
При этом донором аминогруппы является -АК,
находящаяся в избытке, а акцептором аминогруппы кетонокислоты (ПВК, ЩУК, -кетомаслянная кислота).
Процесс происходит с участием фермента трансаминазы и кофермента пиридоксальфосфата.
54. Трансаминирование
Химические свойстваТрансаминирование
R
CH
COOH
1
+
R
C
NH2
COOH
Трансаминаза
O
Аминокислота I
Кетокислота I
R
C
O
Кетокислота II
COOH
+
1
R
CH
COOH
NH2
Аминокислота II
55.
Химические свойстваТрансаминирование
Процесс трансаминирования связывает обмен белков и
углеводов в организме, регулирует содержание и синтез
заменимых -аминокислот.
56. Пептиды и белки
Пептиды (греч. πεπτος — питательный) и белки биополимеры, построенные из -аминокислот.Пептиды содержат до 100, белки свыше 100,
олигопептиды - не более 10 аминокислотных
остатков. Молекулярная масса пептидов до 10000,
белков от 10000 до нескольких миллионов.
57.
Функции белков1. Ферментативная
2. Структурная
3. Питательная
4. Защитная функция
5. Транспортная
6. Регуляторная
7. Запасающая
8. Двигательная
58. Классификация пептидов и белков
II. По составу белки делят на простые(неконъюгированные)
и
сложные
(конъюгированные). Сложные белки состоят из
белковой и небелковой простетической группы.
По ряду характерных свойств простые белки
можно разделить на несколько подгрупп:
альбумины, глобулины, гистоны, протамины,
проламины, склеропротеины.
К сложным белкам относятся: фосфопротеины,
нуклеопротеины,
хромопротеины,
гликопротеины, липопротеины.
59.
Пептиды и белкиСхема образования пептидов
H
O
NH2 CH
R
H
C
N
OH
NH2 CH
R
CH
COOH
-H2O
R
O
H
C
N
CH
R
Пептидная связь
COOH
дипептид
60.
Образование пептидовH
O
NH2 CH
CH3 CH
H
C
N
OH
H
O
H
CH C
CH2
N
OH
CH
COOH
CH2
OH
Треонин
NH2 CH
CH3 CH
Фенилаланин
O
H
O
H
C
N
CH C
N
CH2
OH
Тирозин
CH
CH2
OH
Треонил-Фенилаланил-Тирозин
OH
COOH
-H2O
61. Пептиды и белки
Названия пептидов строятся путёмпоследовательного перечисления
аминокислотных остатков, начиная с N-конца, с
добавлением суффикса -ил, кроме последней Сконцевой аминокислоты, для которой
сохраняется её полное название. Для остатка
аспарагиновой кислоты используется название
аспартил.
62.
Пространственное строение амиднойгруппы
1. Пептидная группа относится к р, - сопряженной системе.
Все атомы лежат в одной -плоскости.
2. За счет образования единого делокализованного 4 электронного облака вращение вокруг С-N связи
затруднено.
O
O
..
C
C
N
H
N
H
63.
Трипептидметиновый мостик
O
H
O
H
NH2 CH2 C
N
CH C
N
CH2
N-конец
CH
CH2
С-конец
CH2
CH2
CH2
NH2
COOH
OH
Глицил-лизил-тирозин
64. Пептиды и белки
Трипептид:NH2 CH
O
H
O
H
C
N
CH C
N
CH2
CH3
CH
CH2
SH
CH2
COOH
Глутамил-аланил-цистеин
COOH
65.
Изоэлектрическая точка белка (pI)Молекула белка имеет электрический заряд.
В нейтральной среде заряд белковой молекулы
определяется соотношением количества свободных
групп –COOH, –OH, –SH и –NH2 и степенью их
диссоциации.
66.
Изоэлектрическая точка белка (pI)Схематично диссоциацию
можно представить в виде:
COOH
R
учетом
R
гидратации)
COO- + H+
COOH
+ HOH
NH2
(с
R
NH3OH
NH3+ + OHбиполярный
ион
(цвиттер-форма)
67. Изоэлектрическая точка белка
Чем больше –COOH, –OH, –SH групп, тем вышеотрицательный заряд, и белок будет проявлять
свойства слабой кислоты.
Преобладание –NH2-групп сообщает белку
основные свойства и положительный заряд.
В сильнокислой среде белок заряжается
положительно, в сильнощелочной отрицательно.
68.
Химические свойства пептидов и белковI. Аминокислоты, пептиды и белки
являются амфотерными соединениями,
содержащими и кислотные группы (–COOH)
и оснóвные группы (–NH2).
69. Химические свойства
II. По месту пептидных связей молекулы белковгидролизуются:
а) in vivo с участием ферментов - пептидаз. Среди
пептидаз выделяют:
- эндопептидазы, расщепляющие связи внутри макромолекулы;
- экзопептидазы, отщепляющие N- или C- концевую
аминокислоту.
В организме белки расщепляются полностью, т.к. для
жизнедеятельности необходимы только свободные аминокислоты.
70. Химические свойства пептидов и белков
б) Гидролиз in vitro происходит всильнокислой или сильнощелочной
среде и используется для расшифровки
состава белков. В настоящее время
расшифрован состав 1500 белков, в том
числе ферментов и гормонов.
71. Биуретовая реакция
Цветные реакцииБиуретовая реакция
В реакцию вступают все пептиды и
белки, содержащие не менее двух
пептидных связей. Реактив свежеприготовленный раствор
гидроксида меди (II). Наблюдается
характерное фиолетовое
окрашивание. Пептиды и белки
реагируют аналогично биурету.
72. Биуретовая реакция
Химические свойства пептидов и белковБиуретовая реакция
Биурет образуется из мочевины при
медленном нагревании до температуры
150 - 160 С.
O
O
O
O
H2N - C - NH2 + H2N - C - NH2 H2N - C - NH - C - NH2
- NH3
Биурет
73. Биуретовая реакция
При взаимодействии пептидов в щелочныхрастворах с ионами меди (II) образуется хелатный
комплекс (фиолетовое окрашивание).
74. Нингидринная реакция на - аминокислоты
Химические свойства пептидов и белковНингидринная реакция на - аминокислоты
Реактив - нингидрин. Продукт реакции
имеет сине-фиолетовый цвет.
O
O
OH
OH
O
+ RCHCOO H
NH2
O
+ RCHO + CO 2 + 3H2O
N
O
O
75. Ксантопротеиновая реакция
Химические свойства пептидов и белковКсантопротеиновая
реакция
Определяет присутствие в
белке ароматических и
гетероциклических
- аминокислот:
• триптофана,
• фенилаланина,
• тирозина,
• гистидина.
76. Ксантопротеиновая реакция
Химические свойства пептидов и белковКсантопротеиновая реакция
Реактив: конц. HNO3
Образуется нитросоединение,
окрашенное в желтый цвет. При
добавлении к нему щёлочи окраска
становится оранжевой.
77. Реакция Миллона на тирозин
Химические свойства пептидов и белковРеакция Миллона на тирозин
Реактив Миллона: раствор
HgNO3 и Hg(NO2)2 в
разбавленной HNO3,
содержащей примесь HNO2.
78. Реакция Миллона
Химические свойства пептидов и белковРеакция Миллона
Реактив Миллона взаимодействует с тирозином с
образованием ртутной соли нитропроизводного
тирозина, окрашенной в розовато-красный цвет:
79. Реакция Фоля
Химические свойства пептидов и белковРеакция Фоля
Это реакция на цистеин и цистин.
80. Реакция Фоля
Химические свойства пептидов и белковРеакция Фоля
При щелочном гидролизе цистеина или цистина
образуется сероводород, который, реагируя со
щелочью, дает сульфиды натрия или калия. При
добавлении ацетата свинца (II) образуется осадок
сульфида свинца( II) серо-черного цвета.
81.
Уровни структурной организации белка82. Первичная структура
Первичная структура – последовательностьаминокислотных остатков в молекуле белка
или пептида:
NH2-Tyr-Pro-Lys-Gly-Phe-Tyr-Lys-COOH.
Первичная структура определяет уровни
структурной организации белка.
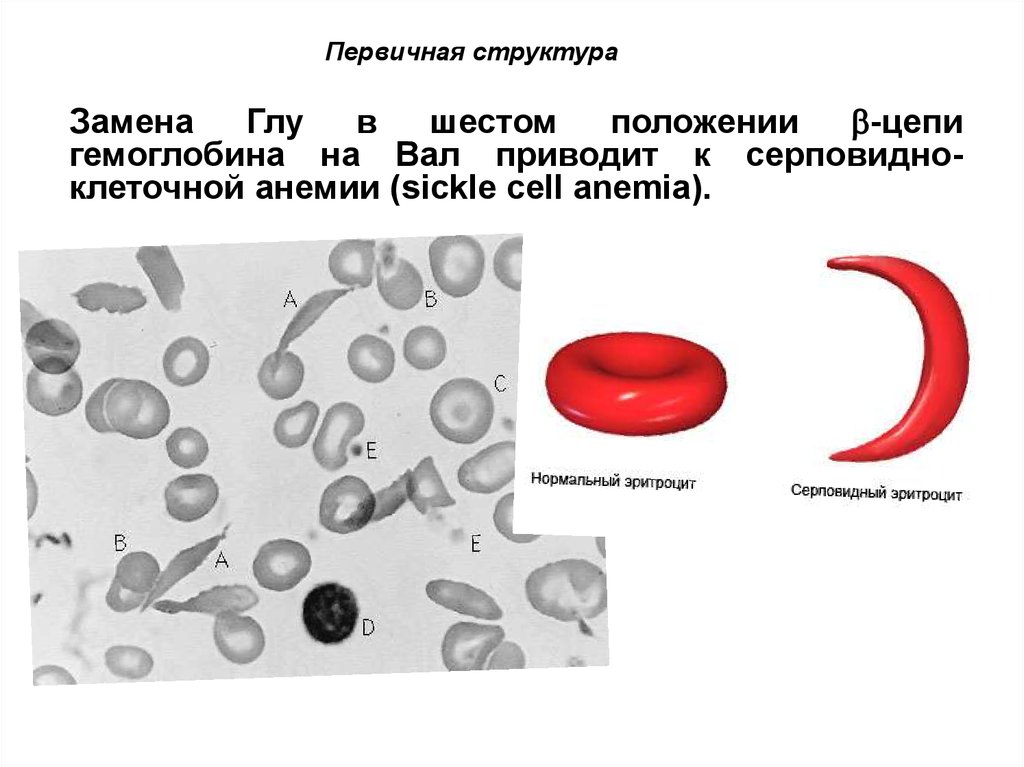
83.
Первичная структураЗамена
Глу
в
шестом
положении
-цепи
гемоглобина на Вал приводит к серповидноклеточной анемии (sickle cell anemia).
84.
Первичная структура20
аминокислот
могут
дать
примерно
1000000000000000000000000000000000000000000000
0000000000000000000000000000000000000000000000
0000000000000000000000000000000000000000000000
0000000000000000000000000000000000000000000000
00000000000000000 белков.
Это астрономическое число
умноженное на число гугол
(число гугол – это 10100)
–
число
гугол
85. Вторичная структура
Вторичная структура - локальныевысокоупорядоченные конформации
белковой цепи – спирали и
складчатые слои.
Примеры:
Альфа-спираль
Бета-складчатый лист
Водородные связи
86.
Вторичная структураПравые -спирали в полипептидной цепи
стабилизируются водородными связями.
87.
Вторичная структураВторичная структура также
стабилизуется
дисульфидными мостиками
по месту цистеиновых
остатков.
88. Водородные связи в a-спиралях -Вал-Фен-Тир-Ала-Лей-
Водородные связи в -спиралях-Вал-Фен-Тир-Ала-Лей-
H
N
CH
CH3 CH
O
H
O
H
O
H
O
H
C
N
CH C
N
CH C
N
CH C
N
CH2
CH2
CH3
O
CH
C
CH2
CH
H3C
CH3
CH3
OH
Остатки АК: Первый
Второй
Третий
Четвёртый
-спираль – 413 спираль: остаток аминокислоты образует водородную связь с
четвёртым по цепи остатком -аминокислоты;
в образующемся цикле 13 атомов.
89. Структура b-складчатых слоев
Структура -складчатых слоев-Структура образуется из нескольких
полипептидых цепей связанных водородными
связями.
90. Структура b-складчатых слоев Водородные связи
Структура -складчатых слоевВодородные связи
OH
HO
COOH
CH3
CH O
NH2 CH
C
CH3 O
N
CH C
...H
CH3 CH
C
N
CH2 C
CH2 O
N
CH C
...
...
O
NH2 CH
O
CH2
N
CH
COOH
...
H
H
H
O
O
O
N
CH C
N
CH C
N
CH C
N
CH
H
CH2
H
CH2
H
CH3
H
CH2
COOH
CH
H3C
CH3
CH3
OH
Тре-Ала-Гли-Сер-Асп
Вал-Фен-Тир-Ала-Лей
91. Обозначение вторичной структуры
Укладка -спиралей и-структуры с
образованием
глобулы
92. Третичная структура
Третичная структура – форма белковоймолекулы; трёхмерная структура белка.
Укладка нерегулярных областей и и -структур в
глобулу определяет третичную структуру белка.
Альфа-спираль
Бета-спираль
93. Третичная структура
-Аминокислоты в белковой глобуле
взаимодействуют за счёт:
Ковалентных связей
(дисульфидные –S–S– связи в цистине)
Ионных связей
(Глу-COO- H3N+-Лиз)
Водородных связей
(Глу-COO-…HO-Тир)
Гидрофобных взаимодействий
(Вал, Лей, Иле, Фен)
94. Уровни структурной организации белка
95. Дисульфидные связи в цистине
NHCH
C
R
O
O
O
O
N
CH C
N
CH C
N
CH C
N
CH
H
R
H
CH2
H
R
H
R
COOH
S
S
R
OC
R
H
CH N
C
O
CH2 H
H
CH N
C
O
CH N
R
C
O
H
CH N
R
C
O
CH
NH2
96. Дисульфидные связи
Структура лизоцима.Дисульфидные связи
показаны пунктиром
97. Ионные связи
OO
O
N
CH C
N
CH C
N
CH C
N
CH
H
R
H
CH2
H
R
H
R
Асп
O
C
COOH
O
H
+
H N H
Лиз
CH2
CH2
CH2
R
C
O
CH
H
N
R
CH2 H
C
O
CH
N
C
O
R
H
CH N
C
O
CH NH2
98. Третичная структура
По третичной структуре белки делят на:глобулярные - для них характерна
-спиральная структура (яичный белок,
ферменты, глобин в составе гемоглобина);
фибриллярные - для них характерна
-структура (белки мышечной ткани - миоинозин,
бетта-кератин волос).
99. Пептиды и белки
Глобулярные белки выполняют функции,требующие подвижности и, следовательно,
растворимости.
Они участвуют в регуляции жизненных
процессов: гемоглобин переносит кислород из
лёгких в ткани, ферменты катализируют
многочисленные
химические
реакции,
протекающие
в
организме,
антитела
обеспечивают
защиту
от
чужеродных
организмов и т.д.
100. Пептиды и белки
Фибриллярные белки нерастворимы, склоннык образованию волокон и потому служат
основным строительным материалом животных
клеток.
К числу фибриллярных белков относятся
кератин (в коже, волосах, рогах, ногтях, перьях),
коллаген (в сухожилиях), миозин (в мышцах).
101. Третичная структура
Сериновая протеиназа - трипсинРодопсин
102. Третичная структура
Ацилтрансфераза (КФ 2.3)Пиктатлиаза С
103. Третичная структура
Митохондриальнаясупероксиддисмутаза (КФ 1.15.1.1)
104.
Глиоксилаза I (КФ 4.4.1.5)Figura 4: Cofactores
105.
Цитохром C106. Третичная структура
- и -цепи гемоглобина лошади107. Третичная структура
Параллельные -слоикарбоангидразы
Антипараллельные -слои
лектина
108. Третичная структура
Порин109.
Фолдинг – сворачивание белковой цепи с образованиемнативной структуры.
110.
Две нативные конформациилимфотактина
111.
Белок PrPCЭтот
белок
может
существовать
в
двух
конформациях
–
“здоровой” PrPC, которую
можно
обнаружить
в
здоровых
клетках
и
“патологической” – PrPSc,
которая
является
прионом. Для PrPC формы
характерно преобладание
-спиралей, а для PrPSc –
наличие
-складчатых
слоёв.
112.
Губчатые энцефалопатии (прионныеболезни)
Пространственная
структура приона
– аномального
инфекционного
белка.
Болезнь
Крейтцфельда-Якоба
Новый вариант
Крейцфельда-Якоба –
коровье бешенство
Болезнь Герстманна–
Штройсслера
Летальная семейная
Абориген с
инсомния,
Южных гор
куру
Папуа-Новая
Гвинея.
113. Домены
Домены – глобулярные области в пределах однойбелковой молекулы.
Домены соединены шарнирным участком.
Доменная структура
NAD+-зависимой дегидрогеназы
114. Четвертичная структура
Четвертичная структура - агрегат нескольких белковыхмолекул, образующих одну структуру.
Взаимодействия: ионные, водородные, гидрофобные,
ковалентные (дисульфидные).
Протомер - отдельная полипептидная цепь
Субъединица - функциональная единица.
Субъединица
115.
Молекулагемоглобина состоит
из 4-х субъединиц,
каждая из которых
включает в себя
активный центр – гем.
Субъединицы
удерживаются друг
около друга
гидрофобными
связями.
116. Дисульфидные связи
Дисульфидные связи в иммуноглобулине G117. Четвертичная структура
Фермент состоит изполипептидных
цепей двух типов
— М (от англ.
muscle - мышца) и
Н (от англ. heart –
сердце).
Лактатдегидрогеназа (КФ 1.1.1.27)
118. Четвертичная структура
Пример четвертичной структуры - вирус табачноймозаики: 2130 одинаковых молекул белка
расположены вокруг РНК вируса.
119. Вопросы для самоконтроля
1. Приведите классификацию -аминокислот взависимости от характера радикала.
2. Охарактеризуйте химические свойства
аминокислот.
3. Перечислите известные Вам цветные реакции на
-аминокислоты и белки.
4. Какие уровни структурной организации
белков Вы знаете?
120.
Спасибо за Вашевнимание!


















































































































 Химия
Химия