Похожие презентации:
Строение атома. Атомные орбитали. Типы связей. Основные органогенные элементы, их роль
1. Строение атома. Атомные орбитали. Типы связей. Основные органогенные элементы, их роль
Шлахтер М.Л.Харьков - 2016
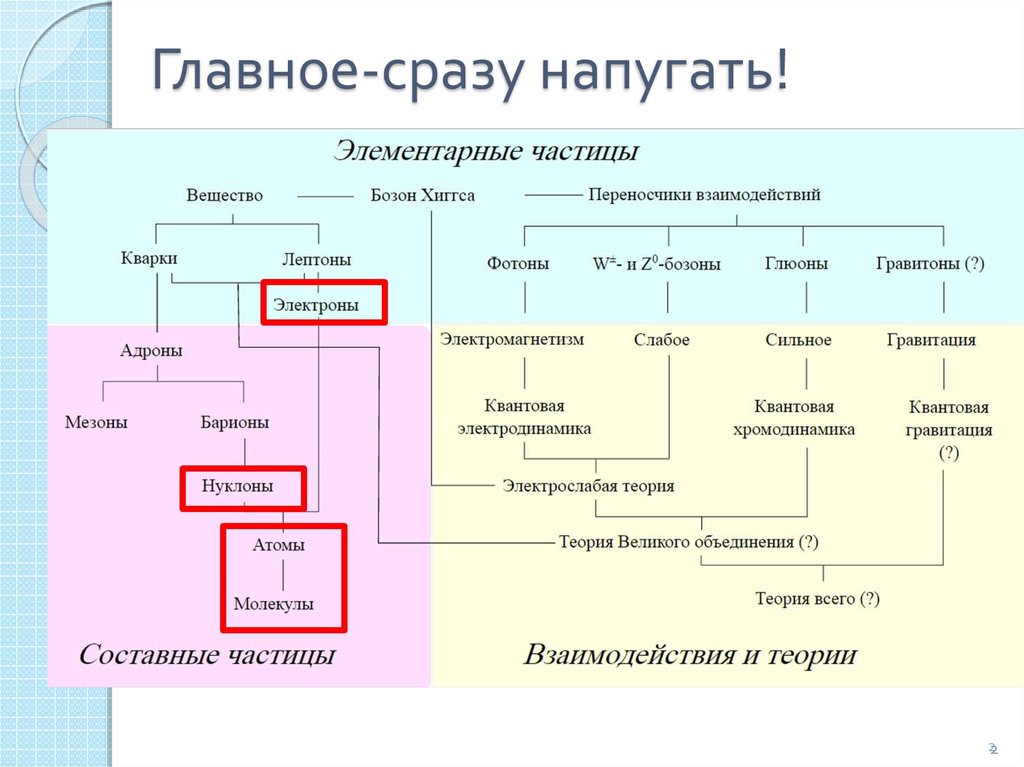
2. Главное-сразу напугать!
23. Строение атома
CHe
4. Типы атомных орбиталей
5. Орбитальная формула атома
56. Каждый уважающий себя атом стремится к электронному состоянию инертного газа!
Нужно отдать электрон – ты донор, как правило, металлНужен электрон – ты акцептор, как правило, неметалл
6
7. Чем сильнее атому нужен электрон, тем он электроотрицательнее
8. Приобрёл стабильность – стал ионом!
89. Понял, что нужно атому – понял, что такое валентность
10. Химическая связь
КовалентнаяОдноэлектронная
Ионная
Одинарная/
кратная
Трёхцентровая/
многоцентровая
n е
е
n
Неполярная
Сэндвичева
n
Полярная
Водородная
Ван-дерваальсова
Металлическая
11. Структура кристалла
Кристаллы NaCl под бинокуляром11
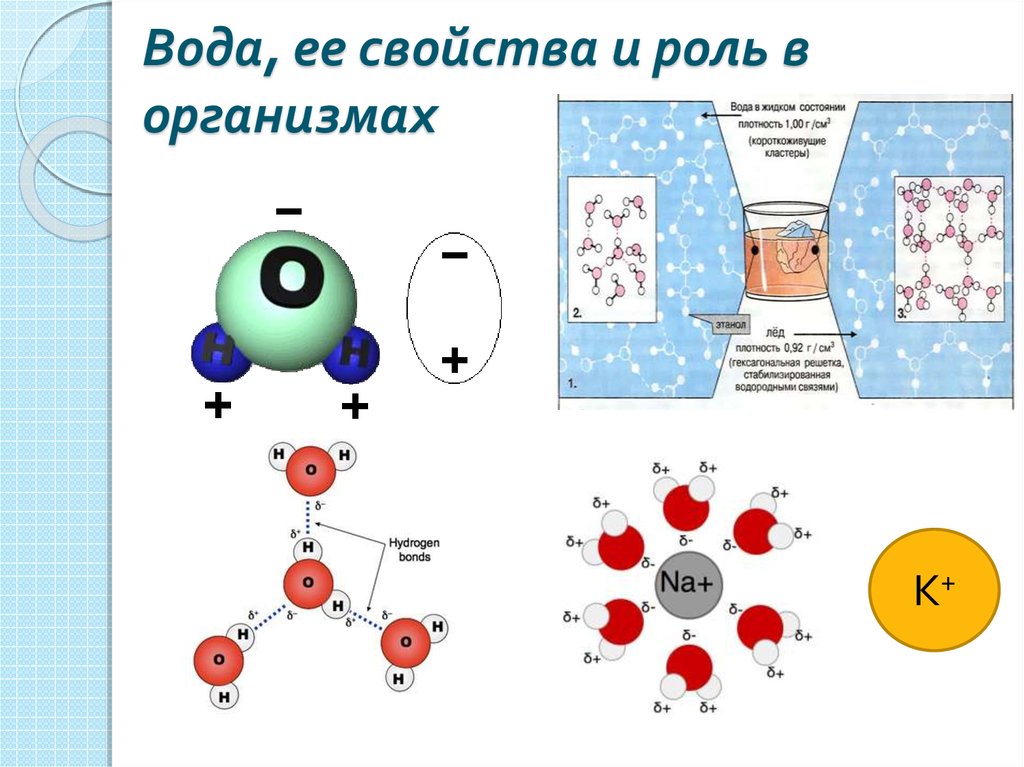
12. Вода, ее свойства и роль в организмах
К+13. Водородные связи
Поверхностное натяжение воды,вязкость
Поддержание структуры белка
Поддержание структуры нуклеиновых
кислот
Поддержание структуры углеводных
полимеров
Гидрофобные взаимодействия
13
14. Гидрофобные взаимодействия
Правилопервое:
полярному
хорошо с
полярным
Правило
второе:
неполярному
хорошо с
неполярным
15. Гидрофобность и гидрофильность
1516. Ван-дер-ваальсовы взаимодействия
Сцепление частиц малых астероидов кольца́ СатурнаСпособность гекконов взбираться по гладким поверхностям, например, по
стеклу
В системе редактирования геномов TALEN второй аминокислотный остаток в
Repeat Variable Diresidue (RVD) взаимодействует с нуклеотидом,но при этом
природа этого взаимодействия различна: аспарагин и аспарагиновая кислота
образуют водородные связи c азотистыми основаниями, а изолейцин и глицин
связываются с целевым нуклеотидом за счет сил Ван-дер-Ваальса.
16
17. Элементный состав человеческого организма
1718. Карбон (углерод)
Органическиесоединения
Карбонаты, оксиды
Карбона (СО, СО₂)
18
19. Оксиген (кислород)
ВодаПростые вещества (О₂,
окислитель)
Органические вещества
Соли неорганических кислот
(фосфаты, карбонаты)
Карбонат-анион
Фосфат-анион
19
20. Гидроген
Простые вещества (катионыводорода Н⁺)
Вода
Все органические соединения
Неорганические кислоты
Если молекула диссоциирует с
образованием протона, то это
Аррениус
кислота, если с образованием
гидроксил-аниона, то это
основание
Хлоридная кислота
21. Нитроген
Тройная связь в молекуле азота(N₂)
Аминокислоты , белки
Хлорофилл
Продукты метаболизма
(алкалоиды растений, мочевина
животных)
АТФ
Нуклеиновые кислоты
Аммиак
NH3+H2O ↔ NH4OH ↔ NH4+ + HO-




















 Химия
Химия








