Похожие презентации:
Введение в биохимию
1. КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КУБАНСКИЙ МЕДИЦИНСКИЙ ИНСТИТУТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ
Лекция по теме:«ВВЕДЕНИЕ в БИОХИМИЮ»
КРАСНОДАР
2008
2. БИОХИМИЯ -
наука, изучающая химическийсостав живых организмов,
химические процессы,
которые лежат в основе
жизнедеятельности и
обеспечивают организму
сложную морфологическую
целостность и высокую
функциональную активность
3. ГЛАВНАЯ ЗАДАЧА БИОХИМИИ -
ПОЗНАНИЕХИМИЧЕСКИХ ОСНОВ
ЖИЗНИ, УСЛОВИЙ И
МЕХАНИЗМОВ ЕЕ
ВОЗНИКНОВЕНИЯ И
РАЗВИТИЯ
4. Основные признаки живого:
• Важнейшее проявление жизни– непрекращающийся обмен
веществом и энергией
организма с окружающей
средой;
5.
• Сложность и высокийуровень структурной
организации живого;
6.
• Наличие строго определенныхфункций у каждого компонента
живого;
• Способность к точному
самовоспроизведению
(способность к росту,
самообновлению,
размножению);
7.
• Необходимостьподдержания постоянства
условий существования;
8. СТРУКТУРНАЯ ОРГАНИЗАЦИЯ ЖИВОГО
Тип соединенияКомпоненты
Предшественники, Аммиак, СО2, Н2О
поступающие из
внешней среды
Промежуточные
Кетокислоты, рибоза,
соединения
карбамоилфосфат,
ацетат, малат
Строительные
Аминокислоты,
блоки
моносахара, жирные
кислоты,
мононуклеотиды
Молеку
лярная
масса,
Да
18-44
50-250
100-350
9.
МакромолекулыБелки, липиды,
сложные углеводы,
нуклеиновые кислоты
Надмолекулярные Полиферментные
комплексы
системы, рибосомы,
сократительные
системы
Клеточные
Ядро, митохондрии,
органеллы
микросомы, лизосомы
ЖИВАЯ КЛЕТКА
3
6
10 - 10
3
9
10 - 10
10. Метаболизм -
Метаболизм Совокупность химическихпревращений веществ от
момента поступления его в
клетку до выделения
конечных продуктов
11. Метаболизм
Катаболизм –совокупность
поэтапных
ферментативных
процессов
расщепления
сложных молекул до
простых.
Идет с
высвобождением
энергии –
экзэргонический
процесс
Анаболизм –
совокупность
поэтапных
ферментативных
процессов построения
сложных веществ из
более простых
предшественников.
Идет с затратой
энергии,
эндэргонический
процесс
12. Разделы биохимии:
• Статическая биохимия;• Динамическая;
• Функциональная;
• Молекулярная биология.
13. Задачи медицинской биохимии:
• Изучение химическогосостава и химических
процессов, протекающих в
больном и здоровом
организме;
14.
• Разработка методов,позволяющих выявлять
нарушение биохимических
процессов с целью
диагностики заболеваний;
15.
• Разработка основфармакотерапии и
• рационального питания
здорового и больного
человека.
16. Объекты биохимического исследования
Целостный организм;
Изолированные органы;
Срезы органов и тканей;
Гомогенаты тканей;
Субклеточные структуры;
Молекулы.
17. Методы биохимии
• Химические (качественный иколичественный анализ);
• Физические (изотопный,
ультрацентрифугирования,
ультразвуковой);
• Физико-химические (рН, хроматография,
электрофорез, диализ);
• Гистологический;
• Биологический (опыты на животных);
• Биохимический (ферментативный анализ).
18. 1903 год Карл Небберг
Предложил термин биохимия.Биохимия-наука о химическом
составе живых организмов,
химических превращениях,
протекающих в организме
животных и растений
19.
Ганс Карл Симонфон Эйлер (ван Улер)
немецко-шведский
биохимик (1873-1964).
Выдающаяся личность:
лауреат Нобелевской
премии (1929 г.), Большого
креста Федеральной службы
ФРГ (1959 г.). Почетный
академик 7 университетов
мира.
Создал первый
учебник по
медицинской
химии
20.
А. Я. Данилевский( 1838 - 1923 )
Первая кафедра
медицинской
химии
(1862 год)
21. Готе-Зебер (1866 год)
Создал первую кафедрубиологической химии в
Германии
22.
Н.И. ЛунинИзучение
витаминов
23.
А.М. БутлеровА.Я. Данилевский
24.
ЭрвинЧАРГАФФ
25. Авторы модели двойной спирали ДНК Джеймс Уотсон и Фрэнсис Крик
26.
А.Н. Белозерский(1905–1972).
Биохимик
растений, один
из основателей
молекулярной
биологии в
России,
академик АН
СССР (1962)
27.
ВладимирПетрович
Скулачев
академик РАН,
доктор
биологических
наук,
профессор
28.
АлександрИванович
Арчаков
академик
РАМН,
профессор,
доктор
медицинских
наук
29. Профессор Н.П.Пятницкий – основатель кафедры биохимии КГМУ
30. Профессор С.И. Крайнев
31. Профессор П.Г.Сторожук
32. Профессор И.М. Быков
33. Направления научной работы кафедры
Гастроэнтеро- Гематологическоелогическое
34. Открытия кафедры фундаментальной и клинической биохимии КГМУ
35.
36.
37.
38.
39. БЕЛКИ-
БЕЛКИВЫСОКОМОЛЕКУЛЯРНЫЕАЗОТСОДЕРЖАЩИЕ
ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ,
МАЛО ОТЛИЧАЮЩИЕСЯ ПО
ЭЛЕМЕНТАРНОМУ СОСТАВУ, НО
РЕЗКО ОТЛИЧАЮЩИЕСЯ ПО
ХИМИЧЕСКОМУ СОСТАВУ,
СТРОЕНИЮ, СВОЙСТВАМ,
ФУНКЦИЯМ И СОСТАВЛЯЮЩИЕ
ОСНОВУ ВСЕГО ЖИВОГО
40. Элементарный состав белков (%)
УглеродКислород
Азот
Водород
Сера
50,5-54,5
21,5-23,5
15,0-17,6
6,5-7,3
0,5-2,5
41. Химический состав белков (аминокислотный)
ЗаменимыеНезаменимые
Глицин
Аланин
Серин
Цистеин
Аспарагиновая к-та
Глутаминовая к-та
Тирозин
Цистин
Пролин
Оксипролин
Метионин
Валин
Лейцин
Изолейцин
Треонин
Лизин
Фенилаланин
Триптофан
Аргинин
Гистидин
42. Строение пептида Радикалы аминокислот
43. Молекулярная масса белков, Да
Инсулин (быка)5 700
Рибонуклеаза
Лизоцим
Миоглобин
13 680
13 930
16 890
Химотрипсин
22 600
Гемоглобин
64 500
Сывороточный альбумин
68 500
Гексокиназа
Глутаматдегидрогеназа
102 000
1 000 000
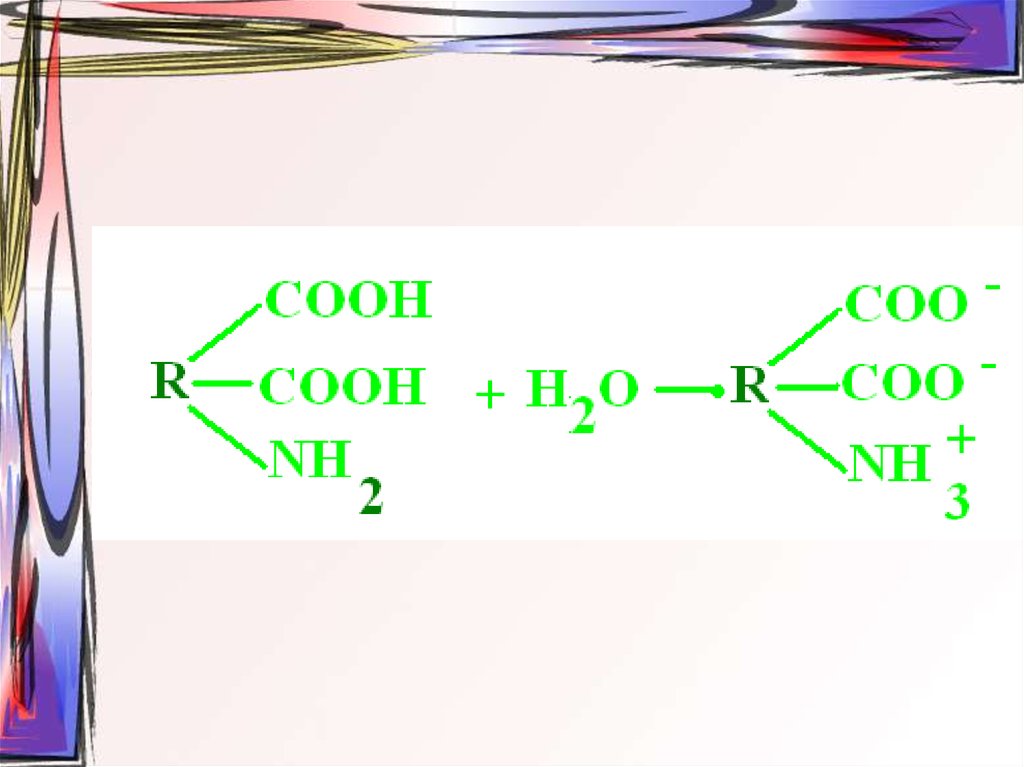
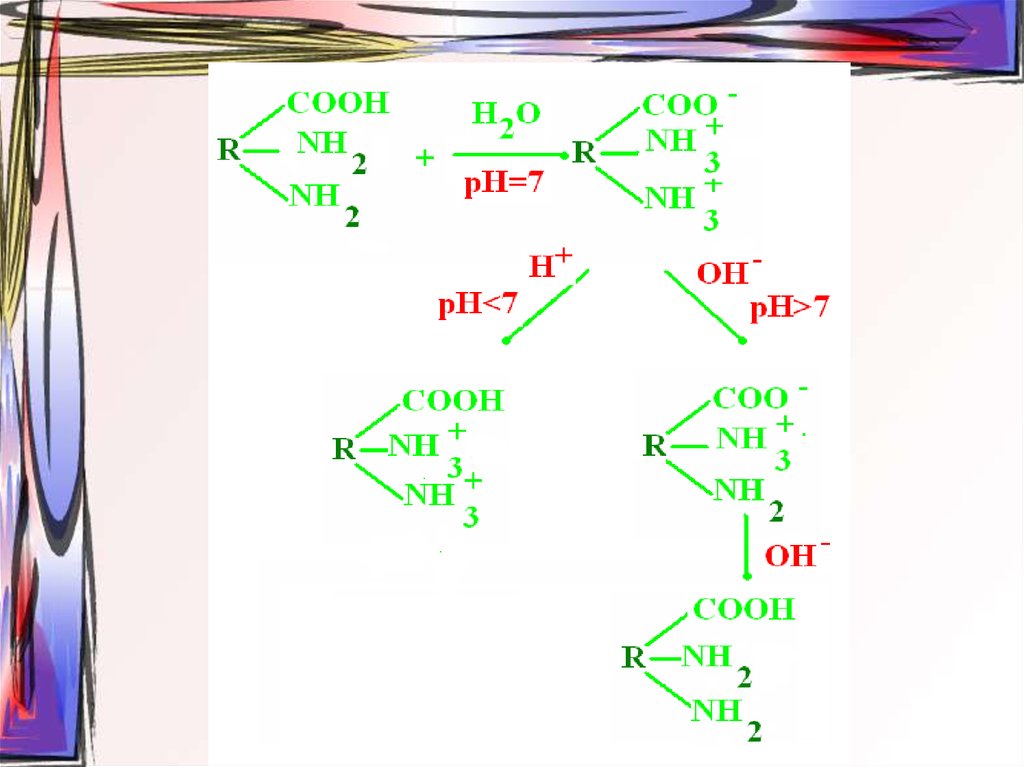
44. Заряд белковой молекулы
45.
46.
47. Физико-химические свойства белков:
• Растворимость;• Гидратация;
• Ионизация.
48. Классификация белков по растворимости
ГидрофильныеГидрофобные


















































 Биология
Биология Химия
Химия








