Похожие презентации:
Классы неорганических соединений
1.
Классынеорганических
соединений
2.
Веществапростые
металлы
сложные
неметаллы
оксиды
ЭО-2
основания
кислоты
соли
МОН
НА
МА
3. Оксиды- бинарные соединения, в которых кислород стоит на втором месте и имеет степень окисления (-2)
ЭОЭ-элемент
4.
Начертите таблицу на страницуОксид
Название
Выпишите формулы оксидов
в левый столбик
5.
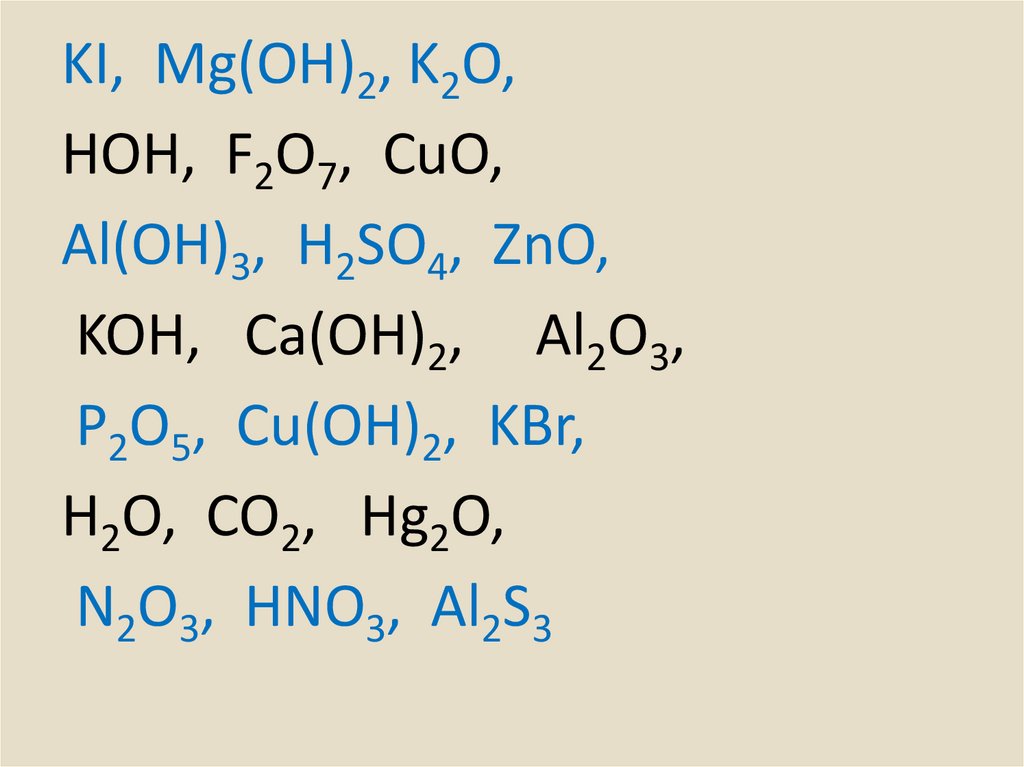
KI, Mg (OH)2, K2O,HOH, F2O7, CuO,
Al(OH)3, H2SO4, ZnO,
KOH, Ca(OH)2, Al2O3,
P2O5, Cu(OH)2, KBr,
H2O, CO2, Hg2O,
N2O3, HNO3, Al2S3
6. Оксиды
• Основные: Э-металл (главные подгруппы I иII групп) или (побочная подгруппа с
валентностью I или II )
• Кислотные: Э- неметалл или элементы
побочных подгрупп(металлы) с
валентностью V и более
• Амфотерные: Э- переходный (Zn, Al,Fe, Cr)
или элементы побочных подгрупп с
валентностью III или IV
7.
K2OF2O7
CuO
ZnO
Al2O3
P2O5
H2O
CO2
Hg2O
N2O3
8. Номенклатура оксидов
“Оксид”+ ”элемента”
+ “переменная валентность”
K2O –оксид калия
P2O3 –оксид фосфора (III)
9. Составьте формулы оксидов
1. Составьте формулы оксидов• Оксид марганца (II)
• Оксид марганца (IV)
• Оксид марганца (VII)
• Оксид хрома (III)
• Оксид хрома (VI)
• Оксид хрома (II)
2. Определите характер оксидов.
10. Основания
-сложные соединения металловс гидроксогруппой (ОН-).
Число гидрокогрупп равно
валентности металла.
М(ОН)n
11.
Продолжите таблицуОснование
Название
Выпишите формулы
оснований в левый столбик
12.
KI, Mg(OH)2, K2O,HOH, F2O7, CuO,
Al(OH)3, H2SO4, ZnO,
KOH, Ca(OH)2, Al2O3,
P2O5, Cu(OH)2, KBr,
H2O, CO2, Hg2O,
N2O3, HNO3, Al2S3
13. Основания
Щелочи- растворимые в водеоснования.
Гидроксиды ( ) –нерастворимые
в воде основания.
14.
Mg(OH)2KOН
Al(OH)3
Ca(OH)2
Cu(OH)2
15.
Номенклатура оснований“гидроксид”
+ название металла
+ переменная валентность металла
Fe(ОН)3- гидроксид
железа (III)
16.
1. Составьте формулы основанийГидроксид хрома (III)
Гидроксид цинка
Гидроксид железа (II)
Гидроксид лития
2. Определите характер оснований
17.
Оксидосновный
Оксид
кислотный
Основание
Кислота
18.
Кислоты (НА)Н- водород
А- кислотный остаток
Н2SO4 –серная кислота
Валентность кислотного
остатка равна числу атомов
водорода
19.
Кислоты (НА)1. Выпишите формулы
кислот в столбик.
2. Назовите их.
3. Определите валентность
кислотного остатка.
Валентность кислотного остатка
равна числу атомов водорода
20.
KI, Mg (OH)2, K2O,H2S, F2O7, CuO,
Al(OH)3, H2SO4, H2CO3,
KBr, HNO3, Al2S3
21.
H2SH2SO4
H2CO3
HNO3
22.
Соли-это
сложные
вещества,
состоящие
из
ионов металлов и кислотных
остатков.
МА
23.
KIKBr
Al2S3
24.
номенклатураНазвание кислотного остатка
+ название металла
+ переменная валентность металла
FeCL3-
хлорид железа (III)
25.
Составьте формулы солейСульфат магния
Карбонат лития
Сульфит хрома (III)
Сульфид железа (II)






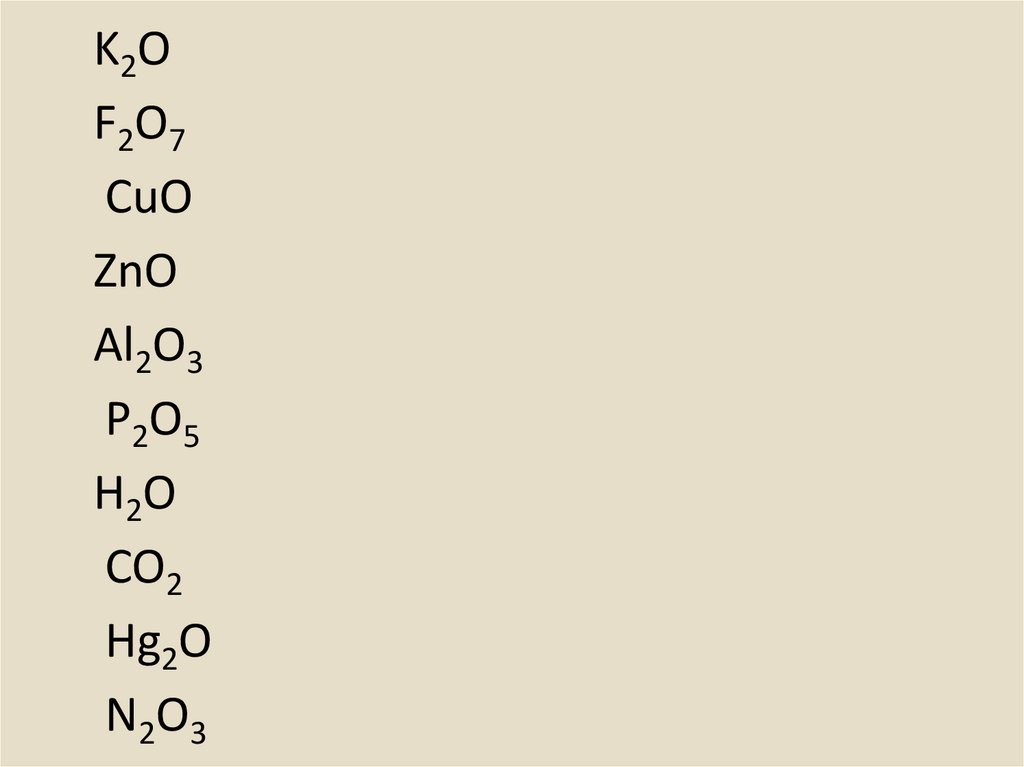

















 Химия
Химия








