Похожие презентации:
Характеристика элемента по положению в периодической системе
1. Характеристика элемента по положению в периодической системе
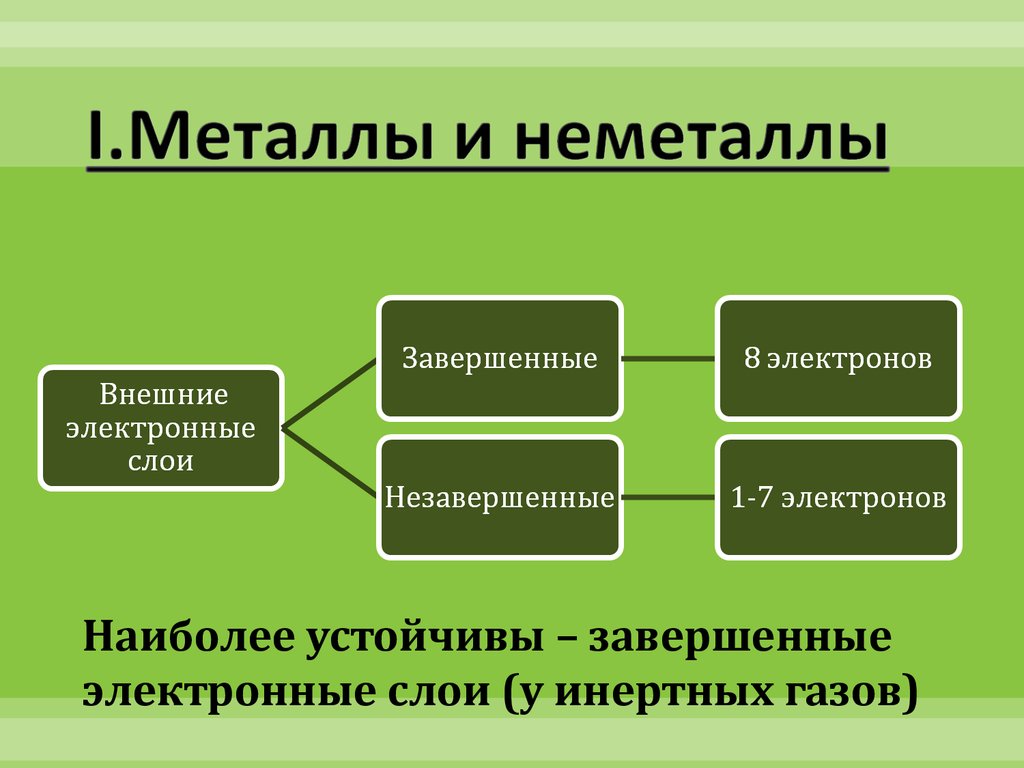
2. I.Металлы и неметаллы
Наиболее устойчивы – завершенныеэлектронные слои (у инертных газов)
3. Элементы начала периода Элементы конца периода Ме неМе
NaCl
+11
+17
2е 8 е 1 е
2е
8е
7е
4.
Атомы металловимеют
небольшое число
электронов на
внешнем
электронном
слое и большие
радиусы атомов,
следовательно
легко отдают
электроны
Me0 – ne Me+n
Атомы неметаллов
имеют большое
число электронов
на внешнем
электронном слое и
небольшие
радиусы атомов,
следовательно
легко принимают
электроны
неMe0 + ne Me-n
5. Энергия ионизации (Eионизации ) -
это энергия, необходимаядля отрыва наименее
связанного с атомом
электрона
6. Энергия сродства к электрону (Eсродства ) -
это энергия, котораявыделяется при
присоединении одного
электрона к атому
7. Электроотрицательность (ЭО)
ЭО = Eионизации + Eсродства2
Чем больше ЭО, тем больше выражены
металлические свойства
ЭО – мера неметалличности элемента
8. Электроотрицательность -
это способностьатомов оттягивать на
себя электроны от
атомов других
элементов
9. II. Изменение характеристик элементов в периодах и группах
10.
Электроны удерживаются в атоме засчет притяжения к положительно
заряженному ядру
Сила притяжения между разноименно
заряженными частицами зависит от
заряда частиц и расстояния между
ними
Чем больше заряды, тем больше сила
притяжения
Чем больше расстояние, тем меньше
сила притяжения
11. В группах:
Заряд ядра увеличиваетсяЧисло электронных слоев
увеличивается
Li
Число электронов на внешнем
слое не изменяется
Радиус атомов увеличивается
Na
K
Энергия ионизации, энергия
сродства к электрону, ЭО
уменьшается
Металлические свойства
усиливаются,
неметаллические ослабевают
12. В периодах:
LiBe
B
Заряд ядра увеличивается
Число электронных слоев не изменяется
Число электронов на внешнем слое увеличивается
Радиус атома уменьшается («атомное сжатие» в
периодах)
Энергия ионизации, энергия сродства к электрону,
ЭО увеличивается
Металлические свойства ослабевают,
неметаллические усиливаются
13. Закрепление
№ 6 – 26 (задачник)14. Домашнее задание
Выучить конспектПисьменно: доделать
№ 6-26













 Химия
Химия








