Похожие презентации:
Простые и сложные вещества (8 класс)
1.
Тема урокаПростые и сложные
вещества
8класс
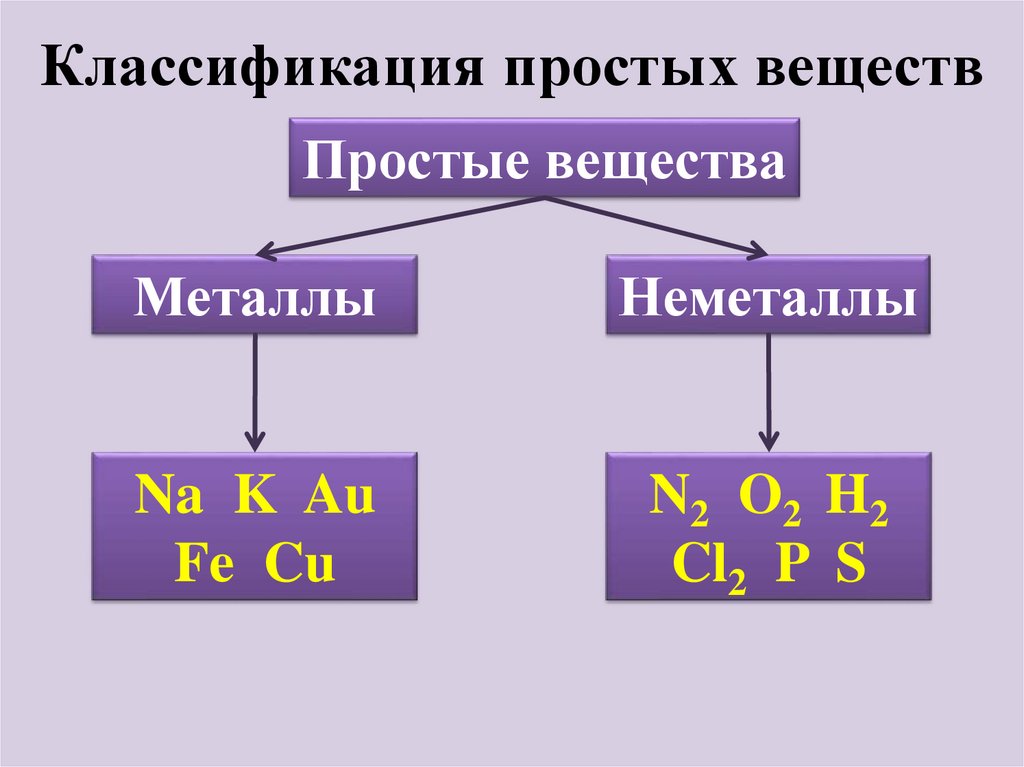
2. Классификация простых веществ
Простые веществаМеталлы
Неметаллы
Na K Au
Fe Cu
N2 O2 H2
Cl2 P S
3.
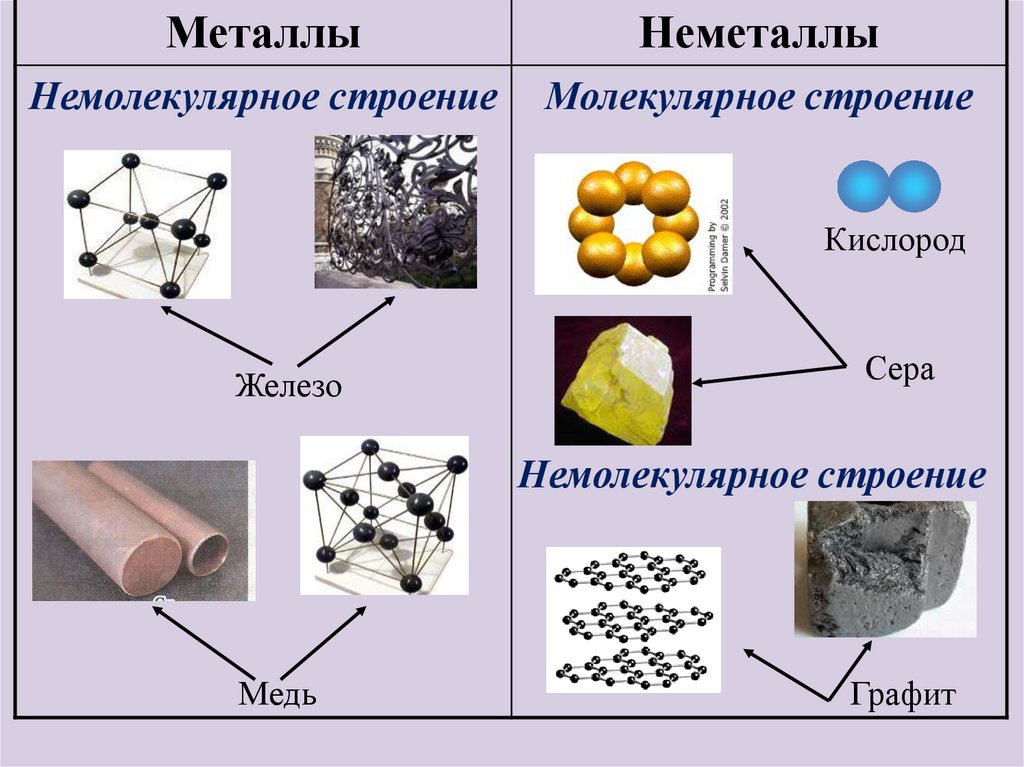
МеталлыНеметаллы
Немолекулярное строение
Молекулярное строение
Кислород
Железо
Сера
Немолекулярное строение
Медь
Графит
4.
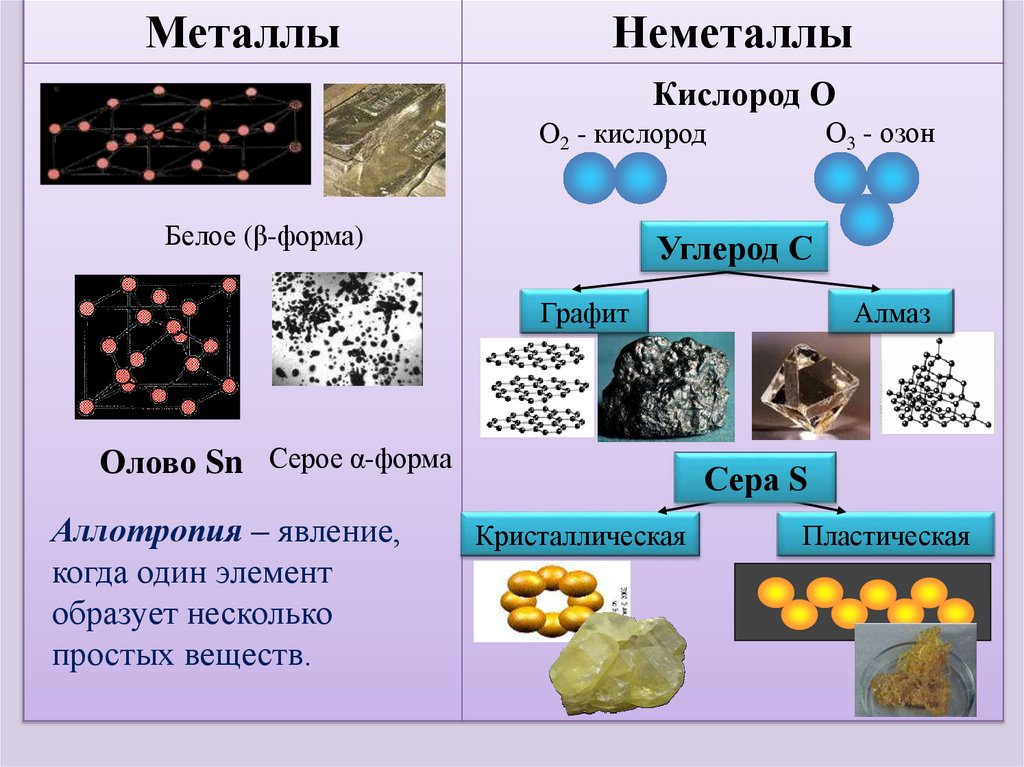
МеталлыНеметаллы
Кислород О
О3 - озон
О2 - кислород
Белое (β-форма)
Углерод С
Графит
Олово Sn Серое α-форма
Аллотропия – явление,
когда один элемент
образует несколько
простых веществ.
Алмаз
Сера S
Кристаллическая
Пластическая
5.
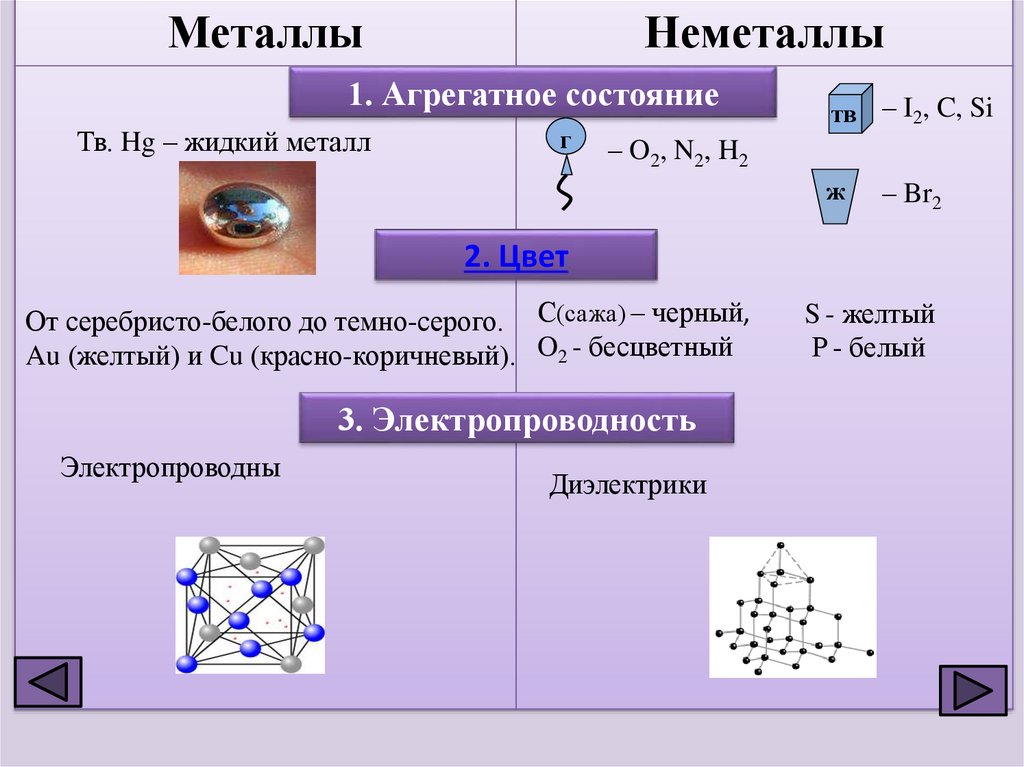
МеталлыНеметаллы
1. Агрегатное состояние
Тв. Hg – жидкий металл
г
тв – I2, C, Si
– O 2 , N 2 , H2
ж
– Br2
2. Цвет
От серебристо-белого до темно-серого. С(сажа) – черный,
Au (желтый) и Cu (красно-коричневый). O2 - бесцветный
3. Электропроводность
Электропроводны
Диэлектрики
S - желтый
Р - белый
6.
МеталлыНеметаллы
От серебристо-белого
до серого
алмаз
бериллий
сера
литий
кремний
фосфор
германий
золото
медь
мышьяк
графит
7.
МеталлыНеметаллы
4. Твердость / мягкость
Существуют твердые (Cr, Fe) и
мягкие (Au, Na, K).
Существуют твердые (Салмаз, Si) и
мягкие (Cграфит).
5. Пластичность/ хрупкость
Пластичные (Au, Ag, Cu, Al и
др.), кроме. Sn (серое).
Хрупкие (S, уголь, I2, др.) При
ударе рассыпаются.
6. Температура плавления
Самая высокая:
Tпл.(W)= +3380°С
Самая низкая?
Tпл.(Hg)= - 38,8°С
Высокая:
Tпл.(алмаза)= +3600°С
Низкая:
Tпл.(азота)= -210°С
8.
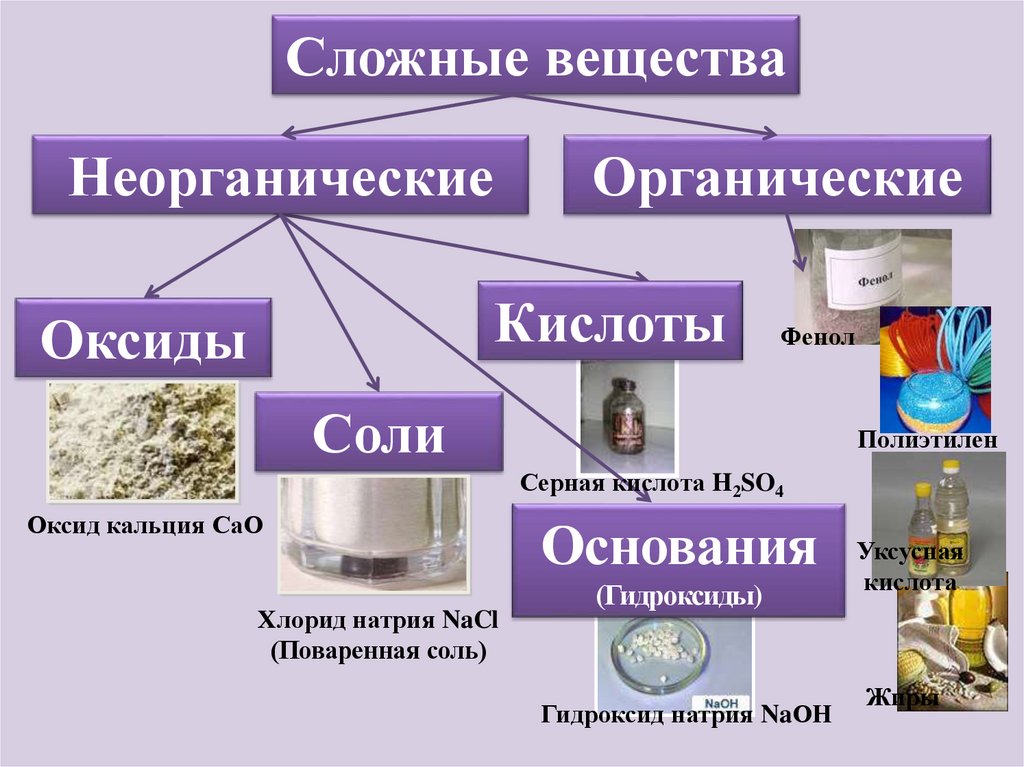
Сложные веществаНеорганические
Органические
Кислоты
Оксиды
Фенол
Соли
Полиэтилен
Серная кислота H2SO4
Оксид кальция СаО
Хлорид натрия NaCl
(Поваренная соль)
Основания
(Гидроксиды)
Гидроксид натрия NaОН
Уксусная
кислота
Жиры
9.
Сложные вещества состоят из атомовразных химических элементов
В химических реакциях могут
разлагаться с образованием нескольких
других веществ
Оксид кальция
Гидроксид натрия
Серная кислота
Хлорид натрия
10.
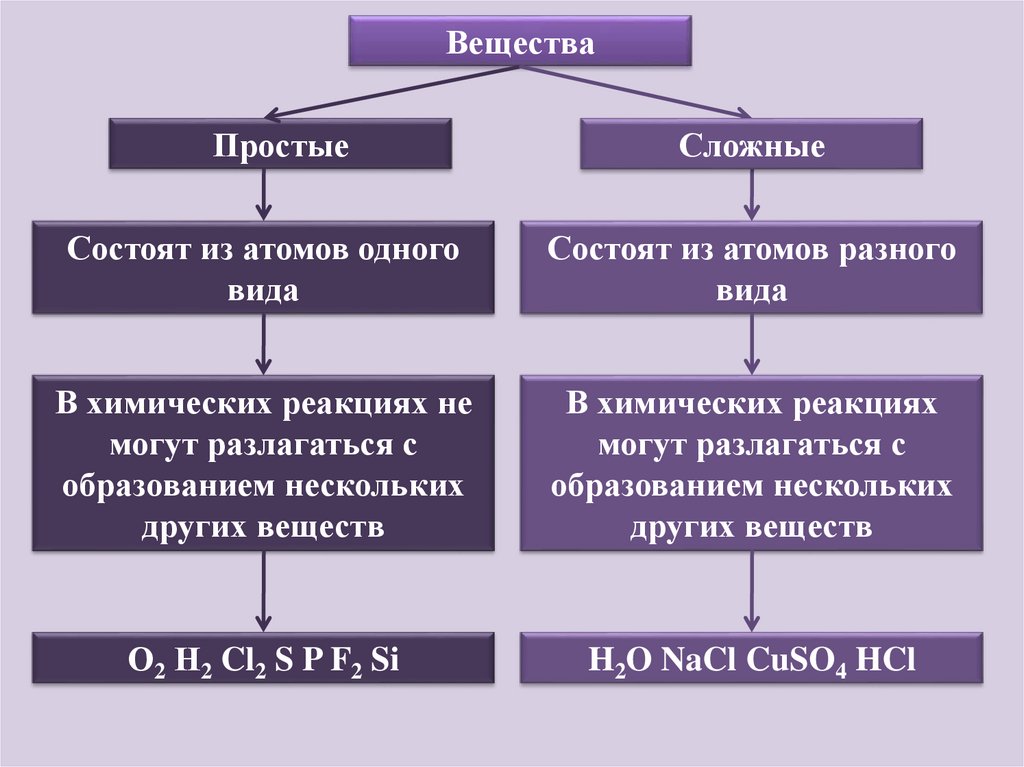
ВеществаПростые
Сложные
Состоят из атомов одного
вида
Состоят из атомов разного
вида
В химических реакциях не
могут разлагаться с
образованием нескольких
других веществ
В химических реакциях
могут разлагаться с
образованием нескольких
других веществ
О2 Н2 Cl2 S P F2 Si
H2O NaCl CuSO4 HCl
11.
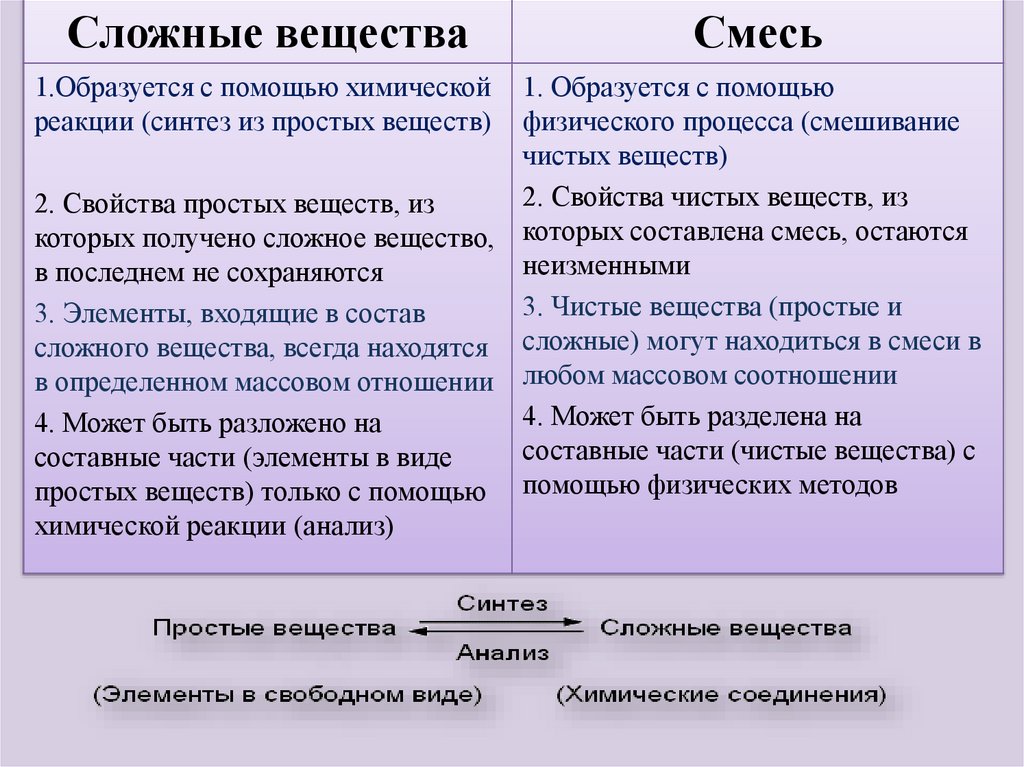
Сложные вещества1.Образуется с помощью химической
реакции (синтез из простых веществ)
Смесь
1. Образуется с помощью
физического процесса (смешивание
чистых веществ)
2. Свойства чистых веществ, из
2. Свойства простых веществ, из
которых получено сложное вещество, которых составлена смесь, остаются
неизменными
в последнем не сохраняются
3. Чистые вещества (простые и
3. Элементы, входящие в состав
сложного вещества, всегда находятся сложные) могут находиться в смеси в
в определенном массовом отношении любом массовом соотношении
4. Может быть разделена на
4. Может быть разложено на
составные части (чистые вещества) с
составные части (элементы в виде
простых веществ) только с помощью помощью физических методов
химической реакции (анализ)
12.
Аллотро́пия (от др.-греч. αλλος —«другой», τροπος — «поворот, свойство») —
существование одного и того же
химического элемента в виде двух и более
простых веществ, различных по строению и
свойствам: так называемых
аллотропических модификаций или
аллотропических форм.
Модификации фосфора
13.
Просты́е вещества́ — вещества, состоящиеисключительно из атомов одного химического
элемента (в отличие от сложных веществ).
Являются формой существования химических
элементов в свободном виде, или, иначе говоря,
элементы, не связанные химически ни с каким
другим элементом, образуют простые
вещества. Известно свыше 400 разновидностей
простых веществ.
Алмаз
Графит
14.
Сложные вещества — это химическиевещества, которые состоят из атомов двух
или более химических элементов.
Сложными веществами являются
большинство неорганических веществ и все
органические.
Вода
Галит
Сильвинит
15.
Смесь — Продукт смешения,механического соединения каких-либо
веществ. Например: горючая смесь,
гелиево-кислородная смесь.
Молоко
Воздух
16.
Хими́ческое соедине́ние— сложноевещество, состоящее из химически
связанных атомов двух или нескольких
элементов. Состав химического
соединения записывается в виде
химических формул, а строение часто
изображается структурными
формулами.









 Химия
Химия








