Похожие презентации:
Соли
1. Эпиграф урока «Не в количестве знаний заключается образование, а в полном понимании и искусном применении того, что знаешь» А.
Дистервег (немецкий педагог)2. Угадайте вещество
1.2.
3.
4.
5.
В чёрном ящике –
вещество, без которого невозможна жизнь растений,
животных и человека.
Это химическое соединение необходимо для
существования в крови эритроцитов, сокращения
мышц, переваривания пищи в желудке.
В год каждый человек потребляет от 3 до 5 кг.
этого вещества.
Это вещество- символ гостеприимства и радушия
русской нации.
Говорят, чтобы узнать человека, надо с ним пуд
этого вещества съесть.
3. Знаете ли вы, что…
Толщина пласта соли в СольИлецке превышает 1,5 км.Поваренной солью, извлеченной
только из морской воды, можно
было бы засыпать всю сушу
Земного шара слоем 130 м.
А для территории Европы этого
количества хватило бы для слоя
толщиной около 5 км.
4. Тема урока: Соли
5.
11
2
2
3
4
6.
- это сложные вещества, состоящие из двухэлементов, один из которых кислород со степенью окисления -2.
Н2О (г)
CaO (негашеная изв.)
Н2О (ж)
Fe2O3
Н2О (тв)
CuO
Al2O3 (глинозём)
MgO
7.
– это сложные вещества, состоящие из ионовметаллов и связанных с ними гидроксидионов.
NaOH
Cu(OH)2
8.
- это сложные вещества, молекулы которыхатомов водорода и кислотного остатка.
состоят из
Н2SО4
HCl
HNO3
Н3ВО3
уксусная
лимонная
лимонная
муравьиная
9.
CuSO4MgSO4
CaCO3(мел)
KNO3
KCl (сильвин)
FeTiO3(ильменит)
KMnO4
FeCl3
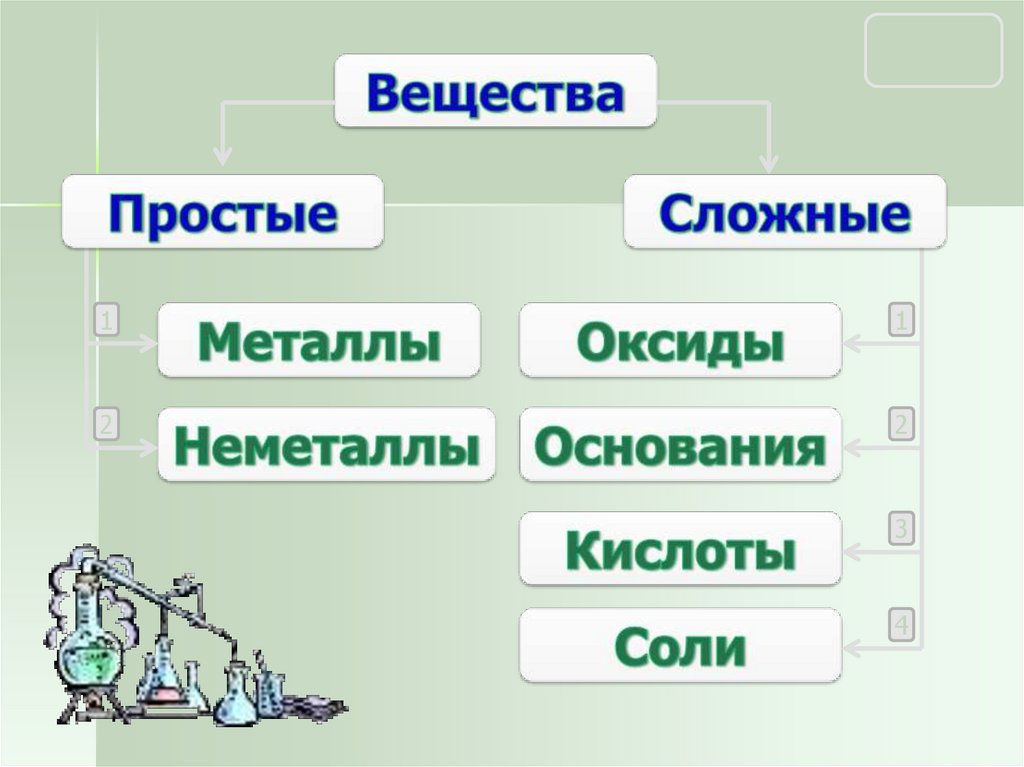
10. Состав солей
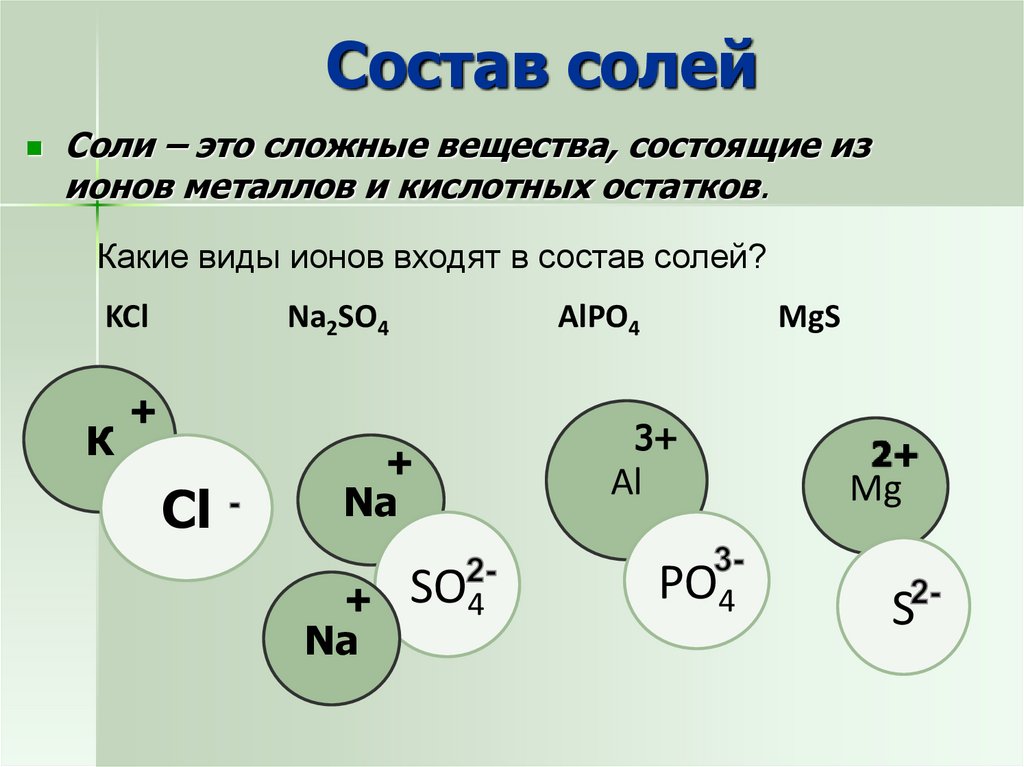
Соли – это сложные вещества, состоящие изионов металлов и кислотных остатков.
Какие виды ионов входят в состав солей?
KCl
Na2SO4
AlPO4
Na
Al
MgS
К
Cl
Na
SO4
Mg
PO4
S
11. Поваренная соль
NaCl
Соленая на вкус.
Хорошо растворяется в воде.
Высокая температура плавления.
Консервирующее
вещество
Приправа к пище
Производство
мыла,СМС
12.
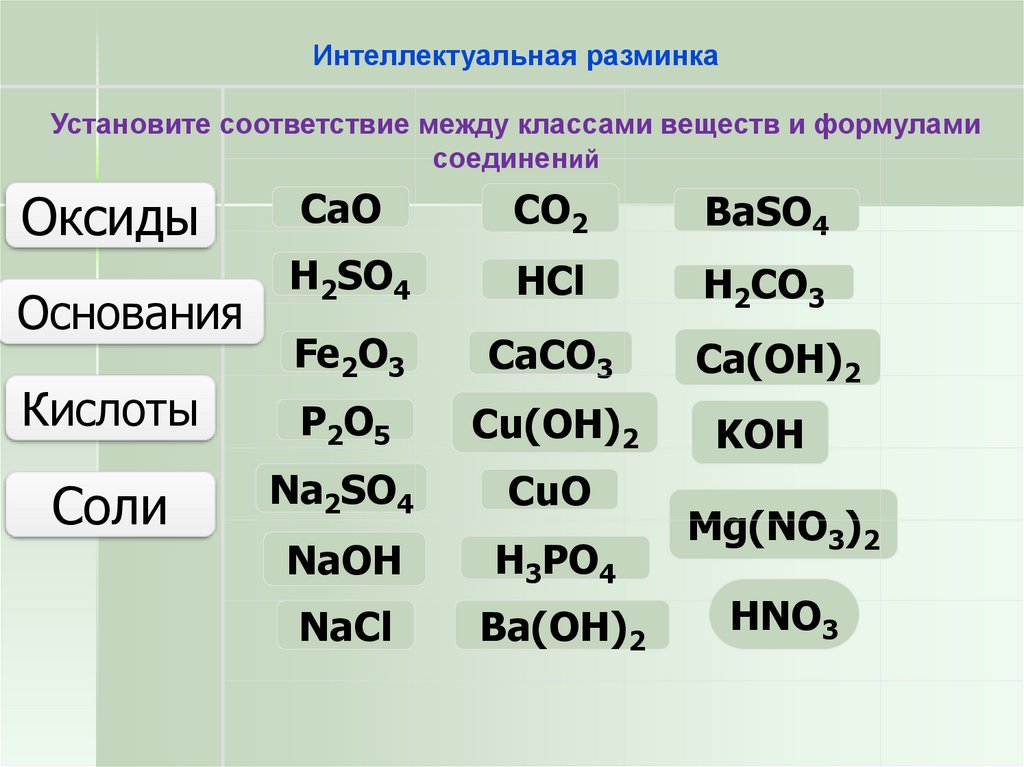
Интеллектуальная разминкаУстановите соответствие между классами веществ и формулами
соединений
Оксиды
Основания
Кислоты
Соли
СaО
CО2
BaSO4
H2SО4
HCl
H2CО3
Fe2О3
CaCO3
P2О5
Сu(ОH)2
Na2SO4
CuО
NaОH
H3PО4
NaCl
Ba(ОH)2
Сa(ОH)2
KОH
Mg(NO3)2
HNO3
13. В трех пробирках под номерами находятся: кислота, щелочь и соль. Определите содержание каждой пробирки.
Экспериментальная задача:«Распознавание веществ»
В трех пробирках под номерами
находятся:
кислота, щелочь и соль.
Определите содержание каждой
пробирки.
14.
15. Порецкое гипсовое месторождение является одним из крупнейших в России, а по запасам ангидрита – крупнейшим в Европе и
единственнымразрабатываемым
в
промышленных масштабах на территории
Европейской части России.
CaSO4
16. Составление формулы соли
Алгоритм действий присоставлении формулы
Порядок действий
3.
число:
4.Разделить
Проверка:полученное
произведение
а) на заряд
металла
и записать
значения
заряда
металла
на его
1.
индекс
Записать
справа
химические
внизу
от знака
знаки
индекс
должно
быть
равно
2. Найти наименьшее общее
металла и кислотного
металла;
остатка,
аналогичному
произведению
кратное значений
зарядов
б) накислотного
заряд
указать
кислотного
ихостатка
зарядыостатка
и записать индекс кислотного
остатка
Шаг 1
Шаг 2 Шаг 3 Шаг 4
Пример
2*3
=2+6 3-3-32+
2+
PO444 )2
СaСa3(PO
6 : 2 = 3 (индекс)
(2+)2*3
∙ 3 == 66+
Сa2+3 PO43(3 -) ∙ 2 = 6 –
6 : 3 = 2 (индекс)
(6 +) + (6-)= 0
Сa2+3(PO43-)2
16
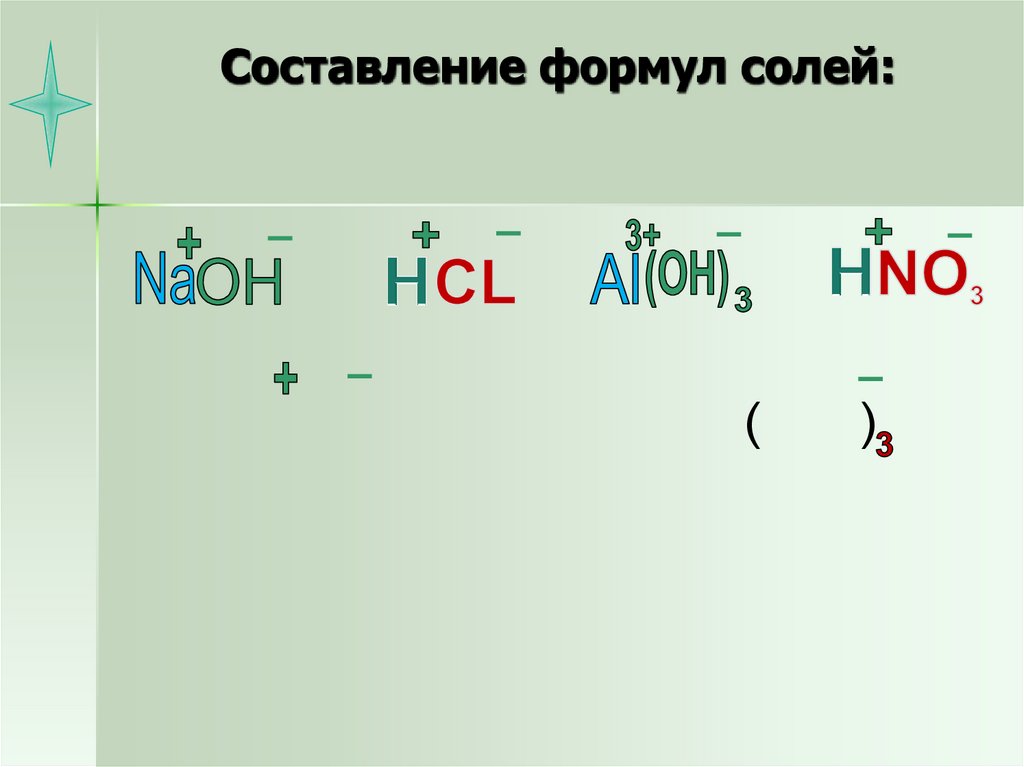
17. Составление формул солей:
()
18.
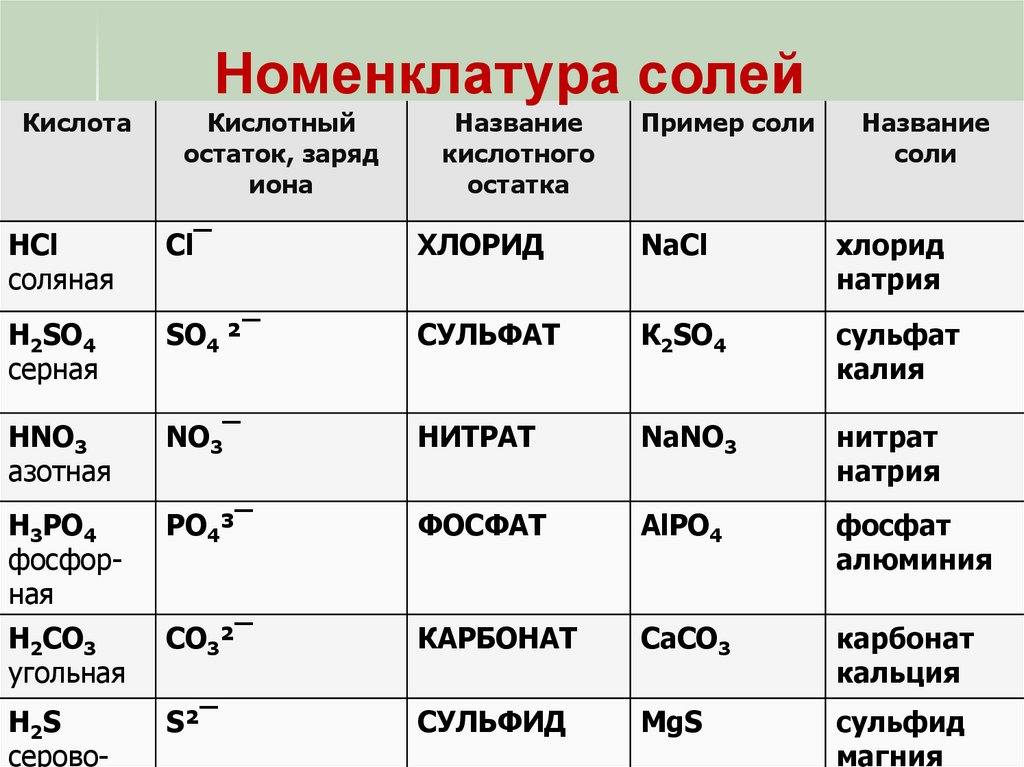
Номенклатура солейКислота
Кислотный
остаток, заряд
иона
Название
кислотного
остатка
Пример соли
Название
соли
HCl
соляная
Cl¯
ХЛОРИД
NaCl
хлорид
натрия
Н2SО4
серная
SО4 ²¯
СУЛЬФАТ
К2SО4
сульфат
калия
НNO3
азотная
NO3¯
НИТРАТ
NaNO3
нитрат
натрия
Н3РО4
фосфорная
РО4³¯
ФОСФАТ
AlPО4
фосфат
алюминия
Н2СО3
угольная
СО3²¯
КАРБОНАТ
СаСО3
карбонат
кальция
Н 2S
серово-
S²¯
СУЛЬФИД
MgS
сульфид
магния
19.
Тренажер «Соли кальция»Составьте формулы солей, укажите зарядов ионов, назовите вещества.
S
CO3
SO4
Са
PO4
N03
Проверка
Ca(NO
CaCO
карбонат
Са
3CaS
(PO344))2кальция
3СаSО
2
20. Домашнее задание:
1.2.
3.
§21;
выучить таблицу 5;
задание 4 по тематической карте.
21.
Ответьте на утверждение знаком«+» или «-»:
1. На уроке было над
чем подумать
2. Я понял новую тему
3. На все возникшие у меня
вопросы я получил ответы
4. На уроке я поработал
добросовестно
5. Оцените свою работу на уроке по
пятибалльной системе.

















 Химия
Химия