Похожие презентации:
Спирты или алканолы
1. Спирты или алканолы
Вводная лекция по теме:«Спирты»
Составила учитель химии МОУ СОШ № 17
Белотелова О.Н.
2. Строение
Спиртами называют органические вещества,молекулы которых содержат одну или
несколько гидроксильных групп (групп –
ОН),соединённых с углеводородным
радикалом.
Номенклатура: алкан+ол.
Назвать спирт: СН3-СН-СН-СН3
ОН СН3
( 3-метилбутанол – 2)
3.
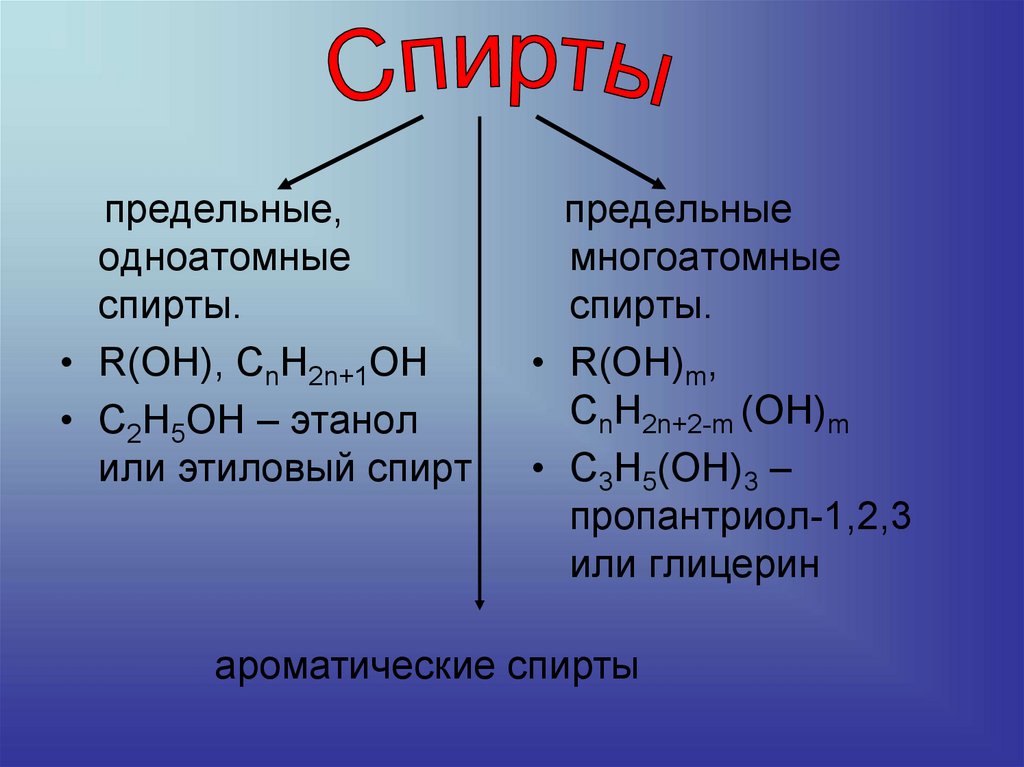
предельные,одноатомные
спирты.
• R(OH), CnH2n+1OН
• С2Н5ОН – этанол
или этиловый спирт
предельные
многоатомные
спирты.
• R(OH)m,
CnH2n+2-m (OH)m
• С3Н5(ОН)3 –
пропантриол-1,2,3
или глицерин
ароматические спирты
4. Изобразите структурные формулы следующих спиртов:
2,2,5,5 – тетраметилгексанол – 3
2 – метилпентанол – 3
Этандиол – 1,2
2,7 – дихлороктандиол – 4,5
2 – фенилбутанол – 2
Фенилметанол (бензиловый спирт)
5. Изомерия
• Разветвление углеродного скелетаСН3-СН2-СН2-СН2-ОН
СН3-СН-СН2-ОН
СН3
(бутанол-1)
(метилпропанол-1)
• Положение функциональной группы
СН3-СН-СН2-СН3
ОН
(бутанол-2)
• Межклассовая (простые эфиры)
СН3-О-СН2-СН2-СН3
(метилпропиловый эфир)
6. Составить и назвать по одному изомеру на каждый возможный вид изомерии для пентанола - 2
7. Физические свойства
• CH3OH - C10H21OH – бесцветныежидкости, с характерным алкогольным
запахом.
• от C12H25OH - твердые вещества
• метанол, этанол, пропанол в воде
растворяются в неограниченных
количествах. Высшие спирты в воде
практически нерастворимы.
• CH3OH(метанол) - очень ядовит!
8. Химические свойства
1.Спирты реагируют с активными металлами, образуяалкоголяты:
2ROH + 2Na = 2RONa + H2
2.Внутримолекулярная дегидратация (при t>1400С, в
присутствии H2SO4):
ROH=CnH2n+H2O
3.Спирты реагируют с галогеноводородными
кислотами:
ROH + HCl = RCl + HOH
4.Спирты горят синеватым пламенем:
C2H5OH + 3O2 =2CO2 +3H2O
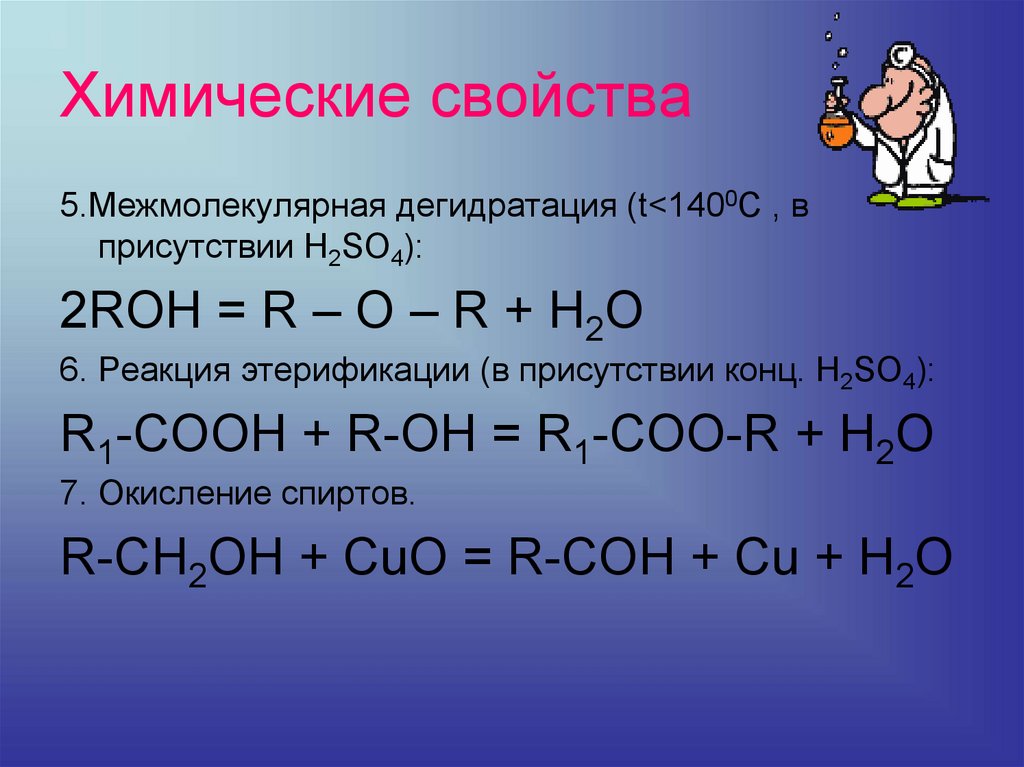
9. Химические свойства
5.Межмолекулярная дегидратация (t<1400C , вприсутствии H2SO4):
2ROH = R – O – R + H2O
6. Реакция этерификации (в присутствии конц. H2SO4):
R1-COOH + R-OH = R1-COO-R + H2O
7. Окисление спиртов.
R-CH2OH + CuO = R-COH + Cu + H2O
10. Составить уравнения реакций, характеризующие химические свойства 1,3 группа 2,4 группа этанола метанола
11. Получение
1. Гидролиз галогеналканов (водный раствор щёлочи)R-Cl + NaOH = R-OH + NaCl
2. Гидратация алкенов
СnH2n + H2O = CnH2n+1OH
3. Восстановление альдегидов и кетонов
R-COH + H2 = R-CH2-OH
R-CO-R1 + H2 = R-CH-R1
OH
4. Окисление алкенов (получение гликолей в водных растворах
перманганата калия KMnO4)
СnH2n + (O) +H2O = CnH2n(OH)2
5. Специфические способы получения спиртов
СО + 2Н2 = СН3-ОН
(t, p, ZnO)
C6H12O6 = 2C2H5OH + 2CO2 (под действием дрожжей)
12. Применение спиртов
• Производство органических веществ.• Производство медицинских препаратов.
• Производство косметики и
парфюмерии.
• Производство синтетических каучуков.
• Производство лаков и красок.
• Топливо.










 Химия
Химия








