Похожие презентации:
Степень окисления. Бинарные соединения
1.
СТЕПЕНЬ ОКИСЛЕНИЯ. БИНАРНЫЕ СОЕДИНЕНИЯ2.
Сложное вещество — этовещество, состоящее из атомов
разных химических элементов.
Cl
O2
3.
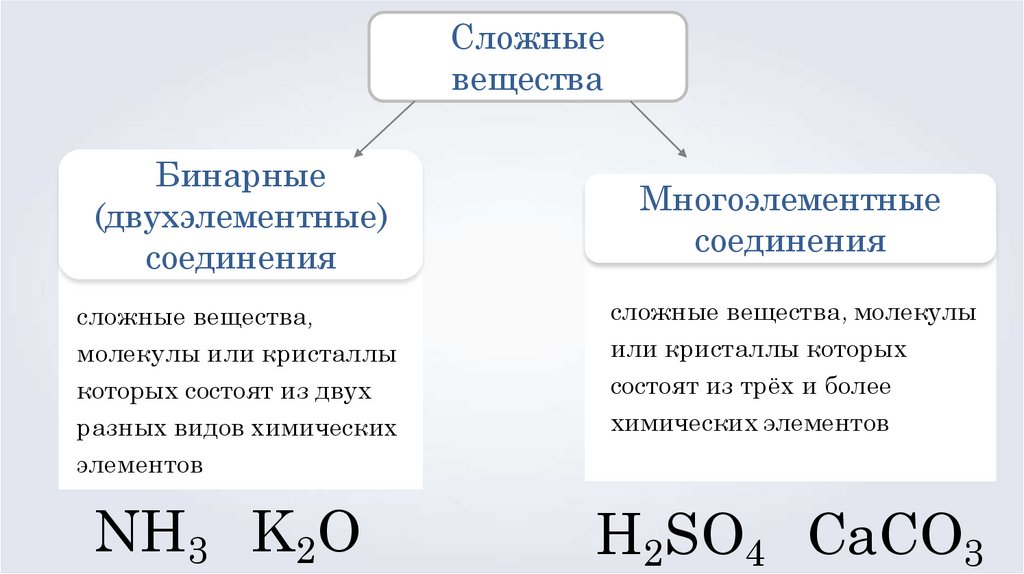
Сложныевещества
Бинарные
(двухэлементные)
соединения
сложные вещества,
молекулы или кристаллы
которых состоят из двух
разных видов химических
элементов
NH3 K2O
Многоэлементные
соединения
сложные вещества, молекулы
или кристаллы которых
состоят из трёх и более
химических элементов
H2SO4 CaCO3
4.
Бинарные веществаNaCl
H2O
CO2
5.
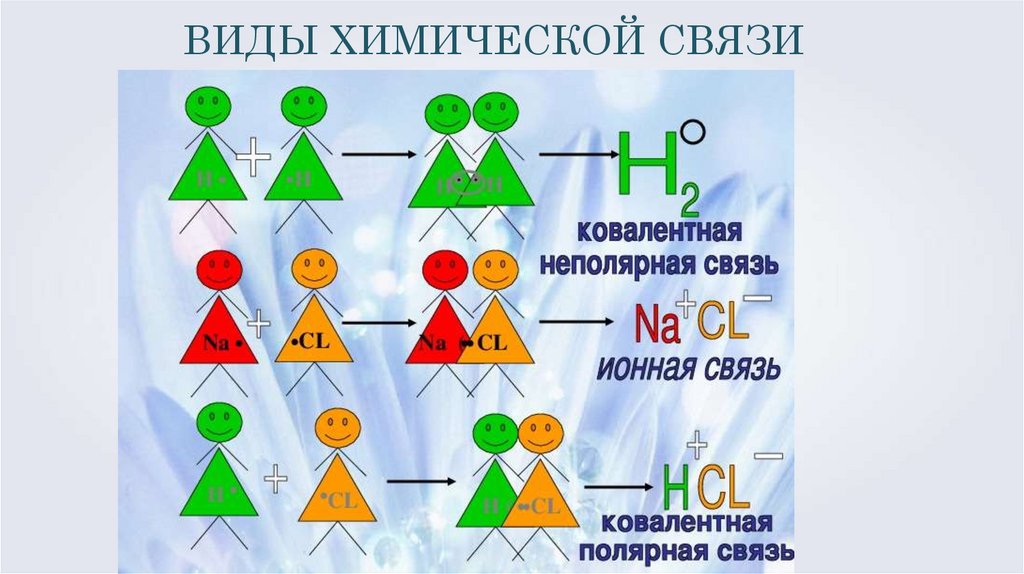
ВИДЫ ХИМИЧЕСКОЙ СВЯЗИ6.
+1-1
HCl
+1
-1
Na Cl
0
Cl2
Степень окисления — это условный
заряд атомов химического элемента в
соединении, вычисленный на основе
предположения, что все соединения (и
ионные, и ковалентно-полярные)
состоят только из ионов.
7.
8.
9.
Определение степеней окисления1. У металлов IА группы
таблицы Менделеева во
всех соединениях степень
окисления равна +1.
+1
–2
Na2O
10.
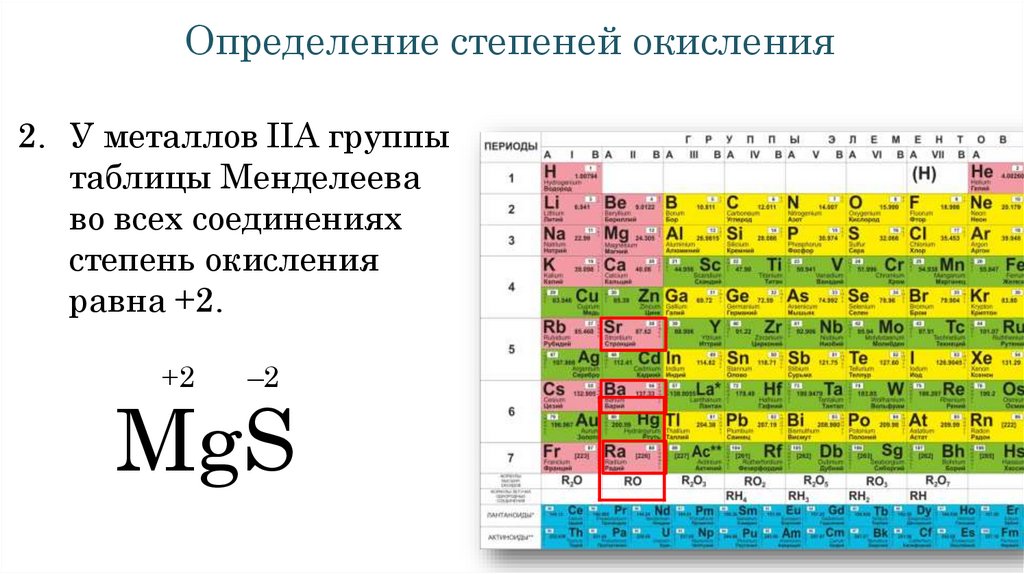
Определение степеней окисления2. У металлов IIА группы
таблицы Менделеева
во всех соединениях
степень окисления
равна +2.
+2
–2
MgS
11.
Определение степеней окисления3. У металлов IIIА
группы таблицы
Менделеева во всех
соединениях степень
окисления равна +3.
+3
–1
AlF3
12.
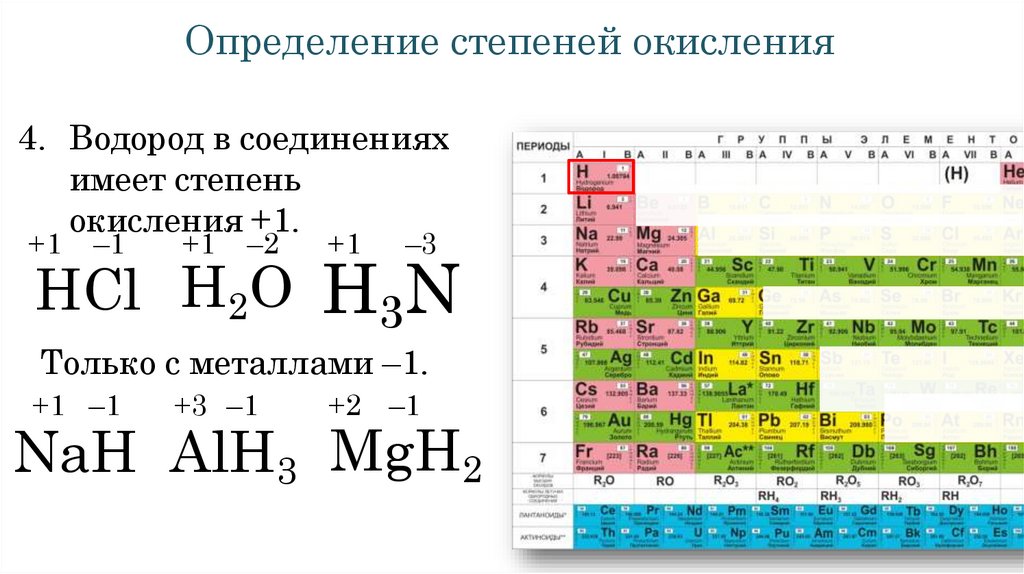
Определение степеней окисления4. Водород в соединениях
имеет степень
окисления +1.
+1
–1
+1
–2
HCl H2O
+1
–3
H3N
Только с металлами –1.
+1 –1
+3 –1
+2 –1
NaH AlH3 MgH2
13.
Определение степеней окисления5. Нулевое значение
степени окисления
имеют атомы в
молекулах простых
веществ и атомы в
свободном состоянии:
0
0
H2 N2
0
0
Fe Na
14.
Исключения в пероксидах -115.
16.
17.
18.
Алгоритм составленияформулы сульфида железа (III)
6
+3 -2
FeS
Fe2S3
1. Запишем знаки железа и серы рядом. Железо как менее
элекроотрицательный элемент становится на первое место, а
сера на второе.
2. Каждый атом железа отдает три внешних электрона атомам серы,
каждому из которых не хватает двух электронов до завершения
внешнего энергетического уровня. Записываем эти значения в
формулу.
3. Находим наименьшее общее кратное для них, которое равно
шести. Рассчитываем и записываем индексы.
19.
Названия бинарных соединенийПервое слово указывает на электроотрицательную часть
соединения, к нему прибавляется окончание –ид в
именительном падеже.
Второе слово записывается в родительном падеже и обозначает
положительную часть соединения. Вторая часть может быть
либо металлом, либо менее электроотрицательным элементом,
чем элемент в первой части.
Пример 1.
KCl — хлорид калия
FeO — оксид железа
CaH2 — гидрид кальция
20.
Названия бинарных соединенийЕсли менее электроотрицательный элемент имеет
переменную с.о., то она указывается после названия вещества
в скобках римскими цифрами.
Пример 2.
SiO2 — оксид кремния
NO — оксид азота (II)
21.
22.
Принципы химической номенклатуры былиразработаны в 1785 г.
Антуан
Лавуазье
Антуан де
Фуркруа
Луи Гитон де
Морво
Клод
Бертолле
















 Химия
Химия








