Похожие презентации:
Валентность (8 класс)
1.
Ar = 1 Ar = 27 Ar =7Ar =9(2-я буква) Ar = 23
Ar =48 Ar = 21 Ar = 119 Ar = 32
Ar =45 Ar = 128
Валентность
2.
Цель:*уметь формулировать определение
«валентность»;
*определять валентность по готовым
формулам
3.
I IHCl
I
II
H2O
I III
H3N
I IV
H4C
Валентность – это свойство
атомов присоединять определенное
число атомов других элементов.
Обозначается:
знаком ХЭ.
римской цифрой над
4.
ВалентностьПостоянная
Переменная
5.
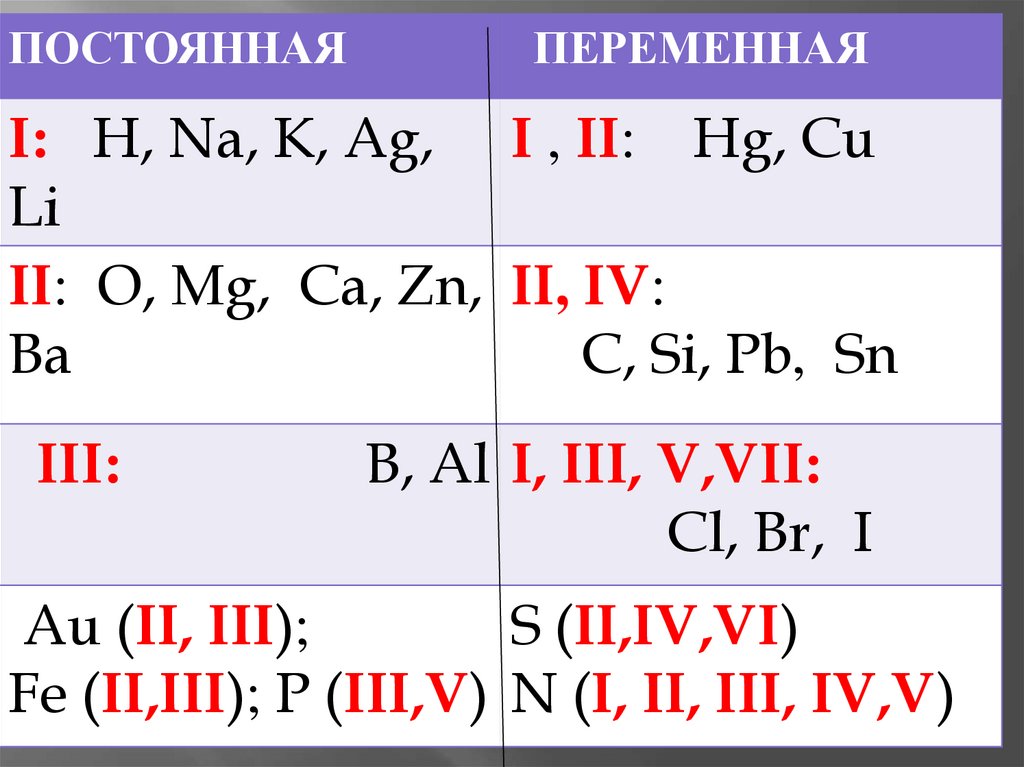
ПОСТОЯННАЯПЕРЕМЕННАЯ
I: H, Na, K, Ag, I , II: Hg, Cu
Li
II: O, Mg, Ca, Zn, II, IV:
Ba
C, Si, Pb, Sn
III:
B, Al I, III, V,VII:
Cl, Br, I
Au (II, III);
S (II,IV,VI)
Fe (II,III); P (III,V) N (I, II, III, IV,V)
6.
1. Пишем химическуюформулу вещества
2. Отмечаем валентность
известного
элемента(постоянную)
3. Находим НОК
(наименьшее общее
кратное). Для этого:
Валентность известного
элемента умножаем на
число атомов (индекс)
этого элемента.
H2S
I
H2S
I * 2 = 2 (НОК)
↓
«индекс» ат. «Н»
I2
H2S
7.
4. Вычисляем ипроставляем
валентность второго
элемента. Для этого:
НОК делим на
«индекс» второго
элемента.
(Аш- два- эс)
2 : 1 = II
2 II
H2S1
I II
H2S
8.
K2O, BaH29.
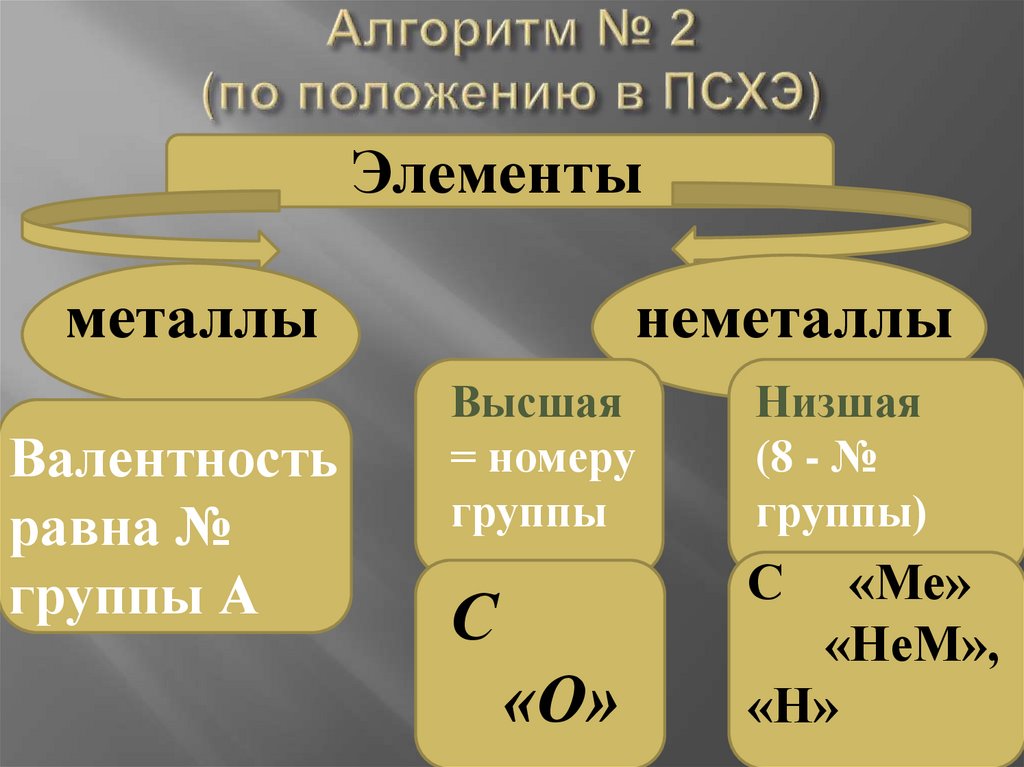
Элементыметаллы
Валентность
равна №
группы А
неметаллы
Высшая
= номеру
группы
Низшая
(8 - №
группы)
С
С
«О»
«Ме»
«НеМ»,
«Н»
10.
CaS,P2O5,
PH3
11.
1)§ 11, 12 стр. 32 – 34
2)
? 4 стр. 37
12.
Вариант 11. Составить формулу:
Оксида азота.
В состав молекулы оксида
азота входят: два атома ХЭ
азота и пять атомов ХЭ
кислорода.
Вариант 2
1. Составить формулу:
Бромида магния.
В состав молекулы бромида
магния входят: один атом ХЭ
магния и два атома ХЭ брома.
2. Вычислить относительную
молекулярную массу оксида
азота.
2. Вычислить относительную
молекулярную массу бромида
магния.
3. Найти массовую долю ХЭ
азота в оксиде азота.
3. Найти массовую долю ХЭ
брома в бромиде магния.
4. Определите валентность ХЭ 4. Определите валентность ХЭ
в оксиде азота.
в бромиде магния.
13.
II IIHgO
I II
Cu2O
I II
K2S
III II
B2O3
IV II
SnO2
II II
ZnO
IV II
MnO2
III II VI II
Ni2O3 SO3
V II
As2O5
II II
NiO
VII II
Cl2O7
Выполнено верно:
11 – 12 формул
8 – 10
6–7
меньше 6
- оценка «5»
«4»
«3»
«2»
14.
Эпиграфы «Все оттенки смыслаУмное число передает»
Н.Гумилев
«Если действовать
Не будешь,
Ни к чему ума палата»
Шота Руставели.
15.
1. Что вы можете рассказать овалентности?
2. Что было бы, если атомы не
соединялись бы друг с другом?
3. Как вы думаете, во сколько раз
валентность углерода больше
валентности хлора в CCl4 ?
4. Что выбираем за единицу
валентности?
5. Для чего нужна валентность?
16.
PCl5,Na2S,
SiCl4
17.
Ag2O,Al2S3,
CO
18.
Общая формулаMexOy, HexOy
MeCly
MexSy
MexNy
MeBry
MeHy
названия
оксид
хлорид
сульфид
нитрид
бромид
гидрид
19.
1). Повторить § 11-12 стр. 32 – 342).
Уровень А.
Определить валентность в формулах:
FeCl3, AlI3, Hg2O
3) Уровень В. Привести примеры к
общим формулам бинарных
соединений
















 Химия
Химия








