Похожие презентации:
Кристаллические решетки
1.
2.
Твердые веществаАморфные
Кристаллические
3.
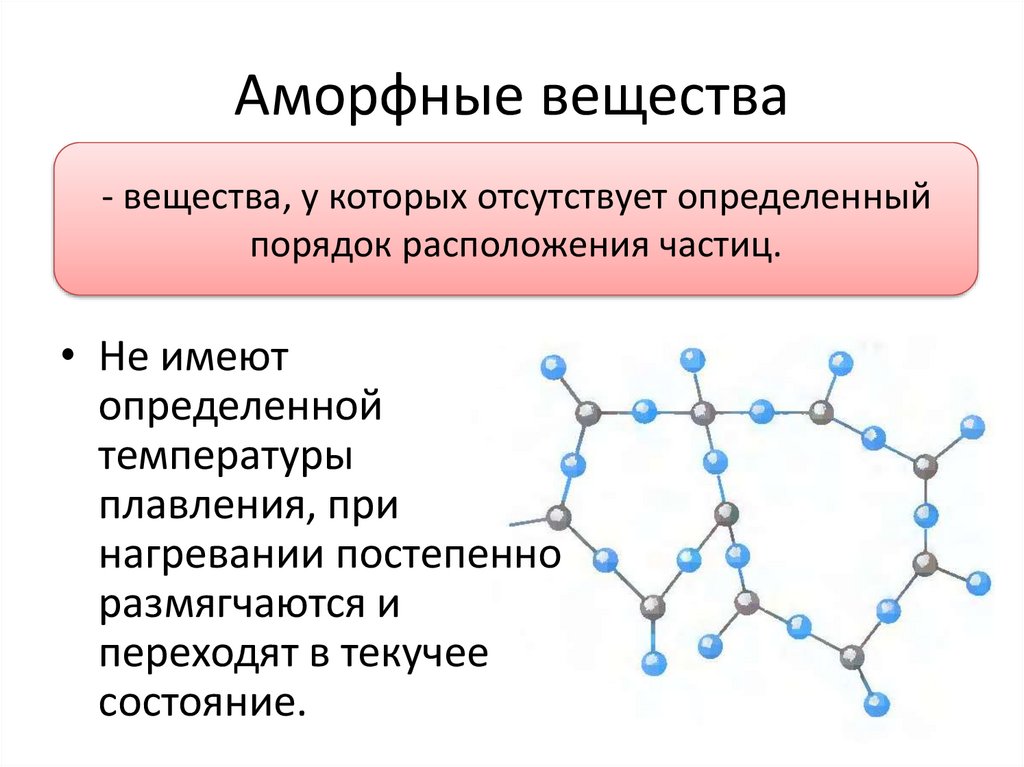
Аморфные вещества- вещества, у которых отсутствует определенный
порядок расположения частиц.
• Не имеют
определенной
температуры
плавления, при
нагревании постепенно
размягчаются и
переходят в текучее
состояние.
4.
ШоколадПластмасса
Воск (парафин)
Стекло
Пластилин
Жевательная резинка
5.
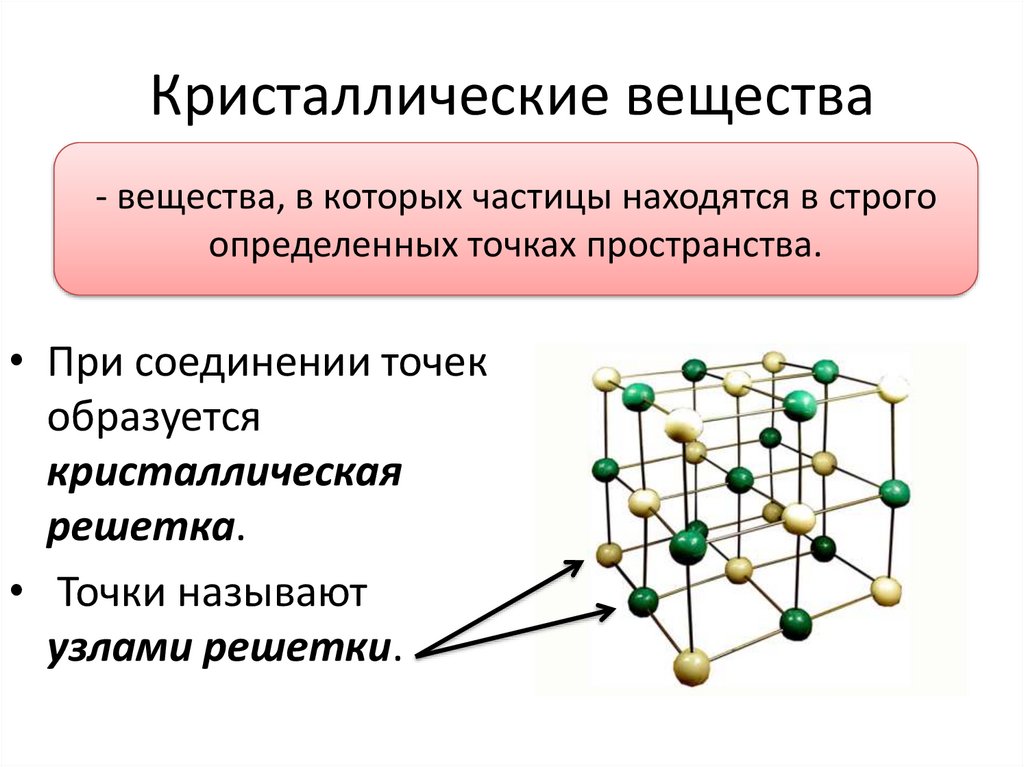
Кристаллические вещества- вещества, в которых частицы находятся в строго
определенных точках пространства.
• При соединении точек
образуется
кристаллическая
решетка.
• Точки называют
узлами решетки.
6.
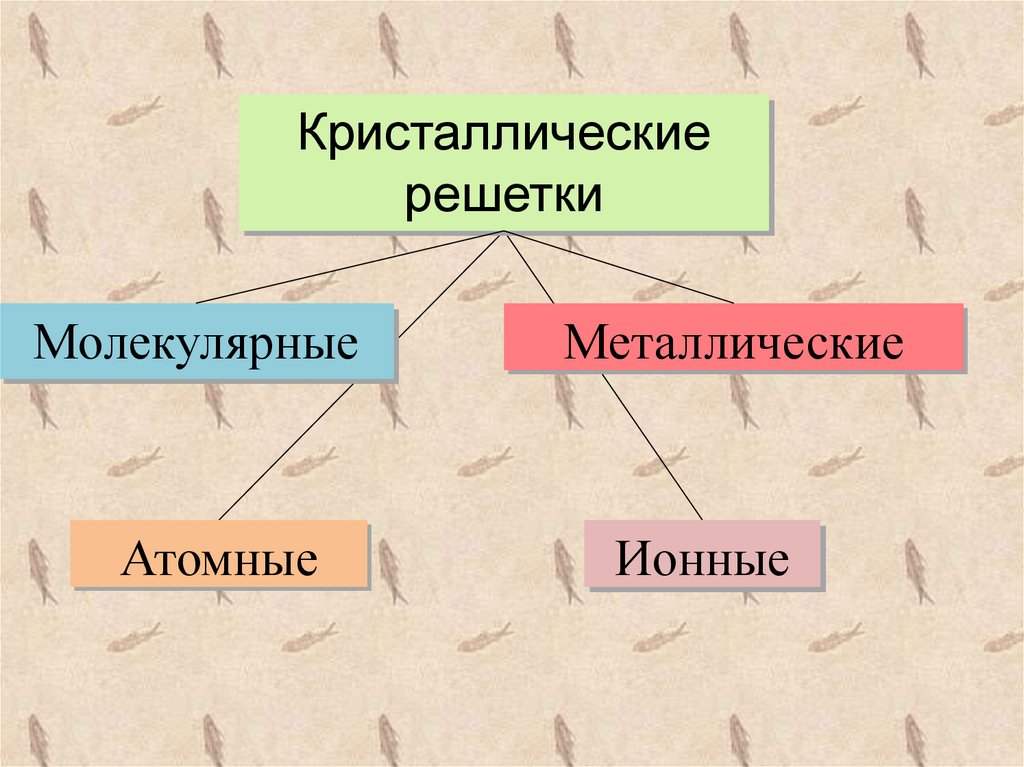
Кристаллическиерешетки
Молекулярные
Атомные
Металлические
Ионные
7.
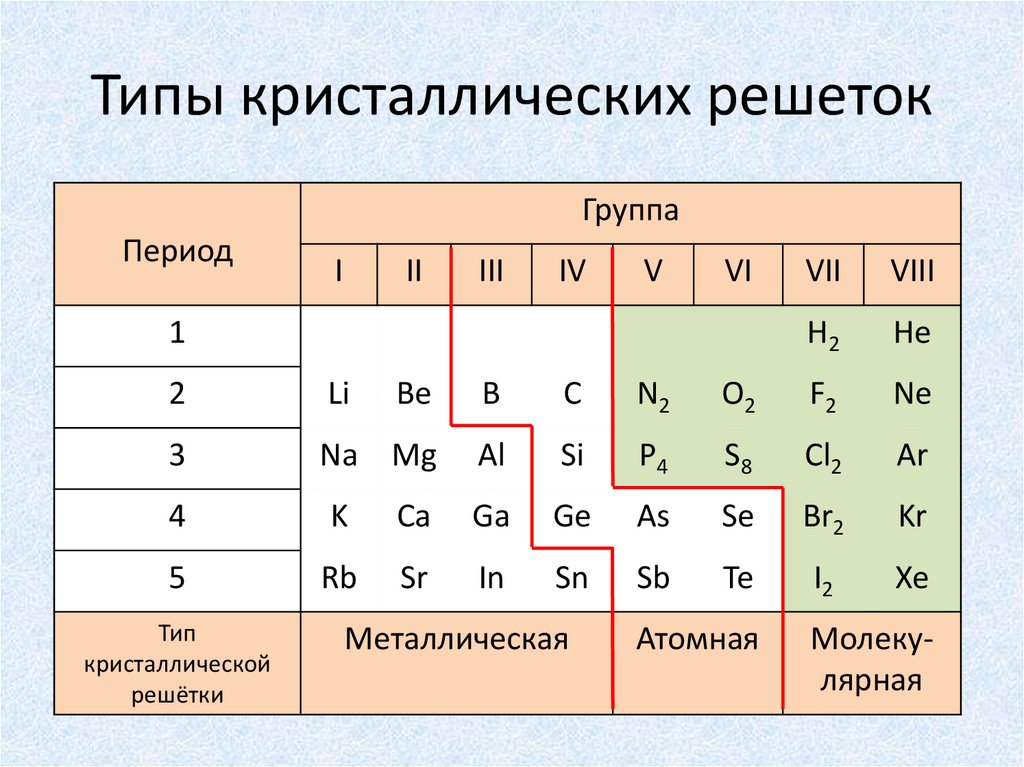
Типы кристаллических решетокГруппа
Период
I
II
III
IV
V
VI
1
VII
VIII
H2
He
2
Li
Be
B
C
N2
O2
F2
Ne
3
Na Mg
Al
Si
P4
S8
Cl2
Ar
4
K
Ca
Ga
Ge
As
Se
Br2
Kr
5
Rb
Sr
In
Sn
Sb
Te
I2
Xe
Тип
кристаллической
решётки
Металлическая
Атомная
Молекулярная
8.
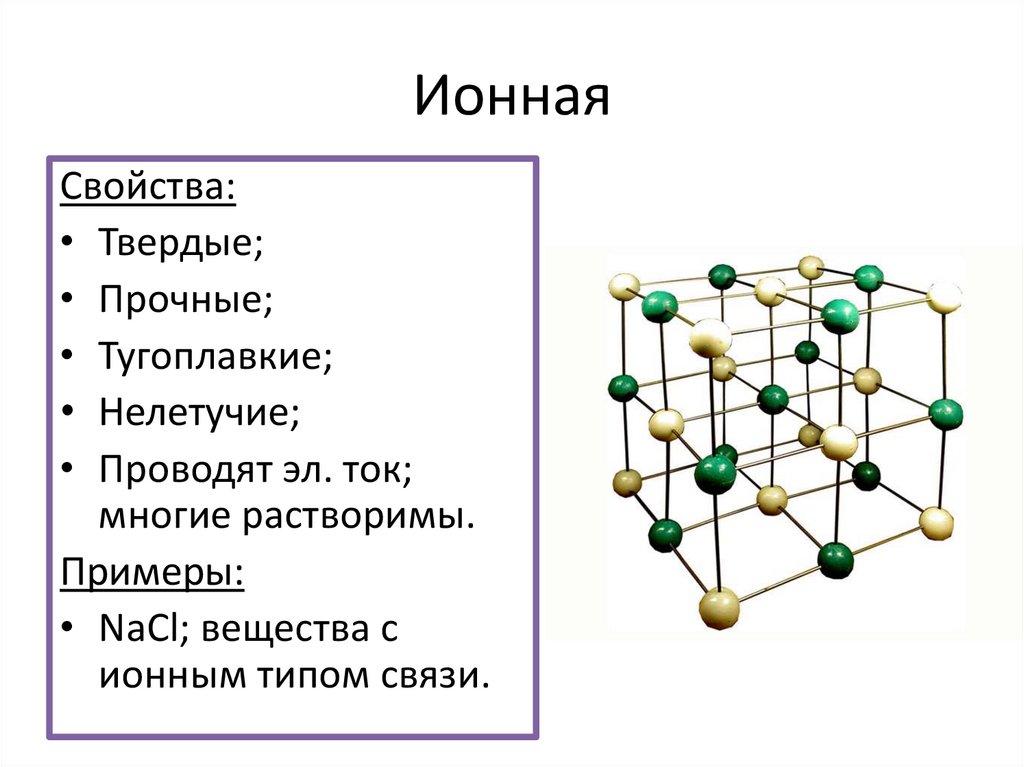
ИоннаяСвойства:
• Твердые;
• Прочные;
• Тугоплавкие;
• Нелетучие;
• Проводят эл. ток;
многие растворимы.
Примеры:
• NaCl; вещества с
ионным типом связи.
9.
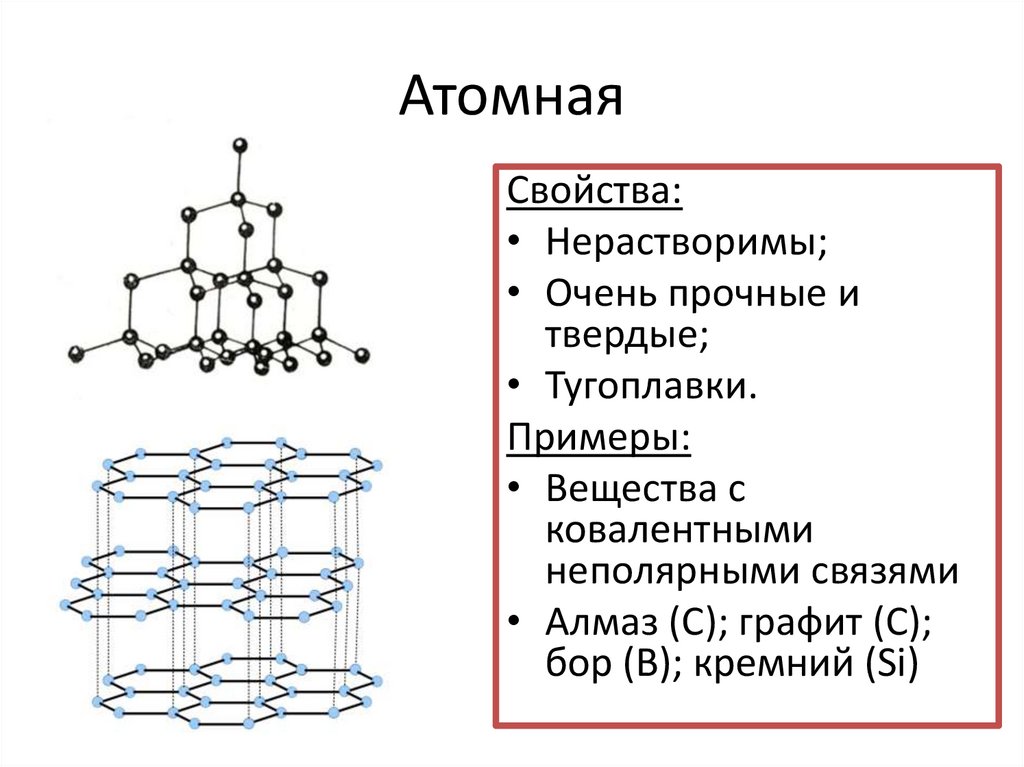
АтомнаяСвойства:
• Нерастворимы;
• Очень прочные и
твердые;
• Тугоплавки.
Примеры:
• Вещества с
ковалентными
неполярными связями
• Алмаз (С); графит (С);
бор (B); кремний (Si)
10.
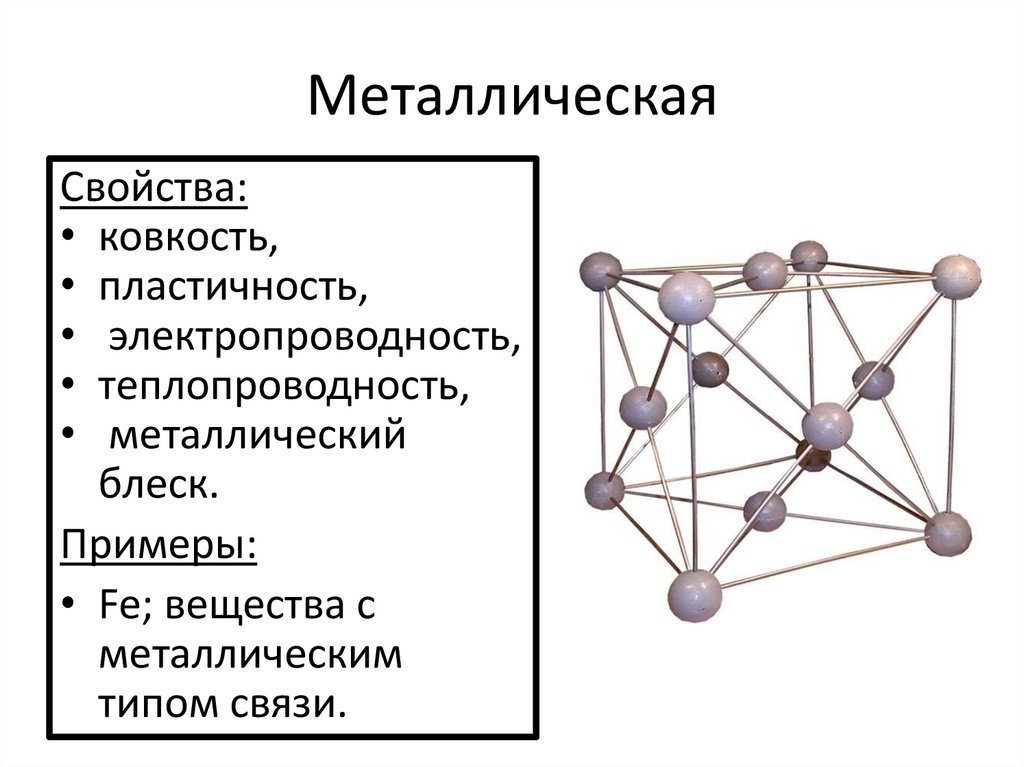
МеталлическаяСвойства:
• ковкость,
• пластичность,
• электропроводность,
• теплопроводность,
• металлический
блеск.
Примеры:
• Fe; вещества с
металлическим
типом связи.
11.
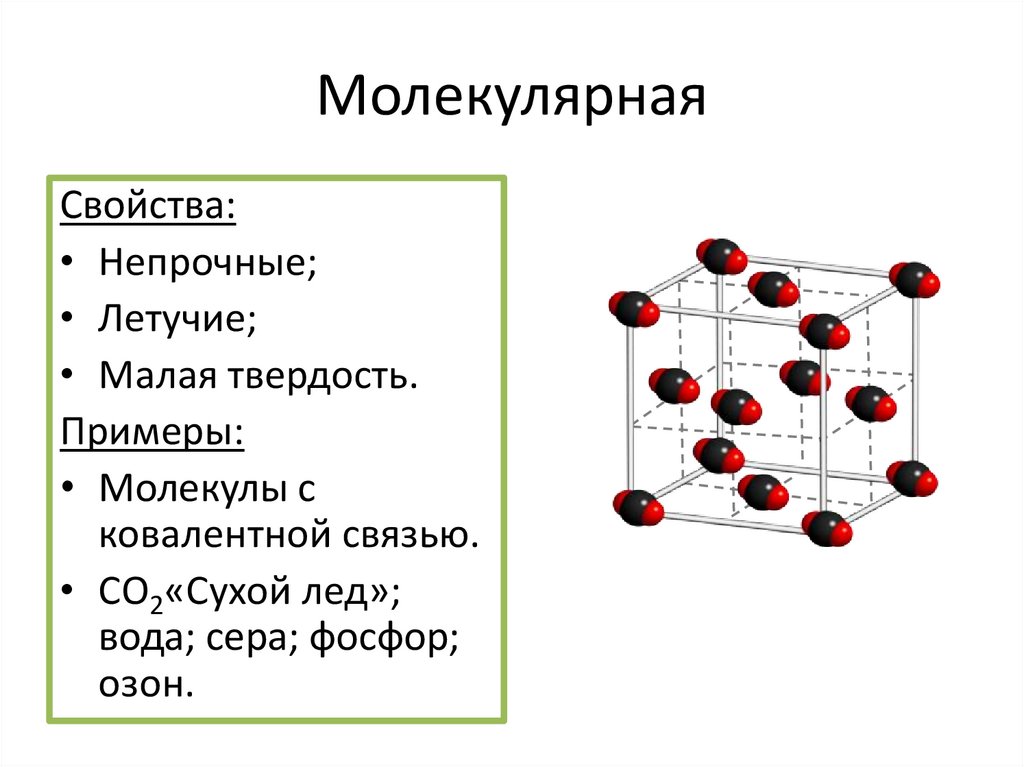
МолекулярнаяСвойства:
• Непрочные;
• Летучие;
• Малая твердость.
Примеры:
• Молекулы с
ковалентной связью.
• СO2«Сухой лед»;
вода; сера; фосфор;
озон.
12.
Закон постоянного составаМолекулярные
химические соединения
независимо от способа
их получения имеют
постоянный состав и
свойства.
Жозеф Луи Пруст



 Химия
Химия