Похожие презентации:
Сложные неорганические вещества
1.
СЛОЖНЫЕНЕОРГАНИЧЕСКИЕ
ВЕЩЕСТВА
2.
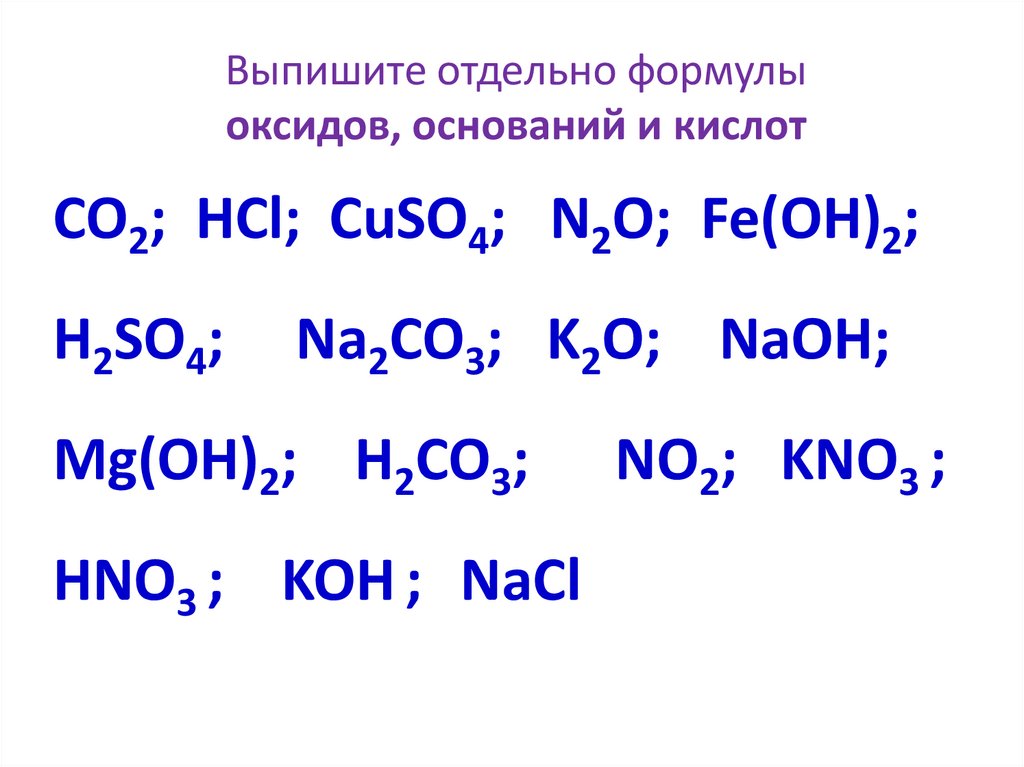
Выпишите отдельно формулыоксидов, оснований и кислот
CO2; HCl; CuSO4; N2O; Fe(OH)2;
H2SO4;
Na2CO3; K2O; NaOH;
Mg(OH)2; H2CO3;
HNO3 ; KOH ; NaCl
NO2; KNO3 ;
3.
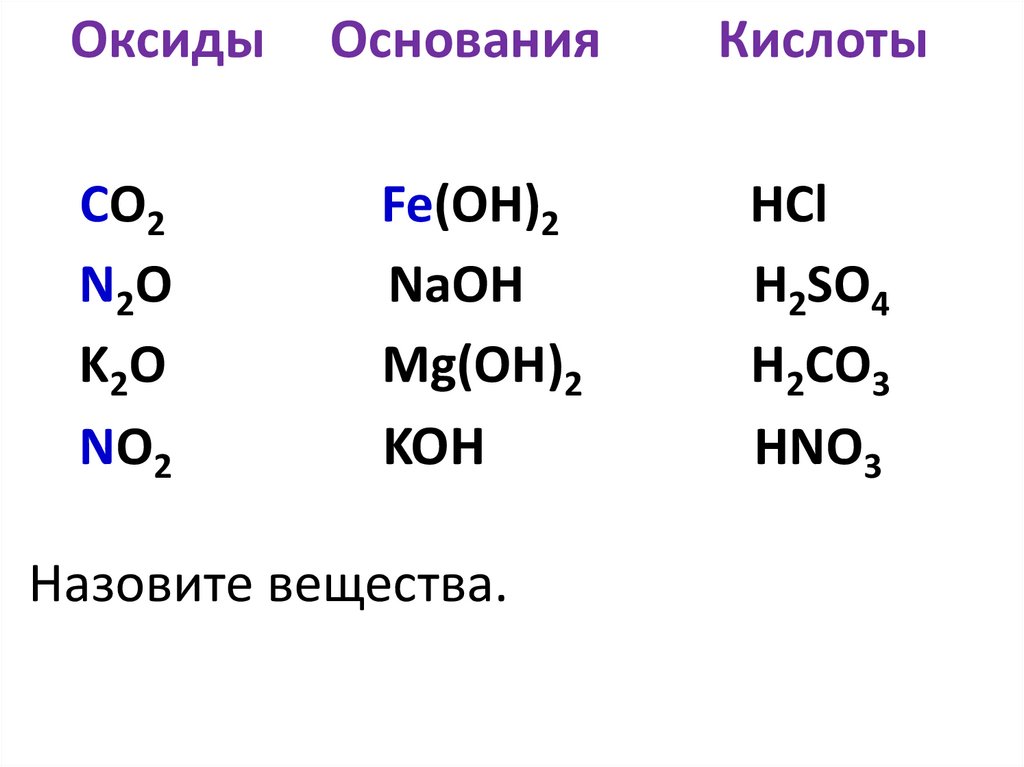
ОксидыCO2
N2O
K2O
NO2
Основания
Кислоты
Fe(OH)2
NaOH
Mg(OH)2
KOH
HCl
H2SO4
H2CO3
HNO3
Назовите вещества.
4.
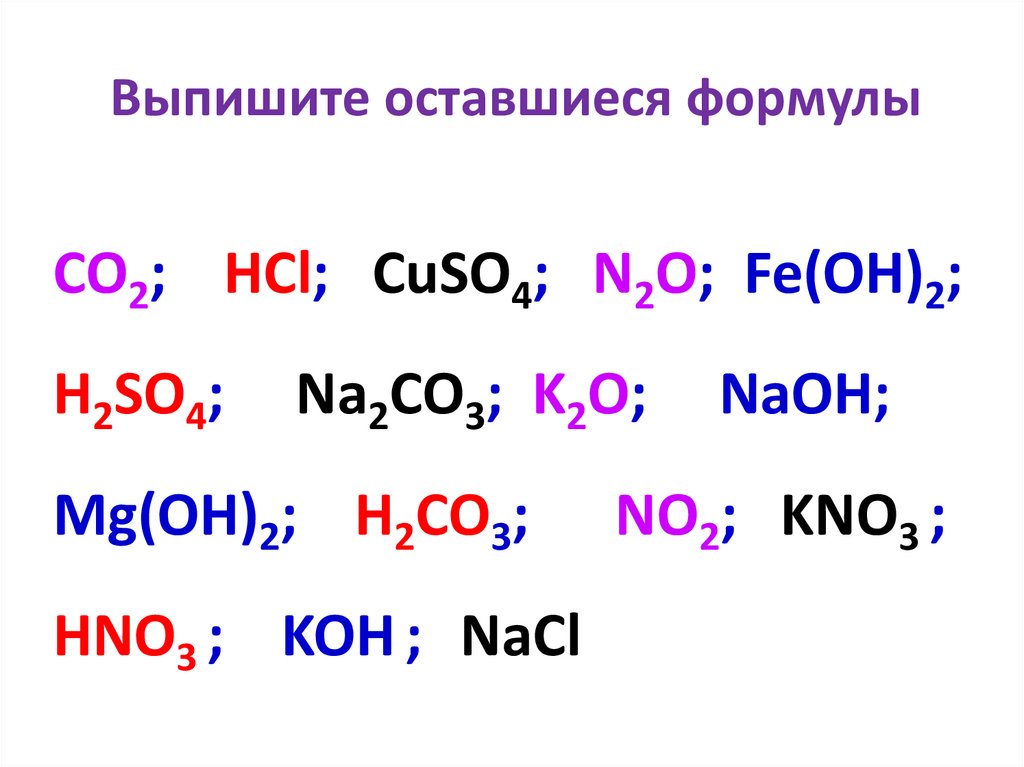
Выпишите оставшиеся формулыCO2; HCl; CuSO4; N2O; Fe(OH)2;
H2SO4;
Na2CO3; K2O;
Mg(OH)2; H2CO3;
HNO3 ; KOH ; NaCl
NaOH;
NO2; KNO3 ;
5.
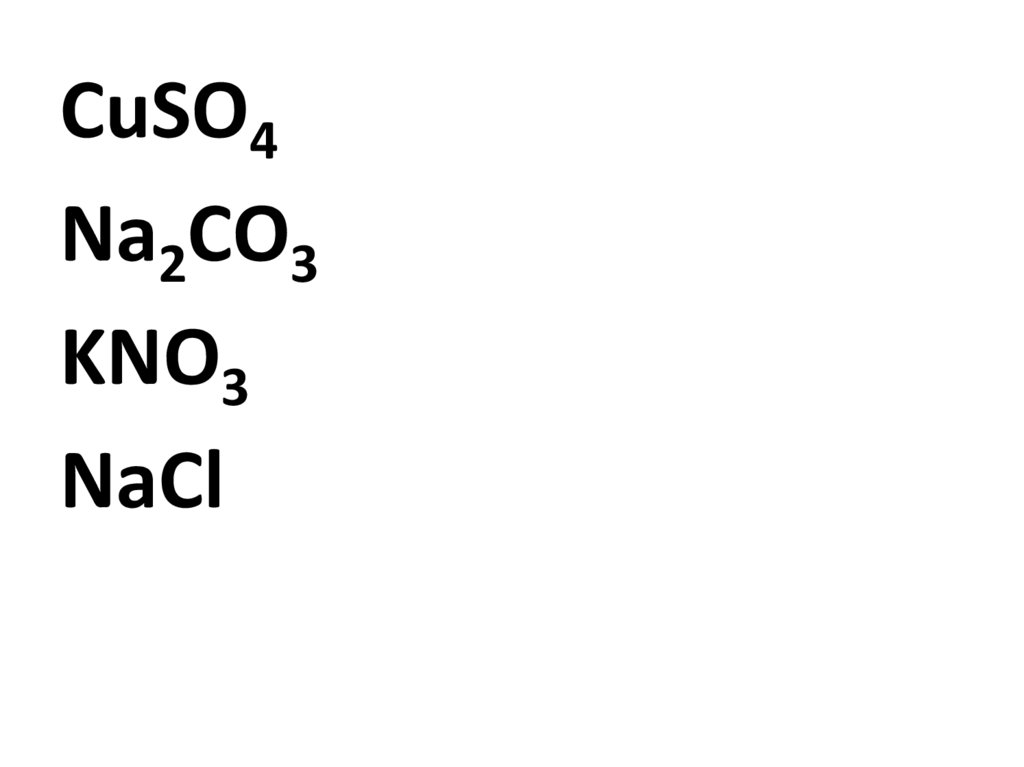
CuSO4Na2CO3
KNO3
NaCl
6.
CuSO4Na2CO3
KNO3
NaCl
H2SO4
H2CO3
HNO3
HCl
7.
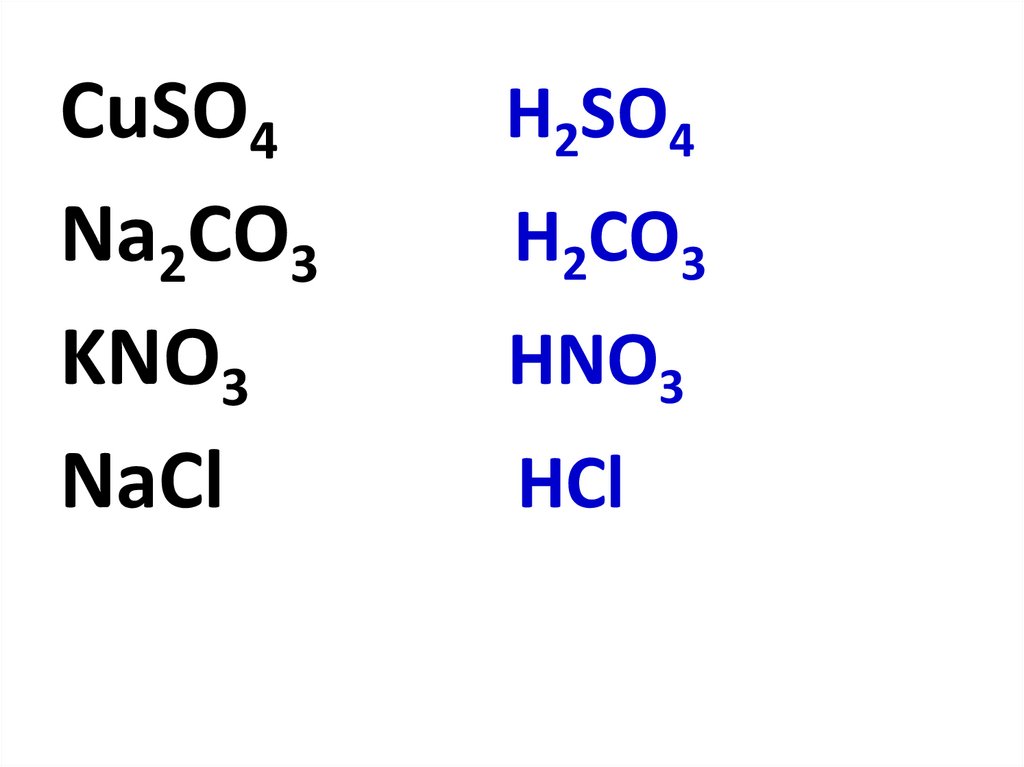
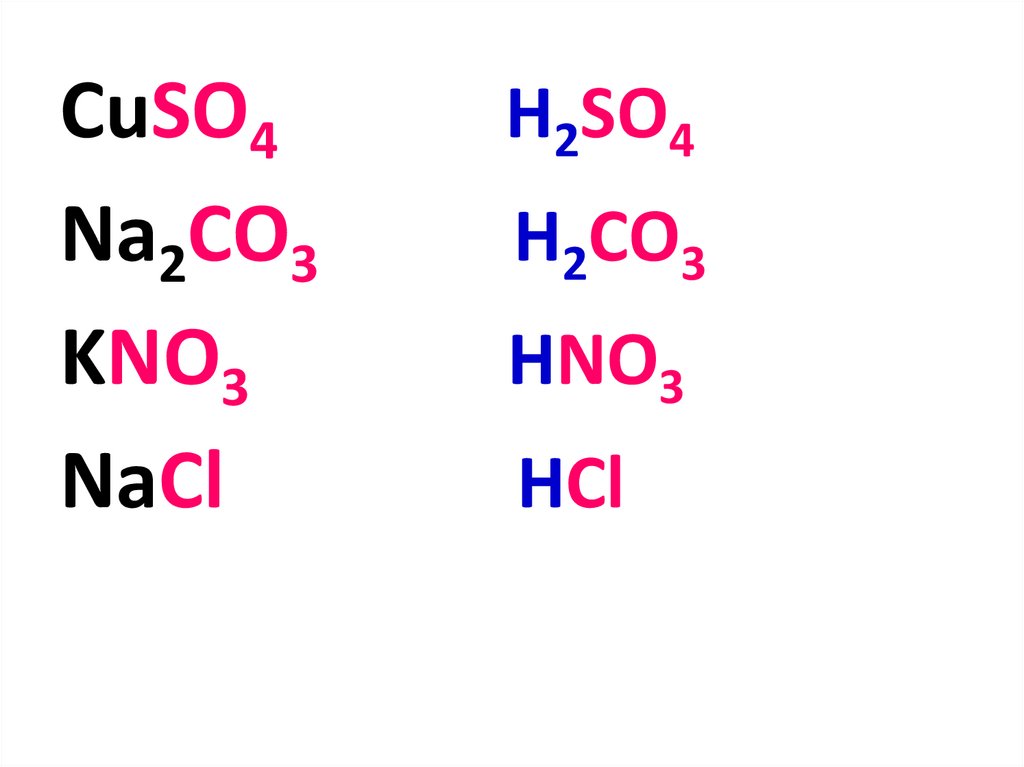
CuSO4Na2CO3
KNO3
NaCl
H2SO4
H2CO3
HNO3
HCl
8.
СОЛИСостав
Номенклатура
Классификация
Получение
Свойства
9.
CuSO4Na2CO3
KNO3
NaCl
Соли – это сложные
вещества, состоящие из
атомов металла и кислотных
остатков.
10.
Номенклатурасолей
11.
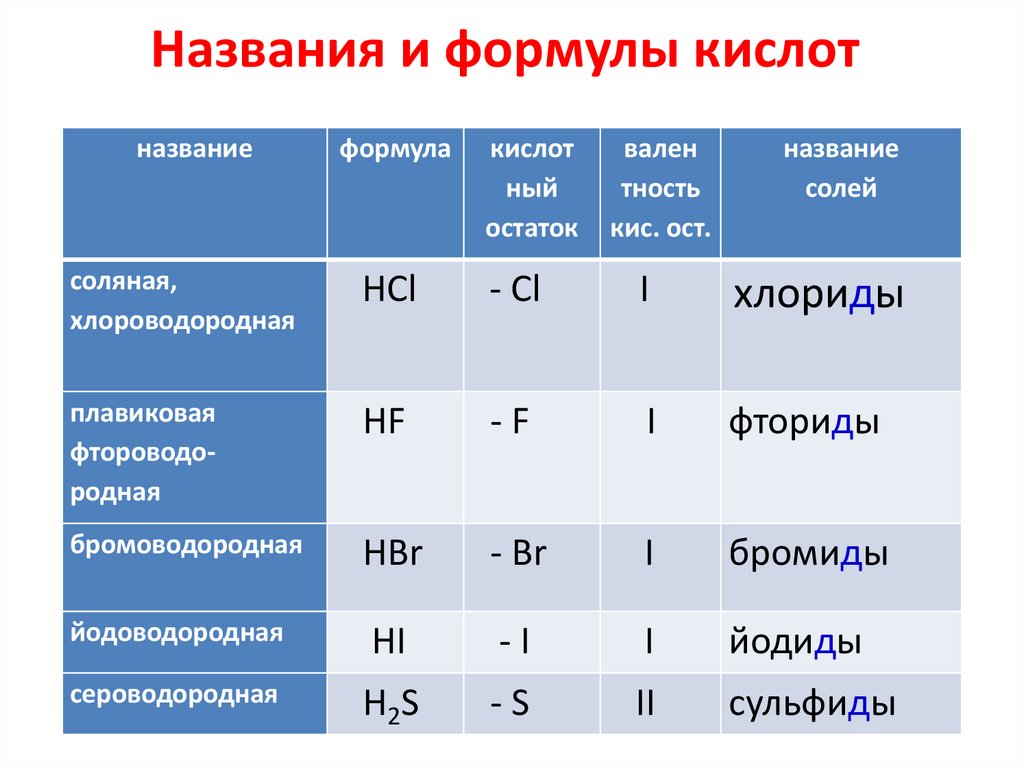
Названия и формулы кислотназвание
формула
кислот
ный
остаток
вален
тность
кис. ост.
название
солей
соляная,
хлороводородная
HCl
- Сl
I
хлориды
плавиковая
фтороводородная
HF
-F
I
фториды
бромоводородная
HBr
- Br
I
бромиды
йодоводородная
HI
-I
I
йодиды
сероводородная
H2S
-S
II
сульфиды
12.
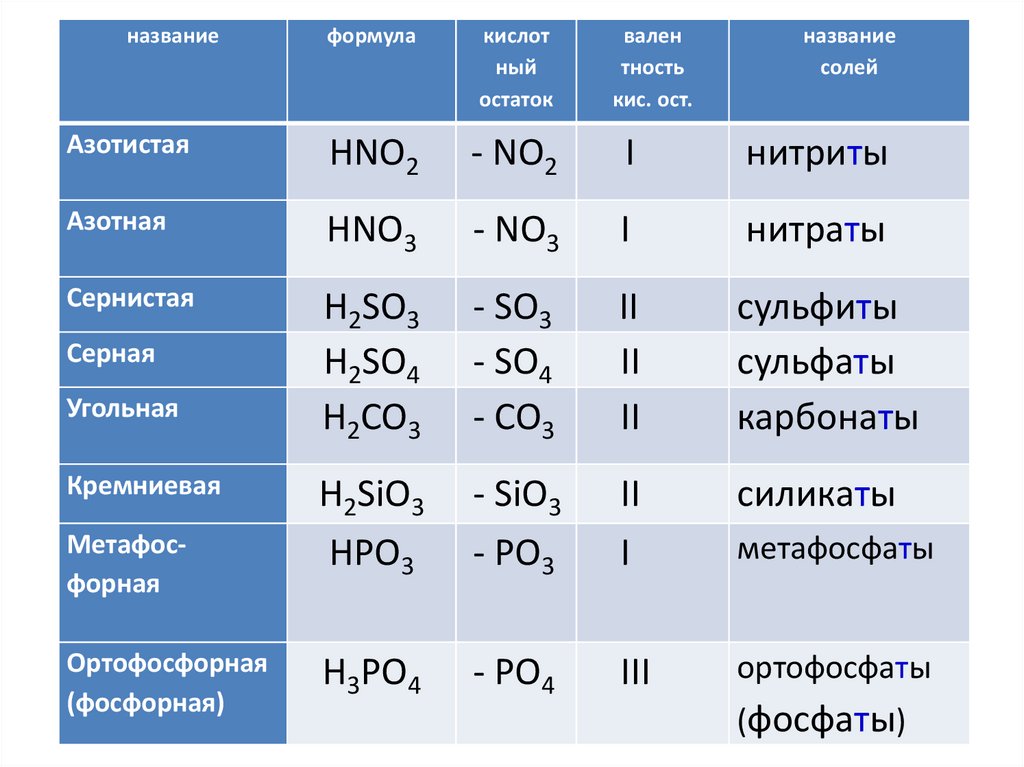
названиеформула
кислот
ный
остаток
Азотистая
HNO2
- NO2
I
нитриты
Азотная
HNO3
- NO3
I
нитраты
Сернистая
H2SO3
H2SO4
H2CO3
- SO3
- SO4
- CO3
II
II
II
сульфиты
сульфаты
карбонаты
H2SiO3
HPO3
- SiO3
- PO3
II
I
силикаты
H3PO4
- PO4
III
ортофосфаты
Серная
Угольная
Кремниевая
Метафосфорная
Ортофосфорная
(фосфорная)
вален
тность
кис. ост.
название
солей
метафосфаты
(фосфаты)
13.
Пользуясь таблицей, назовите соли:CuSO4
Na2CO3
KNO3
NaCl
14.
Пользуясь таблицей, назовите соли:CuSO4 сульфат меди
Na2CO3 карбонат натрия
KNO3
NaCl
нитрат калия
хлорид натрия
15.
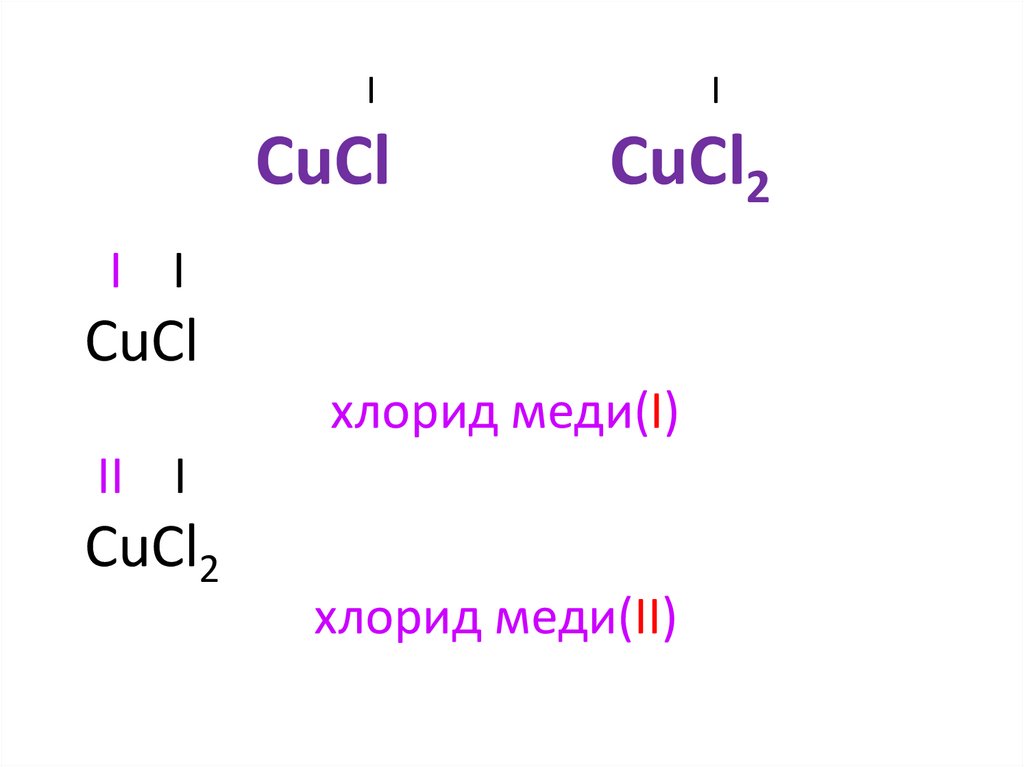
ICuCl
I
CuCl2
I I
CuCl
хлорид меди(I)
II I
CuCl2
хлорид меди(II)
16.
CuSO4 сульфат меди17.
IICuSO4 сульфат меди
18.
II IICuSO4 сульфат меди
19.
II IICuSO4 сульфат меди(II)
20.
Составьте формулы солей:Сульфид калия
Нитрат алюминия
Сульфат бария
21.
Классификациясолей
22.
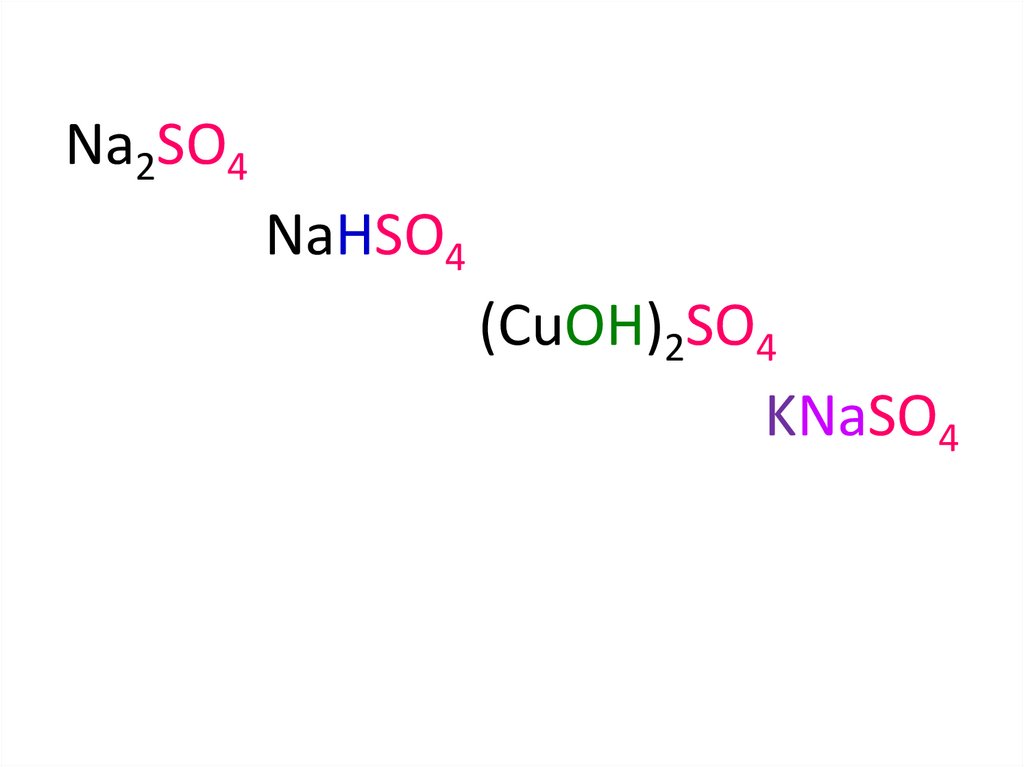
Na2SO4NaHSO4
(CuOH)2SO4
KNaSO4
23.
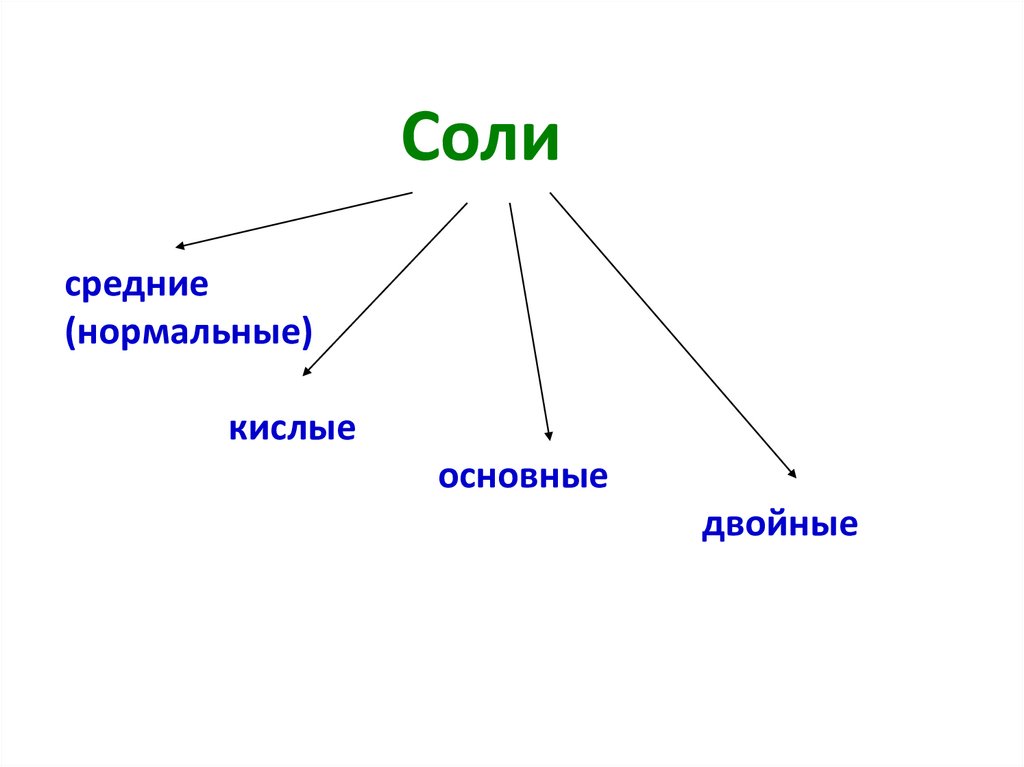
Солисредние
(нормальные)
кислые
основные
двойные
24.
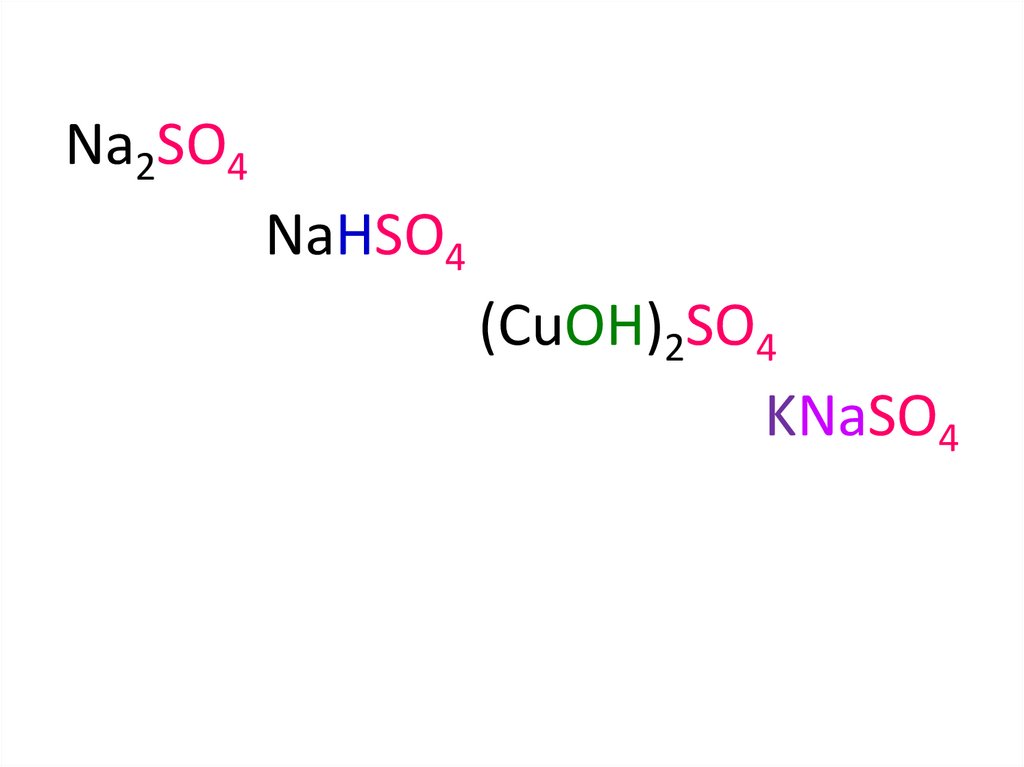
Na2SO4NaHSO4
(CuOH)2SO4
KNaSO4
25.
Оцените свои знания иработу на уроке
Выберите утверждение
1. Я узнаю соли по формулам
2. Я не уверен, что смогу узнать соли по
формулам среди других веществ
26.
Выберите утверждение1.
Я смогу назвать соль
2. Я затрудняюсь в составлении названий
солей
3. Я не смогу самостоятельно дать
название солям
27.
Выберите утверждение1.
Я смогу составить формулу соли по
названию
2. Мне необходима помощь в составлении
формул солей по названиям
28.
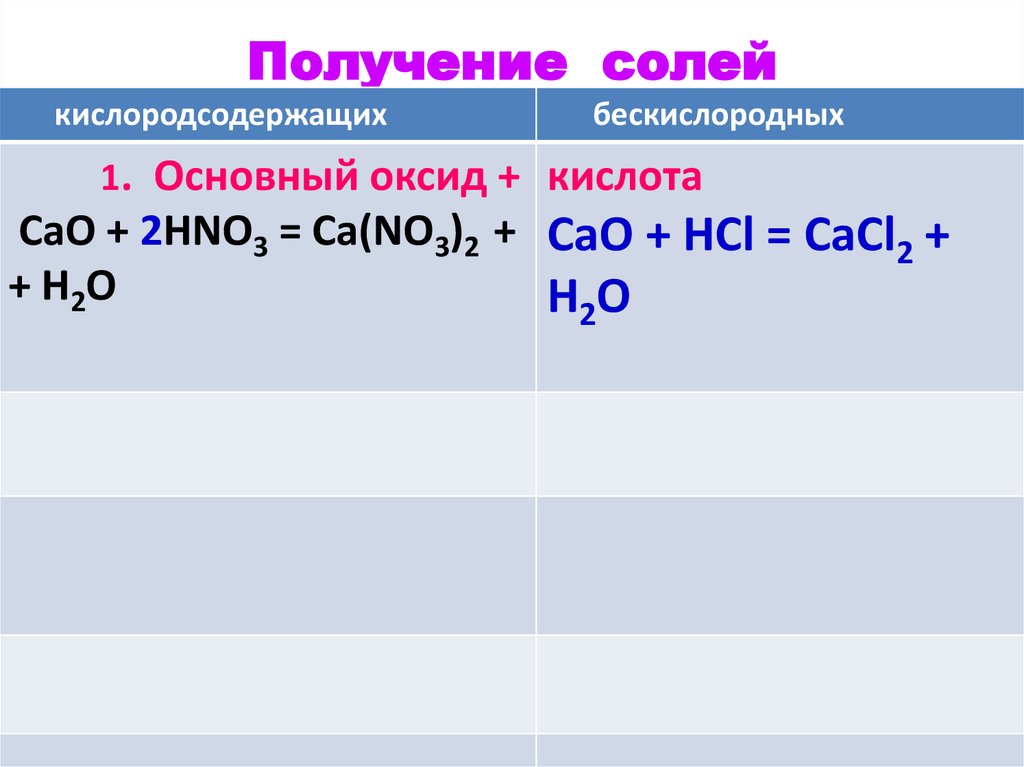
Получение солей29.
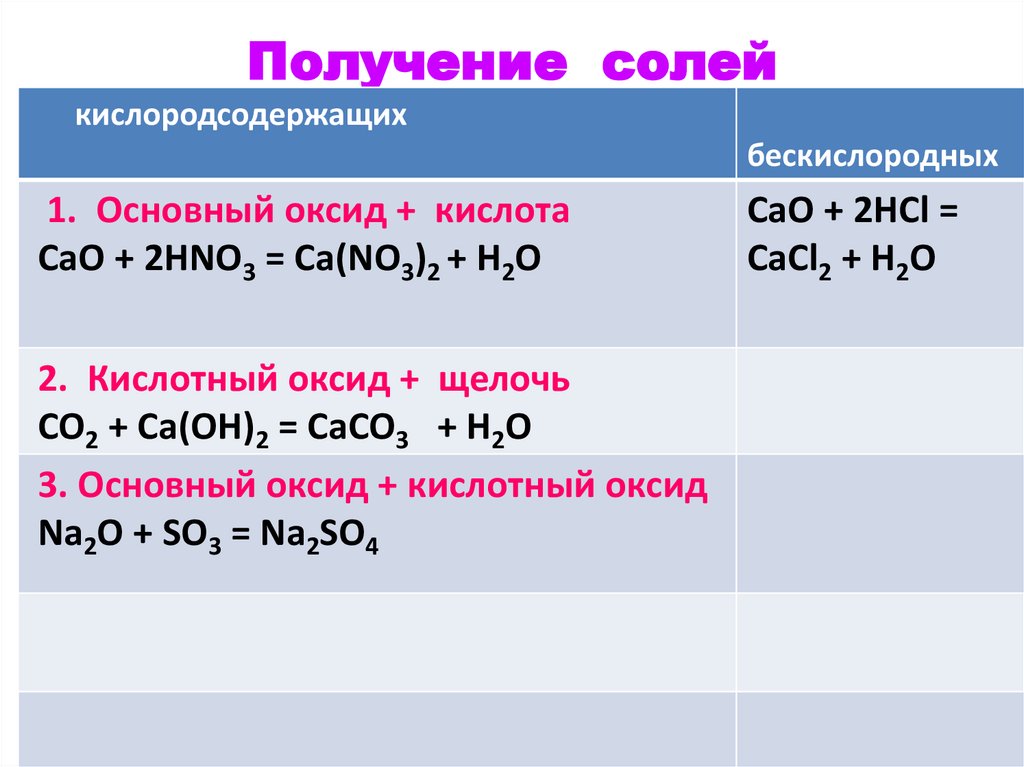
Получение солейкислородсодержащих
бескислородных
30.
Химические свойства оксидовкислотных
основных
1. Взаимодействие
с водой
SO3 + H2O = H2SO4
CaO + H2O = Ca(OH)2
2. Взаимодействие с основаниями
2. Взаимодействие с
CO2 + Ca(OH)2 = CaCO3 + H2O
3. Взаимодействие друг
кислотами
CaO + 2HCl = CaCl2 + H2O
с другом
CaO + CO2 = CaCO3
31.
Получение солейкислородсодержащих
бескислородных
1. Основный оксид + кислота
32.
Получение солейкислородсодержащих
бескислородных
1. Основный оксид + кислота
СаO
33.
Получение солейкислородсодержащих
бескислородных
1. Основный оксид + кислота
II II
СаO
34.
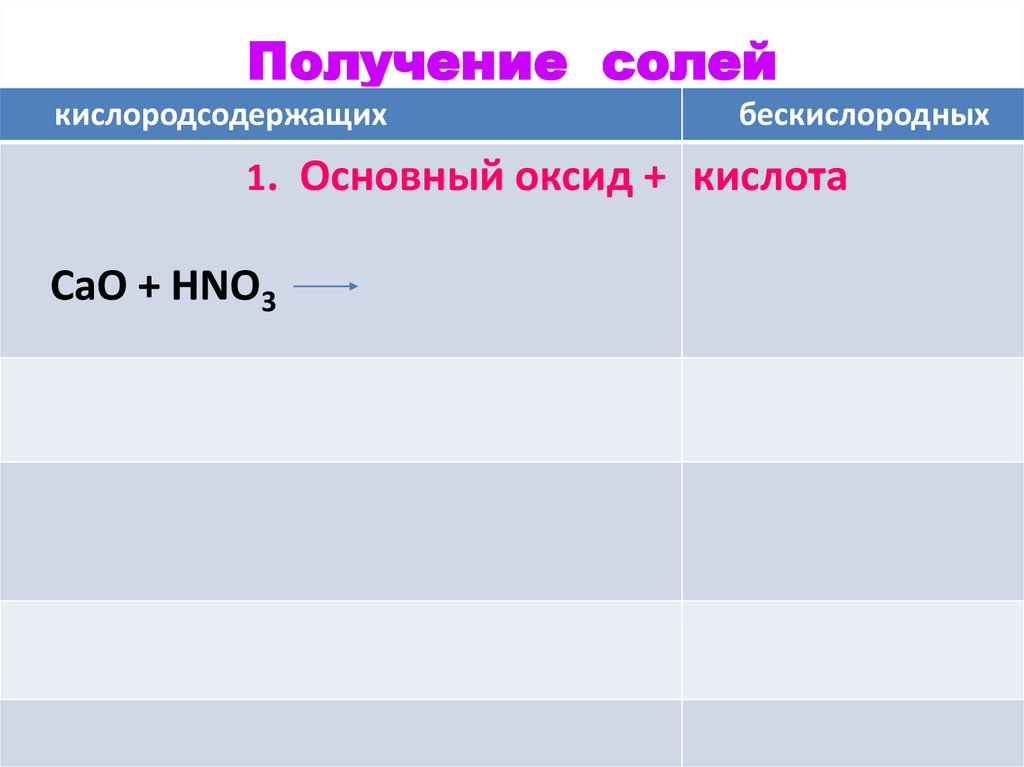
Получение солейкислородсодержащих
бескислородных
1. Основный оксид + кислота
СаO + HNO3
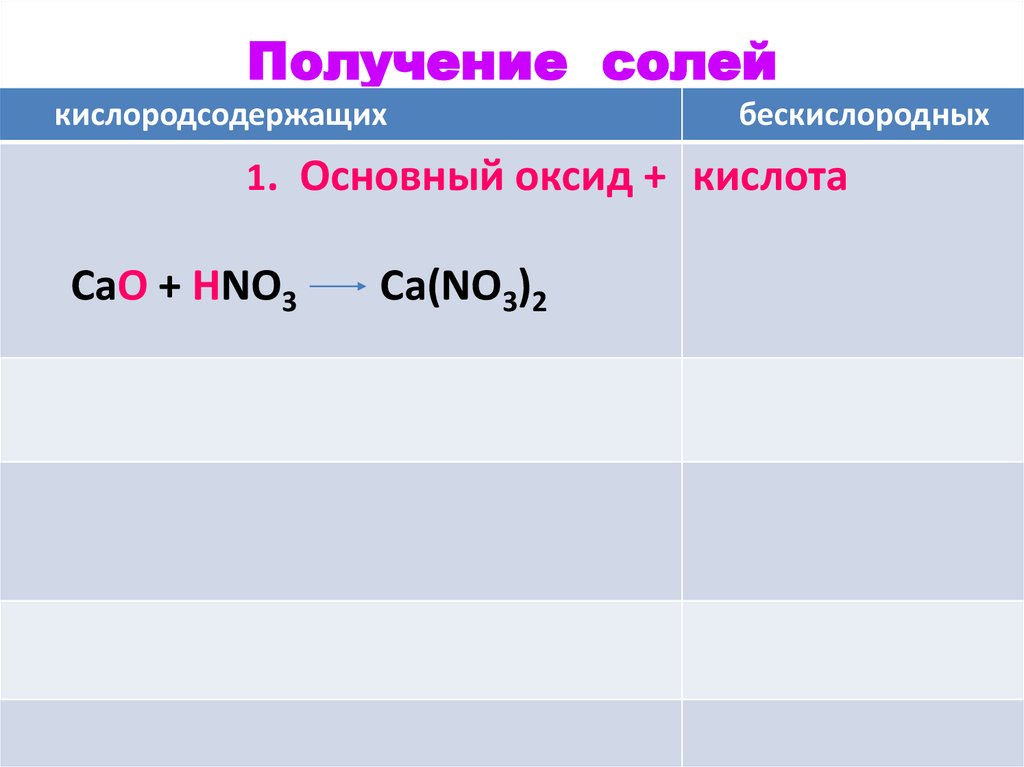
35.
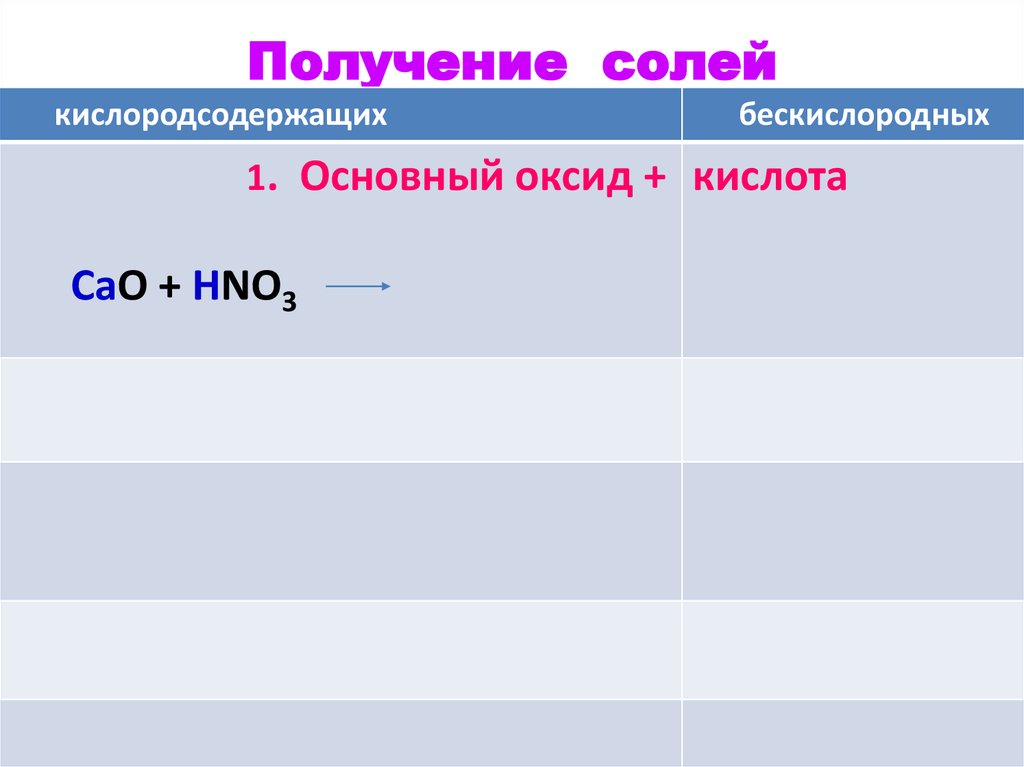
Получение солейкислородсодержащих
бескислородных
1. Основный оксид + кислота
СаO + HNO3
36.
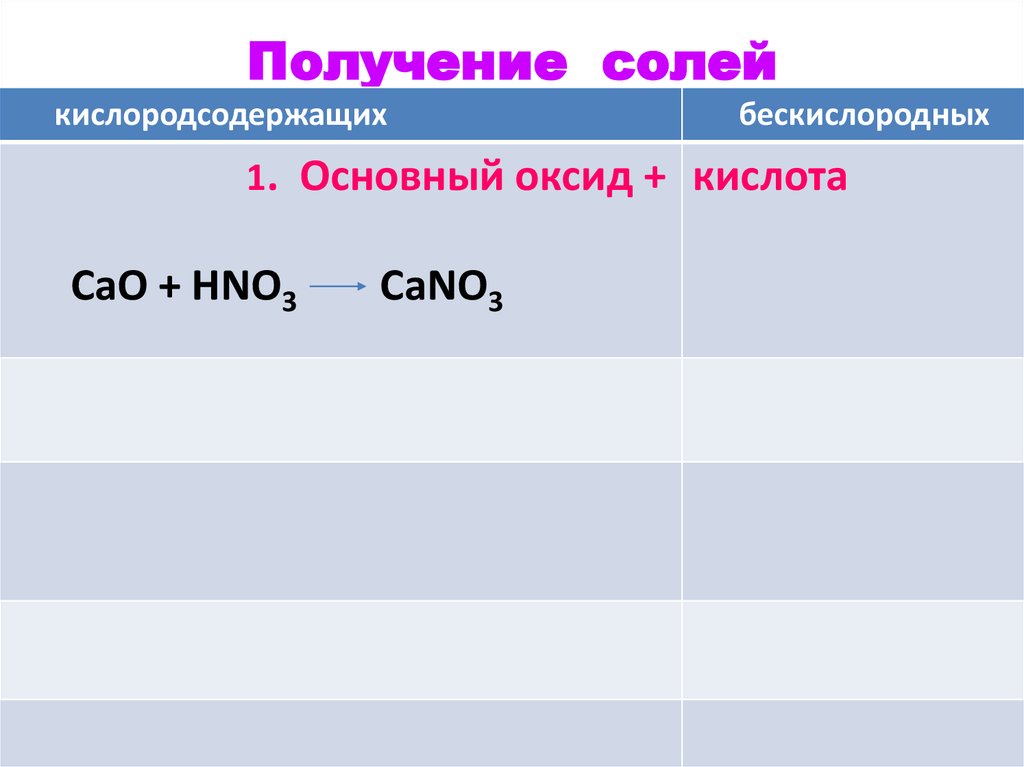
Получение солейкислородсодержащих
бескислородных
1. Основный оксид + кислота
СаO + HNO3
CaNO3
37.
Получение солейкислородсодержащих
бескислородных
1. Основный оксид + кислота
СаO + HNO3
II I
CaNO3
38.
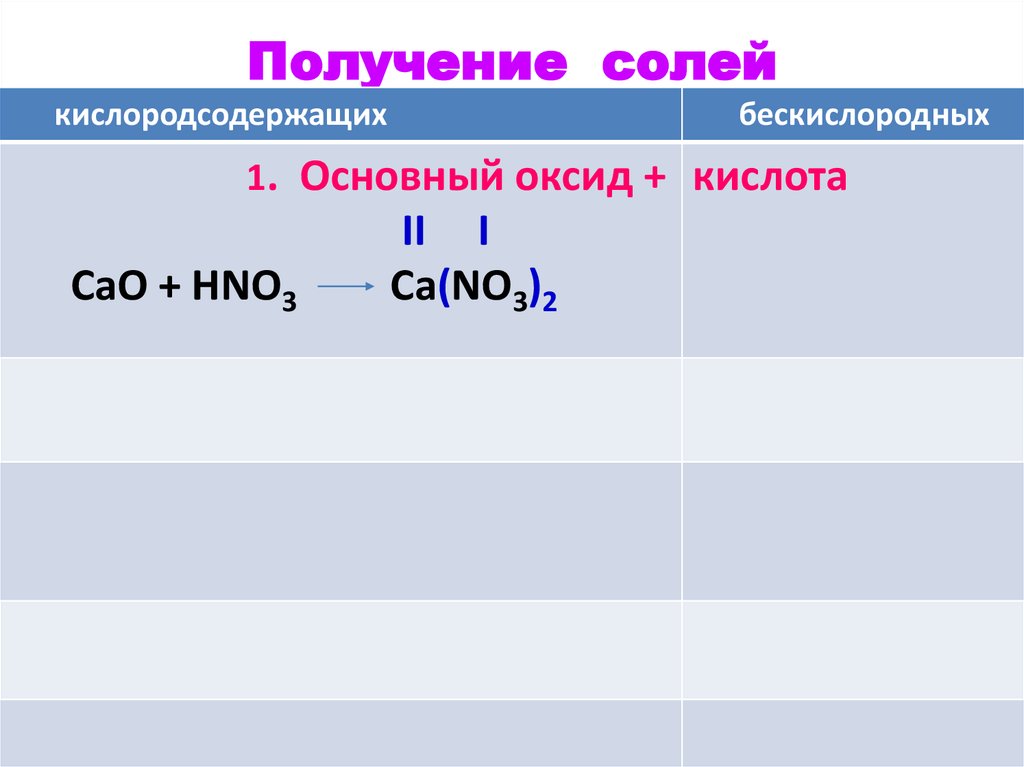
Получение солейкислородсодержащих
бескислородных
1. Основный оксид + кислота
СаO + HNO3
II I
Ca(NO3)2
39.
Получение солейкислородсодержащих
бескислородных
1. Основный оксид + кислота
СаO + HNO3
Ca(NO3)2
40.
Получение солейкислородсодержащих
бескислородных
1. Основный оксид + кислота
СаO + HNO3
Ca(NO3)2 + H2O
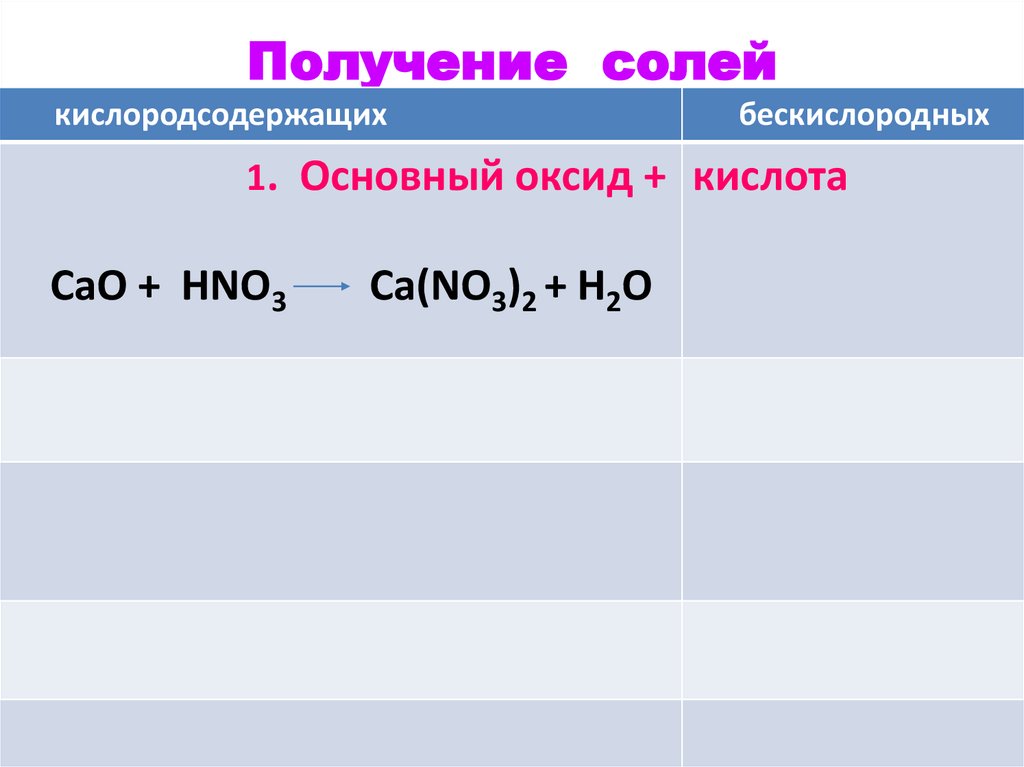
41.
Получение солейкислородсодержащих
бескислородных
1. Основный оксид + кислота
СаO + 2HNO3 = Ca(NO3)2 + H2O
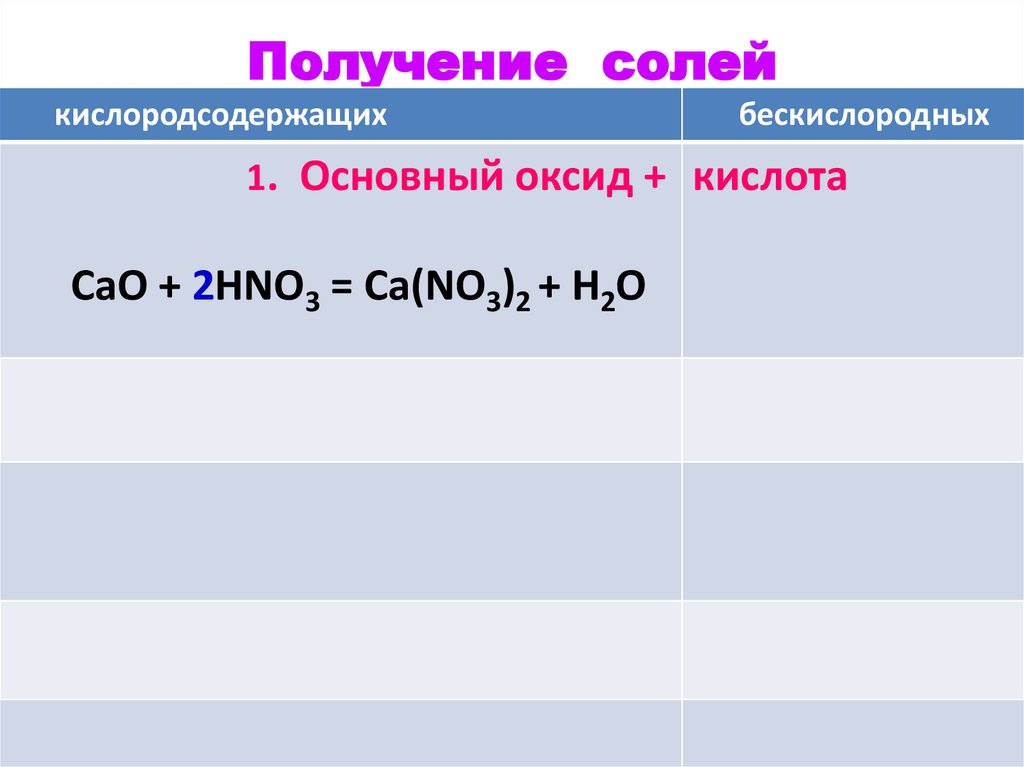
42.
Получение солейкислородсодержащих
бескислородных
1. Основный оксид + кислота
СаO + 2HNO3 = Ca(NO3)2 + CaO + HCl =
+ H2O
43.
Получение солейкислородсодержащих
бескислородных
1. Основный оксид + кислота
СаO + 2HNO3 = Ca(NO3)2 + CaO + HCl = CaCl2 +
+ H2O
HO
2
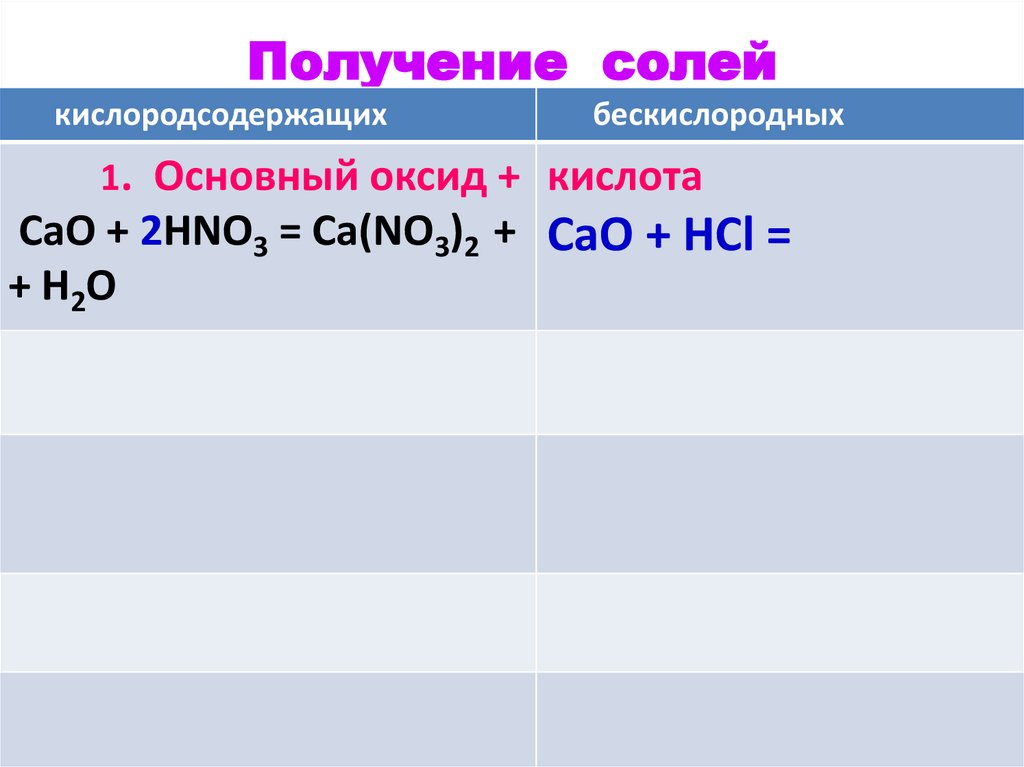
44.
Получение солейкислородсодержащих
бескислородных
1. Основный оксид + кислота
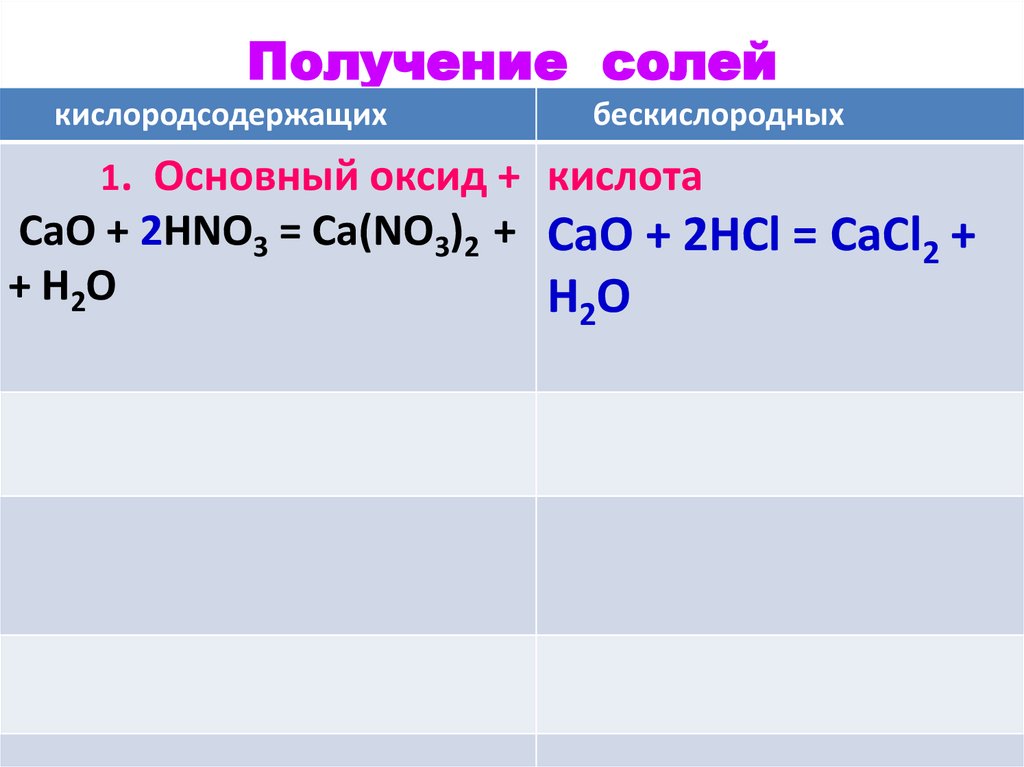
СаO + 2HNO3 = Ca(NO3)2 + CaO + 2HCl = CaCl2 +
+ H2O
HO
2
45.
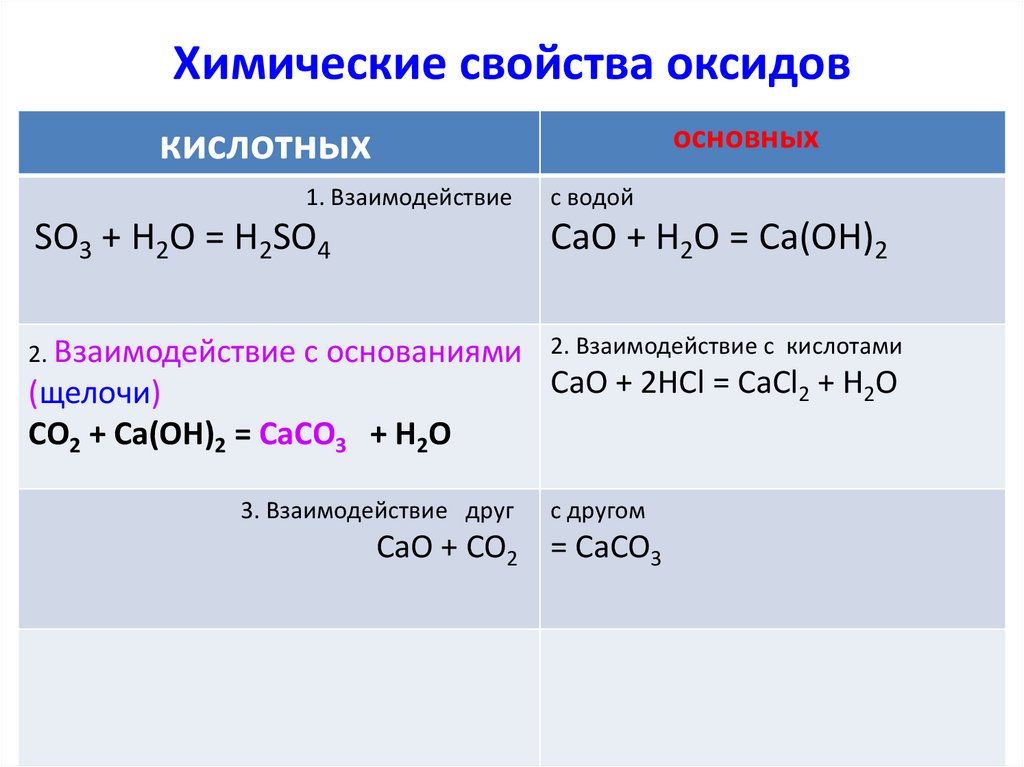
Химические свойства оксидовосновных
кислотных
1. Взаимодействие
с водой
SO3 + H2O = H2SO4
CaO + H2O = Ca(OH)2
2. Взаимодействие с основаниями
2. Взаимодействие с кислотами
(щелочи)
CO2 + Ca(OH)2 = CaCO3 + H2O
3. Взаимодействие друг
CaO + 2HCl = CaCl2 + H2O
с другом
CaO + CO2 = CaCO3
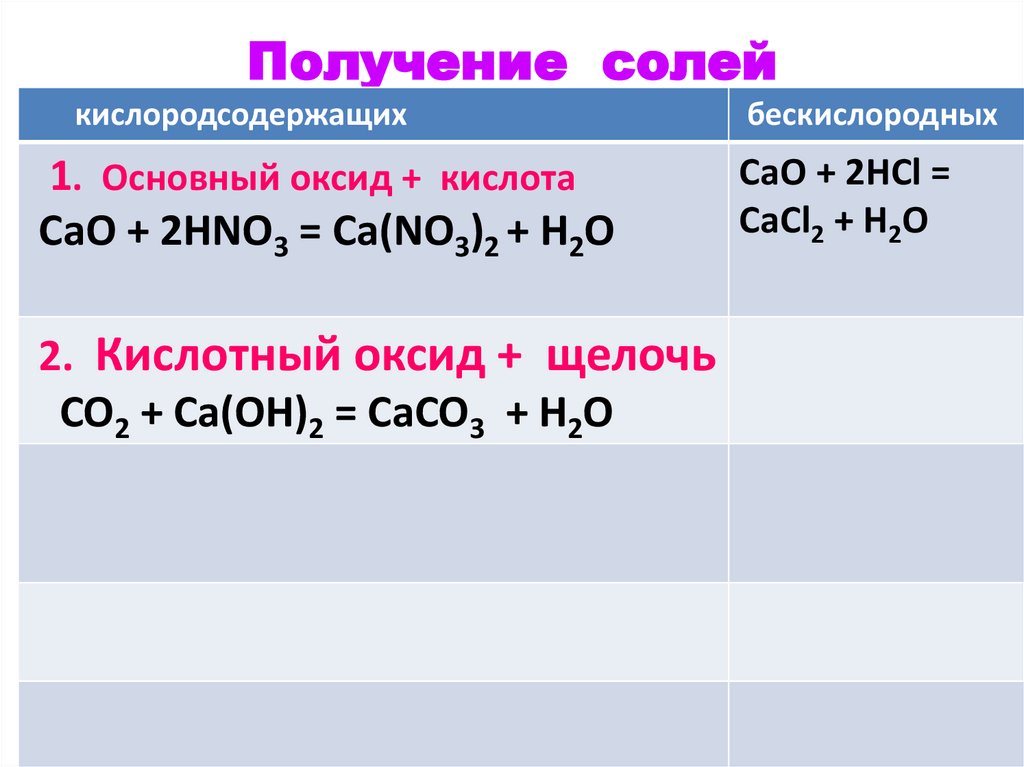
46.
Получение солейкислородсодержащих
1. Основный оксид + кислота
СаO + 2HNO3 = Ca(NO3)2 + H2O
2. Кислотный оксид + щелочь
CO2 + Ca(OH)2 = CaCO3 + H2O
бескислородных
CaO + 2HCl =
CaCl2 + H2O
47.
Химические свойства оксидовосновных
кислотных
1. Взаимодействие
с водой
SO3 + H2O = H2SO4
CaO + H2O = Ca(OH)2
2. Взаимодействие с основаниями
2. Взаимодействие с кислотами
CO2 + Ca(OH)2 = CaCO3 + H2O
CaO + 2HCl = CaCl2 + H2O
3. Взаимодействие друг с другом
CaO + CO2 = CaCO3
48.
Получение солейкислородсодержащих
бескислородных
1. Основный оксид + кислота
СаO + 2HNO3 = Ca(NO3)2 + H2O
2. Кислотный оксид + щелочь
CO2 + Ca(OH)2 = CaCO3 + H2O
3. Основный оксид + кислотный оксид
Na2O + SO3 = Na2SO4
CaO + 2HCl =
CaCl2 + H2O
49.
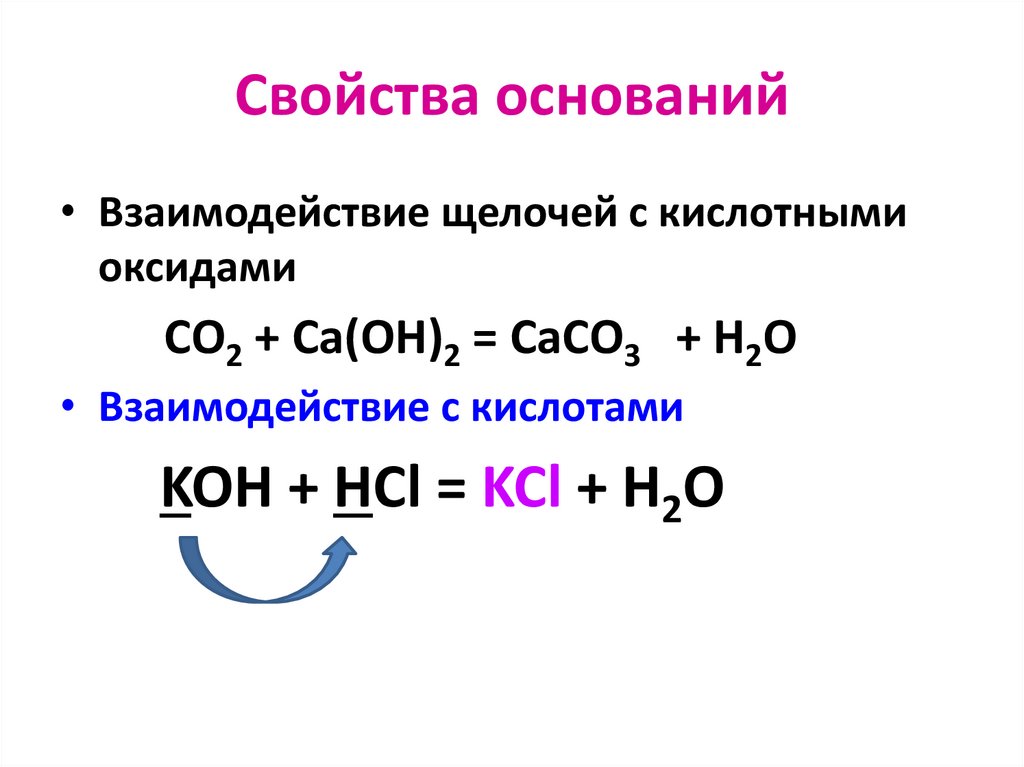
Свойства оснований• Взаимодействие щелочей с кислотными
оксидами
CO2 + Ca(OH)2 = CaCO3 + H2O
• Взаимодействие с кислотами
KOH + HCl = KCl + H2O
50.
Получение солейкислородсодержащих
бескислородных
1. Основный оксид + кислота CaO + 2HCl = CaCl2 +
СаO + 2HNO3 = Ca(NO3)2 + H2O H2O
2. Кислотный оксид + щелочь
CO2 + Ca(OH)2 = CaCO3 + H2O
3. Основный оксид + кислотный оксид
Na2O + SO3 = Na2SO4
4. Основание +
кислота
Cu(OH)2 + H2SO4 = CuSO4 + 2H2O Cu(OH)2 + 2HCl
= CuCl2 + 2H2O
51.
Свойства кислотВзаимодействие с:
индикаторами
металлами
основными оксидами
основаниями
солями
разложение при t
52.
Свойства кислотВзаимодействие с:
индикаторами
металлами
основными оксидами
основаниями
солями
разложение при t
53.
Свойства кислотВзаимодействие с:
индикаторами
металлами
основными оксидами
основаниями
солями
разложение при t
54.
кислородсодержащихПолучение бескислородных
солей
1. Основный оксид + кислота
CaO + 2HCl = CaCl2 + H2O
СаO + 2HNO3 = Ca(NO3)2 + H2O
2. Кислотный оксид + щелочь
CO2 + Ca(OH)2 = CaCO3 + H2O
3. Основный оксид + кислотный
оксид
Na2O + SO3 = Na2SO4
4. Основание + кислота
Cu(OH)2 + H2SO4 = CuSO4 + 2H2O
Cu(OH)2 + 2HCl = CuCl2 + 2H2O
5. Металл + кислота
Mg + H2SO4 = MgSO4 + H2 Mg + 2HCl = MgCl2 + H2
55.
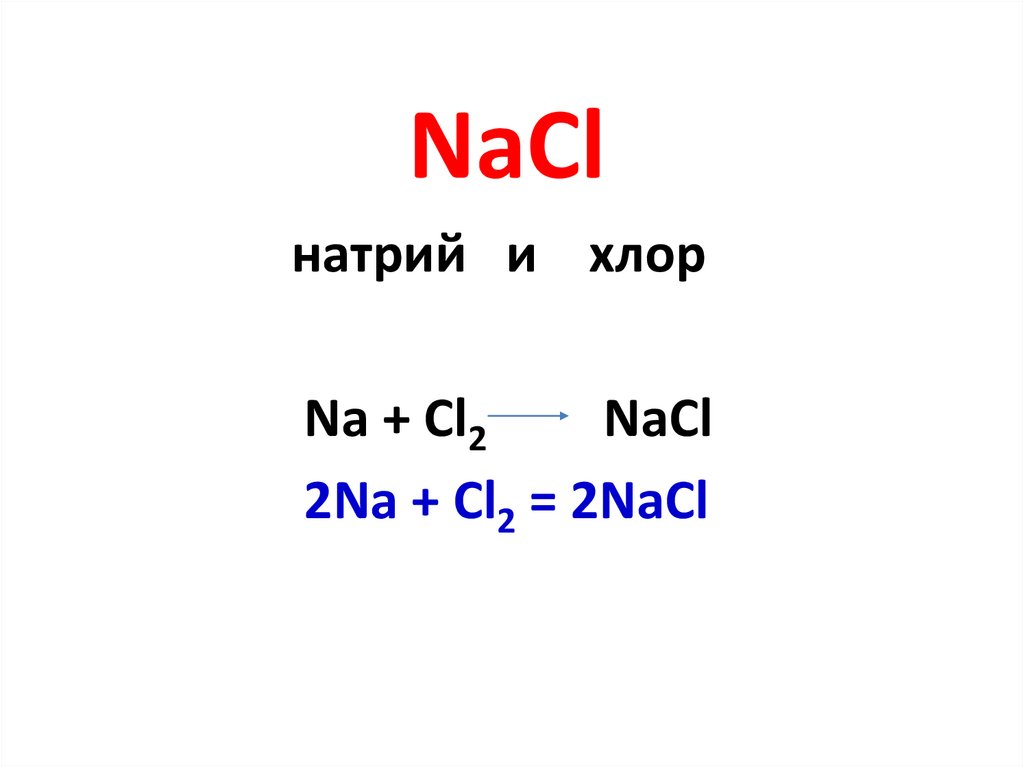
NaClнатрий и хлор
Na + Cl2
NaCl
2Na + Cl2 = 2NaCl
56.
Получение солейкислородсодержащих
бескислородных
1. Основный оксид + кислота
СаO + 2HNO3 = Ca(NO3)2 + H2O
CaO + 2HCl = CaCl2 + H2O
2. Кислотный оксид + щелочь
CO2 + Ca(OH)2 = CaCO3 + H2O
Металл + неметалл
2Na + Cl2 = 2NaCl
3. Основный оксид + кислотный
оксид
Na2O + SO3 = Na2SO4
4. Основание + кислота
Cu(OH)2 + H2SO4 = CuSO4 + 2H2O
Cu(OH)2 + 2HCl = CuCl2 + 2H2O
5. Металл +
Mg + H2SO4 = MgSO4 + H2
кислота
Mg + 2HCl = MgCl2 + H2

























 Химия
Химия








