Похожие презентации:
Реакции разложения
1. Типы реакций
РазложениеСоединение
Обмен
Замещение
2. Реакции разложения
3. Реакции разложения
- этотакие реакции, в
результате которых из одного
сложного вещества
образуется несколько новых
веществ.
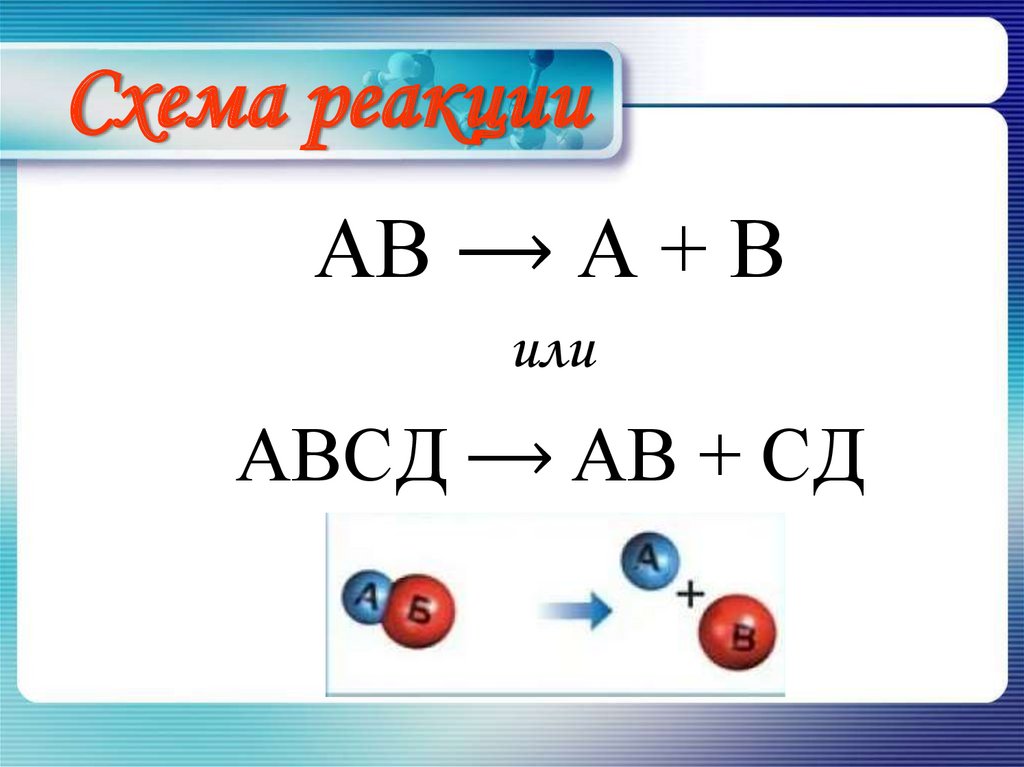
4. Схема реакции
АВ ⟶ А + Вили
АВСД ⟶ АВ + СД
5.
6. Типовые реакции разложения
• 1)Все
нерастворимые
основания
разлагаются
под
действием
t֯,
с
образованием оксида металла этой же
валентности и воды –
2Al(OH)3 → Al2O3 + 3H2O
Cu(OH)2 → CuO + H2O
7. Типовые реакции разложения
• 2) Нерастворимые кислородосодержащиесоли разлагаются под действием t֯, с
образованием оксида металла этой же
валентности и оксида неметалла –
Ca3(PO4)2 → 3CaO + P2O5
CaCO3 → CaO + CO2↑
8.
3)Нерастворимаякислородосодержащая кислота
(H2SiO3) разлагаются под действием t֯,
с образованием оксида неметалла этой
же валентности и воду.
H2SiO3 → SiO2 + H2O
9. Типовые реакции разложения
KMnO4 → K2MnO4 + MnO2 + O2↑HNO3 → NO2↑ + O2↑ + H2O
10. Основные понятия
Катализаторы – это вещества, изменяющиескорость химической реакции, но по окончании
их остающиеся качественно и количественно
неизменным.
Ингибиторы – это вещества, которые замедляют
скорость химической реакции.
Ферменты – катализаторы белковой природы.
11. Закрепление
A) Cu(NO3)2 ⟶ CuO + NO2 + O2↑Б) SO3 + H2O ⟶ H2SO4
В) Mg+O2 ⟶ MgO
Г) HgO ⟶ Hg + O2↑
Д) Na2CO3 + HCl ⟶ NaCl + CO2 + H2O
Е) KClO3 ⟶ KCl + O2
1.
2.
Какие реакции относятся к
реакциям разложения?
Расставить коэффициенты в
реакциях разложения.









 Химия
Химия








