Похожие презентации:
Фосфор. Строение атома фосфора
1.
Найдите химическую ошибку:Артур Конан Дойль
«СОБАКА БАСКЕРВИЛЕЙ»
2.
Шерлок Холмс: «Фосфор! Страннаясмесь…Совершенно без запаха.
Состав преступления теперь
налицо…»
3.
4.
Строение атома фосфора5.
Открытие фосфора• В поисках эликсира молодости
и попытках получения золота
алхимик XVII столетия Геннинг
Бранд из Гамбурга пытался
изготовить "философский
камень".
• В результате Бранд получил
вещество, обладающее
необыкновенными свойствами:
оно светилось в темноте.
6.
В России термин фосфор введен в1746 году Михаилом Васильевичем
Ломоносовым.
7.
Фосфор занимает 13 место средивсех элементов.
8.
Общая характеристика.•Р
неметалл,
Фосфор
Ar=31
V группа, главная подгруппа
• ( Phosphorus3 период, 3 ряд
Cветоносец)
степени окисления -3.0,+1,+3,+5.
оксиды Р2О3 и Р2О5 - оба оксида
кислотные
• Кислоты:
• H 3PO3 –фосфористая кислота
H3PO4 –фосфорная кислота
• летучее водородное соединение
РН3-газ фосфин ( связь ковалентная
почти неполярная)
9.
Способность атомов одного химическогоэлемента образовывать несколько простых
веществ называют аллотропией, а эти
простые вещества – аллотропными
видоизменениями или модификациями
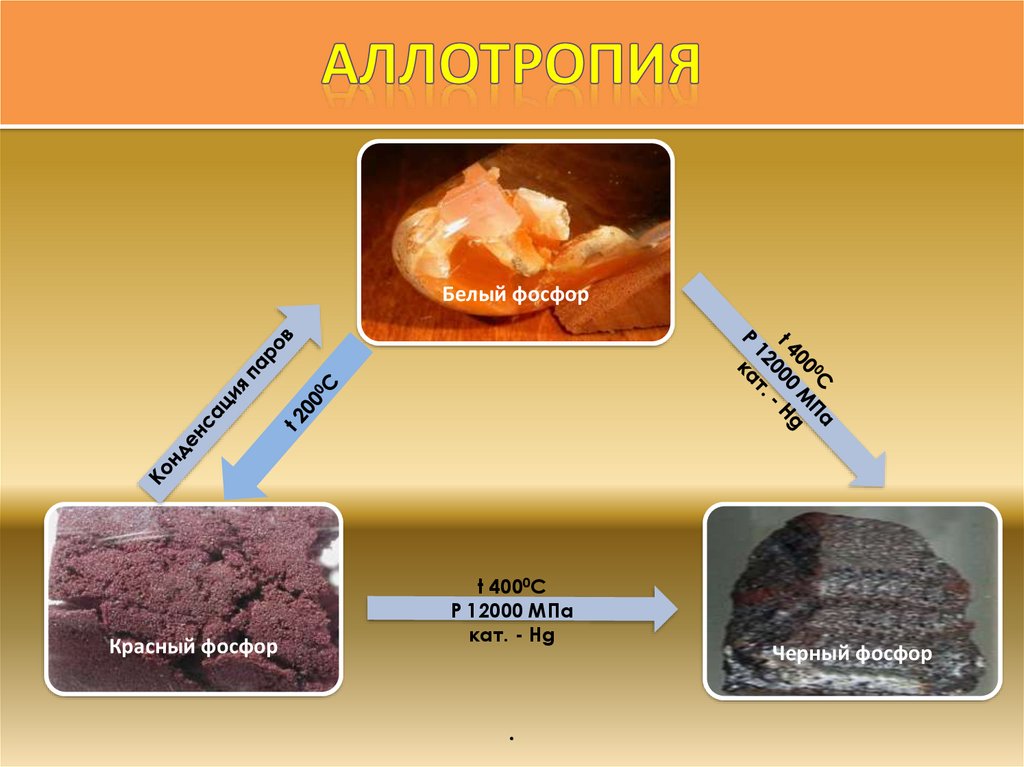
10.
Белый фосфорКрасный фосфор
t 4000C
Р 12000 МПа
кат. - Hg
.
Черный фосфор
11.
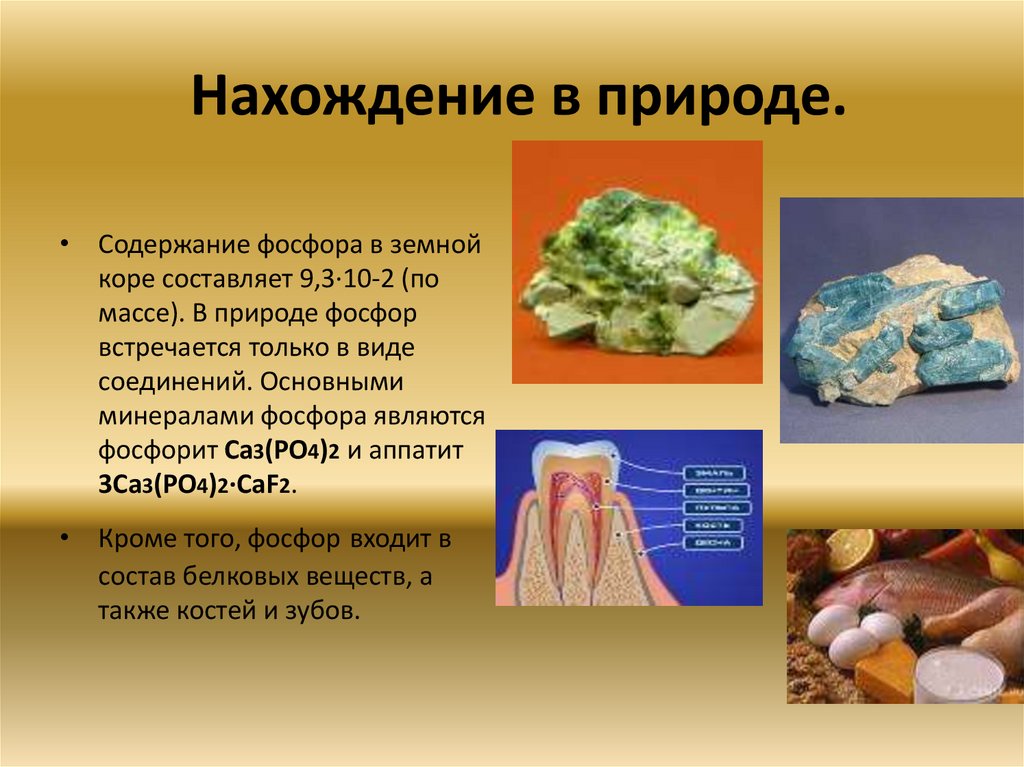
Нахождение в природе.• Содержание фосфора в земной
коре составляет 9,3·10-2 (по
массе). В природе фосфор
встречается только в виде
соединений. Основными
минералами фосфора являются
фосфорит Ca3(PO4)2 и аппатит
3Ca3(PO4)2·CaF2.
• Кроме того, фосфор входит в
состав белковых веществ, а
также костей и зубов.
12.
Химические свойства1) Реакция горения
4Р + 5О2 = 2Р2О5
2) Взаимодействие с
активными металлами
3Mg + 2P = Mg3P2
Фосфид кальция
3) С Н2 не реагирует
Са3 Р2 + 6НСl = 3СаСl2 + 2РН3
фосфин
13.
Фосфор - “элемент жизни имысли”.
• Ортофосфат Са3(Р04)2
• фторапатит 3Са3(Р04)2 • CaF2
• дигидрофосфат Са(Н2Р04)2











 Химия
Химия








