Похожие презентации:
Жёсткость воды. Способы умягчения воды в быту; на производстве
1. Жёсткость воды. Способы умягчения воды в быту; на производстве
Выполнила: Гармаева Амгалана, ученица 9 А класса2.
План:1) Что такое жёсткость воды?
На какие типы делится вода
в зависимости от жёсткости?
2) Что такое умягчение воды?
В чем польза?
3) Способы умягчения в быту
4) Способы умягчения на
производстве
5) Общий вывод
3.
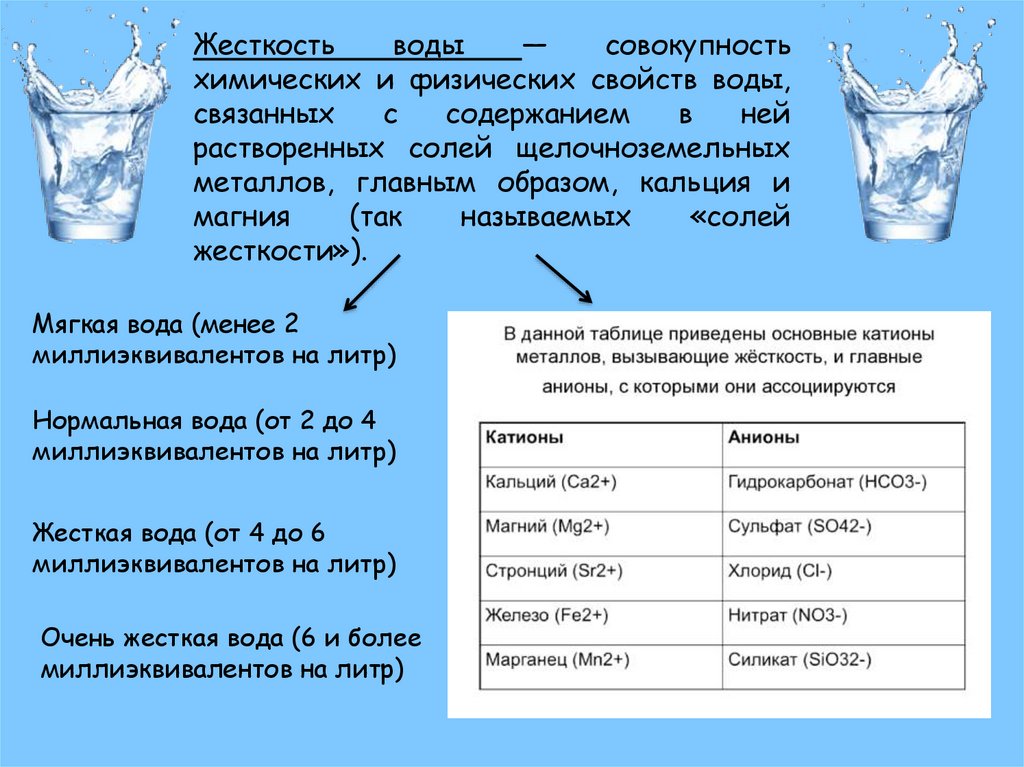
Жесткостьводы
—
совокупность
химических и физических свойств воды,
связанных
с
содержанием
в
ней
растворенных солей щелочноземельных
металлов, главным образом, кальция и
магния
(так
называемых
«солей
жесткости»).
Мягкая вода (менее 2
миллиэквивалентов на литр)
Нормальная вода (от 2 до 4
миллиэквивалентов на литр)
Жесткая вода (от 4 до 6
миллиэквивалентов на литр)
Очень жесткая вода (6 и более
миллиэквивалентов на литр)
4.
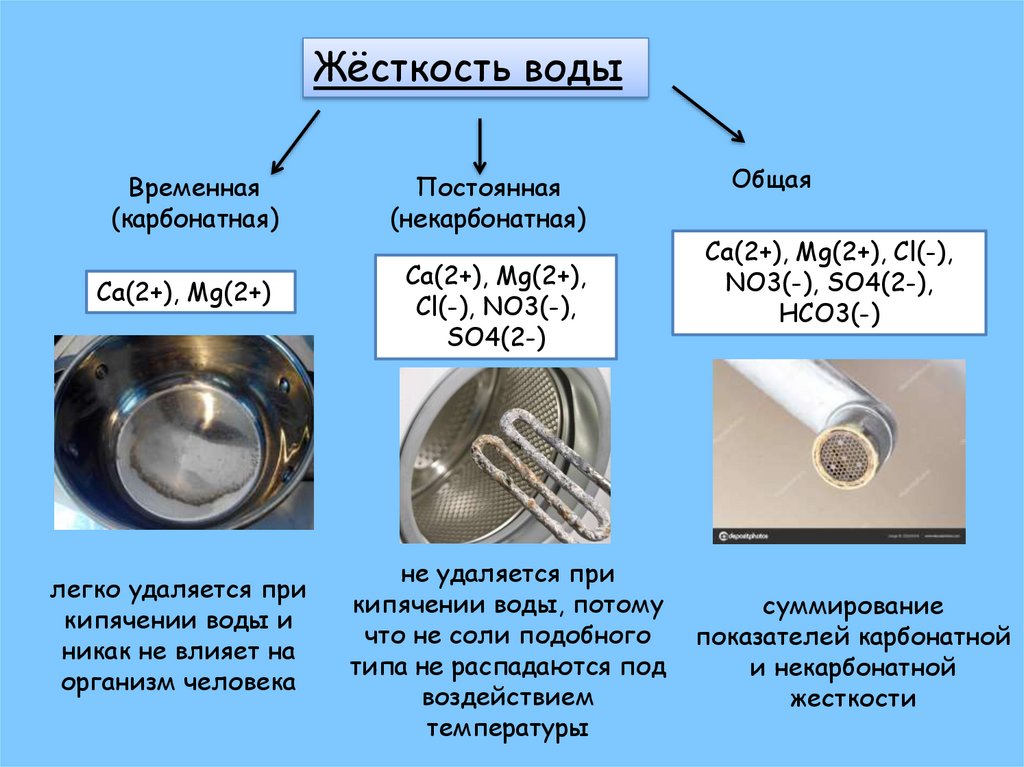
Жёсткость водыВременная
(карбонатная)
Ca(2+), Mg(2+)
легко удаляется при
кипячении воды и
никак не влияет на
организм человека
Постоянная
(некарбонатная)
Ca(2+), Mg(2+),
Cl(-), NO3(-),
SO4(2-)
не удаляется при
кипячении воды, потому
что не соли подобного
типа не распадаются под
воздействием
температуры
Общая
Ca(2+), Mg(2+), Cl(-),
NO3(-), SO4(2-),
HCO3(-)
суммирование
показателей карбонатной
и некарбонатной
жесткости
5.
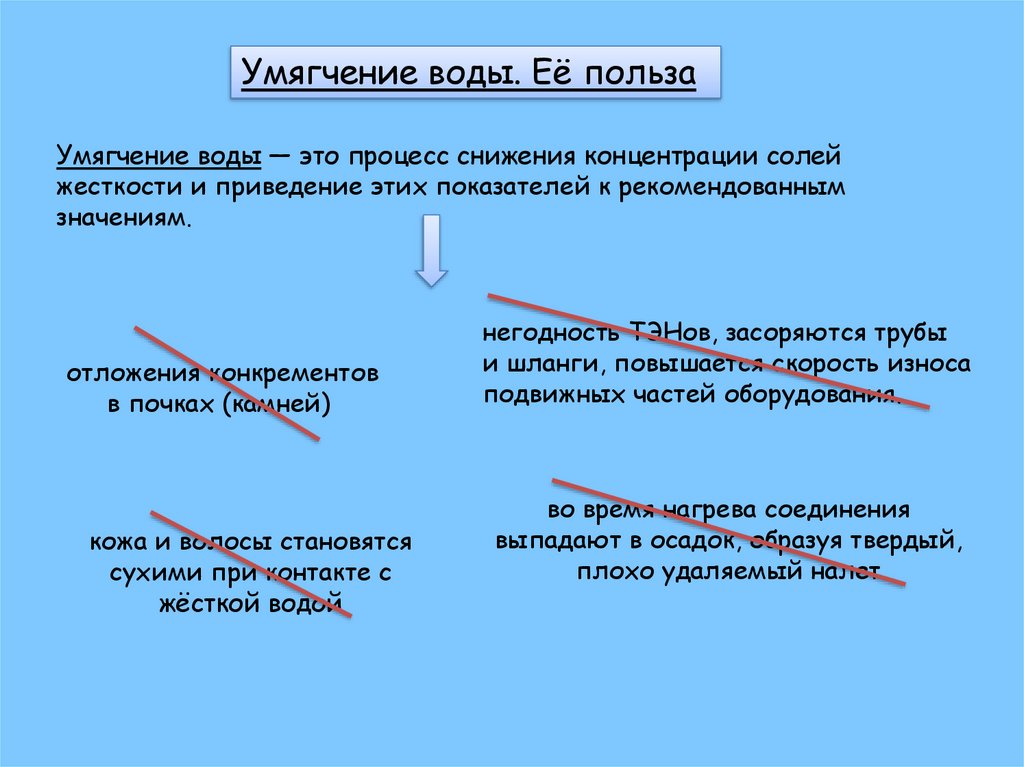
Умягчение воды. Её пользаУмягчение воды — это процесс снижения концентрации солей
жесткости и приведение этих показателей к рекомендованным
значениям.
отложения конкрементов
в почках (камней)
кожа и волосы становятся
сухими при контакте с
жёсткой водой
негодность ТЭНов, засоряются трубы
и шланги, повышается скорость износа
подвижных частей оборудования.
во время нагрева соединения
выпадают в осадок, образуя твердый,
плохо удаляемый налет
6.
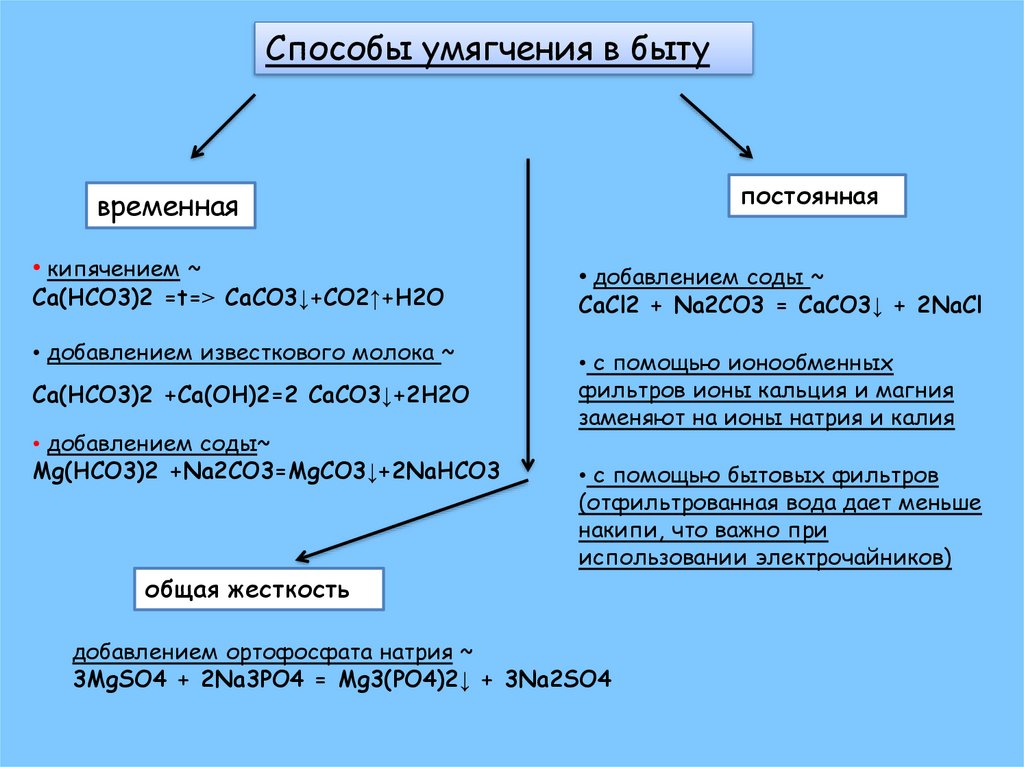
Способы умягчения в бытупостоянная
временная
• кипячением ~
Ca(HCO3)2 =t=˃ CaCO3↓+CO2↑+H2O
• добавлением известкового молока ~
Ca(HCO3)2 +Ca(OH)2=2 CaCO3↓+2H2O
• добавлением соды~
Mg(HCO3)2 +Na2CO3=MgCO3↓+2NaHCO3
общая жесткость
• добавлением соды ~
CaCl2 + Na2CO3 = CaCO3↓ + 2NaСl
• с помощью ионообменных
фильтров ионы кальция и магния
заменяют на ионы натрия и калия
• с помощью бытовых фильтров
(отфильтрованная вода дает меньше
накипи, что важно при
использовании электрочайников)
добавлением ортофосфата натрия ~
3MgSO4 + 2Na3PO4 = Mg3(PO4)2↓ + 3Na2SO4
7.
Способы умягчения на производстве1) Щелочной метод
• Ca(HCO3)2 + 2NaOH = CaCO3↓ + Na2CO3 +
H2O
• Mg(HCO3)2 + 2NaOH = Mg(OH)2↓ + Na2CO3 +
H2O + CO2 CaSO4 + Na2CO3 = CaCO3↓ +
Na2SO4
• CaCl2 + Na2CO3 = CaCO3↓ + 2NaCl
• CO2 +NaOH = Na2CO3 + H2O
• MgSO4 + 2NaOH = Mg(OH)2↓ + Na2SO4
• MgCl2 + 2NaOH = Mg(OH)2↓ + 2NaCl
Вывод:
1) гидроксид натрия (NaOH) в процессе умягчения воды
расходуется на устранение карбонатной жесткости и
нейтрализацию углекислого газа, растворенного в воде.
2) сода (Na2CO3), образующаяся при распаде
гидрокарбонатов и нейтрализации углекислого газа,
используется для удаления некарбонатной жесткости.
8.
2) Фосфатный метод.Данный метод умягчения воды является
наиболее эффективным реагентным методом.
Сущность метода заключается в образовании
кальциевых и магниевых солей фосфорной
кислоты, которые обладают малой
растворимостью в воде и поэтому достаточно
полно выпадают в осадок.
9.
3) Бариевый методУмягчение воды основано на введении в нее
гидроксида бария или алюмината бария и
образовании практически нерастворимых
соединений кальция и магния, а также
сульфата бария.
10.
Технологические схемы и аппаратурноеоформление установок реагентного умягчения
Схема устройства
вихревого реактора:
7 — подача воды в
реактор; 2 —
патрубки для подачи
известкового молока
и раствора соды; 3 —
воздушник; 4 — отвод
умягченной воды
Установка умягчения воды с
вихревым реактором:
7 — бункер с контактной массой;
2,7 — подача исходной и отвод
умягченной воды; 3 — вихревой
реактор (спирактор); 4 — ввод
реагентов; 5 — скорый фильтр;
6 — резервуар умягченной воды; 8
— эжектор; 9 — сброс контактной
массы
Установка известковосодового умягчения воды с
осветлителем:
1,8 — подача исходной и
отвод умягченной воды; 2
— эжектор; 3 — бункер для
контактной массы; 4 —
вихревой реактор; 5 — ввод
реагентов; 6 — осветлитель
со взвешенным осадком; 7
— скорый фильтр
11.
Вывод• Жесткость определяет не только возможность использования
воды в питьевых целях, но и ее применение в бытовых или
промышленных нуждах.
• Чем выше параметр жесткости, тем сильнее
значение каждого вида вредного воздействия.
• При круговороте воды в природе жидкость превращается в
пар и поднимается в верхние слои атмосферы.
• После конденсации она выпадает в виде осадков и не
содержит примесей влияющих на жёсткость, но проходя через
слой земной коры, жидкость растворяет различные породы, в
которых содержатся калий и магний.
• В последнее время появилось множество смягчителей воды,
защищающих стиральные машины от накипи, а также различные
фильтры, смягчающие воду. Одновременно производители
стиральных порошков ввели компоненты предотвращающие
образование накипи. Calgon - снижает жесткость воды на 100%.








 Химия
Химия








