Похожие презентации:
Водород- «зеленое топливо»
1. Водород- «зеленое топливо»
2.
Паровой риформингОдним из распространенных в настоящее время в промышлен¬
ности способов получения водорода и его смесей с азотом и
окисью углерода является конверсия углеводородных газов.
В качестве первичного продукта конверсии углеводородных газов
получается смесь Н2 + СО (или Н2 + СО +N2), которая для
выработки из нее водорода (или соответственно азотоводородной
смеси) направляется на конверсию окиси углерода.
Конверсия углеводородных газов (и в частности метана) с целью
получения водорода и газов для синтеза проводится с помощью
окислителей — Н2О (пар), О2 и СО2— по следующим основным
обратимым реакциям:
СН4 + Н20 = СО + ЗН2 — Q,
СО + Н20 = С02+Н2 + Q.
СН4 + С02 = 2СО + 2Н2 — Q,
3.
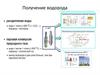
Диоксид углерода может быть отделен от природного газа сэффективностью 70-85% для получения водорода. Основная часть
водорода
обычно
получают
с
помощью
парового
риформинга метана или природного газа. Производства
водорода из природного газа является самым дешевым
источником водорода. Этот процесс состоит из нагрева газа до
температуры между 700-1100 ° С в присутствии водяного пара и
Ni-катализатора.
В
результате
эндотермической
реакции образует монооксид углерода СО и водород H2 . Окись
углерода подвергается реакции конверсии газа водой
над оксидом железа или других оксидов и для получения
дополнительных количеств H2.
Недостаток этого способа является то ,что его основными
побочными продуктами являются CO, CO 2 и других парниковых
газов.
Новая технология
предусматривает хранение CO2 в
глубоких
геологических
формациях
в
виде
минеральных карбонатов.
4.
Частичное окислениеПроизводство водорода из природного газа или других
углеводородов достигается за счет частичного окисления. :
С п Н m + п / 2 O 2 → n СО + m / 2 Н 2
Из угля
Пропускание паров воды над раскалённым углем при
температуре около 1000 °C: Старейший способ получения
водорода.
Электролиз водных растворов гидроксидов активных
металлов (преимущественно, гидроксида калия)
5.
Из биомассыВодород из биомассы получается термохимическим,
или биохимическим способом.
При термохимическом методе биомассу нагревают
без доступа кислорода до температуры 500°-800° (для
отходов древесины), что намного ниже температуры
процесса газификации угля. В результате процесса
выделяется H2, CO и CH4.
В биохимическом процессе водород вырабатывают
различные бактерии, например, Rodobacter speriodes.
Возможно применение различных энзимов для
ускорения
производства
водорода
из полисахаридов
содержащихся в биомассе.
Процесс проходит при температуре 30° Цельсия при
нормальном давлении.
6.
Химическая реакция воды с металламиВ 2007 году Университет Purdue (США) разработал метод
производства водорода из воды при помощи алюминиевого
сплава. Сплав алюминия с галлием формируется в пеллеты.
Пеллеты помещают в бак с водой. В результате химической
реакции производится водород. Галлий препятствует
образованию оксидной пленки на поверхности алюминия,
тормозящую процесс окисления алюминия. В результате
реакции создаётся водород и оксид алюминия.
С использованием водорослей
В 1999 году обнаружили, что если водорослям не хватает
кислорода и серы, то процессы фотосинтеза у них резко
ослабевают, и начинается бурная выработка водорода.
Водород может производить группа зелёных водорослей.
Водоросли могут производить водород из морской воды, или
канализационных стоков.






 Химия
Химия