Похожие презентации:
Опыты Беккереля. Опыты Резерфорда. Планетарная модель атома
1. Кислицын А.А. Физика атома, атомного ядра и элементарных частиц
02.(0). Опыты Беккереля.Опыты Резерфорда.
Планетарная модель атома.
2. Строение вещества
"Молекулярно-кинетическая теория: все теласостоят из атомов и молекул - маленьких
частиц, которые находятся в беспрерывном
движении, притягиваются на небольшом
расстоянии, но отталкиваются, если одно из
них плотнее прижать к другому" - в одной
этой фразе содержится огромное количество информации о мире, стоит лишь приложить к ней немного воображения и чуть соображения" (Р.Фейнман)
3. Краткая история
Молекула - мельчайшая частица сложного вещества, атом - мельчайшая частица простого вещества- химического элемента. В начале XIX века было
известно 50 атомов, сейчас (вместе с созданными
искусственно) - 118.
До середины XIX века никаких сведений о строении
атомов в физике не было (слово "атом" - буквально означает "неделимый"). Первые сведения о
сложной структуре атомов появились в конце XIX
века. В 1895 году - Рентген открыл излучение, названное его именем (нобелевская премия 1901г). В
1896 году А.Беккерель открыл радиоактивность
урана (нобелевская премия 1903г). В 1897 году
Дж.Дж.Томсон открыл электрон и предложил первую модель атома (нобелевская премия 1906г).
4. Краткая история
Окись урана золотистого цвета находили в рудникахдве тысячи лет назад. Ее использовали как краску
для узоров на глиняных вазах, а позже стали добавлять в расплав при варке цветного стекла. В
1804 году немецкий химик А.Гелен заметил, что
раствор хлорида урана на свету флуоресцирует:
меняет ярко-желтый цвет на зеленый. В 1841 году
французский химик Э.М.Пелиго получил чистый
уран: тяжелый серебристо-серый металл.
В 1896 году А.Беккерель обнаружил, что фотопластинка, завернутая в черную бумагу, защищающую
от любых видимых лучей, находясь рядом с солями урана, засвечивается каким-то невидимым излучением, которое не зависит от температуры и
вызывает ионизацию воздуха так же, как лучи
Рентгена.
5. Флуоресценция соединений урана
Урансодержащий минерал отенит(водный уранил-ванадат кальция).
Слева - при дневном свете,
Справа - флуоресцирует при облучении
ультрафиолетом.
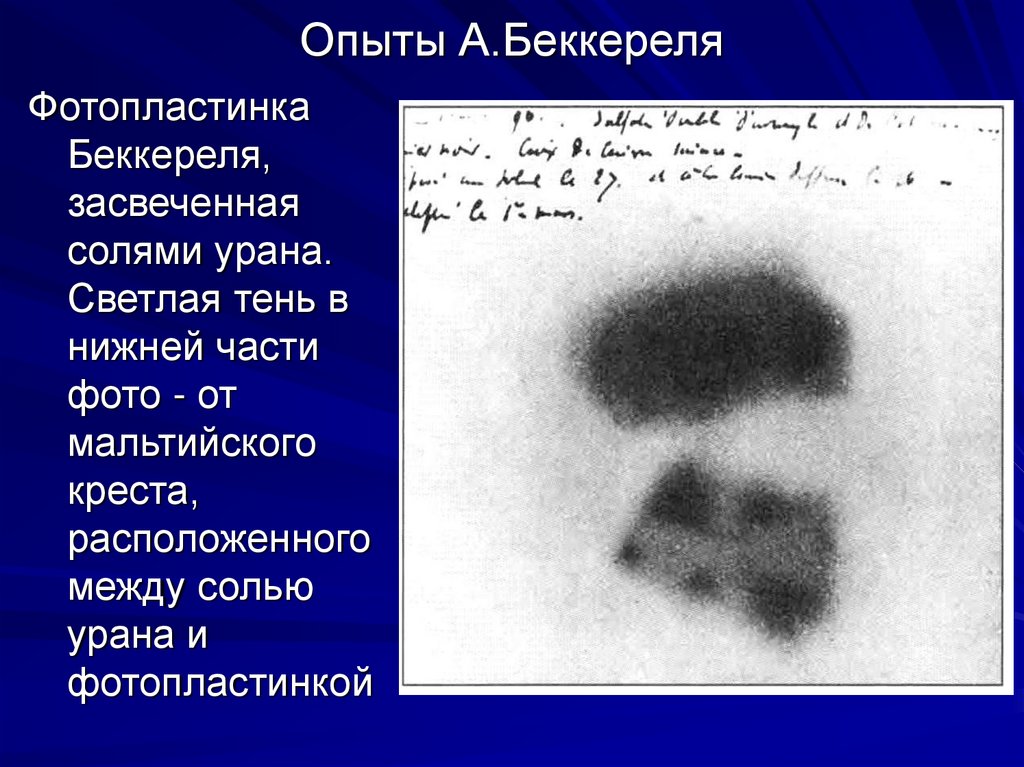
6. Опыты А.Беккереля
ФотопластинкаБеккереля,
засвеченная
солями урана.
Светлая тень в
нижней части
фото - от
мальтийского
креста,
расположенного
между солью
урана и
фотопластинкой
7.
8. Опыты Э.Резерфорда
Э.Резерфорд (Rutherford E.) в результатебольшого количества экспериментов (1906
- 1920 гг, нобелевская премия 1908г)
установил, что любой атом состоит из ядра
и окружающих его электронов.
Основные результаты были получены к 1911
году. Этот год (условно) можно считать годом рождения атомной и ядерной физики.
9. Опыты Э.Резерфорда
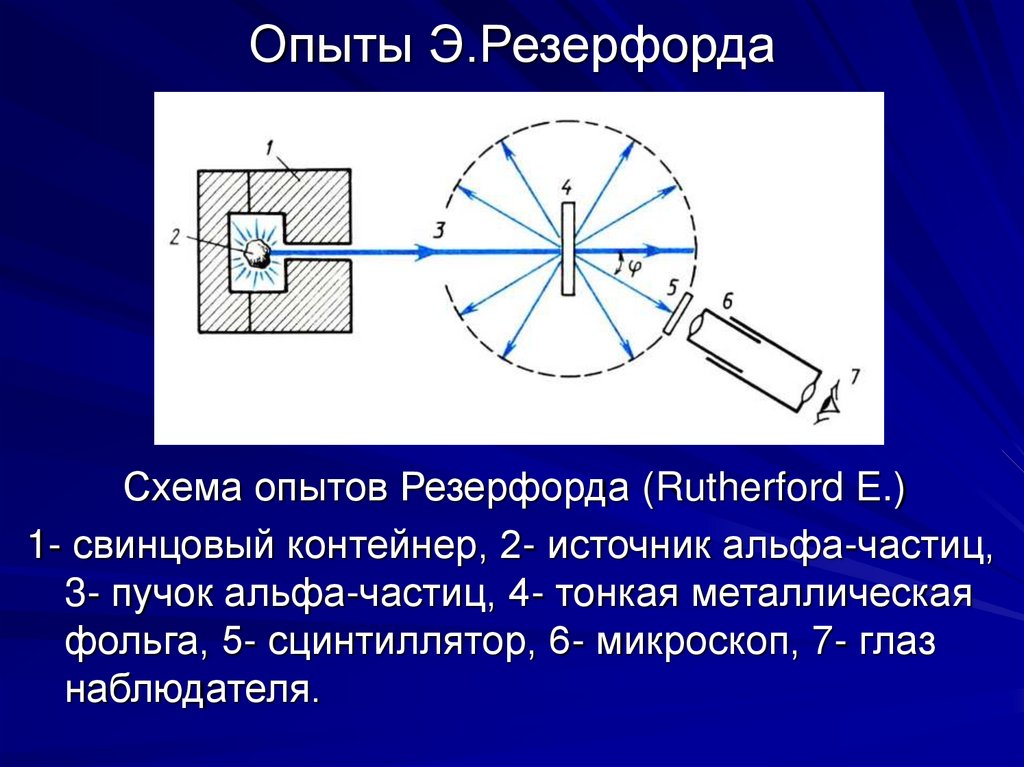
Схема опытов Резерфорда (Rutherford E.)1- свинцовый контейнер, 2- источник альфа-частиц,
3- пучок альфа-частиц, 4- тонкая металлическая
фольга, 5- сцинтиллятор, 6- микроскоп, 7- глаз
наблюдателя.
10. Вид установки Резерфорда
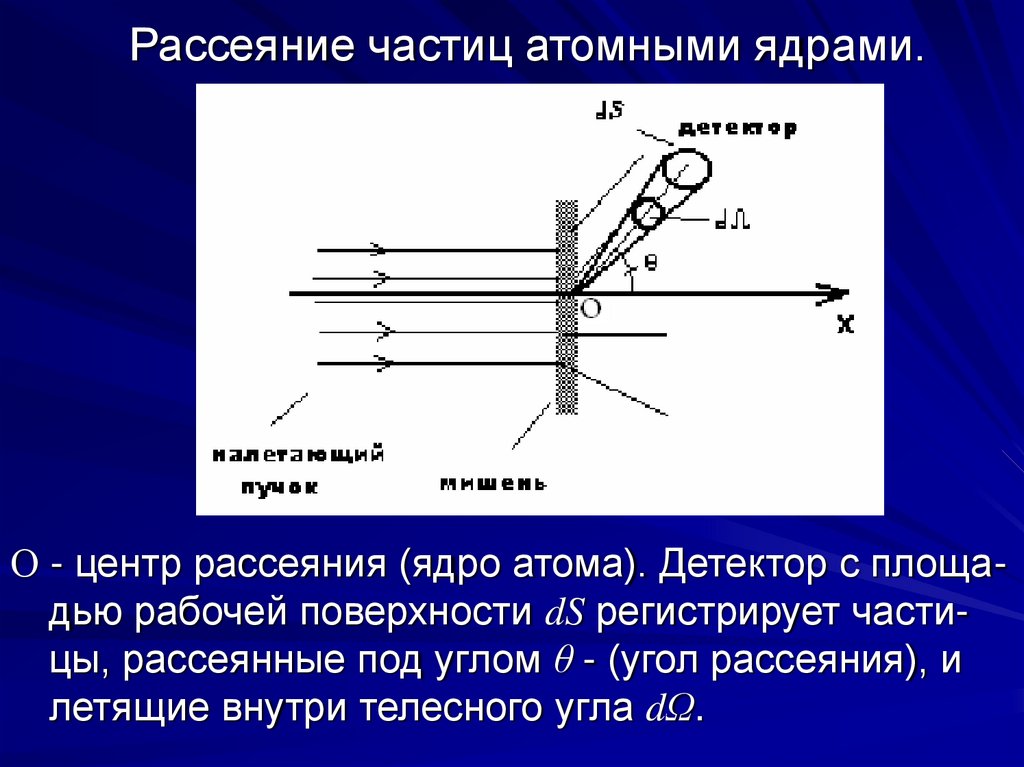
11. Рассеяние частиц атомными ядрами.
О - центр рассеяния (ядро атома). Детектор с площадью рабочей поверхности dS регистрирует частицы, рассеянные под углом θ - (угол рассеяния), илетящие внутри телесного угла dΩ.
12.
Количество частиц dN, летящих внутри телесного угла dΩ, и зарегистрированных детектором за единицу времени, равно:dN = dσ·n1·v1·n2·V ,
(2.1)
где n1 - плотность частиц в налетающем пучке, v1 - их
скорость, n2 - число ядер в единице объема мишени, V - рабочий объем мишени, равный произведению площади поперечного сечения пучка на толщину мишени, если частицы пролетают сквозь мишень (в этом случае мишень называется "тонкая").
Если частицы останавливаются внутри мишени, то
площадь поперечного сечения пучка надо умножить на глубину проникновения частиц, в этом случае мишень называется "толстая". Коэффициент
dσ называется "эффективным сечением".
13.
Из формулы (2.1) находим эффективное сечение:dN
d
n1v1n2V
(2.2)
Разделив обе части формулы (2.2) на dΩ, находим
характеристику, которая называется "дифференциальное эффективное сечение":
dN
d
d
d n1v1n2V
(2.3)
Проинтегрировав (2.2) или (2.3) по всему телесному
углу Ω, получаем величину, которая называется
"полное сечение":
d
N
(2.4)
d
d
d
n1v1n2V
14.
Иногда удобно обозначить через I поток расходящихся от мишени частиц, отнесенный к одномуатому мишени:
N
I
n2V
Тогда полное сечение можно записать в виде:
I
n1v1
Полное сечение можно наглядно интерпретировать
как площадку, попадая в пределы которой, налетающая частица производит интересующую нас реакцию. В атомной и ядерной физике за единицу
сечения принят 1 барн:
1 барн = 10-24 см2 = 10-28 м2.
15.
Параметры n1, v1, n2, V могут быть заданы экспериментатором, а эффективное сечение dσ, дифференциальное эффективное сечение dσ/dΩ и полноесечение σ определяются характером взаимодействия частиц с ядром, т.е. несут информацию о физических законах этого взаимодействия. Поэтому
именно определение этих величин является главной целью экспериментов по рассеянию частиц на
атомных ядрах или на других элементарных частицах.
В экспериментах задают параметры n1, v1, n2, V, измеряют dN, dN/dΩ, и ΔN, а далее по формулам (2.2),
(2.3), (2.4) вычисляют эффективное, дифференциальное и полное сечения изучаемого взаимодействия.
16. Вернемся к опытам Резерфорда, и изобразим траек-торию какой-либо из альфа-частиц, пролетающей мимо ядра атома мишени,
Вернемся к опытам Резерфорда, и изобразим траекторию какой-либо из альфа-частиц, пролетающеймимо ядра атома мишени, находящегося в точке О
(рассеяние Резерфорда)
17.
Для этого процесса (упругого рассеяния альфа-частиц на ядрах атомов) Э.Резерфорд получил формулу, носящую его имя (формула Резерфорда):2
1 q1q2 d
d
(2.5)
2
4 4 0 mv sin 4
2
Обозначения: m, v - масса и скорость налетающей
частицы, q1 и q2 - электрические заряды налетающей частицы и ядра соответственно. Для альфачастицы q1 = 2e, для ядра q2 = Ze, e - элементарный
электрический заряд, по абсолютной величине
равный заряду электрона; Z - число протонов в ядре атома мишени, ε0 - электрическая постоянная.
Вывод этой формулы - в следующей презентации.
18. Главный результат опытов Резерфорда.
Внутри атома имеется положительно заряженное ядро с зарядом +Ze, в котором сосредоточена почти вся масса атома; размер ядра ~ 10-14 м. Этотважнейший вывод был сделан на основании того, что измеренное в экспериментах эффективное сечение, т.е. угловое распределение рассеянных альфа-частиц, совпадает с результатами
вычислений по формуле Резерфорда (2.5).
Т.е. атом построен приблизительно так, как построена солнечная система: в центре, как Солнце, находится положительно заряженное ядро, вокруг
которого как планеты движутся отрицательно заряженные электроны (планетарная, или ядерная
модель).
19.
Отсюда следует, что модель атома Томсона (левыйрисунок) в которой положительный заряд, подобно
мякоти пудинга, распределен по всему объему
атома, а электроны, как изюминки, находятся внутри этой мякоти, неверна. Справа схематически
изображена ядерная модель.
20.
Другой важнейший результат опытов по рассеяниюальфа-частиц был получен позднее, в 1920 году
одним из сотрудников Резерфорда Чедвиком
(Chadwick J., нобелевская премия 1935г).
Этот результат заключается в том, что число Z (его
часто называют зарядовым числом), измеряющее заряд ядра в единицах e, т.е. равное числу
протонов в ядре, совпадает с порядковым номером элемента в таблице Менделеева.
Опыты Резерфорда и выводы, сделанные на их основе – отправной пункт
современной физики атома, основа
дальнейших ее успехов.
21.
Согласие формулы Резерфорда с опытом показывает справедливость планетарной модели атома. Однако согласно классическойэлектродинамике электрон, вращающийся
вокруг ядра, должен излучать электромагнитные волны, терять энергию и, следовательно, в конце концов упасть на ядро.
Оценки дают время жизни атома ~ 10-11 сек,
что, конечно, противоречит опыту. С другой
стороны, никакой иной интерпретации результаты опытов Резерфорда не допускают. Из этого противоречия может быть сделан только один вывод: создать теорию
атома в рамках классической физики невозможно.


















 Физика
Физика








