Похожие презентации:
Химия. Основные понятия и законы
1. Общая химия
ОБЩАЯ ХИМИЯВас приветствует доцент кафедры
фундаментальной и прикладной
химии Кожухова Татьяна Юрьевна
Мой компьютер пока конфликтует с программой
ZOOM и некоторые функции не работают. Поэтому, я
сегодня без видео и без голоса, но Вас я слышу. Очень
надеюсь, что на следующей неделе всё будет работать.
Сегодня работаем в режиме презентации. Все
микрофоны выключены. Если есть вопросы, включаете
микрофон и задаете вопрос, а я отвечаю в чате.
2. Конференция в программе ZOOM рассчитана на 40 минут, поэтому работаем с 19:00 до 19:40, перерыв 5 минут, опять подключаемся к
КОНФЕРЕНЦИЯВ ПРОГРАММЕ
ZOOM
40 МИНУТ, ПОЭТОМУ
19:00 ДО 19:40, ПЕРЕРЫВ
РАССЧИТАНА НА
РАБОТАЕМ С
5
МИНУТ, ОПЯТЬ ПОДКЛЮЧАЕМСЯ К
КОНФЕРЕНЦИИ И РАБОТАЕМ С
ЕСЛИ БУДЕТЕ БЫСТРО
ЗАПИСЫВАТЬ, ТО МОЖЕМ ЗАВЕРШИТЬ
РАНЬШЕ.
ДО
20:20.
19:45
3. Пожалуйста, материал конспектируйте. Особое внимание уделяем основным понятиям и законам. По этой теме далее будет практическое
ПОЖАЛУЙСТА, МАТЕРИАЛ КОНСПЕКТИРУЙТЕ.ОСОБОЕ ВНИМАНИЕ УДЕЛЯЕМ ОСНОВНЫМ
ПОНЯТИЯМ И ЗАКОНАМ. ПО ЭТОЙ ТЕМЕ ДАЛЕЕ
БУДЕТ ПРАКТИЧЕСКОЕ ЗАНЯТИЕ (РЕШЕНИЕ
ЗАДАЧ).
ЕСЛИ НЕ УСПЕВАЕТЕ (Я ПЕРЕКЛЮЧАЮ СЛАЙДЫ
БЫСТРЕЕ), ТО ОБЯЗАТЕЛЬНО ГОВОРИТЕ, БУДЕМ
ВОЗВРАЩАТЬСЯ.
ВСЕ ВОПРОСЫ СЕБЕ ПОМЕЧАЙТЕ, ПРИ ЛИЧНОЙ
ВСТРЕЧЕ (ВО ВТОРНИК) БУДЕМ РАЗБИРАТЬ.
4.
Тема лекцииРазвитие материалистических
представлений в химии.
Основные химические понятия и
законы.
4
5. ВВЕДЕНИЕ
Цель дисциплинысоздать основу для дальнейшего изучения химических
дисциплин, сформировать элементарные навыки работы
в химической лаборатории
СОДЕРЖАНИЕ дисциплины
основные понятия и законы химии;
теория строения атома и образования химических связей
в молекулах;
классы неорганических соединений;
общие закономерности протекания химических реакций,
в том числе элементы химической термодинамики и
химической кинетики;
основы теории растворов электролитов и неэлектролитов,
закономерности окислительно-восстановительных и
электрохимических процессов
5
типовые расчетные задачи
элементарные лабораторные навыки
6. Происхождение термина “химия”
ПРОИСХОЖДЕНИЕ ТЕРМИНА“ХИМИЯ”
-
Есть несколько версий:
от египетского слова "Хем" - арабского
названия этой страны - "египетская наука".
-
из греческого χυμος ("хюмос"), которое
можно перевести как "сок растения".
-
от другого греческого слова - χυμα
("хюма"), означающего "литье", "сплав это искусство литья выплавки металлов, то
есть металлургии.
6
7. Периодизация истории химии
ПЕРИОДИЗАЦИЯ ИСТОРИИХИМИИ
Выделяют 2 основных периода:
а) эмпирический (с древности до
XVIIIв);
процесс познания через эксперимент.
б) теоретический. (XVIII – по н.в.)
В XVIII столетии все большее
внимание ученые стали уделять
осмыслению полученных опытных
данных, попыткам объяснить их при
помощи единой умозрительной
концепции.
7
8. Основные периоды в истории химии
ОСНОВНЫЕ ПЕРИОДЫ В ИСТОРИИХИМИИ
1. Период алхимии - с древности до XVI в. нашей
эры. (создание основ рациональной фармации,
обучение правилам приготовления целебных
препаратов, а также составление списка лекарств).
2. Период зарождения научной химии (XVI - XVIII
век).
3. Период открытия основных законов химии конец XVIII - первая половина XIX века
4. Современный период с 60-х годов XIX века до
наших дней.
Разработаны периодическая классификация
элементов, теория химического строения и
стереохимия, теория электролитической
диссоциации Аррениуса и т.д.
8
9.
Античная атомистика V-IV в до н.э.Основателями
первой
древнегреческой
атомистической теории считают Левкиппа и
Демокрита. В системе Демокрита атом ( ζ)
являлся мельчайшей однородной и неделимой
частицей мироздания.
9
Демокрит.
Левкипп
10.
Благодаря исследованиям великого английского ученогоРоберта Бойля в XVII вв. химия сформировалась как
самостоятельная наука.
Он положили начало рождению
новой
химической
науки,
отдельной от медицины.
Систематизируя многочисленные
цветные реакции и реакции
осаждения,
Бойль
положил
начало аналитической химии.
Он же стал автором одного из
первых законов рождающейся
физико-химической науки. 10
Роберт Бойль
11.
Период открытия основных законов химии(с 90-х г. XVIII в. до середины XIX в.)
К концу XVIII в. в химии был накоплен большой объем
экспериментальных
данных,
которые
необходимо
было
систематизировать в рамках единой теории. Создателем такой теории
стал французский химик Антуан-Лоран Лавуазье.
Он открыл закон сохранения веществ.
Лавуазье был автором первой
классификации химических веществ
11
Лабораторное оборудование, которое использовал А.Л. Лавуазье
в восьмидесятых годах XVIII столетия.
12. Период научной химии XIX—XX вв
ПЕРИОД НАУЧНОЙ ХИМИИ XIX—XX ВВ
За открытым Лавуазье законом сохранения массы
последовал целый ряд новых количественных
закономерностей — стехиометрические законы:
Закон эквивалентов (И. В. Рихтер, 1791—1798)
Закон постоянства состава (Ж. Л. Пруст, 1799—
1806)
Закон кратных отношений (Дж. Дальтон, 1803)
Закон объёмных отношений, или закон соединения
газов (Ж. Л. Гей-Люссак, 1808)
Закон Авогадро (А. Авогадро, 1811)
Закон удельных теплоёмкостей (П. Л. Дюлонг и
А. Т. Пти, 1819)
12
Законы электролиза (М. Фарадей, 1830-е гг.)
Закон постоянства количества теплоты (Г. Гесс,
13.
М. В. ЛОМОНОСОВ - ОСНОВОПОЛОЖНИКНАУЧНОЙ ХИМИИ В РОССИИ
М.В. Ломоносов - создатель школы российских
химиков.
Ему принадлежит идея разделения химии на
теоретическую (“физическая химия”) и
практическую части (“техническая химия”).
Самыми
выдающимися
заслугами
М.В.
Ломоносова в области химии являются создание
основ
атомно-молекулярного
учения
и
открытие закона сохранения массы вещества.
Также им был разработан, создан и внедрен в методику лабораторных
исследований целый ряд приборов: вискозиметр, прибор для
13
фильтрования под вакуумом, прибор для определения твердости,
газовый барометр, пирометр и другие.
14.
Й. Я. БЕРЦЕЛИУС вычислилотносительные атомные
массы всех известных к
тому времени элементов
(45).
Берцелиус ввел в
употребление буквенные
символы для обозначения
элементов (1818 - 1819 гг.).
Йенс Якоб Берцелиус.14
15.
МОЛЕКУЛЯРНАЯ ТЕОРИЯ АВОГАДРОВ 1814 г. итальянский физик и химик А. Авогадро
сформулировал закон, который носит его имя:
закон Авогадро
Центральным местом в теории
А. Авогадро было разъяснение
различий между понятиями атом
и молекула.
А. Авогадро впервые показал,
что газообразные простые вещества
состоят из двухатомных молекул.15
16.
МЕЖДУНАРОДНЫЙ СЪЕЗД ХИМИКОВ В КАРЛСРУЭ.РЕФОРМА АТОМНО-МОЛЕКУЛЯРНОЙ ТЕОРИИ
В середине XIX в. у различных школ и групп
ученых не было единых критериев определения
связанных с химической номенклатурой,
обозначениями и атомной массой.
В 1860 г первая международная конференция,
посвященная химии (конгресс в Карлсруэ).
Среди участников российской делегации были Н.Н.
Зинин и Д.И. Менделеев.
Результатом съезда химиков в Карлсруэ стало
утверждение атомно-молекулярного учения, были
определены понятия атомного веса, а также 16
молекулы и атома.
17. Основные понятия и законы химии
ОСНОВНЫЕ ПОНЯТИЯ ИЗАКОНЫ ХИМИИ
17
18.
Химия – это наука о составе, строении,свойствах и превращениях веществ.
Вещество – один из видов материи,
который характеризуется массой покоя.
Вещество состоит из частиц, например,
атомов, молекул, ионов.
18
19. Задачи химии
ЗАДАЧИ ХИМИИИзучение
веществ, их физических и
химических свойств
Изучение превращений веществ и
процессов, сопровождающих эти
превращения
Превращения веществ,
сопровождающиеся изменением
состава, называются химическими
реакциями.
19
20. Основные понятия химии
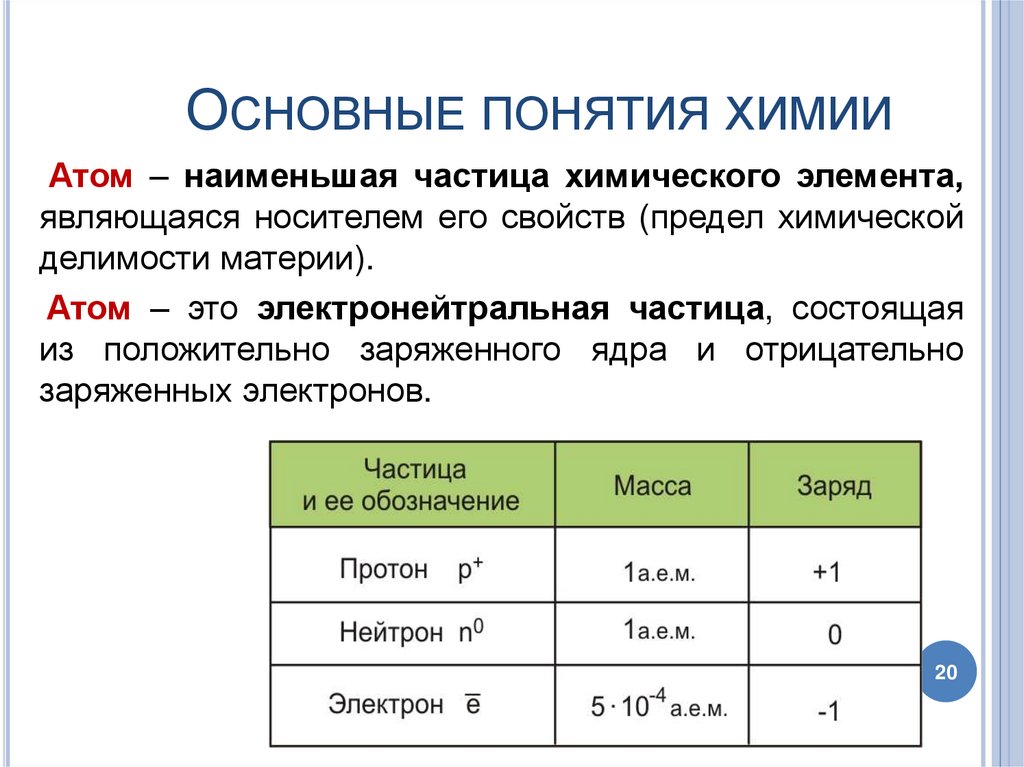
ОСНОВНЫЕ ПОНЯТИЯ ХИМИИАтом – наименьшая частица химического элемента,
являющаяся носителем его свойств (предел химической
делимости материи).
Атом – это электронейтральная частица, состоящая
из положительно заряженного ядра и отрицательно
заряженных электронов.
20
21. Основные понятия химии
ОСНОВНЫЕ ПОНЯТИЯ ХИМИИХимический элемент – это совокупность
атомов с одинаковым зарядом ядра.
Объектом изучения в химии являются
химические элементы и их соединения
21
22. Основные понятия химии
ОСНОВНЫЕ ПОНЯТИЯ ХИМИИЭлементы принято обозначать первой
или первой и одной из последующих
букв латинских названий элементов.
22
23. Химический знак (символ)
ХИМИЧЕСКИЙ ЗНАК (СИМВОЛ)– обозначает название
элемента, один его атом, один
моль атомов этого элемента.
По символу химического
элемента можно определить его
атомный номер и
относительную атомную массу.
23
24. Основные понятия химии
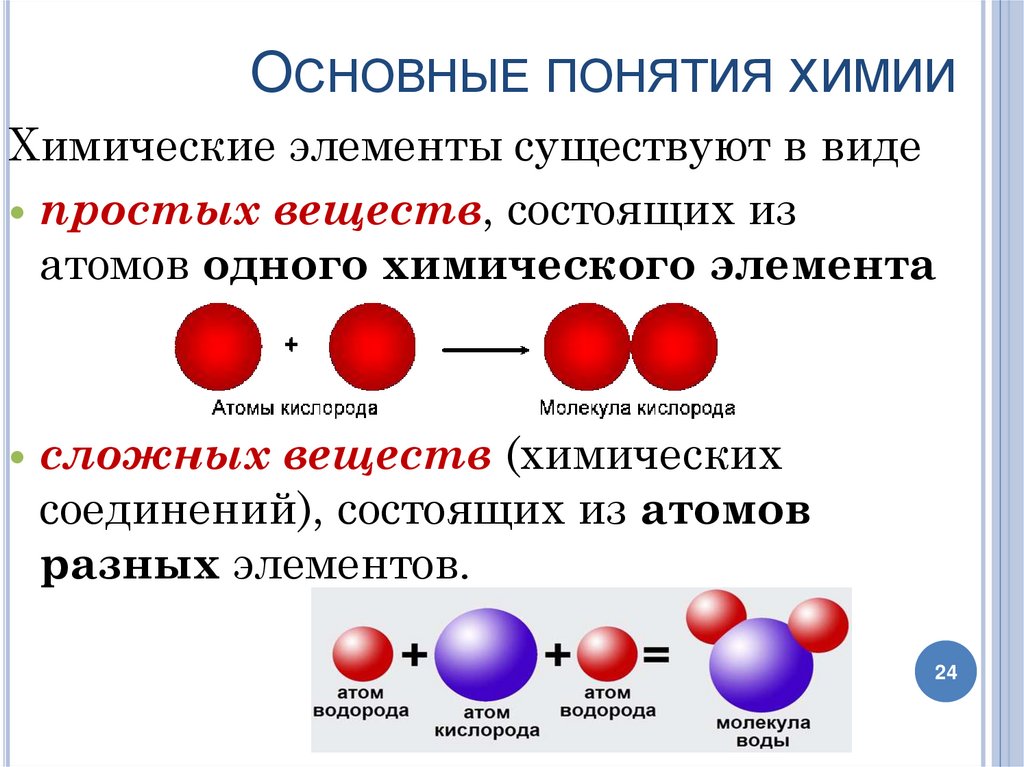
ОСНОВНЫЕ ПОНЯТИЯ ХИМИИХимические элементы существуют в виде
простых веществ, состоящих из
атомов одного химического элемента
сложных веществ (химических
соединений), состоящих из атомов
разных элементов.
24
25. Примеры простых и сложных веществ:
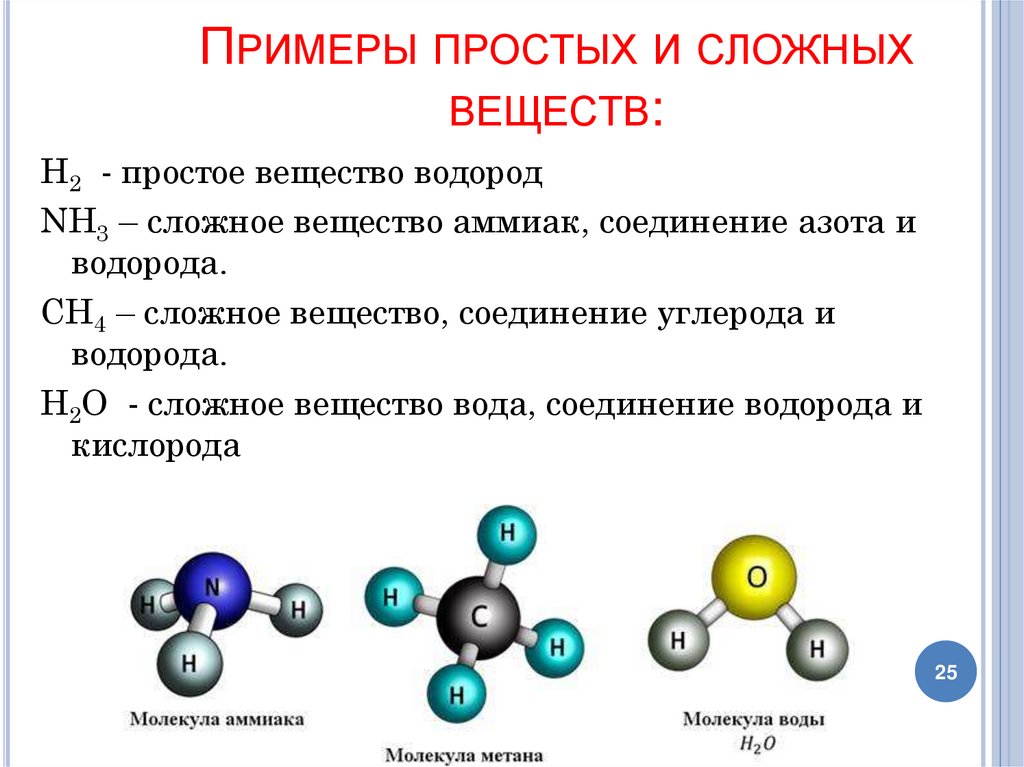
ПРИМЕРЫ ПРОСТЫХ И СЛОЖНЫХВЕЩЕСТВ:
Н2 - простое вещество водород
NH3 – сложное вещество аммиак, соединение азота и
водорода.
СH4 – сложное вещество, соединение углерода и
водорода.
Н2О - сложное вещество вода, соединение водорода и
кислорода
25
26. Основные понятия химии
ОСНОВНЫЕ ПОНЯТИЯ ХИМИИАллотропия – способность
химического элемента образовывать
несколько простых веществ,
называемых аллотропными
модификациями
27. Основные понятия химии
ОСНОВНЫЕ ПОНЯТИЯ ХИМИИАллотропные модификации
углерода (С): алмаз, графит,
фуллерен, графен, нанотрубки
27
28. Аллотропия
АЛЛОТРОПИЯАллотропные
модификации фосфора Р:
белый (желтый), красный и черный
28
29. Основные понятия химии
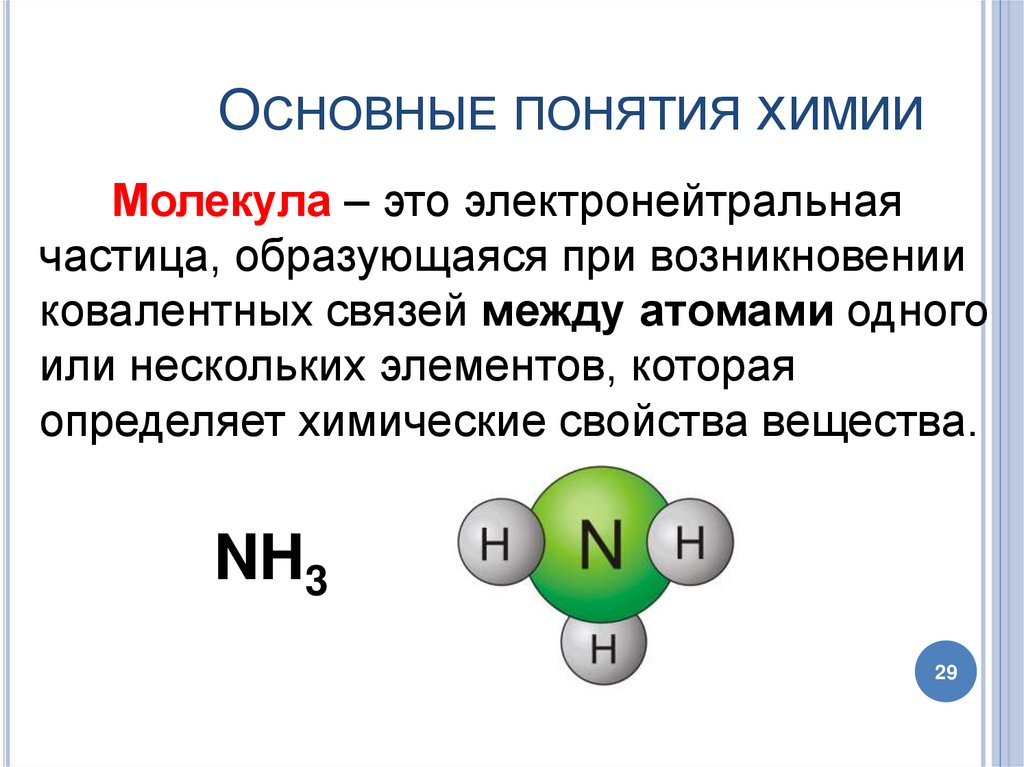
ОСНОВНЫЕ ПОНЯТИЯ ХИМИИМолекула – это электронейтральная
частица, образующаяся при возникновении
ковалентных связей между атомами одного
или нескольких элементов, которая
определяет химические свойства вещества.
NH3
29
30. Химическая формула -
ХИМИЧЕСКАЯ ФОРМУЛА это условная запись качественного и количественногосостава вещества при помощи химических знаков и
индексов.
Индекс - это цифра в химической формуле, которая
ставится внизу после химического знака и обозначает
число атомов данного вида.
30
31. Основные понятия химии
ОСНОВНЫЕ ПОНЯТИЯ ХИМИИ1.
2.
3.
Широко
используются
несколько
видов
химических формул:
Простейшая (эмпирическая) формула показывает
качественный состав и соотношения, в которых
находятся частицы, образующие данное вещество.
Молекулярная (истинная) формула показывает
качественный состав и число составляющих вещество
частиц, но не показывает порядок связей частиц в
веществе, т. е. его структуру.
Графическая формула отражает порядок соединения
атомов, т. е. связи между ними.
31
32. Атомная масса элемента
АТОМНАЯ МАССА ЭЛЕМЕНТАМасса атомов, молекул и ионов очень
мала, 10-24 – 10-23 г
Например,
масса атома водорода
m(H) = 1,67·10-24 г или 1,67·10-27
кг,
масса атома урана (самого тяжелого
элемента)
32
-25
33.
Атомная единица массы (а.е.м.) внесистемная единица массы.Атомная
единица массы –
это единица массы, равная
1/12 массы атома изотопа
углерода 12С
m(С) = 1,99·10-26 кг
1/12 m(C) = 1/12 x 1,99·10-26 кг = 1,66·10-27 кг =
1,66·10-24 г
33
1 а.е.м. = 1,66·10-27 кг = 1,66·10-24 г
1 а.е.м. ≈ массе протона или
34.
Относительнаяатомная масса
элемента Ar
Относительная атомная масса элемента
показывает во сколько раз масса его
атома больше 1/12 массы атома
углерода.
Например:
Аr(S) = 32, т.е. атом серы в 32 раза тяжелее
1/12 массы атома углерода.
34
35.
Атомные массы элементов приведены впериодической системе элементов.
35
36. Масса молекулы
МАССА МОЛЕКУЛЫОтносительная
молекулярная масса
Мr (молекулярная масса)
Мr равна сумме относительных атомных
масс всех атомов, образующих молекулу
вещества.
Например:
Мr(О2) = 2Ar(О) = 2•16 = 32;
Mr(NO2) = Ar(N)+2Ar(O) = 14+2•16 = 46;
Мr (Н2О) = 2·1,01 + 16 = 18,01
36
37. Количество вещества
КОЛИЧЕСТВО ВЕЩЕСТВАВ Международной системе СИ за единицу количества
вещества принят моль.
МОЛЬ - это количество вещества (n), которое
содержит 6,02.1023 структурных единиц (атомов,
молекул, ионов) данного вещества (6,02·1023
частиц, число Авогадро NA )
1 моль атомов Н, 1 моль молекул Н2
37
38. Основные понятия химии
ОСНОВНЫЕ ПОНЯТИЯ ХИМИИПостоянная Авогадро ( N A ) – число атомов или
молекул (или других структурных единиц), содержащихся
в одном моле вещества
N A 6,022 *10 моль
23
1
При решении химических задач нужно знать, сколько
структурных частиц (N) вещества содержится в
определённом количестве вещества.
N = NA · n
38
39. Основные понятия химии
ОСНОВНЫЕ ПОНЯТИЯ ХИМИИМоль – единица количества вещества
39
40. Молярная масса (М)
МОЛЯРНАЯ МАССА (М)– масса 1 моля вещества в граммах
[М] = [г/моль]
Молярная масса численно равна относительной
молекулярной массе
М = Мr
Мr (Н2О) = 18,0152 а.е.м.
М(Н2О) = 18,0152 г/моль
Молярная масса равна произведению массы m0 одной
молекулы данного вещества на постоянную Авогадро
М = NA · m0
mв-ва = n · M
40
41. Основные законы химии
ОСНОВНЫЕ ЗАКОНЫ ХИМИИЗакон сохранения массы.
Масса веществ, вступивших в
реакцию, равна массе веществ,
образовавшихся в результате
реакции.
41
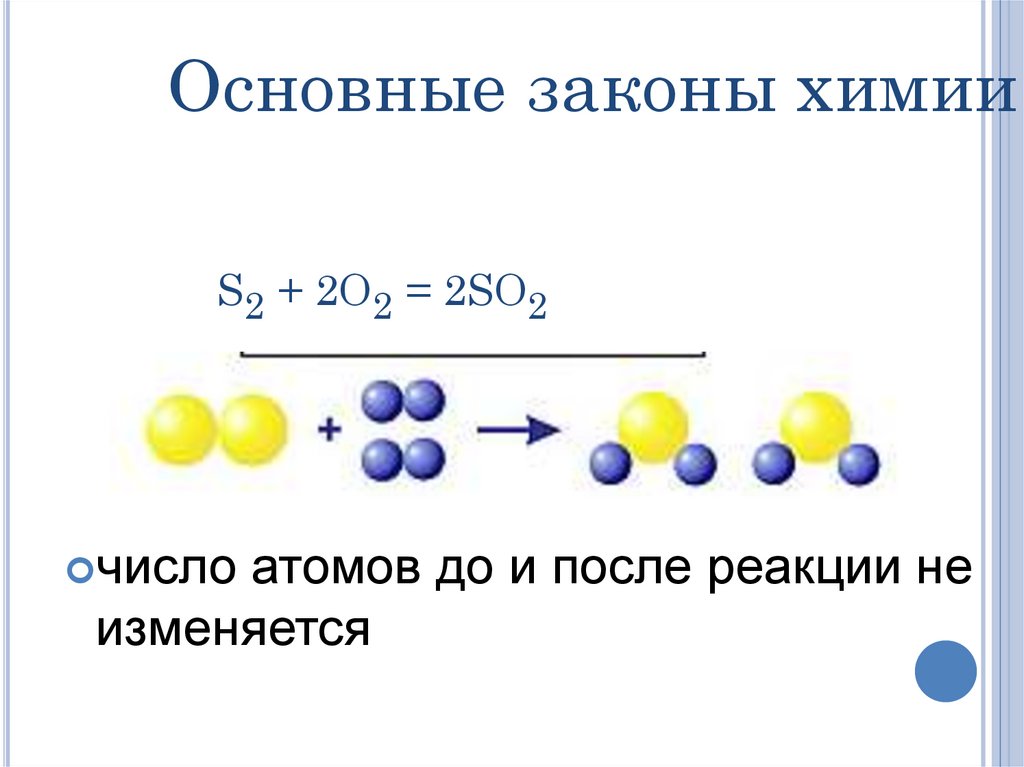
42. S2 + 2O2 = 2SO2
Основные законы химииS2 + 2O2 = 2SO2
число
атомов до и после реакции не
изменяется
42
43. Основные законы химии
ОСНОВНЫЕ ЗАКОНЫ ХИМИИЗакон
объемных отношений
Объемы газов, вступающих в
химическую реакцию, и объемы
газов, образующихся в результате
реакции, относятся между собой
как небольшие целые числа.
43
44. Основные законы химии
ОСНОВНЫЕ ЗАКОНЫ ХИМИИЗакон объемных отношений
Следствие.
Стехиометрические коэффициенты
в уравнениях химических реакций для
газообразных веществ показывают, в
каких объемных отношениях реагируют
или получаются газообразные вещества.
2CO + O2 = 2CO2
2 объема CO реагируют с 1 объемом O2 и получается 2
44
объема CO2
45. Основные законы химии
ОСНОВНЫЕ ЗАКОНЫ ХИМИИII.
Закон постоянства состава вещества.
Сформулирован Ж.-Л. Прустом в 1799 г..
Всякое чистое вещество независимо от способа
его получения всегда имеет постоянный
качественный и количественный состав.
Однако уже в начале XIX в. К. Бертолле показал,
что элементы могут соединятся друг с другом в
разных соотношениях в зависимости от массы
реагирующих веществ.
45
46. Основные законы химии
ОСНОВНЫЕ ЗАКОНЫ ХИМИИСовременная
формулировка
постоянства состава вещества таков:
закона
Состав соединений молекулярной структуры
является постоянным независимо от способа их
получения.
Состав соединений немолекулярной структуры
(с
атомной,
ионной
или
металлической
кристаллической
решеткой)
не
является
постоянным и зависит от способа их получения.
46
47. Основные законы химии
ОСНОВНЫЕ ЗАКОНЫ ХИМИИСоединения постоянного состава дальтониды (в память английского химика и физика
Дальтона).
Состав выражается простыми формулами с целочисленными
стехиометрическими индексами, например:
Н2О, НCl, ССl4, СO2
Соединения переменного состава бертоллиды (в память французского химика Бертолле).
Состав бертоллидов изменяется и не отвечает стехиометрическим
отношениям, например
FeSx, где
1,02 < x < 1,10
47
48. Закон постоянства состава вещества
ЗАКОН ПОСТОЯНСТВА СОСТАВАВЕЩЕСТВА
Так,
СО2
можно получить по любой из
следующих реакций:
С + О2 = СО2
2СО + О2 = 2СО2
СаСО3 = СО2 + СаО
В химически чистом СО2 всегда содержится
27,29% С и 72,71% О.
48
49. Основные законы химии
ОСНОВНЫЕ ЗАКОНЫ ХИМИИЗакон
Авогадро.
В равных объемах различных газов
при одинаковых условиях
(температура, давление и т.д.)
содержится одинаковое число
молекул
49
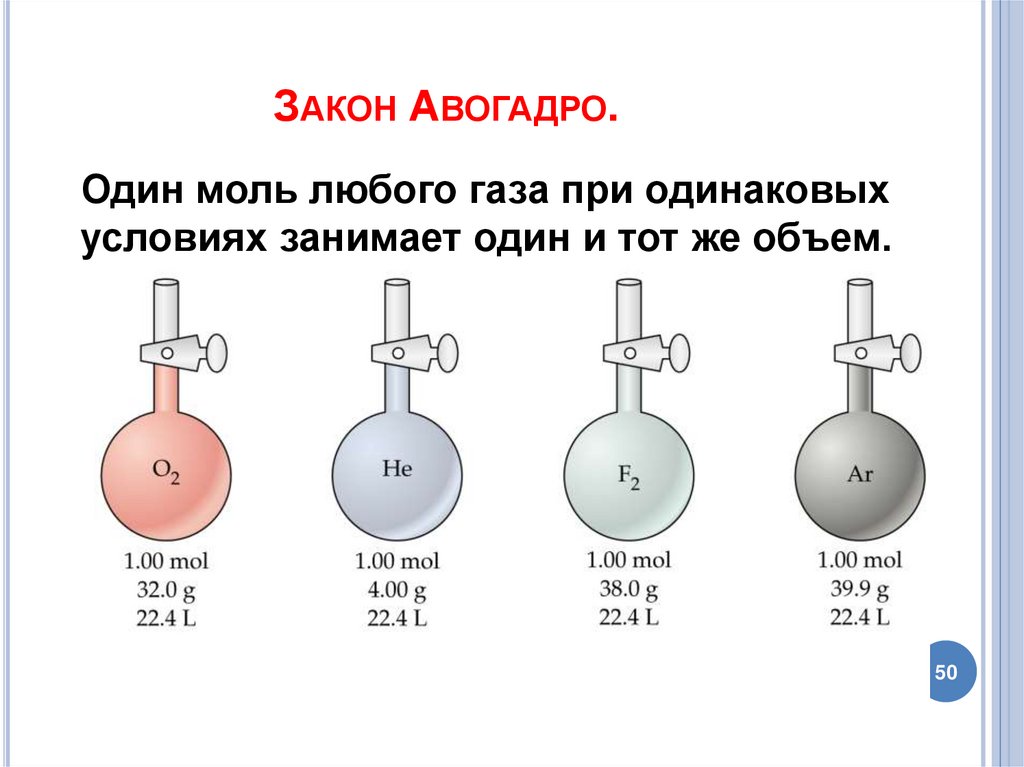
50. Закон Авогадро.
ЗАКОН АВОГАДРО.Один моль любого газа при одинаковых
условиях занимает один и тот же объем.
50
51. Следствия из закона Авогадро :
СЛЕДСТВИЯ ИЗ ЗАКОНА АВОГАДРО :1. Молярный
объем газа Vm –
объем 1 моля газа при нормальных
условиях (н.у.)
Vm = 22,4 л/моль (дм3/моль)
н.у.: Т = 0 °С ; р = 760 мм.рт.ст
Vгаза= n · Vm
51
52. Основные законы химии
ОСНОВНЫЕ ЗАКОНЫ ХИМИИ2.
Массы двух разных газов, занимающих
одинаковый объем при одинаковых
условиях, относятся между собой как их
молярные массы.
D – относительная плотность одного
газа по другому.
m1 M 1
D
m2 M 2
52
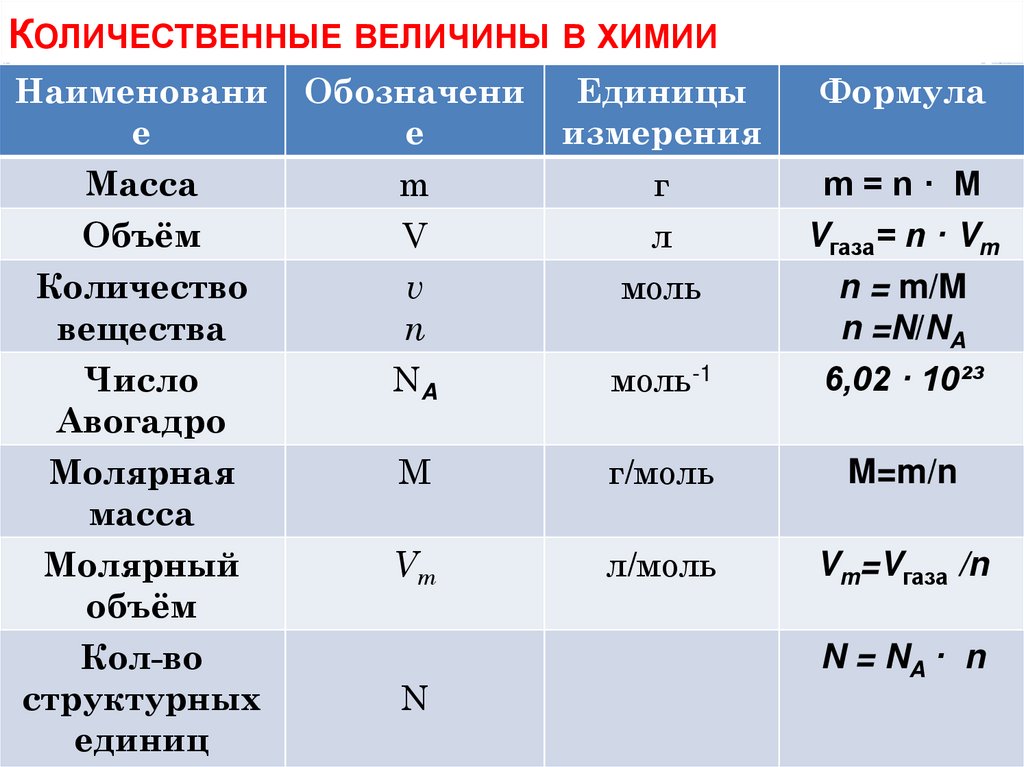
53. Количественные величины в химии
КОЛИЧЕСТВЕННЫЕ ВЕЛИЧИНЫ В ХИМИИНаименовани
е
Обозначени
е
Единицы
измерения
Формула
Масса
Объём
Количество
вещества
Число
Авогадро
Молярная
масса
Молярный
объём
m
V
v
n
г
л
моль
NA
моль-1
m=n· M
Vгаза= n · Vm
n = m/M
n =N/NA
6,02 · 10²³
M
г/моль
M=m/n
Vm
л/моль
Vm=Vгаза /n
Кол-во
структурных
единиц
N
N = NA ·53 n














































 Химия
Химия








