Похожие презентации:
Углероды. Строение и свойства атомов
1. Отгадайте загадку
Удивить готов он нас —Он и уголь, и алмаз,
Он в карандашах сидит,
Потому что он — графит.
Грамотный народ поймет
То, что это...
2. Углерод
1)2)
3)
4)
5)
6)
Строение и свойства атома;
Аллотропные модификации;
Нахождение в природе;
Применение;
Химические свойства
Получение
3. Строение и свойства атомов:
План:1. Охарактеризуйте положение углерода в
ПСХЭ Д.И. Менделеева(порядковый
номер, период, группа)
2. Составьте схему строения атома
3. Металл\неметалл
делите степени окисления
ов углерода в соединениях:
4. Аллотропные модификации
5. Аллотропные модификации
Алмаз
Графит
Карбин
Лонсдейлит
Наноалмаз
Фуллерены
Фуллерит
Углеродное волокно
Углеродные нановолокна
Углеродные нанотрубки
6. Алмаз от греч. «несокрушимый»
Данные минералы отличаютсяособенной твердостью и
повышенной износостойкостью,
поражают своим необычным
блеском, наиболее
высокой теплопроводностью среди
всех твёрдых тел
7. Графит от греч. записывать писать
Структура слоистая. Хорошопроводит электрический ток. В отличие
от алмаза обладает низкой твёрдостью (1
по шкале Мооса). Относительно мягкий.
Благодаря жирности и пластичности имеет
широкое применение в промышленном
производстве
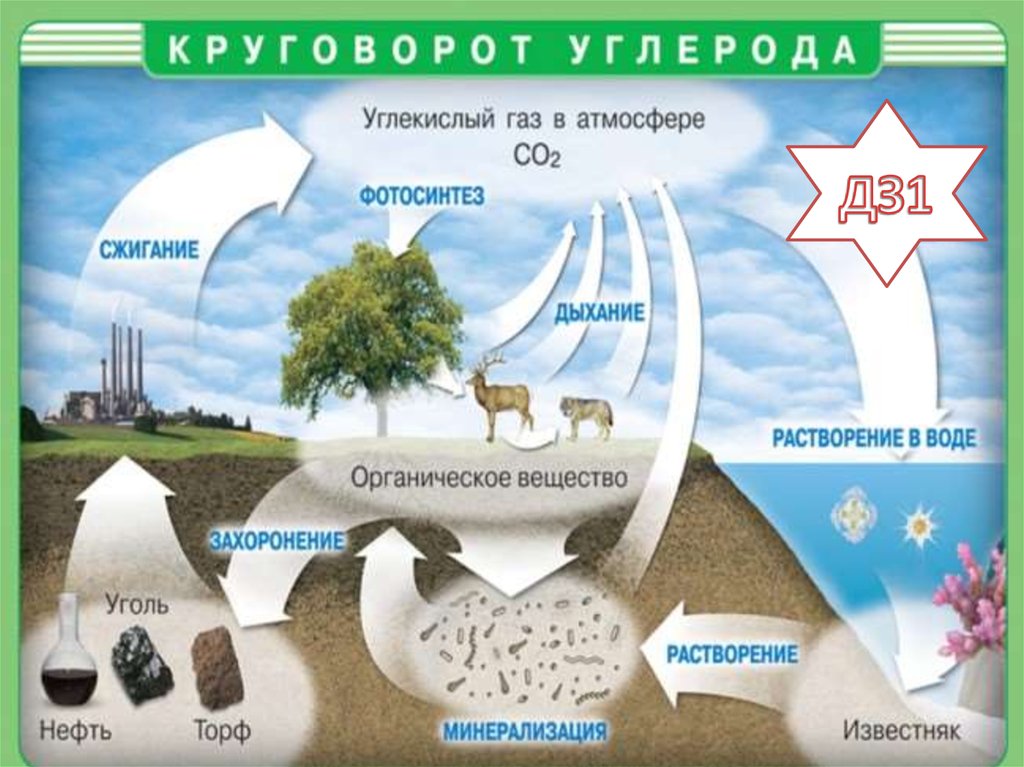
8. Углерод: нахождение в природе
9.
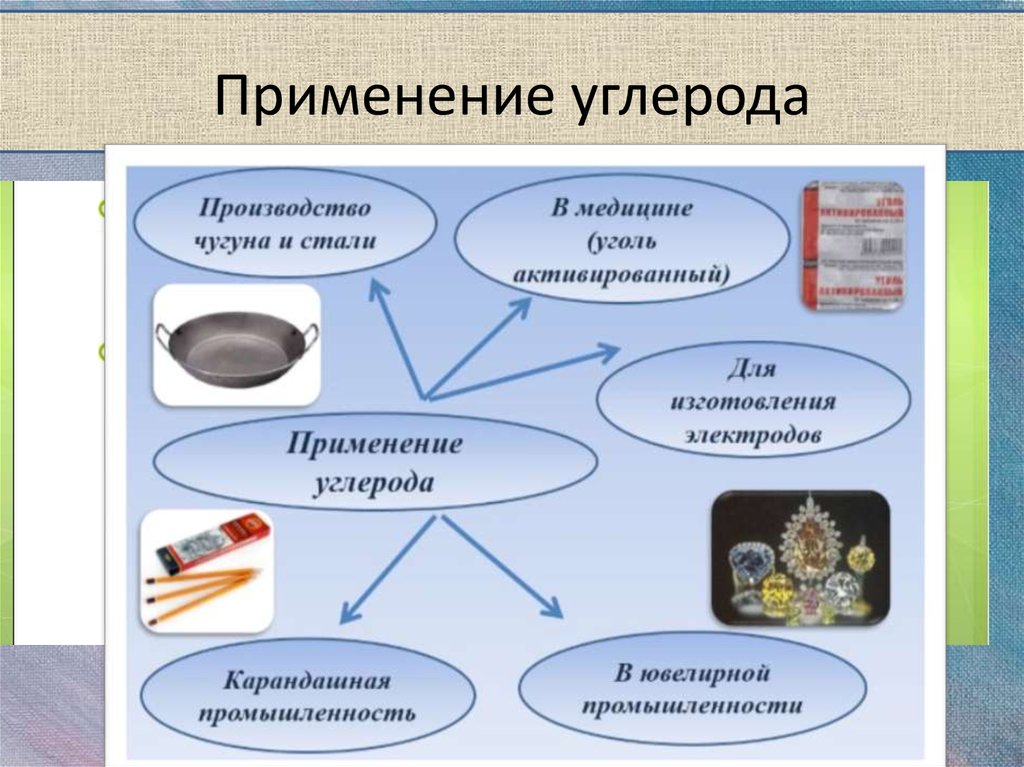
10. Применение углерода
11. Химические свойства углерода
Восстановительные свойства СОкислительные свойства С
Химические свойства углерода
Углерод будет проявлять восстановительные
Углерод может проявлять
свойства по отношению к тем элементам, которые окислительные свойства с
стоят правее него в периодической системе.
элементами левее и ниже его
1. С •+ неметалл:
С + S = CS2
в периодической системе:
Малоактивен!
C + O2 =—
CO2оксид
— оксид углерода
углерода (IV) —(IV) — углекислый газ.
CO2
кислотный
оксид: CO2
+ H2O = H2CO3 —реакции
3C + 4Al
= Al4C3 —
карбид
• Вступает
в химические
только
при
угольная кислота
алюминия
2C + O2 = 2CO — оксид углерода (II)несолеобразующий оксид
С + Si =SiC -карбид кремния
При
этом
химическая
активность
углерода
C + H2O (t) =—
CO +
H2 водяной газ
H2CO3
угольная
кислота.
Кислотный оксид.
нагревании.
убывает
в—
ряду
сажа—древесный
уголь—
Очень
слабая
тут
же
распадается
на
CO2 и H2O
2. С + оксид:
графит—алмаз.
С + Na2O
= 2Na + CO
C + CO2 = 2CO
3. С + кислота-окислитель:
С + 2H2SO4 =CO2 + 2SO2 + 2H2O
C + 4HNO3 = CO2 + 4NO2 + 2H2O
12. Качественные реакции на CO3(2-):
Качественные реакции на CO3(2-):CO3(-2) + 2H(+) = H2CO3 = CO2↑ + H2O — выделение газа
CO3(-2) + Ca(+2) = CaCO3↓ — белый осадок
13. Ответьте на вопросы
3) При сгорании любых1) Оксид
2)
Углерод
углерода
проявляет
(II):свойства
органических веществ образуется:
Только
Основный
окислителя;
C
H2CO3
Только
Кислотный
восстановителя;
CO2
CO
ИАмфотерный
окислителя и восстановителя










 Химия
Химия








