Похожие презентации:
Электроотрицательность. Степень окисления. Валентность химических элементов
1.
2.
3. Электроотрицательность Степень окисления Валентность химических элементов
4.
5.
6.
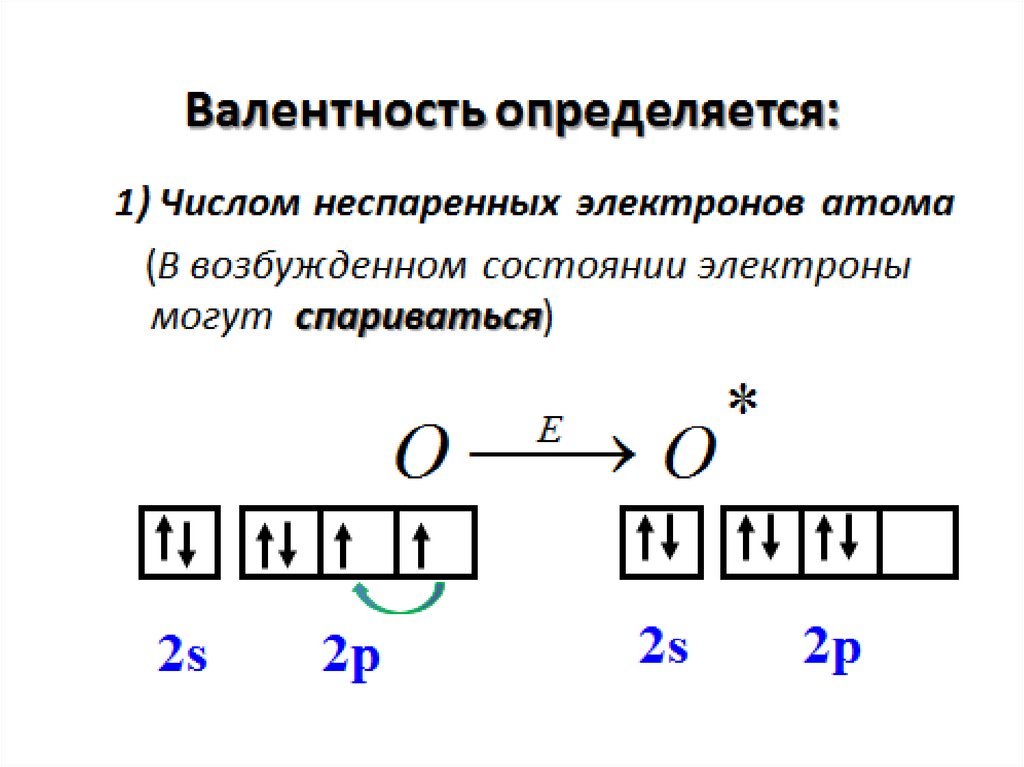
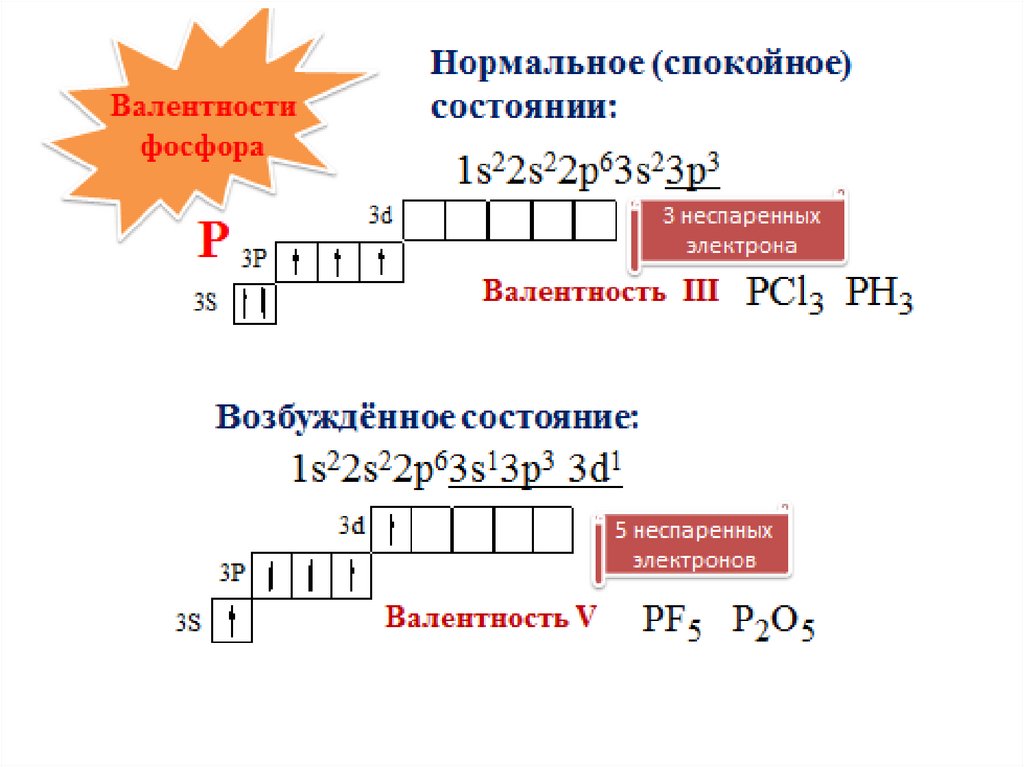
7. Валентность -
Валентность это число химических связей, которое данныйатом образует с другими атомами.
Электроны, принимающие участие в образовании
химических связей называют валентными
Валентные электроны располагаются на внешнем
уровне (для главных подгрупп)
на внешнем s-подуровне + предвнешнем dподуровне (для побочных подгрупп)
8.
Атом водорода был выбран в качествестандарта, обладающего валентностью,
равной 1.
Валентность обозначается римскими
цифрами.
I I
I II
III I
IV I
НCl H2O
NH3
CH4
9. Переменная и постоянная валентность
Есть элементы, которые имеютпостоянную валентность:
H, Li, Na, К, Rb, Cs, F, Ag
I
О, Be, Mg, Ca, Sr, Ba, Zn, Cd II
B, Al
III
10. Элементы с переменной валентностью
Cu, HgI,II
Fe, Co, Ni II, III
Sn, Pb, C
II, IV
P, As
III, V
S
II, IV, VI
Cr
II, III, VI
Mn
II, IV, VI, VII
Cl, Br, I
I, III, V, VII
11. Алгоритм определения валентности элемента по формуле вещества:
1. над символами химических элементов с постоянной валентностью надписать
валентность элемента
? II
Fe2O3
2. умножить валентность на число атомов этого элемента
IIx3=6
3.разделить полученное число на число атомов элемента с неизвестной
валентностью; частное является значением валентности данного элемента
6:2=III
III II
Fe2O3
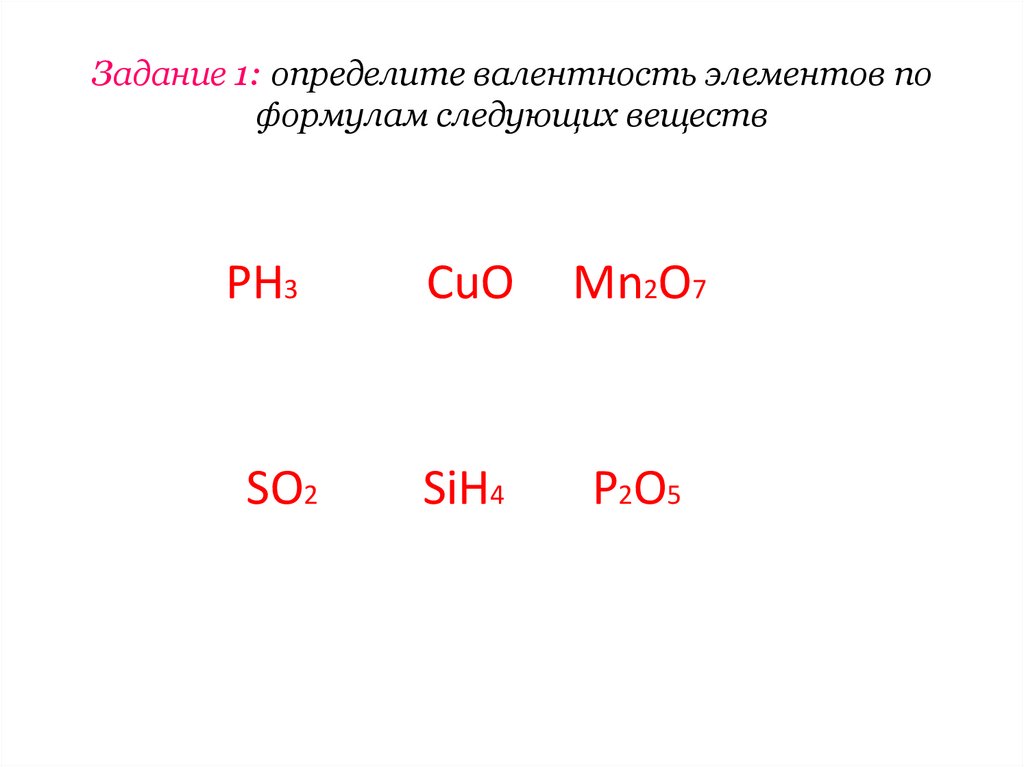
12. Задание 1: определите валентность элементов по формулам следующих веществ
PH3CuO
Mn2O7
SO2
SiH4
P2O5
13. Алгоритм составления формулы вещества по валентности элементов
1. над символами элементов надписать валентности элементов
VI II
S O
2.найти НОК для чисел валентности: 6
3. разделить НОК на значение валентности этих элементов:
S (6 : VI=1);
O (6 : II=3)
4.полученные числа это индексы этих элементов в формуле:
SO3
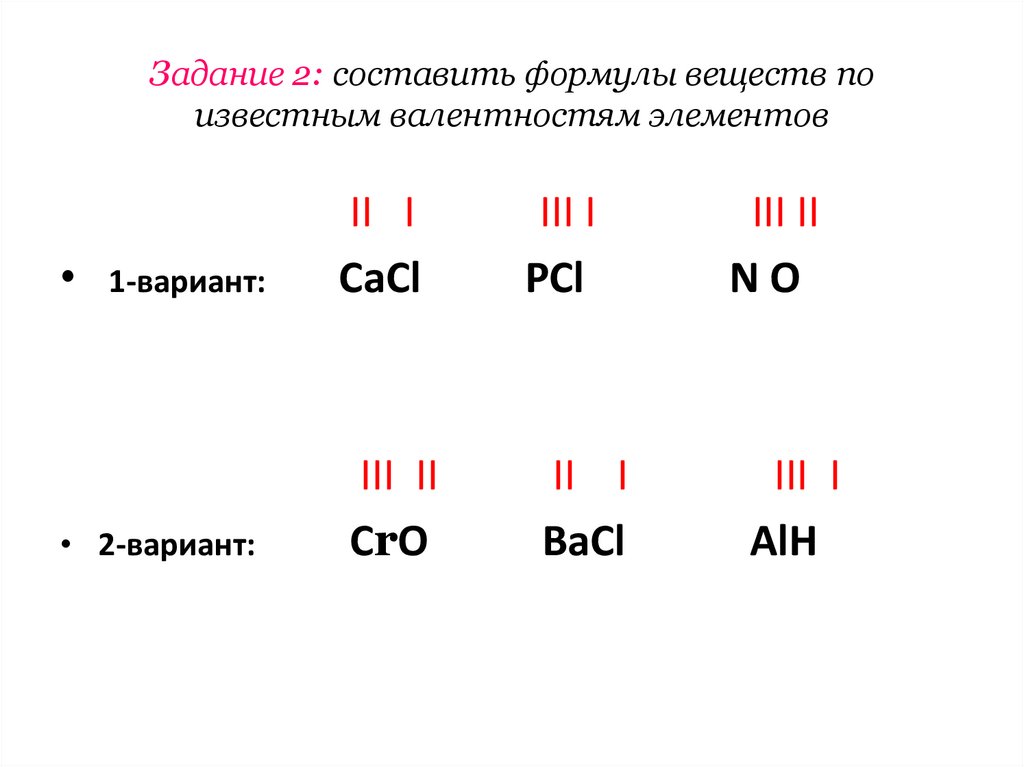
14. Задание 2: составить формулы веществ по известным валентностям элементов
1-вариант:II I
CaCl
III I
PCl
III II
NO
• 2-вариант:
III II
СrO
II I
BaCl
III I
AlH
15.
16.
17.
18.
19.
20.
21.
22.
23.
24.
25.
26.
27.
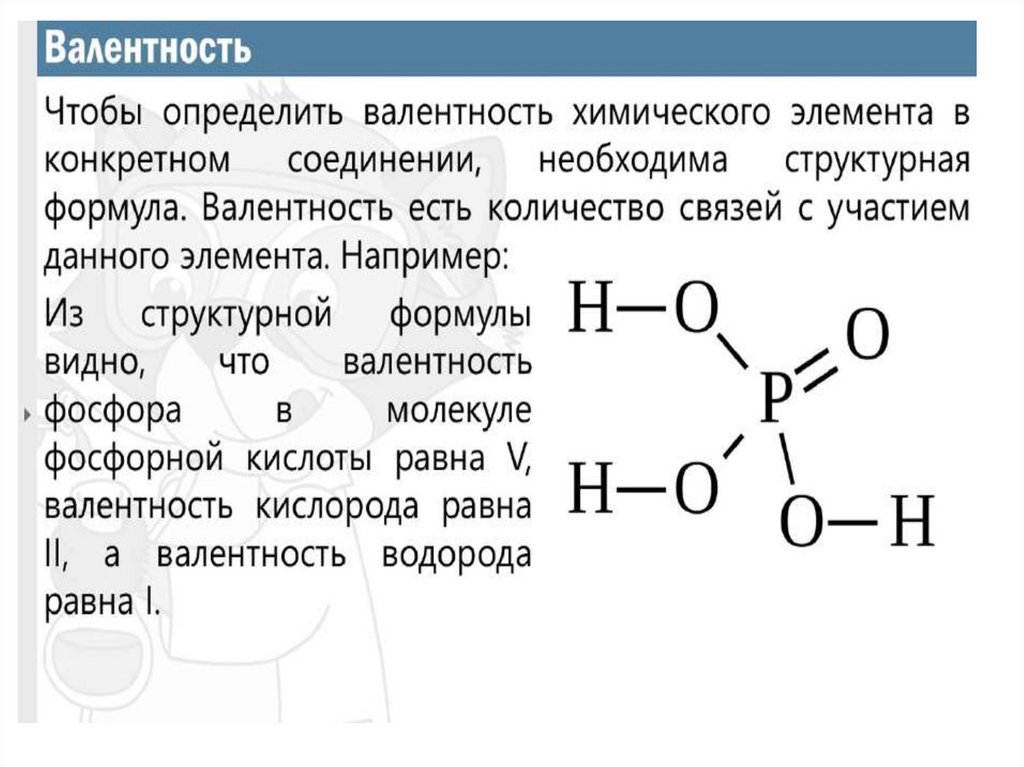
28. Структурная формула -
Структурная формула • это графическое изображениехимического строения молекулы
вещества, в котором
показывается порядок связи
атомов, их геометрическое
расположение. Кроме того, она
наглядно показывает
валентность атомов входящих в
ее состав.
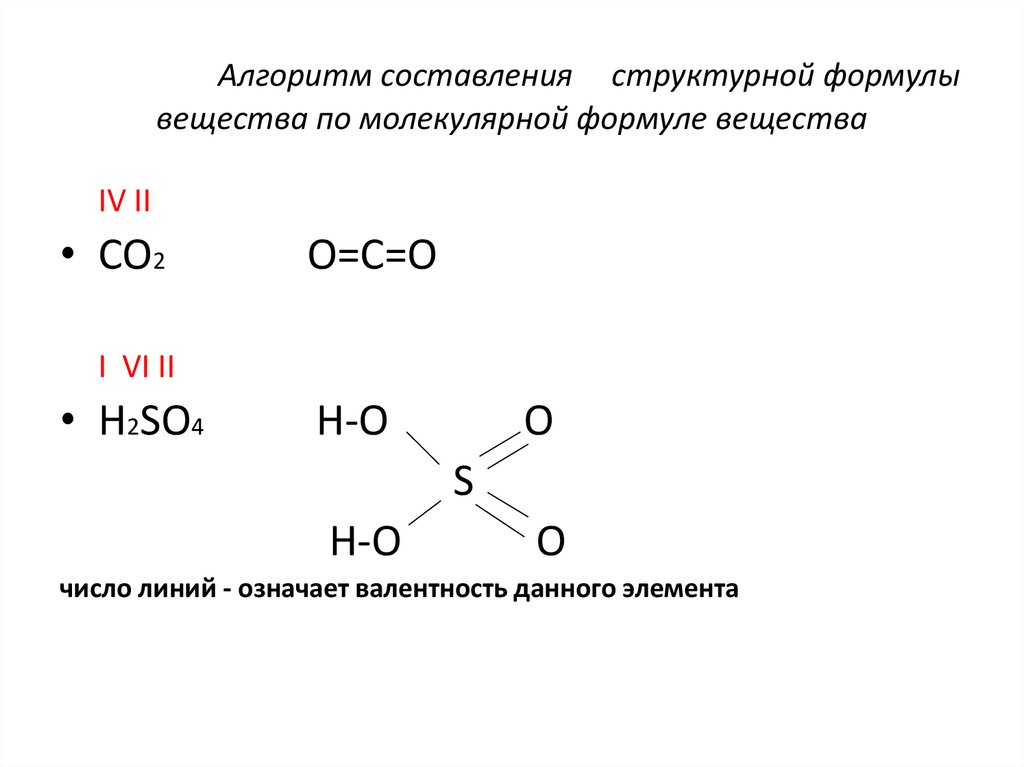
29. Алгоритм составления структурной формулы вещества по молекулярной формуле вещества
IV II• CO2
O=C=O
I VI II
• H2SO4
H-O
O
S
H-O
O
число линий - означает валентность данного элемента
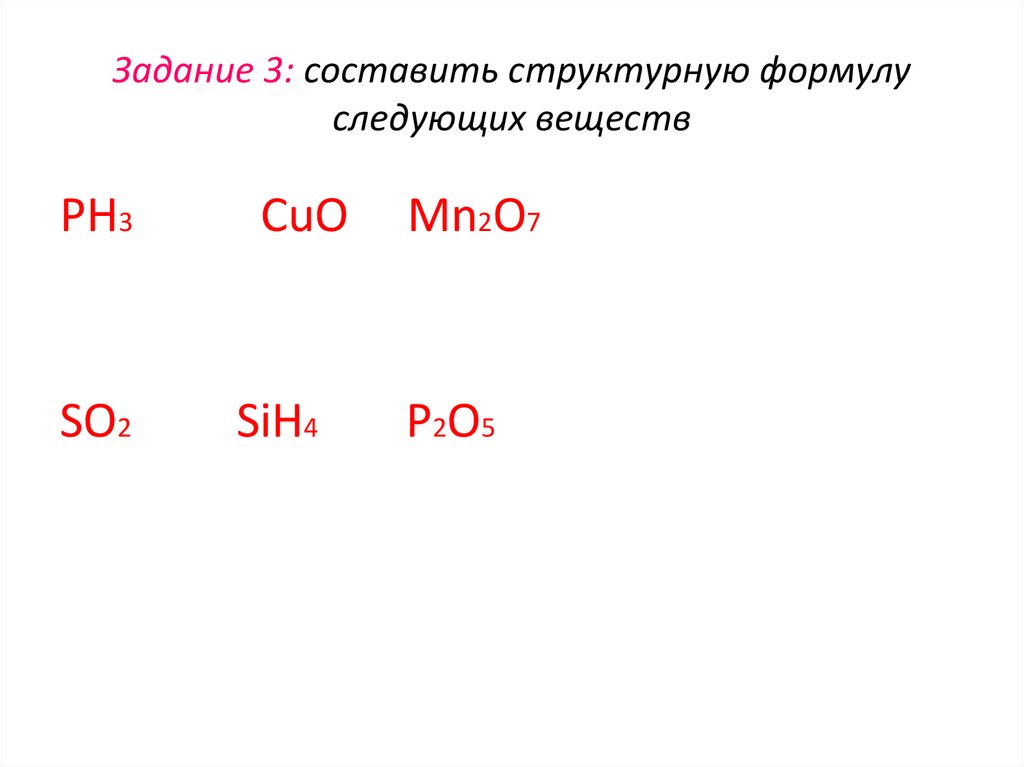
30. Задание 3: составить структурную формулу следующих веществ
PH3CuO
Mn2O7
SO2
SiH4
P2O5
31.
32.
33.
34.
35.
36.
37.
38.
39.
40.
41.
42.
43.
44.
45.
46.
47.
48.
49.
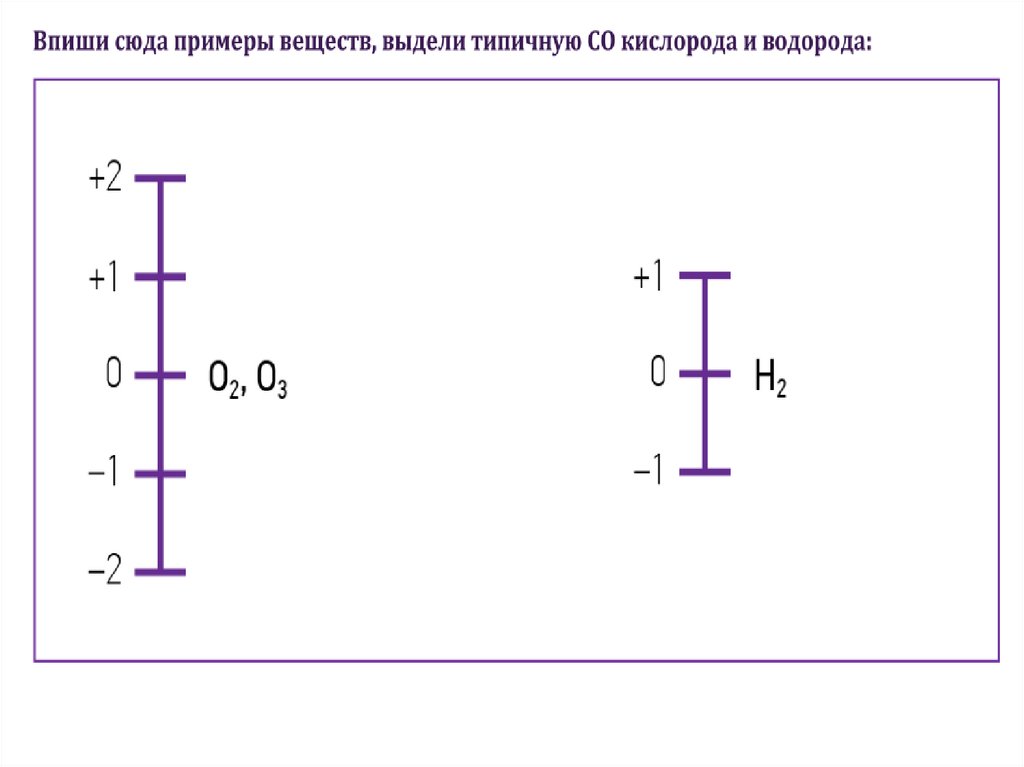
1)Степень окисления простых веществ равна нулю
Например: S0, H02, Cl02, O02, Na0.
2) Максимальная (высшая) степень окисления равна + номер
группы (элемент на первом месте)
Например: P2+5O5 , S+6F6.
Если степень окисления переменная – будет указано в скобках.
3) Минимальная степень окисления равна – ( 8 – номер группы)
(элемент на втором месте)
Например: SCl2-1 , Li3P-3.
4) Постоянные степени окисления:
* H +1 (кроме гидридов активных металлов, например:Na+1H-1)
* O-2 (кроме O+2F2, H2O2-1,пероксидов металлов)
* F-1
* металлы первой А группы–степень окисления +1
* металлы второй А группы– степень окисления +2
* металлы третьей А группы – степень окисления +3
50.
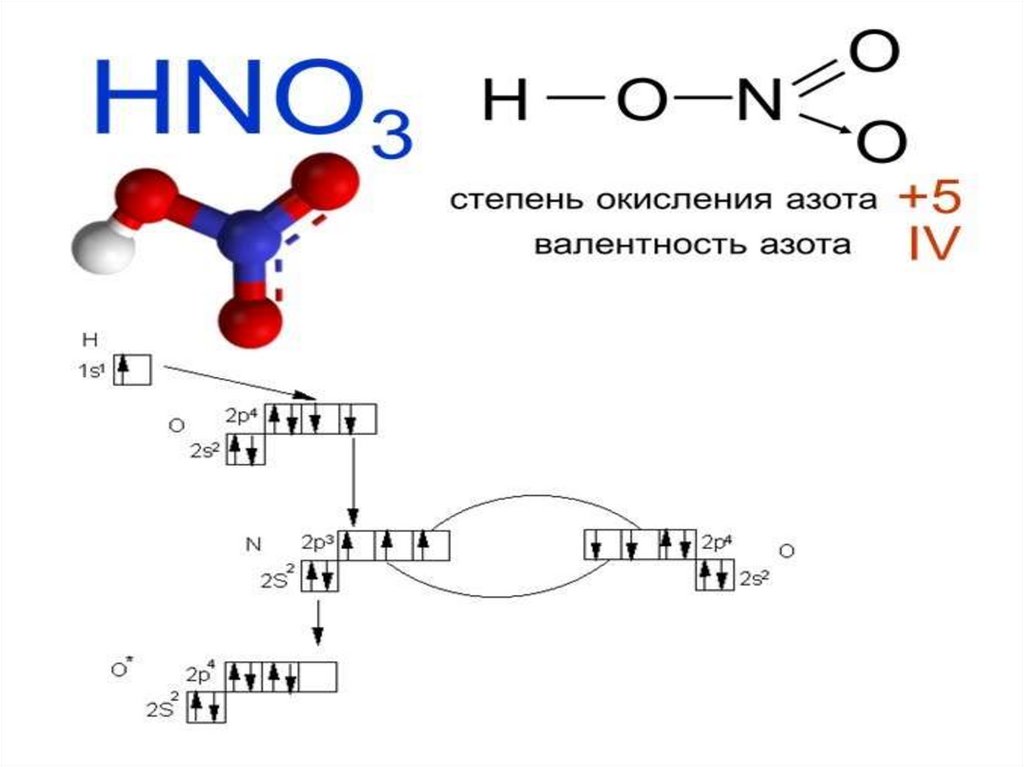
Cl+14
+7
2
O
-2
7
-14 =0
В соединениях суммарная степень окисления всегда равна
нулю. Зная это и степень одного из элементов, всегда можно
найти степень окисления другого элемента по формуле
бинарного соединения. Например, найдём степень окисления
хлора в соединении Cl2O7. Обозначим степень окисления
кислорода: Cl2O7-2.Следовательно, семь атомов кислорода
будут иметь общий отрицательный заряд(-2).7=-14. Тогда
общий заряд двух атомов хлора будет равен+14, а степень
окисления одного атома:
(+14):2=+7
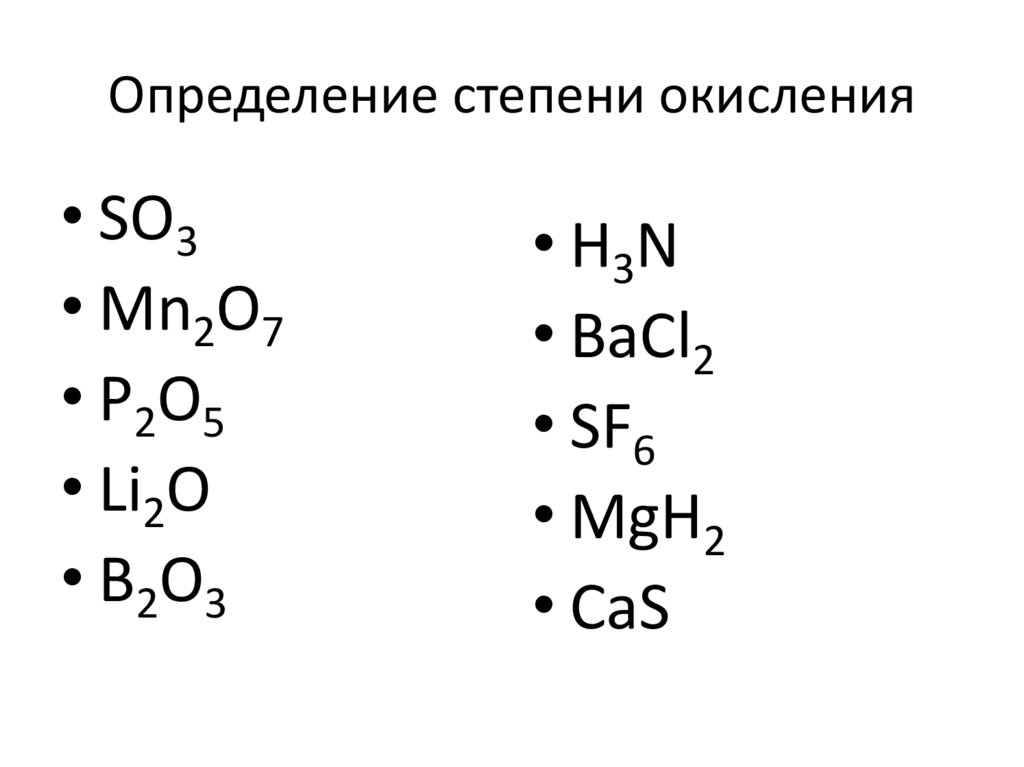
51. Определение степени окисления
• SO3• Mn2O7
• P2O5
• Li2O
• B2O3
• H3N
• BaCl2
• SF6
• MgH2
• CaS
52.
53.
Правило: алгебраическая сумма степеней окисления всложном ионе равна суммарному заряду этого иона.
(S2 O3-2)2Рассмотрим пример:
+4
-6
=-2
Обозначим степень окисления кислорода-2 .Три иона
кислорода будут иметь общий отрицательный заряд
(-2).3=-6. Тогда общий заряд двух ионов серы будет
равен+4, а одного иона (+4):2=+2
(S22+O3-2)2-
54.
ZnS, Ca3N2Si
Fe
N2
O2
H
Cl3
Ba
C
O3
Na
Cl
O4
O3
N
K3
S
O3
P
O4
O3
55. Составление формул по степени окисления
Оксид натрия Хлорид железа (III) Нитрид магния Оксид серы (IV) -Сульфид алюминия Гидрид магния -
56.
1)Расставьте
степени
окисления в
соединениях и в
ионах:
MgO
Zn
KNO3
HMnO4
CaSО3
Na3PO4
(CrO4)-2
(IO4)-
2) Составьте формулы
следующих соединений:
Хлорид железа(III)
Оксид серы(VI)
Гидрид калия
Нитрид бария
3) Назовите вещества,
представленные формулами:
P2O5
AgBr
CuS
NaH
57. Расставьте степени окисления в соединениях и в ионах:
Проверочная работаI вариант
II вариант
1) Расставьте степени окисления в соединениях и в ионах:
H2SO3 H4P2O7 ZnF2
BaCO3 O2 Na2SO4
(PO4)3-, (MnO4)-
CaBr2 KClO4 S8
Na2Cr2O7 Li2SO4 MgSiO3
(ClO2)- ,(NO3)-
2) Составьте формулы следующих соединений:
Хлорид магния
Сульфид железа (III)
Оксид бора
Нитрид кальция
Оксид азота(II)
Фторид алюминия
Гидрид бария
Оксид серы(IV)
Сульфид магния
Нитрид лития
3) Назовите вещества, представленные формулами:
LiH , CuO, FeCl3, Ag2S
FeCl2, CaH2, CO2, Al2S3





































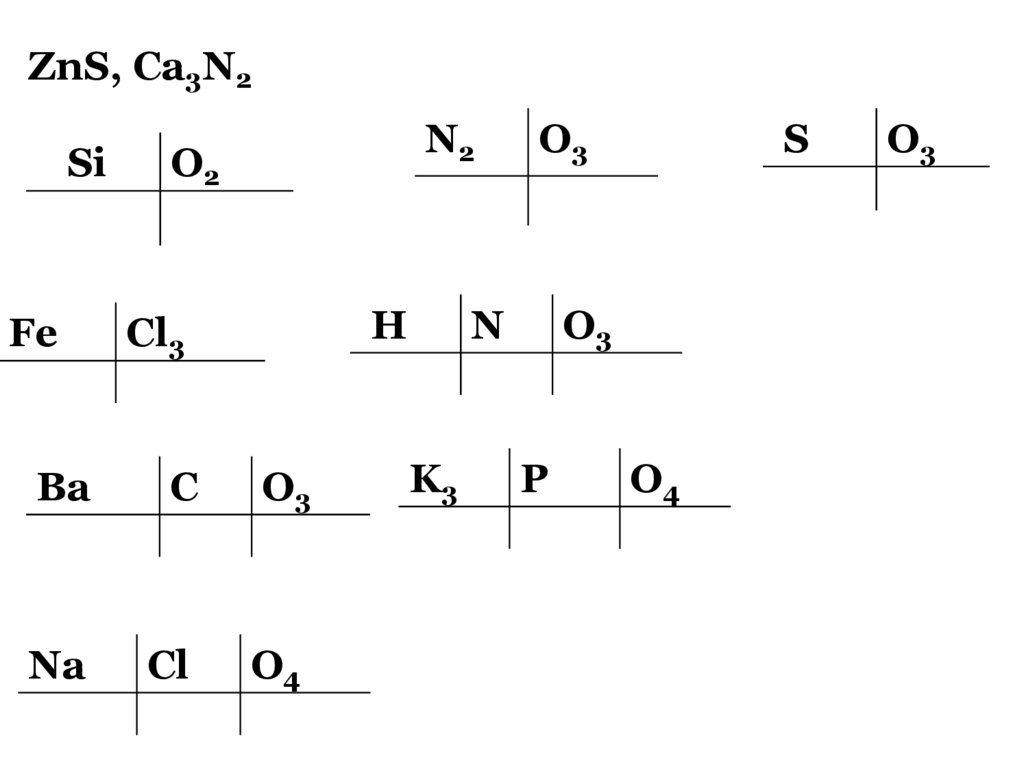




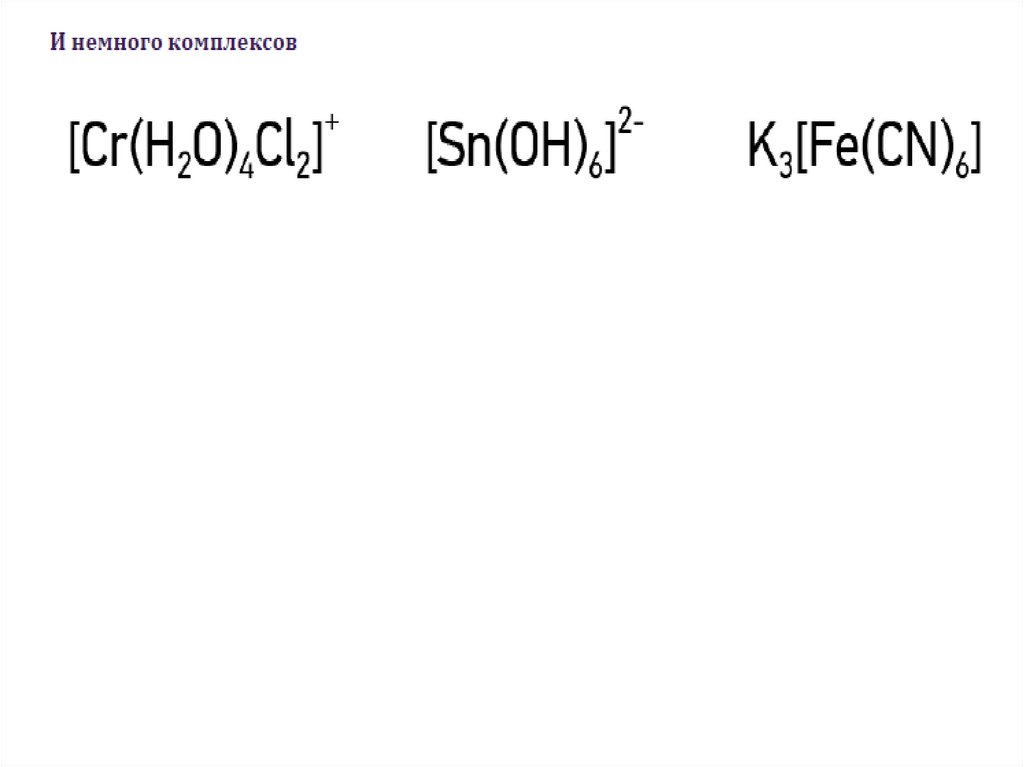


























 Химия
Химия