Похожие презентации:
Реакції обміну між розчинами електролітів, умови їх перебігу. Реакція обміну в розчинах електролітів
1. Реакції обміну між розчинами електролітів, умови їх перебігу.
Дем.4 Реакція обміну врозчинах електролітів
2.
Мета: поглибити знання про умовипротікання реакцій обміну;
повторити правила складання
молекулярних рівнянь реакцій
обміну; навчитися визначати чи
відбувається іонний обмін між
розчинами електролітів та складати
іонні рівняння для реакцій обміну.
3. Актуалізація знань:
Які типи хімічних реакцій намвідомі?
Сполучення – А+В=АВ
Заміщення – АВ + С = СВ + А
Обміну – АВ + СД = СВ + АД
Розкладу , як виняток вчать
напам'ять.
4. Актуалізація знань:
Запишітьрозв’язок рівнянь
реакцій:
P(V) + O2 =
Li + O2 =
Fe(ІІІ) + Cl2 =
FeCl2 + Cl2 =
H2 + F2 =
Ca + O2 =
N2(ІІІ) +
O2 =
Al(OH)3 + HCl =
FeBr3 + Cl2 =
P2O5 + H2O =
Ca + H3PO4 =
KClO3 =
Na + Br2 =
Ag + S(ІІ) =
5. Алгоритм складання рівнянь реакцій іонного обміну
Записуємо умову рівняння:FeBr3 + Ba(OH)2 =
Складаємо молекулярне рівняння:
3FeBr3 + 2Ba(OH)2=2Fe(OH)3 + 3BaBr2
р
р
н
Класифікуємо речовини на
електроліти та неелктроліти.
р
6. Алгоритм складання рівнянь реакцій іонного обміну
Кожний електролітрозщеплюємо на іони,
неелектроліти залишаємо в
молекулярному вигляді:
Fe3+ + Br- +Ba2+ +ОН- =
= 2Fe(OH)3 + Ba2+ + Fe3+
7. Алгоритм складання рівнянь реакцій іонного обміну
Урівнюємо іонне і молекулярнерівняння:
2FeBr3 + 3Ba(OH)2=2Fe(OH)3 + 3BaBr2
2Fe3+ + 6Br- +3Ba2+ +6ОН- =
= 2Fe(OH)3 +3Ba2+ + 6Br-
8. Алгоритм складання рівнянь реакцій іонного обміну
Однакові іони не впливають наперебіг іонного обміну, тому в
рівнянні їх скорочують:
2Fe3+ + 6Br- +3Ba2+ +6ОН- =
= 2Fe(OH)3 +3Ba2+ + 6Br Отримуємо скорочене іонне
ріняння:
2Fe3+ 6ОН- = 2Fe(OH)3
9. Результат роботи:
3FeBr3 + 3Ba(OH)2=2Fe(OH)3 + 3BaBr2Fe3+ + 6Br- +3Ba2+ +6ОН- =
= 2Fe(OH)3 +3Ba2+ + 6Br 2Fe3+ 6ОН- = 2Fe(OH)3
10. Підсумки:
Отже запам'ятайте – реакції іонногообміну відбуваються, якщо:
Випадає осад ( утворюється
нерозчинна речовина);
Виділяється газ: H2CO3=H2O+CO2 ↑
H2SO3=H2O+SO2 ↑
H2S ↑
Утворюється вода : H2O
11. Обмін не відбувається:
Якщо в результаті реакції всіутворені речовини електроліти:
2NaOH + K2SO4 = Na2SO4 + 2KOH
р
р
р
р
2NaOH + K2SO4 ↔Na2SO4 + 2KOH
12. Завдання на закріплення:
Визначте чи відбувається іоннийобмін, та запишіть рівняння іонного
обміну:
CaCl2 + Na2CO3 =
K2S + HCl =
KOH + H3PO4 =
ZnBr2 + NaNO3 =
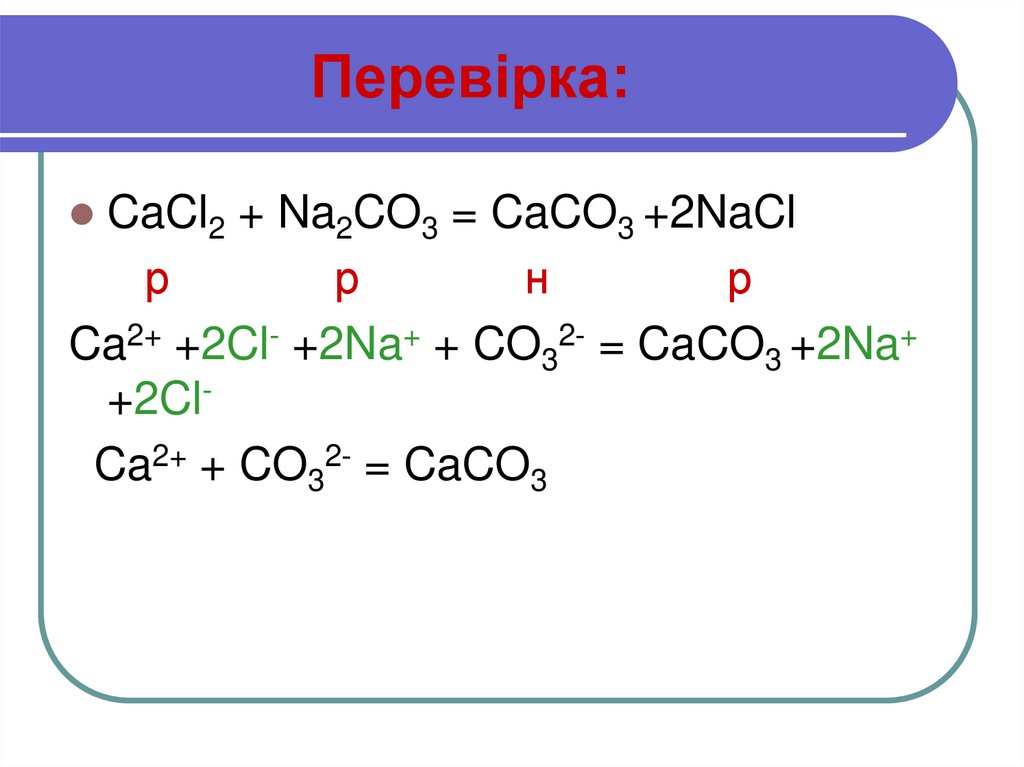
13. Перевірка:
CaCl2 + Na2CO3 = CaCO3 +2NaClр
р
н
р
Ca2+ +2Cl- +2Na+ + CO32- = CaCO3 +2Na+
+2ClCa2+ + CO32- = CaCO3
14. Перевірка:
K2S + 2HCl =2KCl +H2Sр
р
р
н
2K++ S2- + 2H+ +2Cl- =2K+ +2Cl- +H2S
S2- + 2H+ = H2S
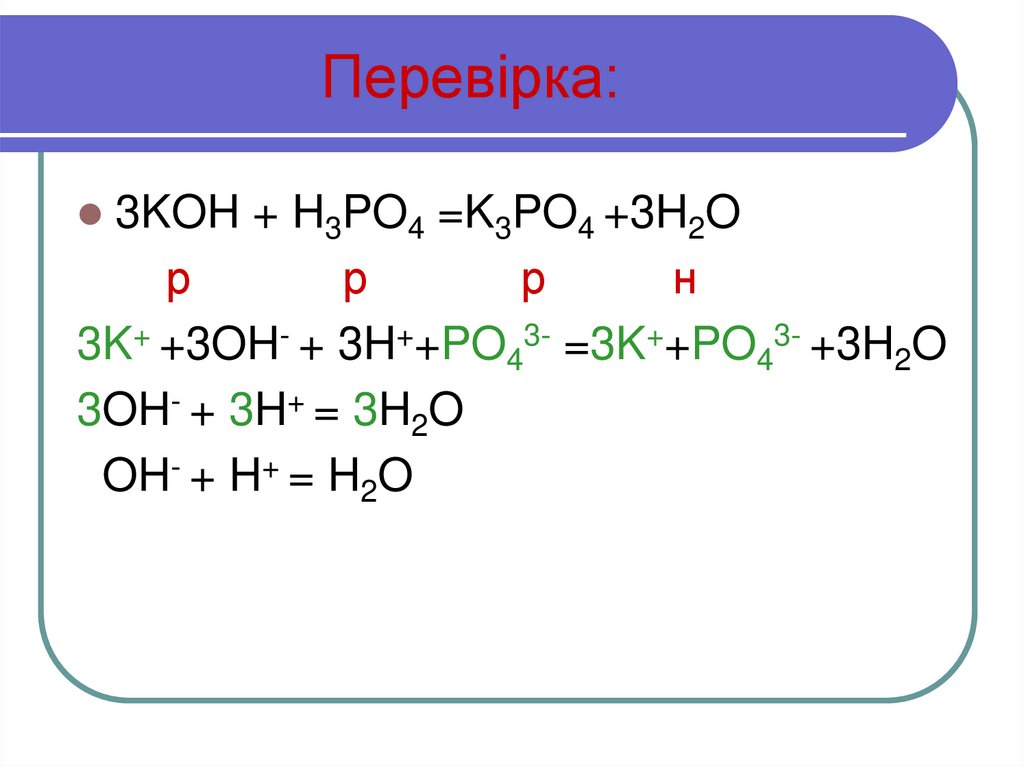
15. Перевірка:
3KOH + H3PO4 =K3PO4 +3H2Oр
р
р
н
3K+ +3OH- + 3H++PO43- =3K++PO43- +3H2O
3OH- + 3H+ = 3H2O
OH- + H+ = H2O
16. Перевірка:
ZnBr2 + 2NaNO3 =Zn(NO3)2 + 2NaBrр
р
р
р
ZnBr2 + 2NaNO3 ↔ Zn(NO3)2 + 2NaBr














 Химия
Химия








