Похожие презентации:
Электрохимические методы обработки и очистки сточных вод
1. Электрохимические методы обработки и очистки сточных вод
2.
Процесс электрохимической очистки сточных вод отцианистых соединений
на аноде
CN– + 2OH– – 2е → CNO– + H2O
2CNO– + 4OH– – 6e → 2CO2 + N2 + 2H2O
на катоде
2H2O + 4e → 2OH– + H2
Cu2+ + 2e → Cu0
на аноде
2Cl– – 2e → Cl2
Cl2 + CN– + 2OH– → CNO– + 2Cl– + H2O
2CNO- + CI2 + 4OH- → 2CO2 + N2 + 2CI- + 2H2O.
3.
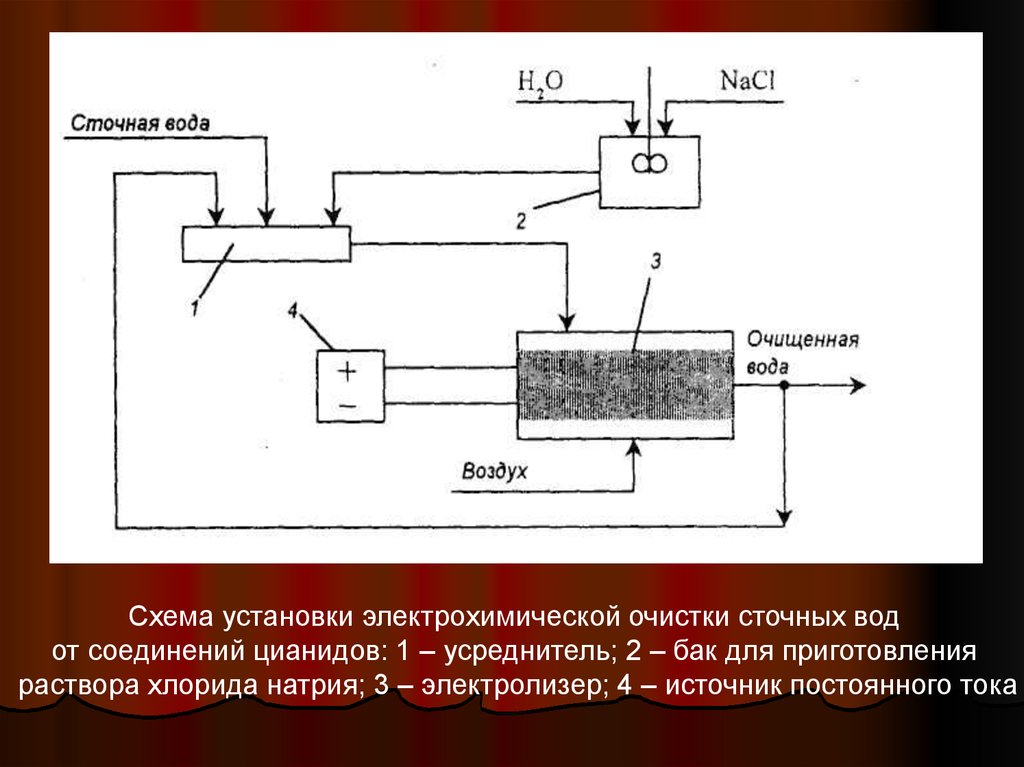
Схема установки электрохимической очистки сточных водот соединений цианидов: 1 – усреднитель; 2 – бак для приготовления
раствора хлорида натрия; 3 – электролизер; 4 – источник постоянного тока
4.
В результате растворения стальных анодов вода обогащается ионамижелеза (II) по реакции:
образующими затем при рН > 5,5 гидроксид железа (II):
который под действием растворенного в воде кислорода переходит в
гидроксид железа (III):
Растворение алюминиевого анода протекает по реакции:
с последующей гидратацией ионов алюминия:
Кроме того, при катодной поляризации алюминия возможно протекание
химической реакции взаимодействия алюминия с водой:
5.
Электрокоагуляторы на очистныхсооружениях
металлообрабатывающего
предприятия
Электродные блоки электрокоагулятора
6.
Схема электрокоагуляционной установки: 1 – усреднитель;2 – бак для приготовления раствора; 3 – источник постоянного тока;
4 – электрокоагулятор; 5 – отстойник;
6 – аппарат для обезвоживания осадка
7.
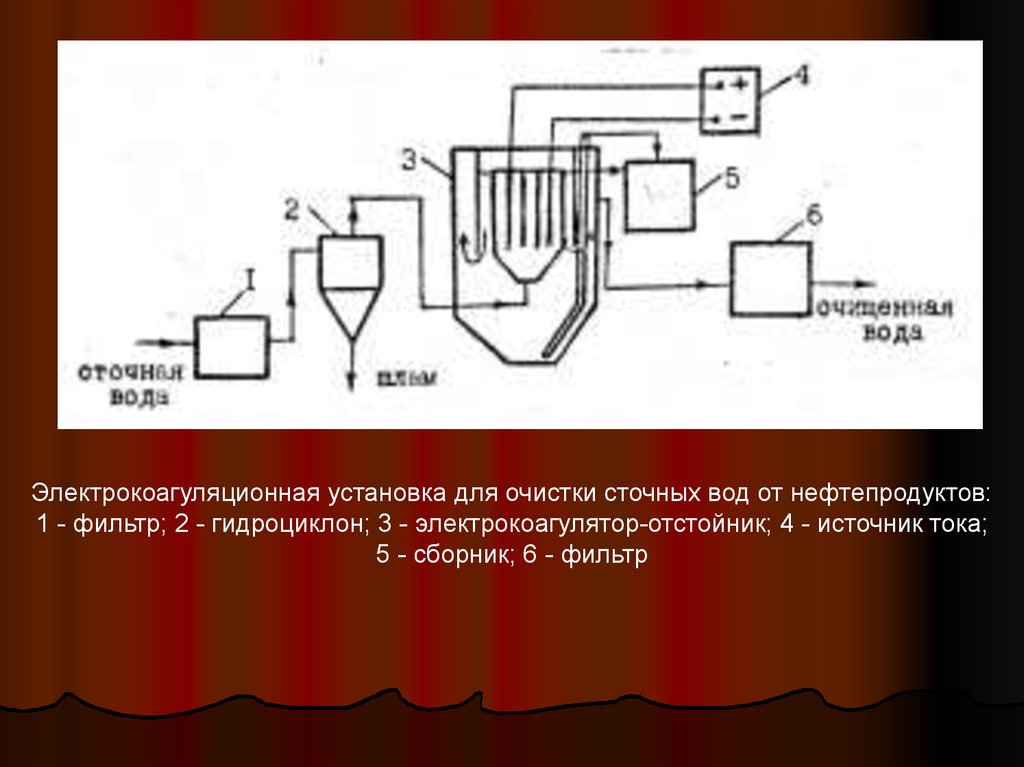
Электрокоагуляционная установка для очистки сточных вод от нефтепродуктов:1 - фильтр; 2 - гидроциклон; 3 - электрокоагулятор-отстойник; 4 - источник тока;
5 - сборник; 6 - фильтр
8.
Метод гальванокоагуляцииСтандартные потенциалы в водных растворах:
-
Al (Е0н = –1,662 В);
Fe (Е0н = –0,44 В);
Сu (Е0н = +0,337 В);
С (Е0н = +0,36 В).
Процесс химического и электрохимического
растворения металлического скрапа и переход ионов
скрапа в раствор:
Fe0 + 2H+ → Fe2+ + H2.
9.
Гальванокоагулятор для очистки сточных вод: 1 – обечайка;2 – воронка; 3 – барбатер; 4-7 – трубки; 8 – патрубок для сжатого
воздуха; 9 - патрубок для подачи очищаемой воды
10.
Процесс восстановления хрома протекает в кислой,нейтральной и щелочной среде:
- в кислой среде
6Fe2+ + Cr2O72- + 14H+ → 6Fe3+ + 2Cr3+ + 7H2O;
- в слабокислой или нейтральной среде
6Fe(OH)2 + Cr2O72- + 7H2O → 6Fe(OH)3↓ + 2Cr(OH)3↓
+ 2OH-;
- в слабощелочной среде
3Fe(OH)2 + CrO42- + 4H2O → 3Fe(OH)3↓ + Cr(OH)3↓ +
2OH-.
11.
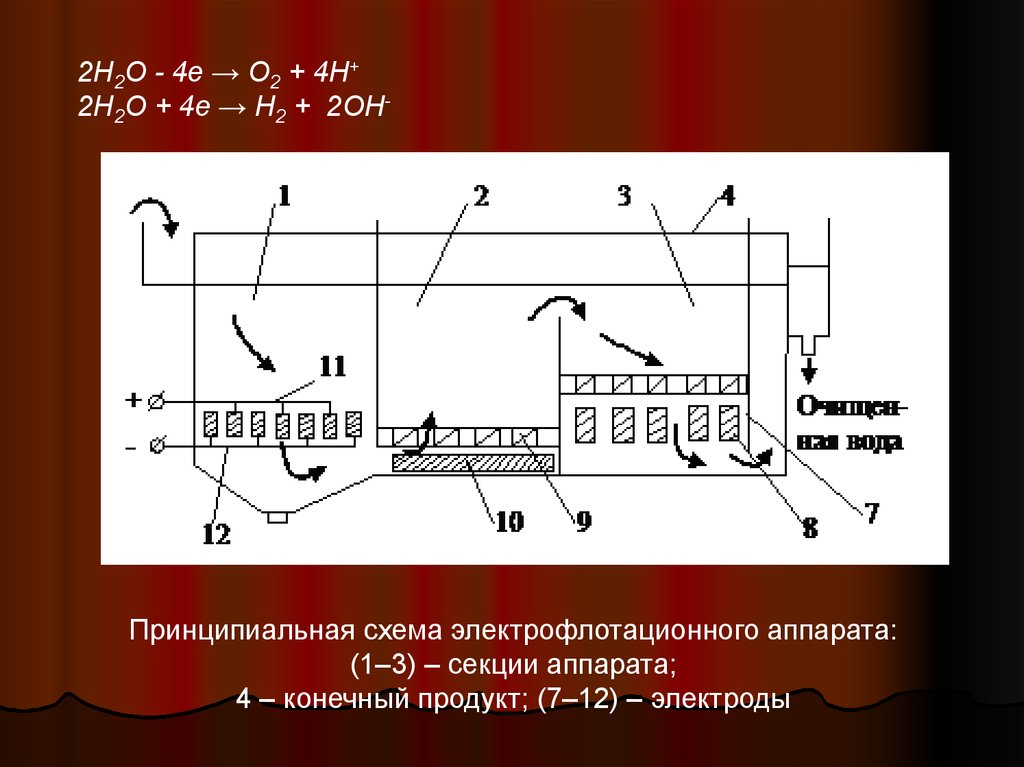
2Н2O - 4e → O2 + 4H+2H2O + 4e → H2 + 2OH-
Принципиальная схема электрофлотационного аппарата:
(1–3) – секции аппарата;
4 – конечный продукт; (7–12) – электроды
12.
Электрофлотатор производительностью 10 м3/ч всистеме оборотного водоснабжения
http://enviropark.ru/
13.
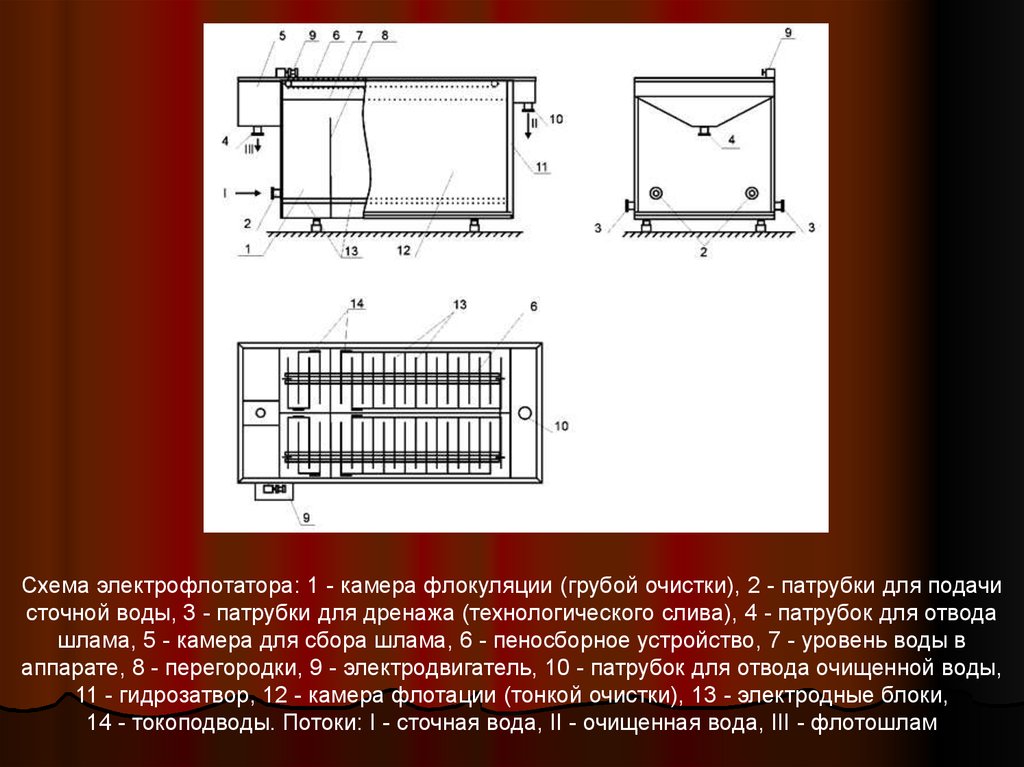
Схема электрофлотатора: 1 - камера флокуляции (грубой очистки), 2 - патрубки для подачисточной воды, 3 - патрубки для дренажа (технологического слива), 4 - патрубок для отвода
шлама, 5 - камера для сбора шлама, 6 - пеносборное устройство, 7 - уровень воды в
аппарате, 8 - перегородки, 9 - электродвигатель, 10 - патрубок для отвода очищенной воды,
11 - гидрозатвор, 12 - камера флотации (тонкой очистки), 13 - электродные блоки,
14 - токоподводы. Потоки: I - сточная вода, II - очищенная вода, III - флотошлам
14.
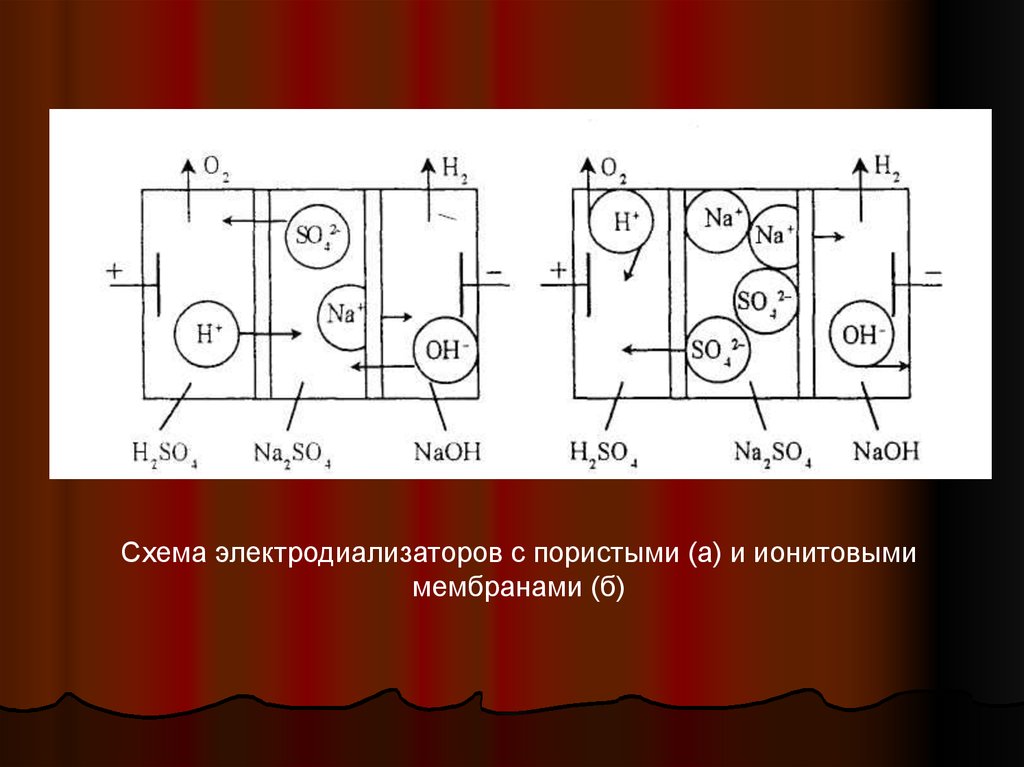
Схема электродиализаторов с пористыми (а) и ионитовымимембранами (б)
15.
Электродиализная установка16.
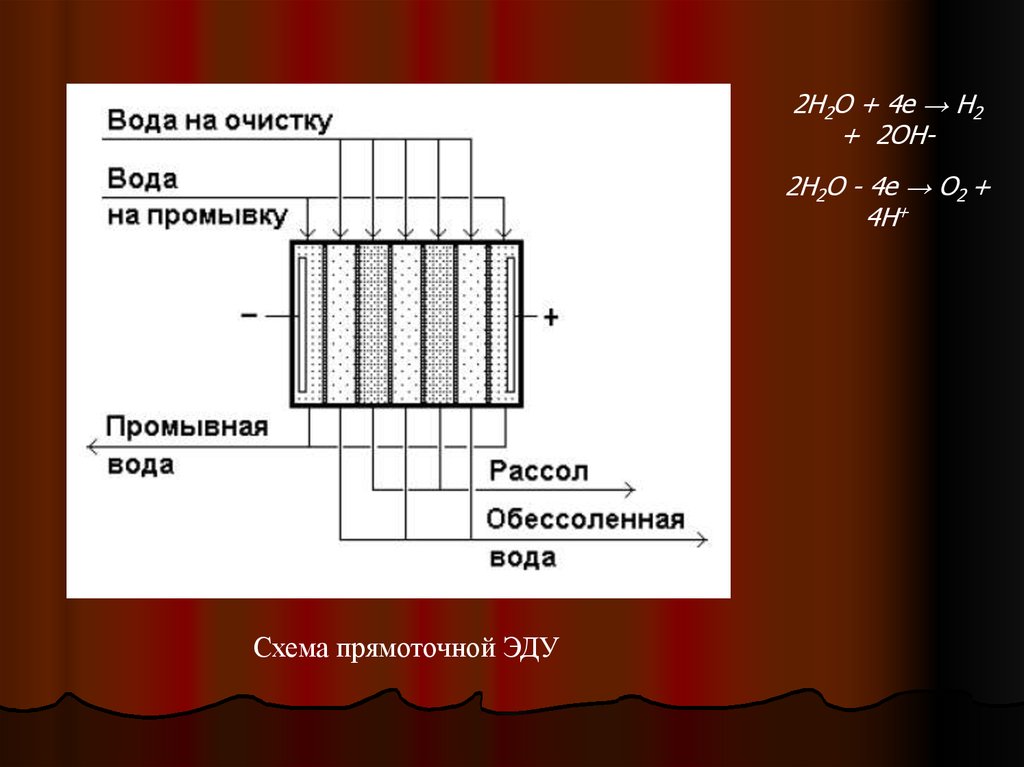
2H2O + 4e → H2+ 2OH2Н2O - 4e → O2 +
4H+
Схема прямоточной ЭДУ
17.
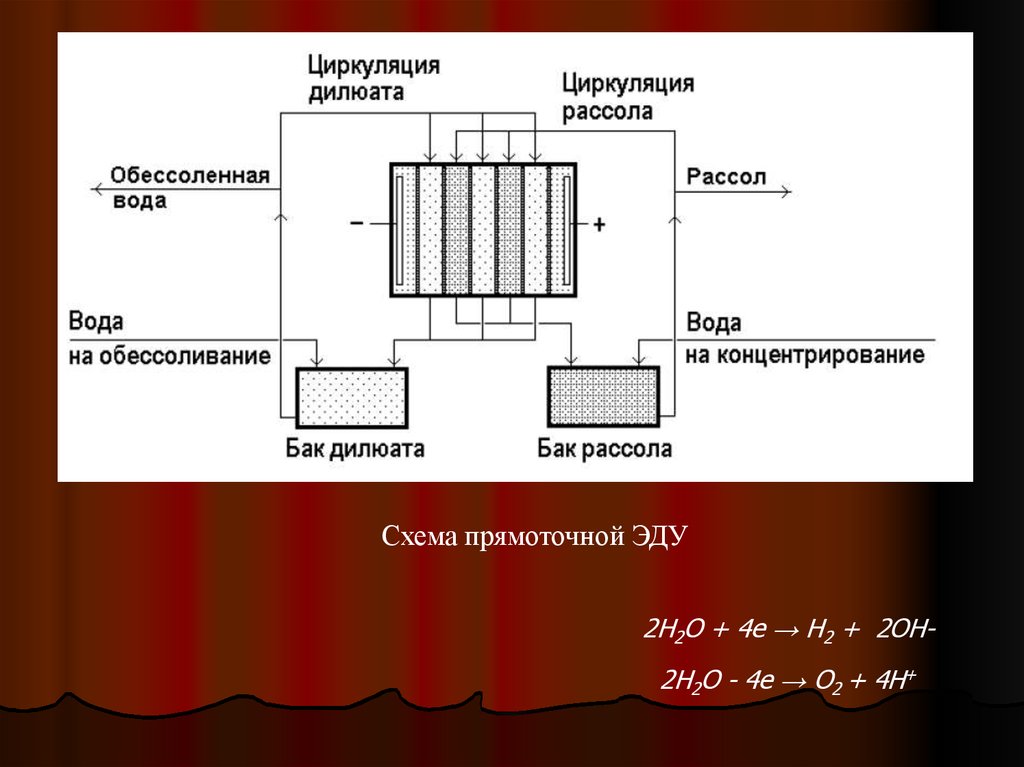
Схема прямоточной ЭДУ2H2O + 4e → H2 + 2OH2Н2O - 4e → O2 + 4H+










 Промышленность
Промышленность








