Похожие презентации:
Термодинамика
1.
2. Термодинамика -
Термодинамика раздел физики, в котором изучаютсянаиболее общие свойства
макроскопических систем, находящихся в
состоянии термодинамического
равновесия, и процессы перехода между
этими состояниями.
3. Внутренняя энергия U -
Внутренняя энергия U складывается из энергии беспорядочного(теплового) движения атомов, молекул и энергии
межмолекулярных и внутриатомных движений и
взаимодействий.
i
i
U N к NkT RT
2
2
4.
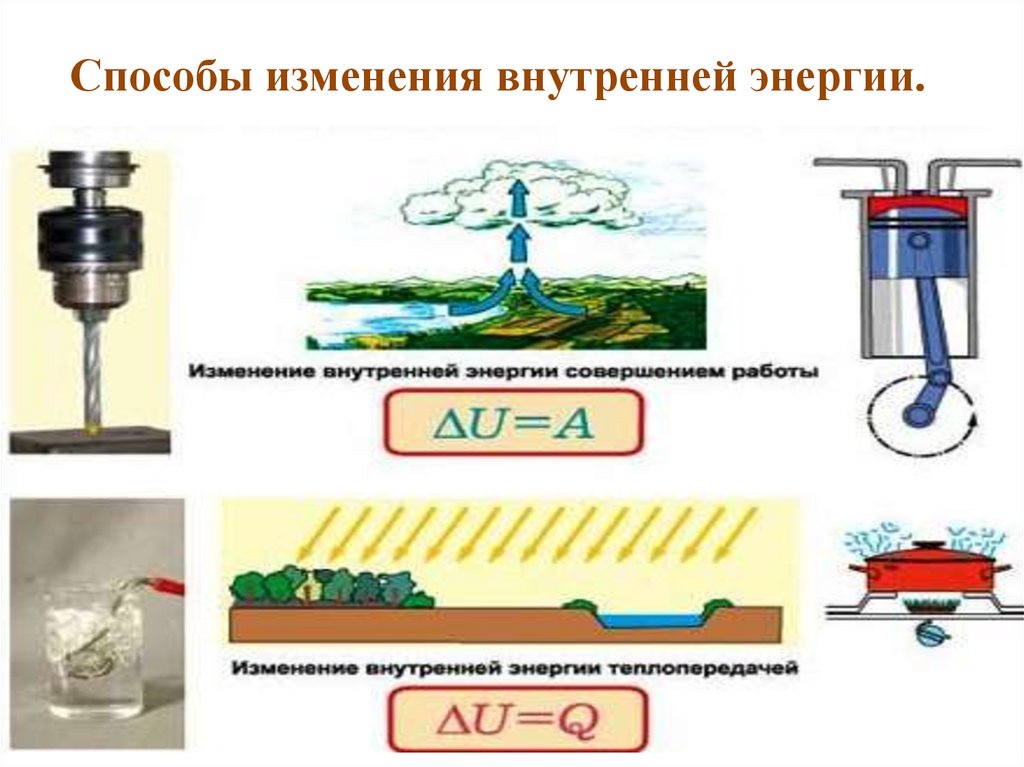
Способы изменения внутренней энергии.5. Работа в термодинамике -
Работа в термодинамике это способ изменения внутренней энергиитермодинамической системы, при которой
энергия передается в процессе силового
взаимодействия тел и происходит
изменение внешних параметров состояния
системы.
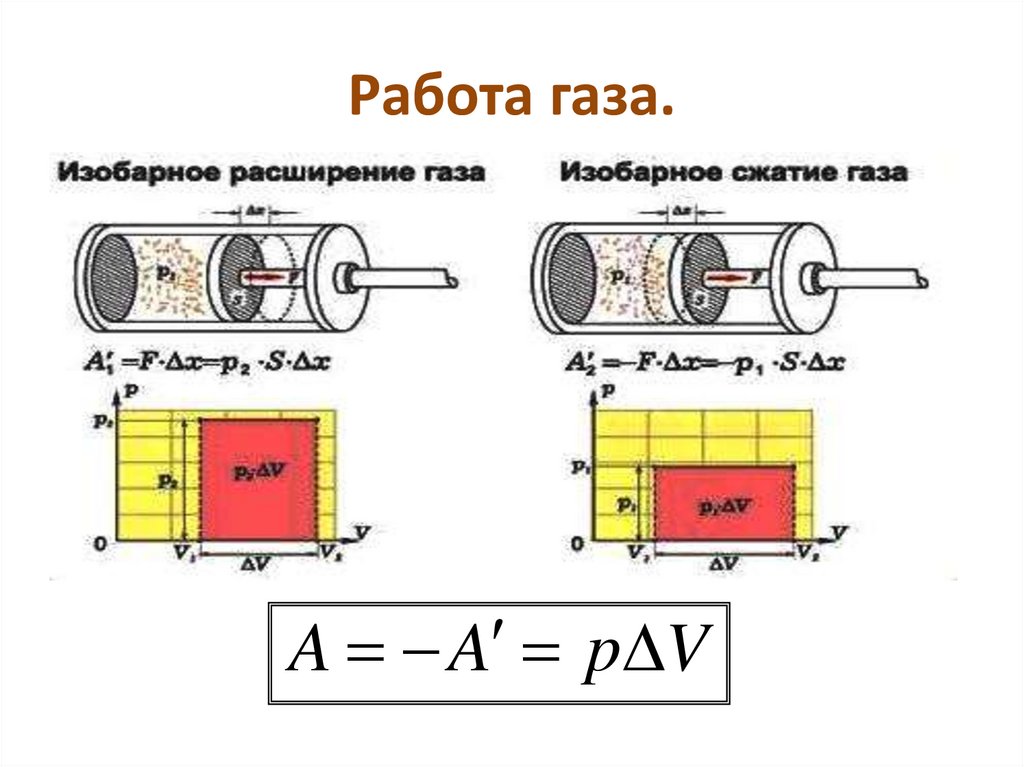
6. Работа газа.
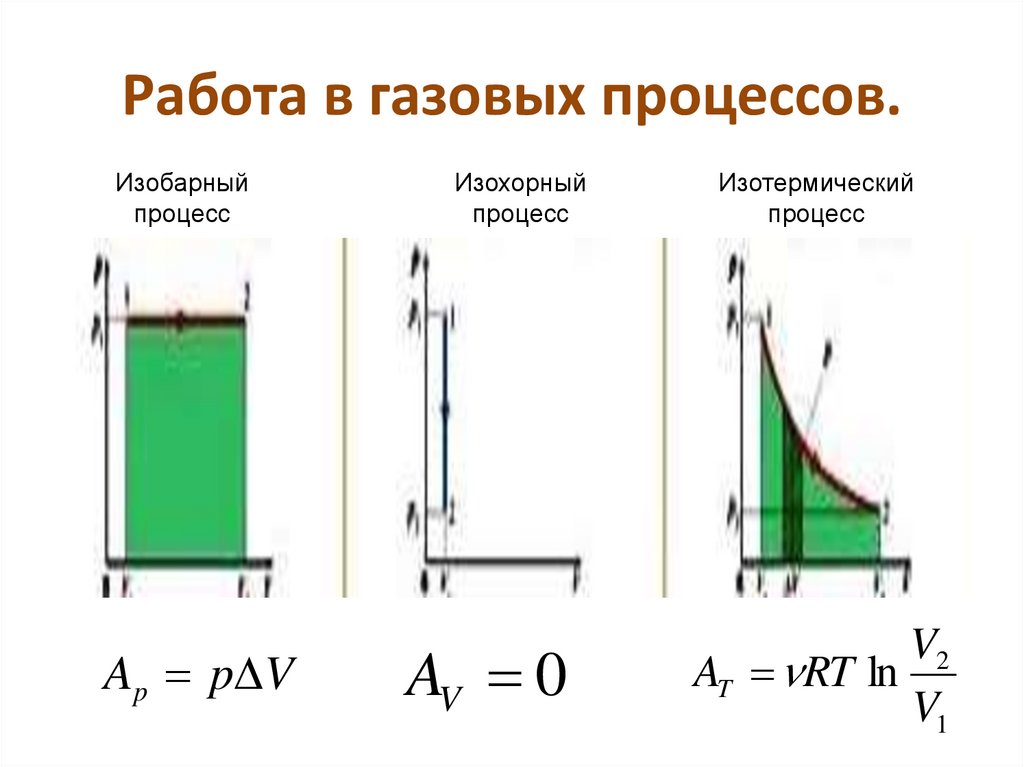
A A p V7. Работа в газовых процессов.
Изобарныйпроцесс
A p p V
Изохорный
процесс
AV 0
Изотермический
процесс
V2
AT RT ln
V1
8. Количеством теплоты
Количеством теплоты— это энергия, которую тело отдает при
теплообмене (без совершения работы).
Количество теплоты называют
количественную меру изменения
внутренней энергии тела при теплообмене
(или теплопередаче).
9. Три вида теплообмена.
10. Теплопроводность
— способность материальных тел проводить энергию(теплоту) от более нагретых частей тела к менее
нагретым частям тела путём хаотического движения
частиц тела . Такой теплообмен может происходить в
любых телах с неоднородным
распределением температур, но механизм переноса
теплоты будет зависеть от агрегатного состояния
вещества.
11. Конвекция
(от лат. convectiō —«перенесение») — вид
теплообмена , при котором
внутренняя энергия
передаётся струями и
потоками самого
вещества. При конвекции
нижние слои вещества
нагреваются, становятся
легче и всплывают, а
верхние слои, наоборот,
остывают, становятся
тяжелее и опускаются
вниз, после чего процесс
повторяется снова и снова.
12. Излучение
Излучение— это
передача энергии в
форме волн или
частиц через
пространство или
через
материальную
среду.
13. Тепловое излучение —
Тепловое излучение —электромагнитное
изучение, испускаемое
телами за счёт их
внутренней энергии.
i
k 2 kT
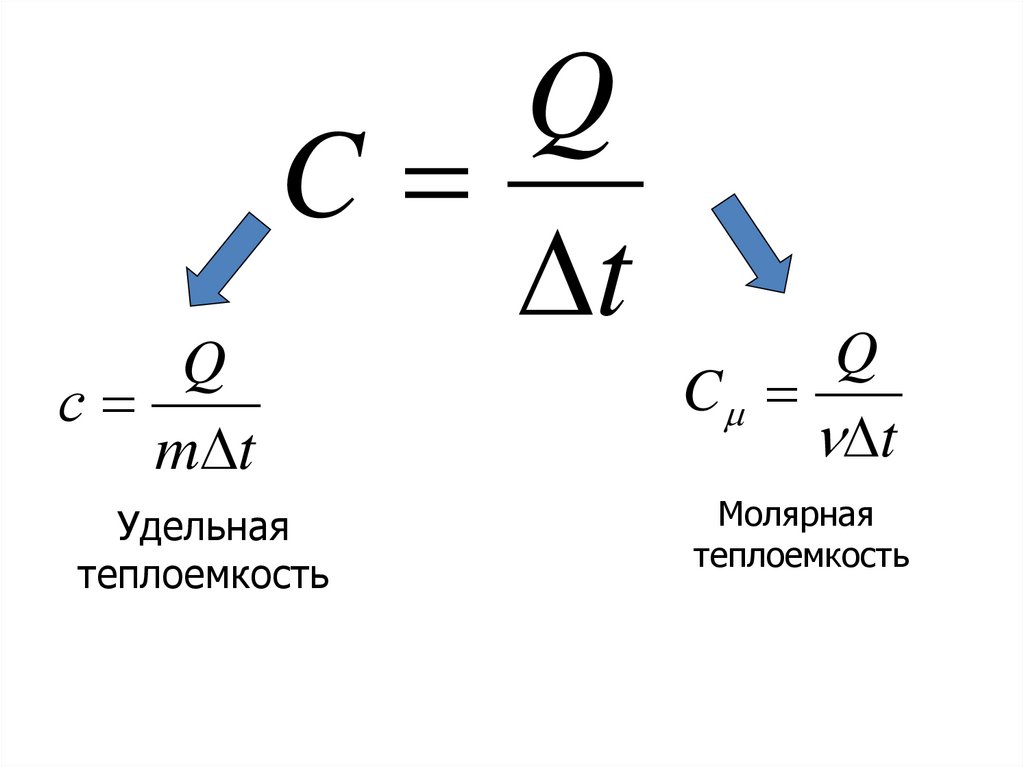
14. Теплоемкость С – величина, равная отношению количества теплоты Q, сообщенного телу, к изменению температуры ∆t.
1 ДжДж
C 0 1
1С
К
15.
Qс
m t
Q
C
t
Удельная
теплоемкость
Q
C
t
Молярная
теплоемкость
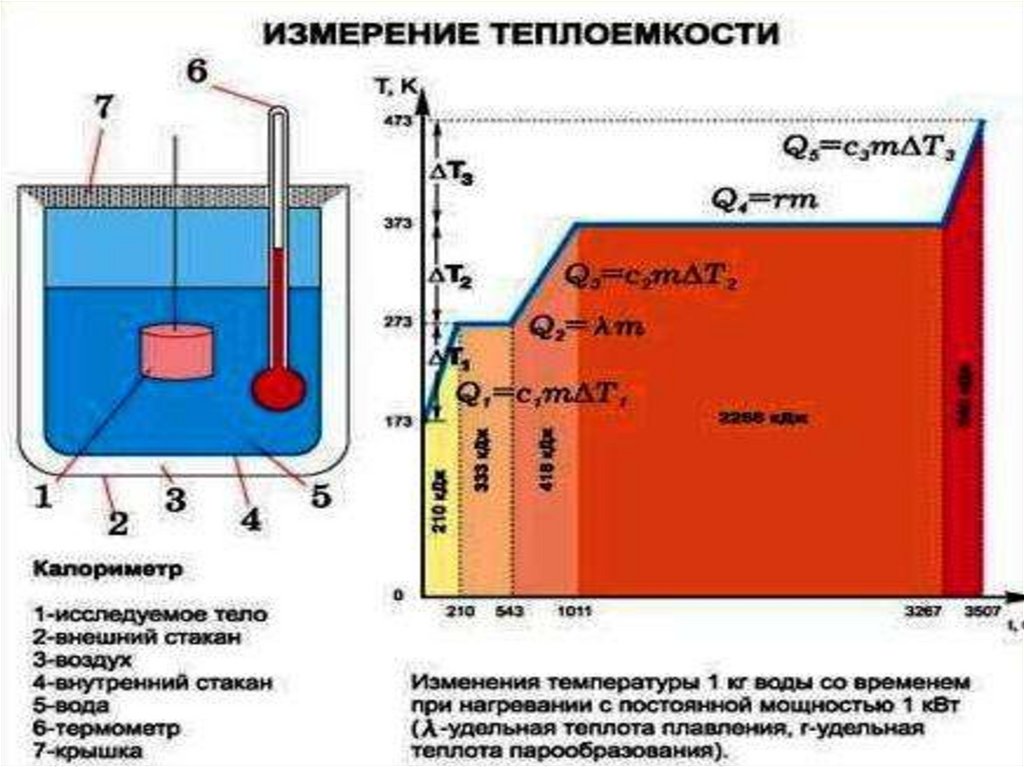
16.
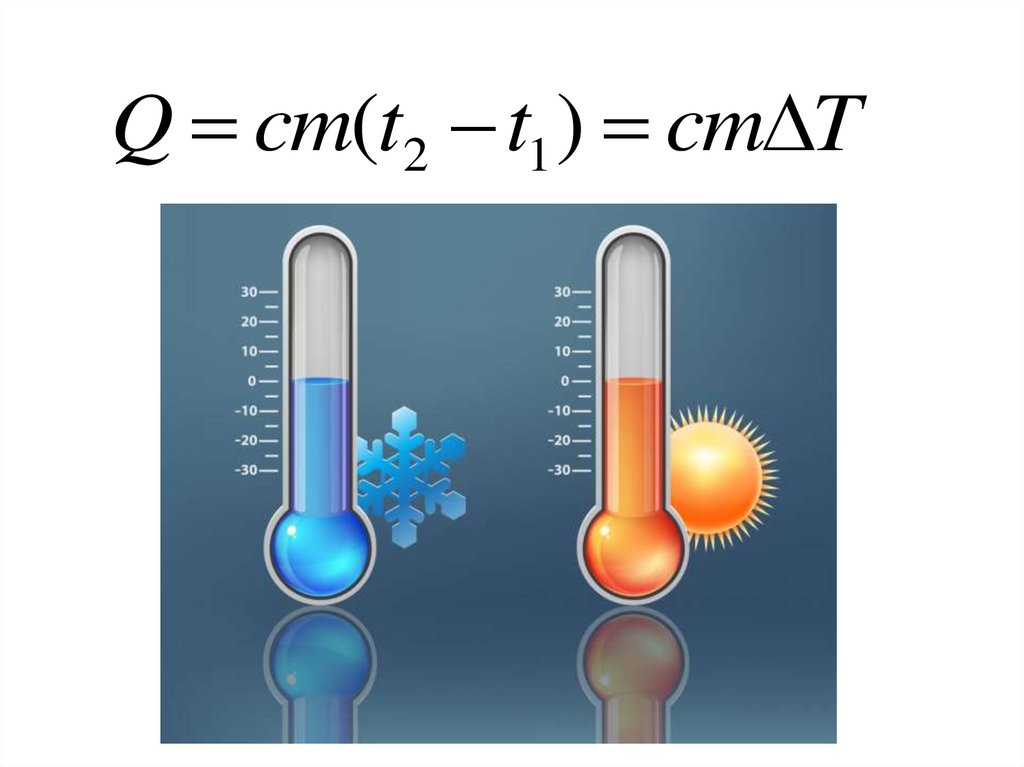
17.
Q cm(t2 t1 ) cm T18. КОЛИЧЕСТВО ТЕПЛОНЫ СООБЩЕННОЕ ГАЗУ ИДЕТ НА ИЗМЕНЕНИЯ ЕГО ВНУТРЕННЕЙ ЭНЕРГИИ И НА СОВЕРШЕНИЕ РАБОТЫ ГАЗОМ.
Q U A19. Вечный двигатель.
Из первого начала термодинамики вытекаетневозможность создания перпетуум мобиле
(вечного двигателя) первого рода, то есть
устройства, способного как угодно долго
совершать работу не получая энергию.
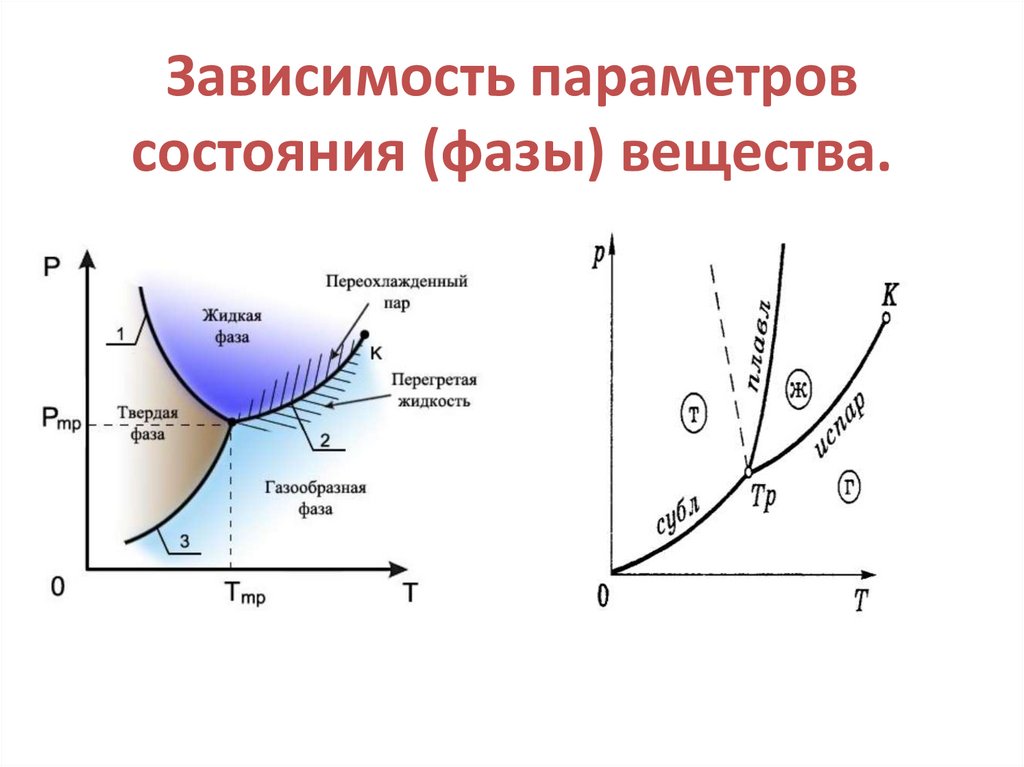
20. Зависимость параметров состояния (фазы) вещества.
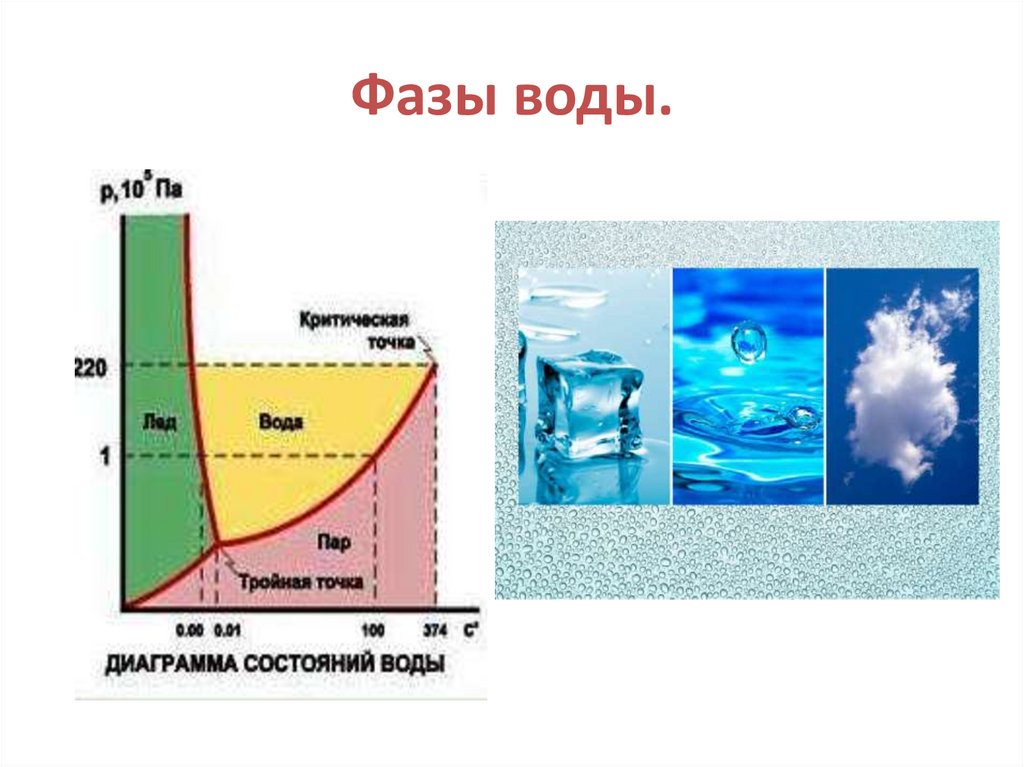
21. Фазы воды.
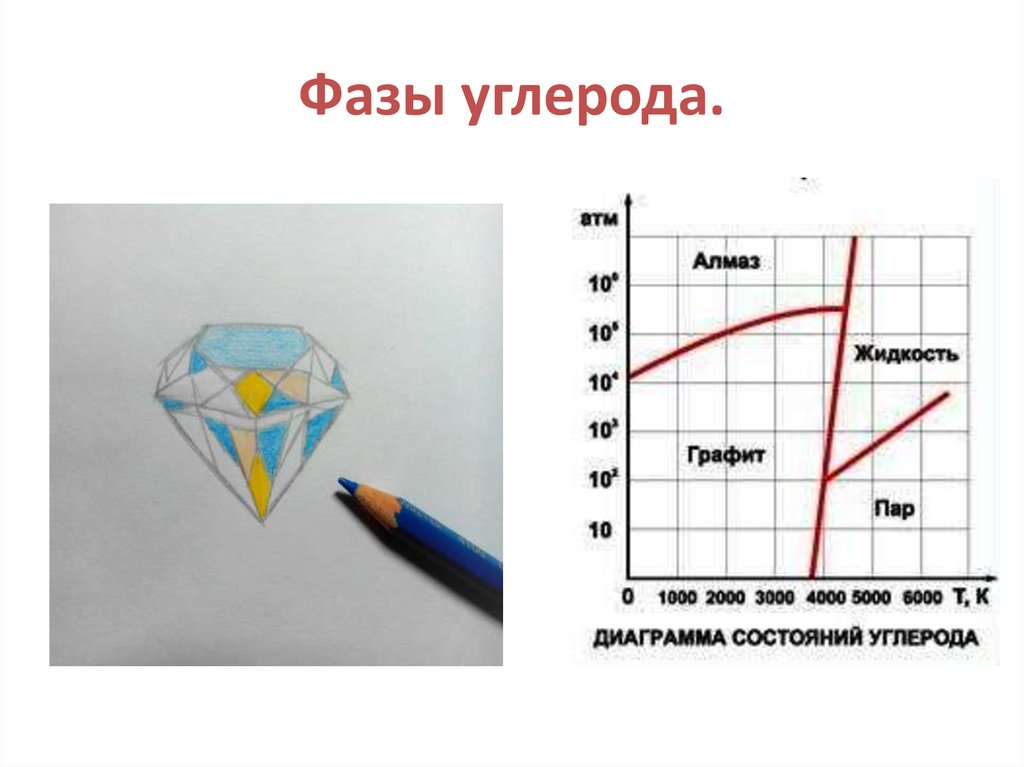
22. Фазы углерода.
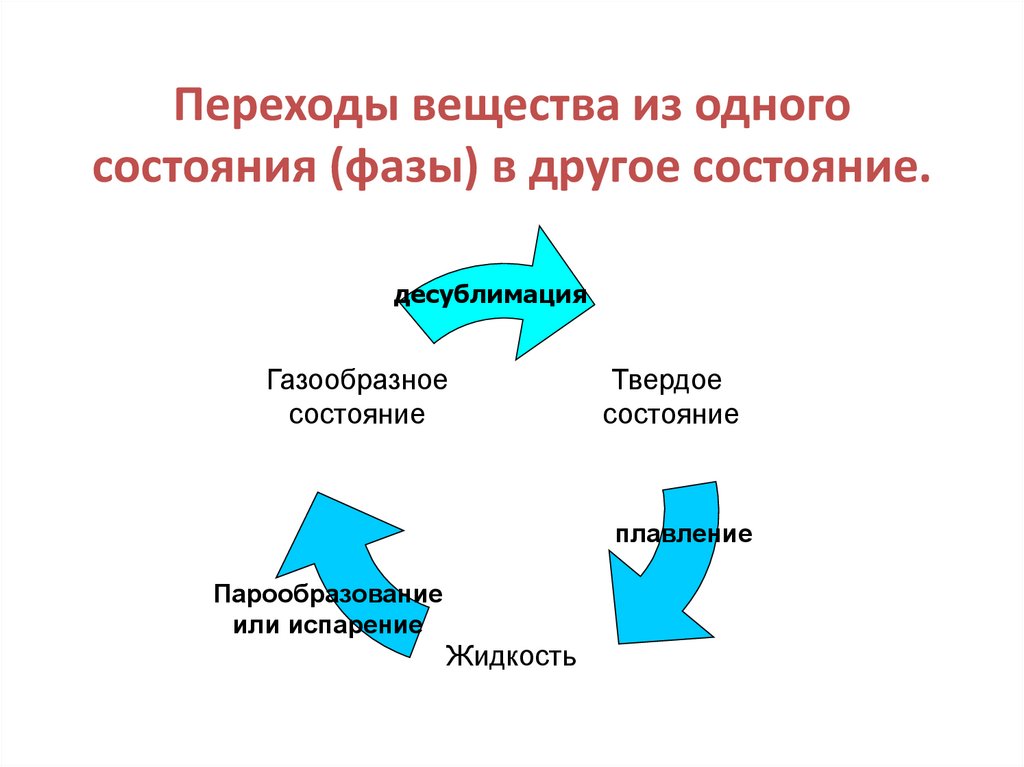
23. Переходы вещества из одного состояния (фазы) в другое состояние.
десублимацияГазообразное
состояние
Твердое
состояние
плавление
Парообразование
или испарение
Жидкость
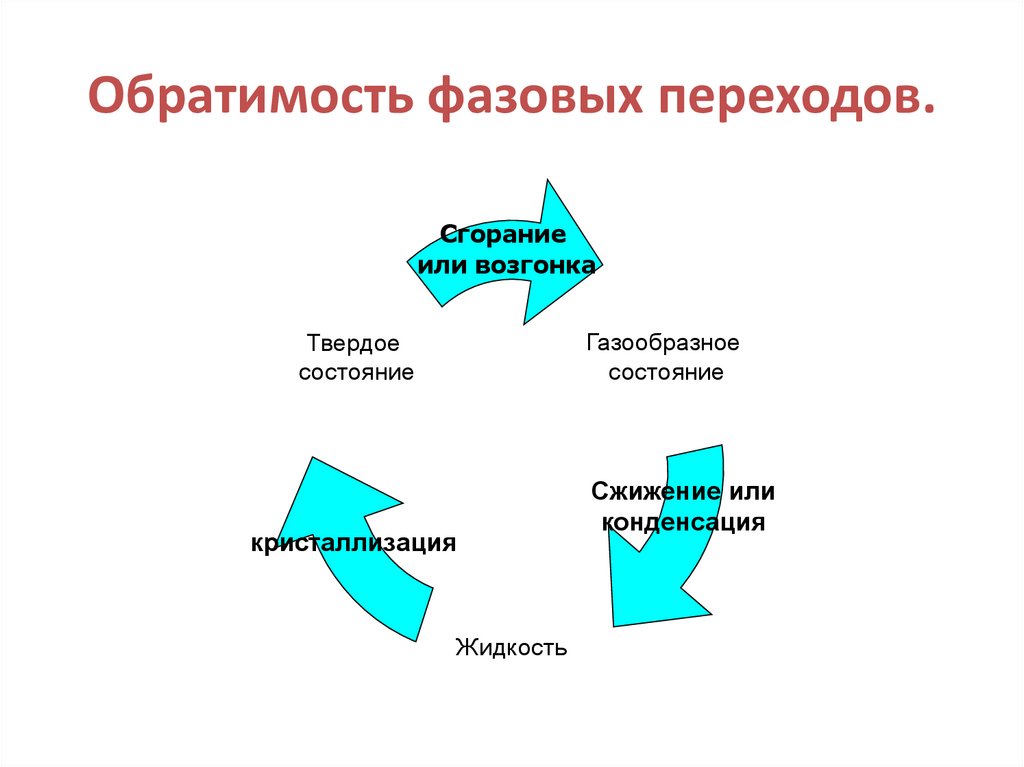
24. Обратимость фазовых переходов.
Сгораниеили возгонка
Газообразное
состояние
Твердое
состояние
кристаллизация
Жидкость
Сжижение или
конденсация
25. Количество теплоты фазовых переходов первого рода (Q>0), второго рода (Q<0).
Количество теплоты фазовыхпереходов первого рода (Q>0),
второго рода (Q<0).
26.
Q m27.
Q rm28.
Q qm29. Уравнение теплового баланса.
Если тела участвуют только в процессетеплообмена:
Q Q .... 0
1 2















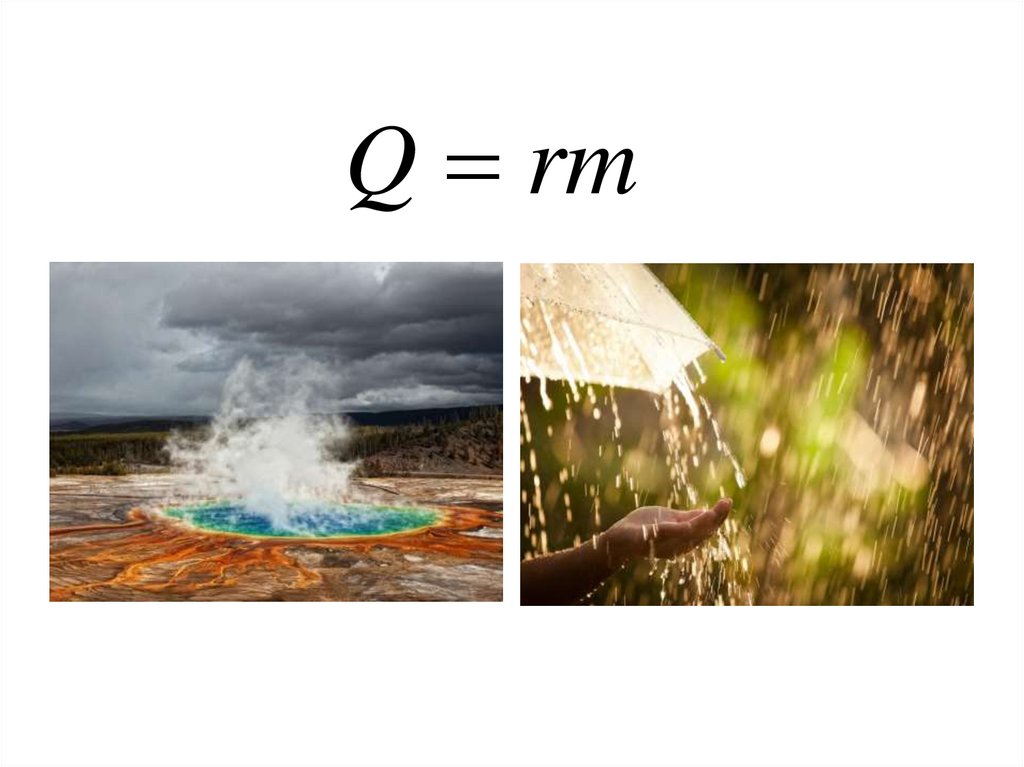



 Физика
Физика