Похожие презентации:
Основные положения МКТ. Термодинамические параметры
1.
2.
Демокрит считал, чтосуществуют только атомы
и пустота. Атомы — неделимые
материальные элементы,
вечные, неразрушимые,
непроницаемые, отличаются
формой.
Демокрит
460–370 гг. до н.э.
3.
Лукреций Кар99–55 гг. до н.э.
Эпикур
342–271 гг. до н.э.
Учения Демокрита
поддерживали Лукреций
Кар и Эпикур. Все эти
учёные жили до нашей
эры. В 1026 году
во Франции было
запрещено атомистическое
учение.
4.
Причины зарождениямолекулярно-кинетической теории
В классической механике
изучалось механическое
движение.
5.
Изменение температуры телспособно изменить его
до неузнаваемости. Данные
изменения связаны с движением
и взаимодействием частиц,
составляющих тело.
6.
Молекулярно-кинетическая теория (МКТ) занимаетсяизучением свойств веществ, основываясь при этом
на представлениях о частицах вещества.
7.
Цель молекулярно-кинетической теории —объяснение свойств макроскопических тел
и тепловых процессов, протекающих в них.
8.
Основные положениямолекулярно-кинетической теории
Вещество
Молекула
Атом
Все вещества состоят из частиц — молекул, атомов и ионов.
9.
Основные положениямолекулярно-кинетической теории
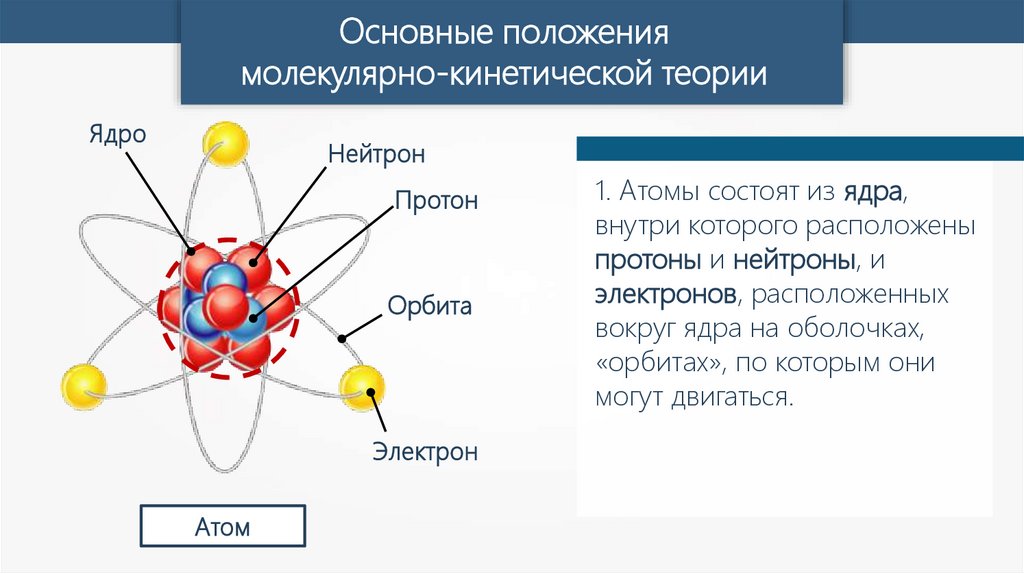
Ядро
Нейтрон
Протон
Орбита
Электрон
Атом
1. Атомы состоят из ядра,
внутри которого расположены
протоны и нейтроны, и
электронов, расположенных
вокруг ядра на оболочках,
«орбитах», по которым они
могут двигаться.
10.
Основные положениямолекулярно-кинетической теории
2. Частицы вещества
беспрерывно и беспорядочно
движутся.
11.
Основные положениямолекулярно-кинетической теории
3. Частицы вещества
взаимодействуют друг с другом.
12.
Беспорядочное (хаотичное)движение атомов и молекул
в веществе называют
тепловым движением,
потому что скорость
движения частиц
увеличивается с ростом
температуры.
13.
Справедливостьмолекулярно-кинетической теории
Оценка размеров молекул,
наличие у веществ
проницаемости,
растворимости, сжимаемости.
14.
Справедливостьмолекулярно-кинетической теории
Наличие прочности,
упругости, смачивания,
прилипания.
15.
АтомМолекула
Все вещества и тела в природе состоят из атомов
и молекул — групп атомов.
16.
17.
18.
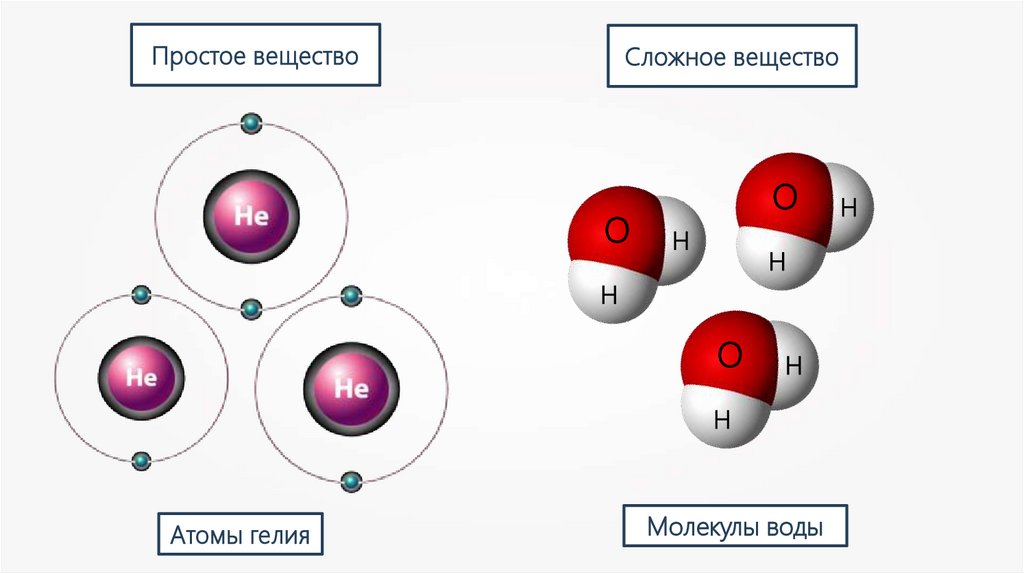
Простое веществоСложное вещество
O
O
H
H
H
O
H
H
Атомы гелия
Молекулы воды
H
19.
Что такое ионы?Ионы соли NaCl
20.
Ионы — атомы, имеющиеизбыток или недостаток
электронов.
Ионы
Атом
Положительные
Отрицательные
21.
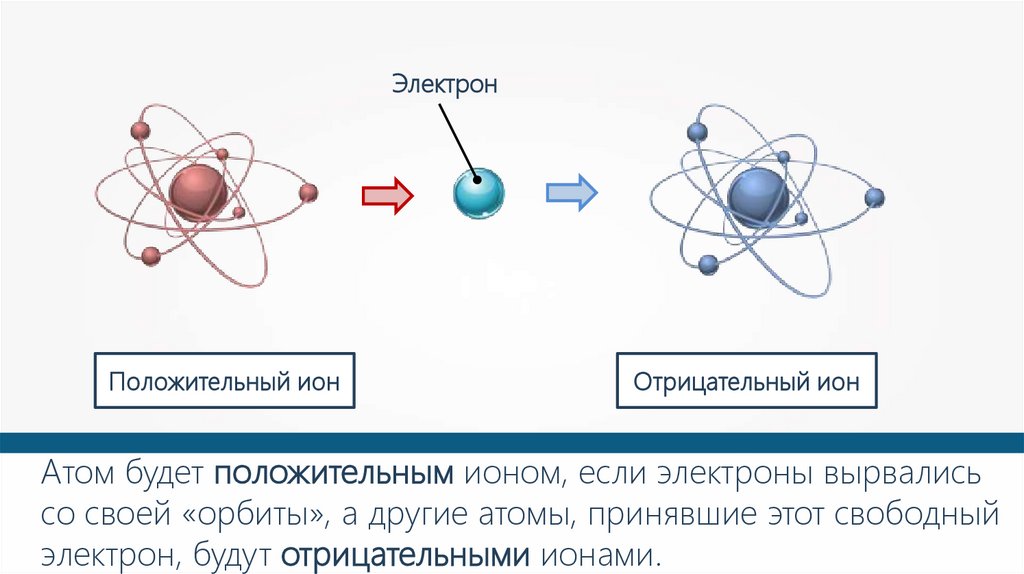
ЭлектронПоложительный ион
Отрицательный ион
Атом будет положительным ионом, если электроны вырвались
со своей «орбиты», а другие атомы, принявшие этот свободный
электрон, будут отрицательными ионами.
22.
Силы взаимодействия междумолекулами
Частицы вещества
беспрерывно и беспорядочно
движутся и взаимодействуют
друг с другом.
Greg L
23.
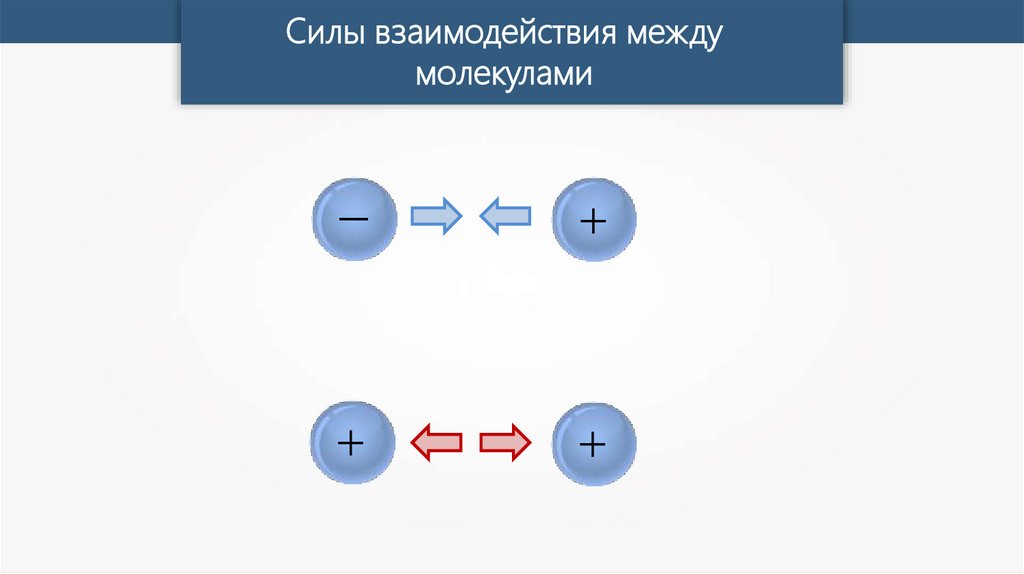
Силы взаимодействия междумолекулами
–
+
+
+
24.
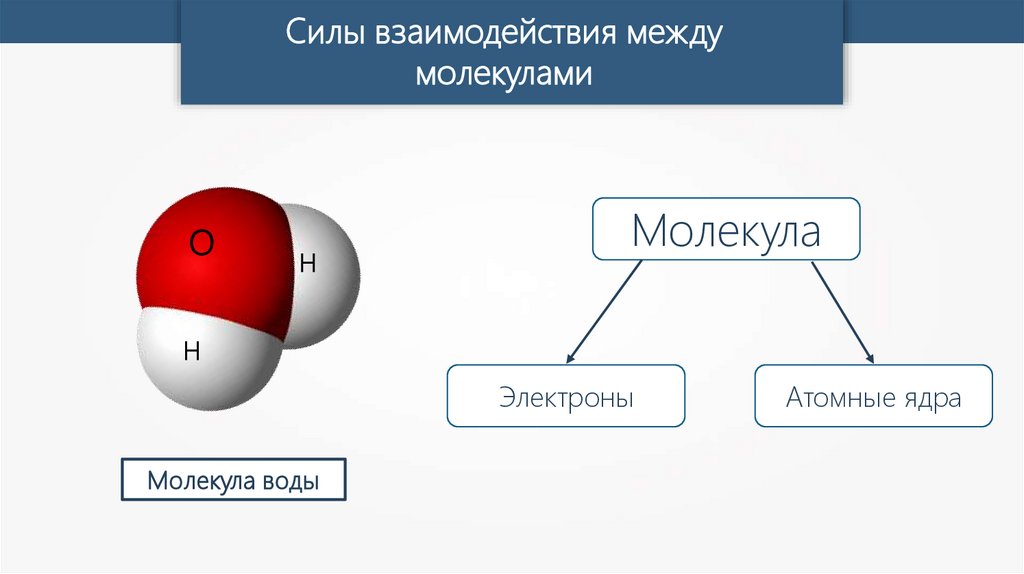
Силы взаимодействия междумолекулами
O
H
Молекула
H
Электроны
Молекула воды
Атомные ядра
25.
OO
H
H
H
H
d1
r
d2
Если молекулы находятся на расстояниях, превышающих
их размеры в несколько раз, то силы взаимодействия
практически не сказываются.
26.
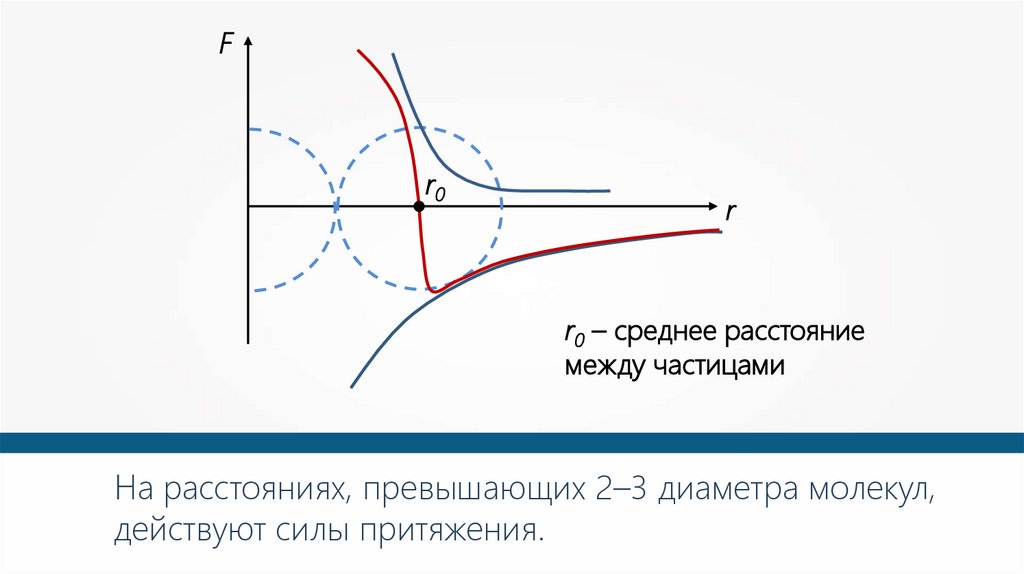
Fr0
r
r0 – среднее расстояние
между частицами
На расстояниях, превышающих 2–3 диаметра молекул,
действуют силы притяжения.
27.
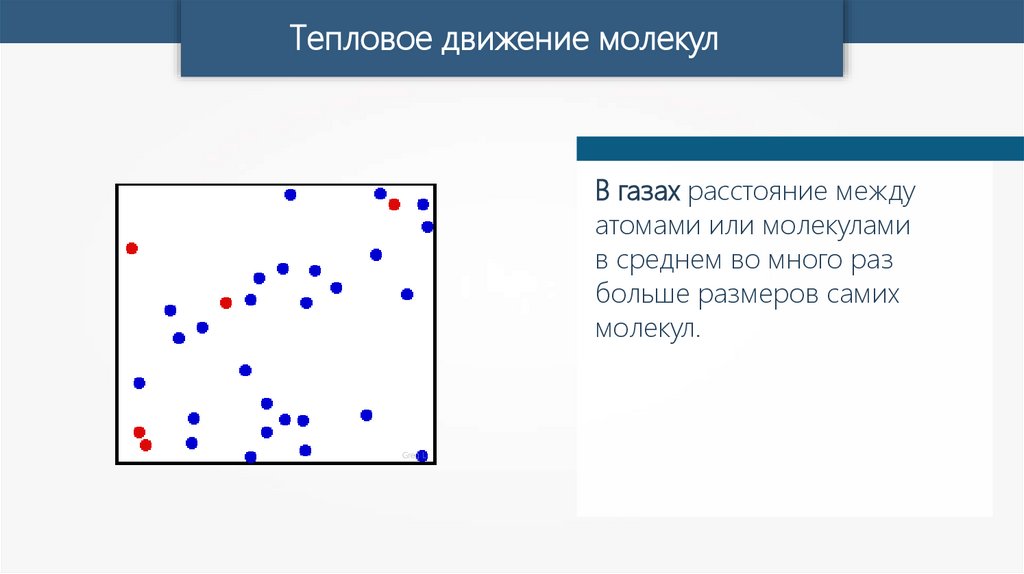
Тепловое движение молекулВ газах расстояние между
атомами или молекулами
в среднем во много раз
больше размеров самих
молекул.
Greg L
28.
Тепловое движение молекулГаз
При больших расстояниях
между молекулами силы
притяжения малы и
не способны удержать
молекулы газа друг возле
друга. Поэтому газы могут
неограниченно расширяться.
29.
Тепловое движение молекулГаз
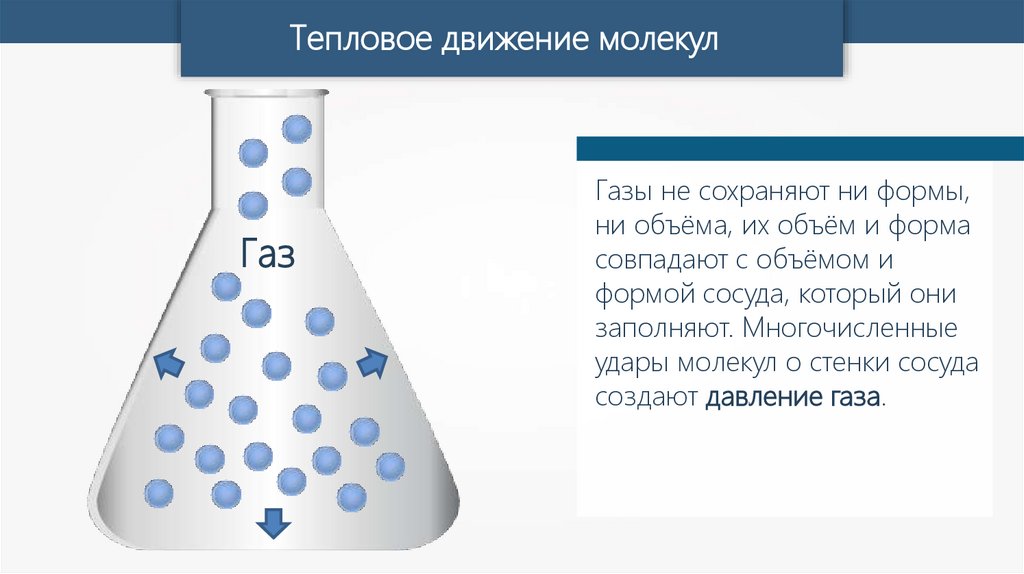
Газы не сохраняют ни формы,
ни объёма, их объём и форма
совпадают с объёмом и
формой сосуда, который они
заполняют. Многочисленные
удары молекул о стенки сосуда
создают давление газа.
30.
Тепловое движение молекулМолекулы жидкости
расположены почти вплотную
друг к другу. Поэтому
жидкости очень плохо
сжимаются и сохраняют свой
объём.
31.
Тепловое движение молекулO
H
H
O
H
H
O
O
H
H
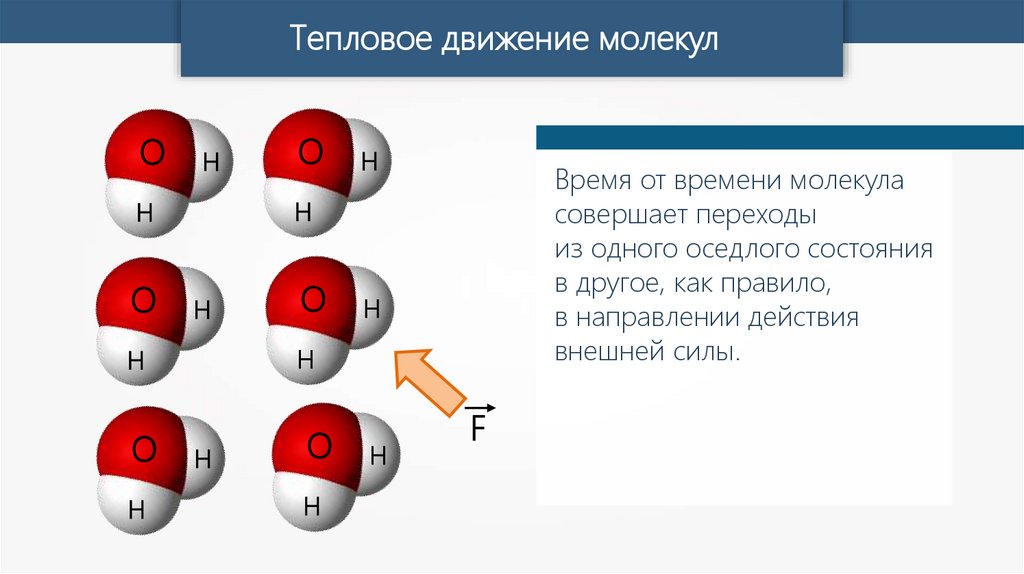
Время от времени молекула
совершает переходы
из одного оседлого состояния
в другое, как правило,
в направлении действия
внешней силы.
H
H
O
O
H
H
H
H
F
32.
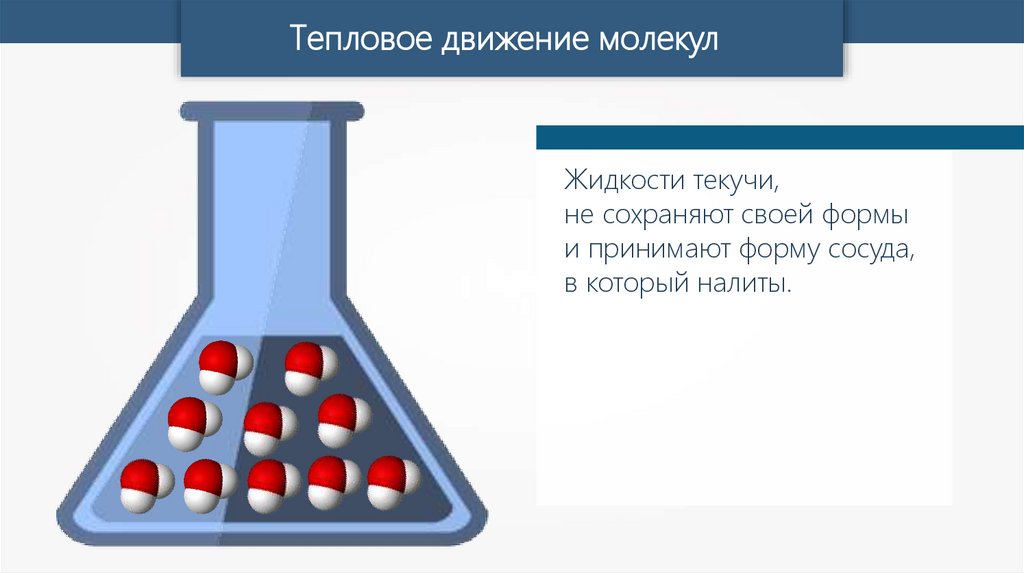
Тепловое движение молекулЖидкости текучи,
не сохраняют своей формы
и принимают форму сосуда,
в который налиты.
33.
Тепловое движение молекулТеория жидкого состояния
вещества впервые была
разработана крупным
советским физикомтеоретиком Яковом
Ильичом Френкелем.
Яков Ильич
Френкель
1894–1952 гг.
34.
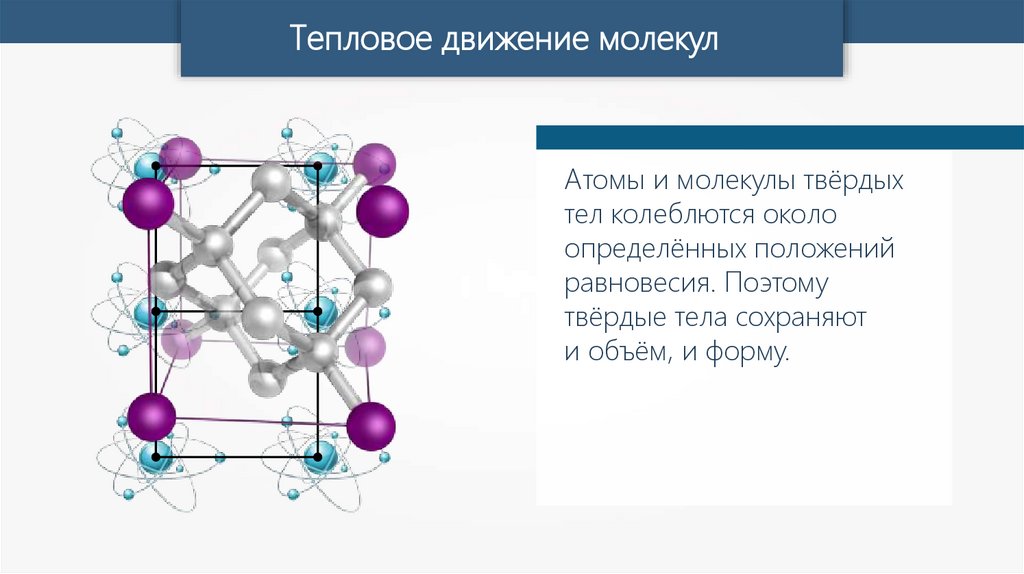
Тепловое движение молекулАтомы и молекулы твёрдых
тел колеблются около
определённых положений
равновесия. Поэтому
твёрдые тела сохраняют
и объём, и форму.
35.
Greg LБроуновское движение — это тепловое
движение мельчайших частиц, взвешенных
в жидкости или газе.
36.
Броуновское движение частицбыло открыто английским
ботаником Броуном в 1827 г.
и явилось наглядным
доказательством хаотичного
молекулярного движения.
Роберт Броун
1773–1858 гг.
37.
Броуновские частицы движутсяпод влиянием ударов молекул.
Из-за хаотичности теплового
движения молекул эти удары
никогда не уравновешивают
друг друга.
Greg L
38.
Молекулярно-кинетическаятеория броуновского
движения была создана
Альбертом Эйнштейном
в 1905 году.
Альберт Эйнштейн
1879–1955 гг.
39.
Диффузия — явление самопроизвольногопроникновения частиц одного вещества
в другое вещество.
40.
Диффузией также называетсяпроцесс самопроизвольного
выравнивания концентраций
молекул жидкости или газа
в различных частях объёма.
41.
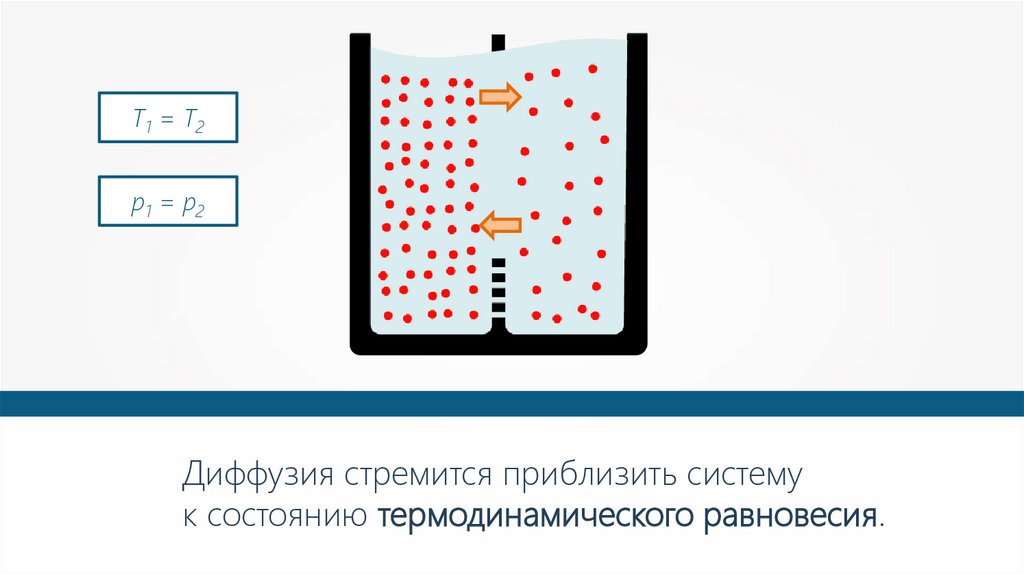
T1 = T2p1 = p2
Диффузия стремится приблизить систему
к состоянию термодинамического равновесия.
42.
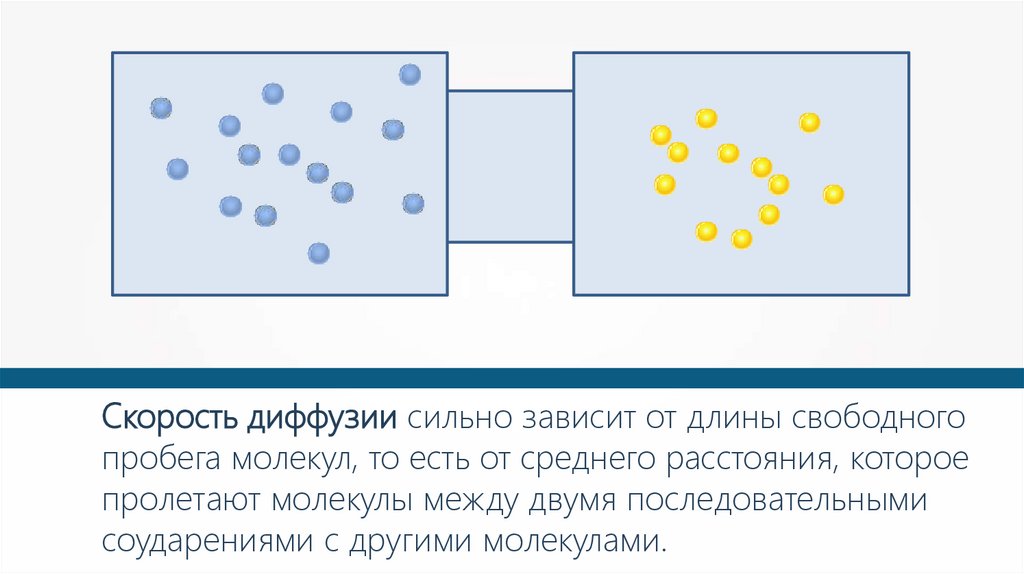
Скорость диффузии сильно зависит от длины свободногопробега молекул, то есть от среднего расстояния, которое
пролетают молекулы между двумя последовательными
соударениями с другими молекулами.
43.
ДиффузияВ твёрдых телах
В газах
В жидкостях
44.
ДиффузияВ твёрдых телах
В газах
В жидкостях
Диффузия газов происходит очень быстро.
45.
ДиффузияВ твёрдых телах
В газах
В жидкостях
Диффузия твёрдых тел происходит очень медленно.
46.
Чем выше температура, темдиффузия происходит быстрее.
47.
48.
49.
50.
51.
52.
2. Какова средняя кинетическая энергия атома аргона, еслитемпература газа 17 °С?

































 Физика
Физика








