Похожие презентации:
Парообразование и конденсация. Уроки физики в 8 классе
1.
Уроки физики в 8 классе1
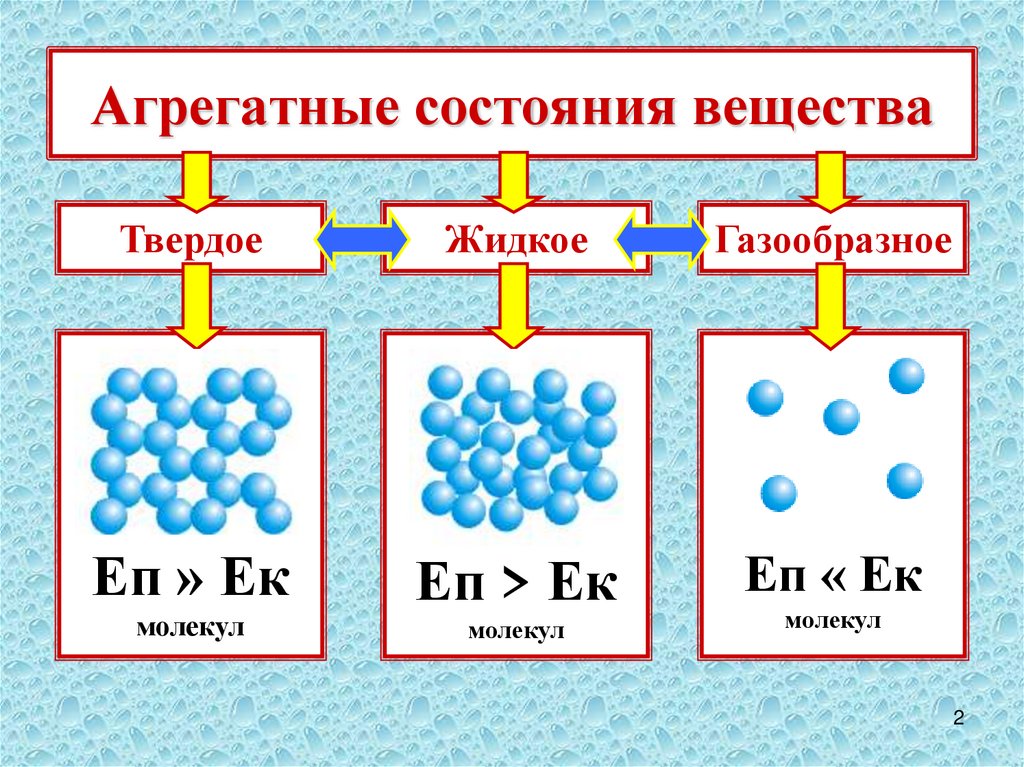
2. Агрегатные состояния вещества
ТвердоеЖидкое
Газообразное
Еп » Ек
Еп > Ек
Еп « Ек
молекул
молекул
молекул
2
3.
Парообразование – переход веществаиз жидкого состояния в газообразное
Жидкость
получает энергию
парообразование
Внутренняя
энергия пара
больше,
чем жидкости
1. Как изменяется внутренняя энергия вещества при
парообразовании?
2. Как изменяется характер движения молекул и их
расположение?
3. Как изменяется энергия молекул?
4. Изменяются ли молекулы вещества при парообразовании?
5. Как изменяется температура и энергия вещества при
парообразовании?
3
4.
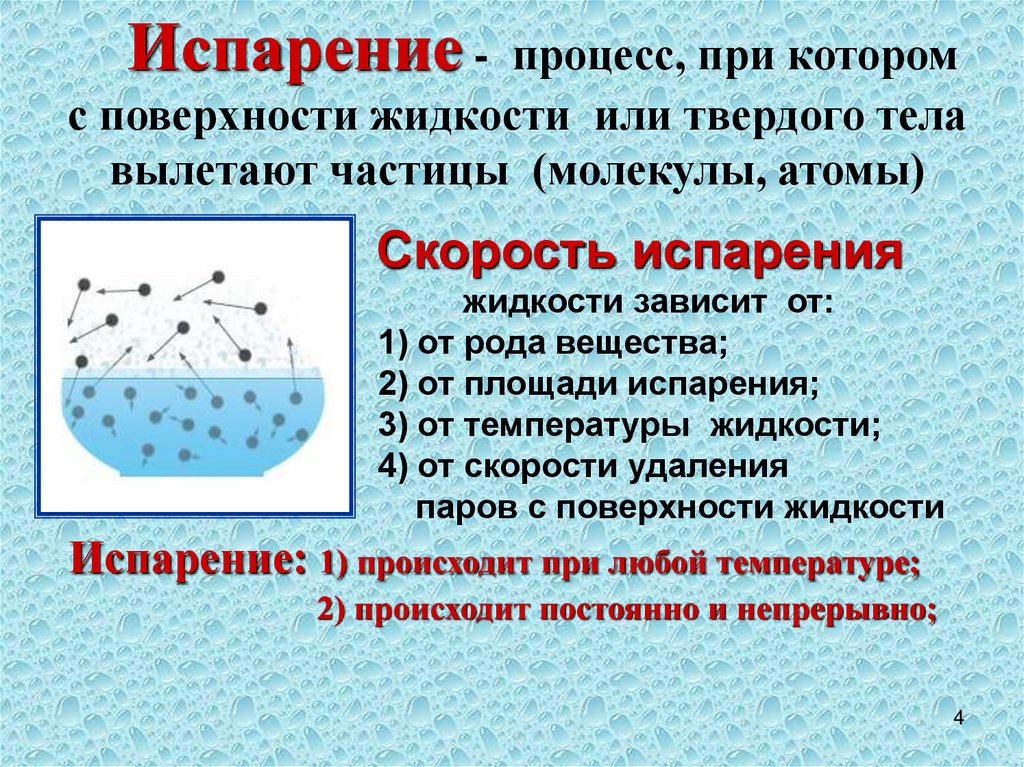
Испарение - процесс, при которомс поверхности жидкости или твердого тела
вылетают частицы (молекулы, атомы)
Скорость испарения
жидкости зависит от:
1) от рода вещества;
2) от площади испарения;
3) от температуры жидкости;
4) от скорости удаления
паров с поверхности жидкости
Испарение: 1) происходит при любой температуре;
2) происходит постоянно и непрерывно;
4
5.
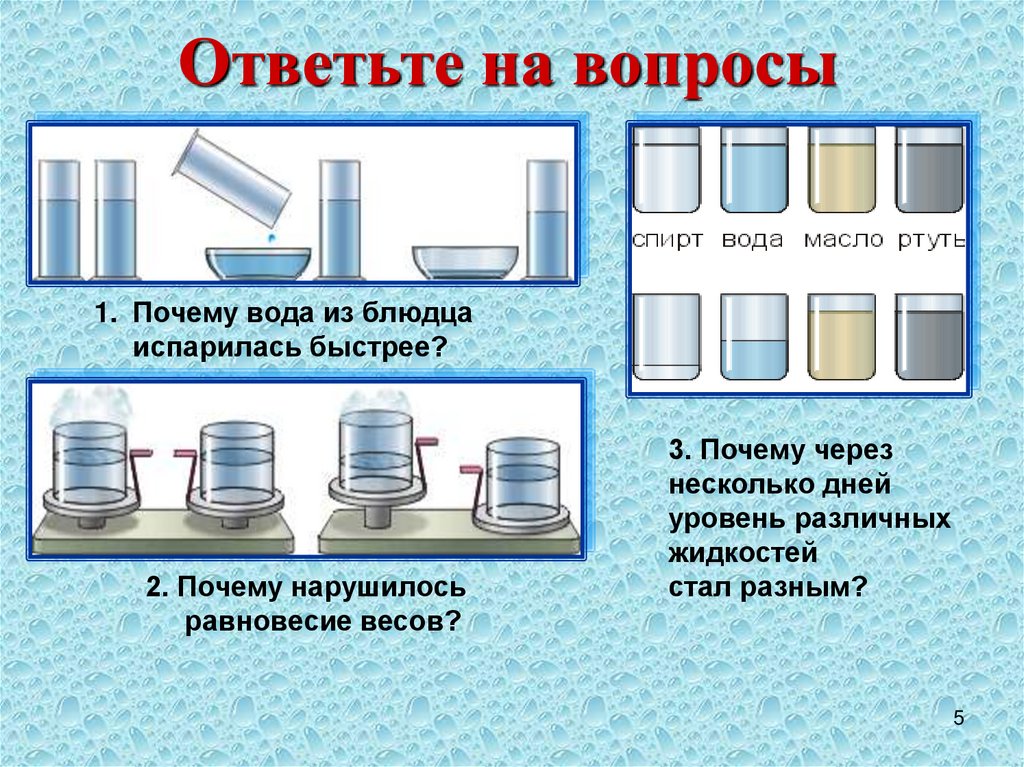
Ответьте на вопросы1. Почему вода из блюдца
испарилась быстрее?
2. Почему нарушилось
равновесие весов?
3. Почему через
несколько дней
уровень различных
жидкостей
стал разным?
5
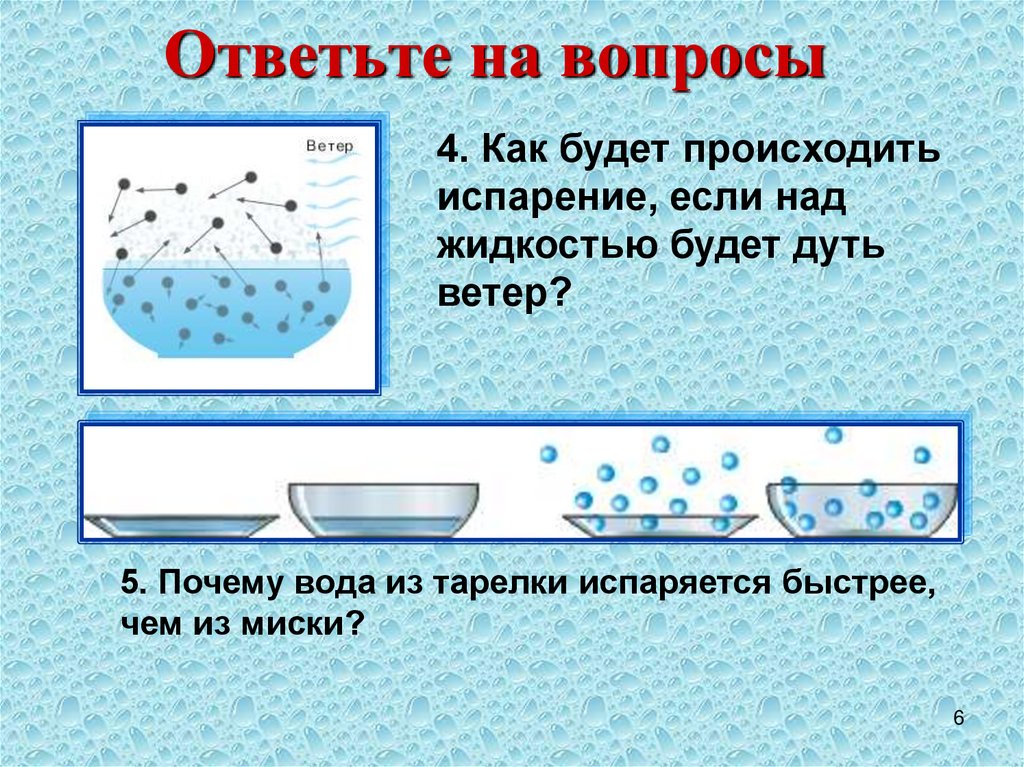
6. Ответьте на вопросы
4. Как будет происходитьиспарение, если над
жидкостью будет дуть
ветер?
5. Почему вода из тарелки испаряется быстрее,
чем из миски?
6
7. насыщенный
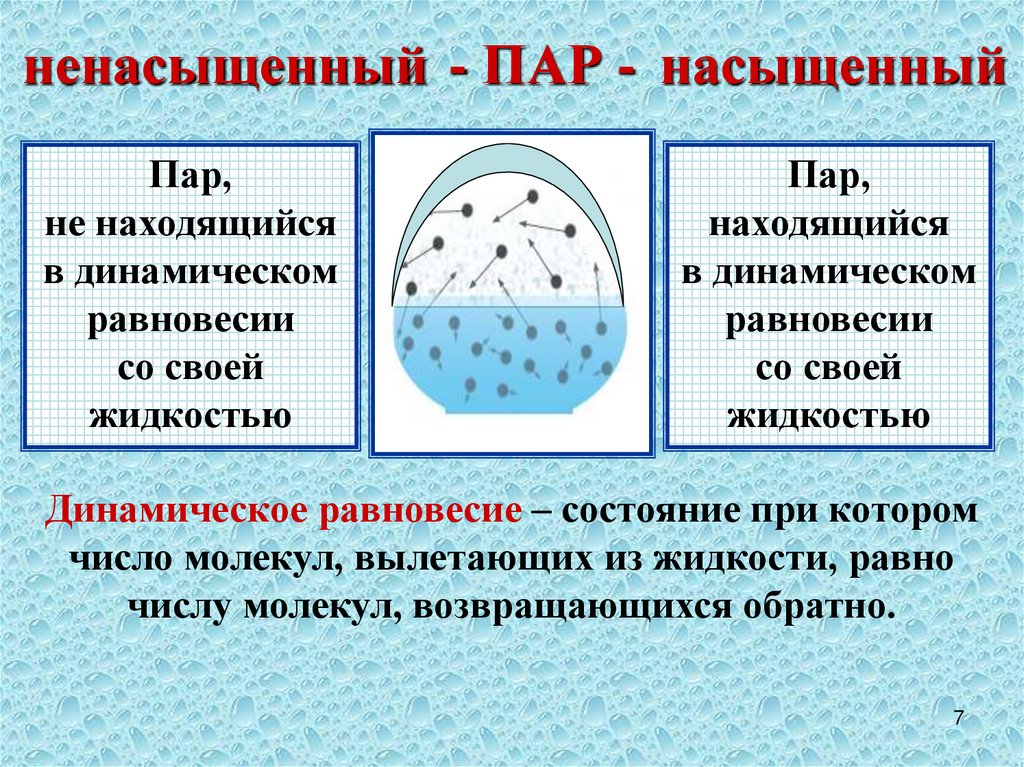
ненасыщенный - ПАР - насыщенныйПар,
не находящийся
в динамическом
равновесии
со своей
жидкостью
Пар,
находящийся
в динамическом
равновесии
со своей
жидкостью
Динамическое равновесие – состояние при котором
число молекул, вылетающих из жидкости, равно
числу молекул, возвращающихся обратно.
7
8.
Кипение1. Кипение – это интенсивное парообразование,
происходящее одновременно внутри
и с поверхности жидкости.
2. Кипение - это процесс, при котором жидкость
переходит в пар при определенной
и постоянной для каждой жидкости
температуре и не только с поверхности,
но и по всему объему жидкости.
3. Кипение происходит с поглощением теплоты.
4. С изменением атмосферного давления
изменяется и температура кипения: при
повышении давления температура кипения
повышается.
8
9. Механизм кипения воды
1. При нагревании испарение с поверхностиводы усиливается.
2. Появление в жидкости многочисленных
мелких пузырьков воздуха, растворённого
в воде. При нагревании излишек воздуха
выделяется в виде пузырьков
с насыщенным водяным паром - испарение
внутрь жидкости.
3. Пузырьки становятся крупнее
и многочисленнее.
4. Архимедова сила, действующая
на пузырьки, возрастает и при температуре
близкой к кипению они всплывают.
5. С приближением к поверхности объём
пузырьков резко возрастает, на поверхности
они лопаются, находящийся в них
насыщенный пар выходит в атмосферу –
слышен характерный шум – вода кипит.
9
10. Температура кипения некоторых веществ
Водород -253 °СКислород -183 °С
Вода
100 °С
Молоко
100 °С
Свинец
1 740 °С
Железо
2 750 °С
11.
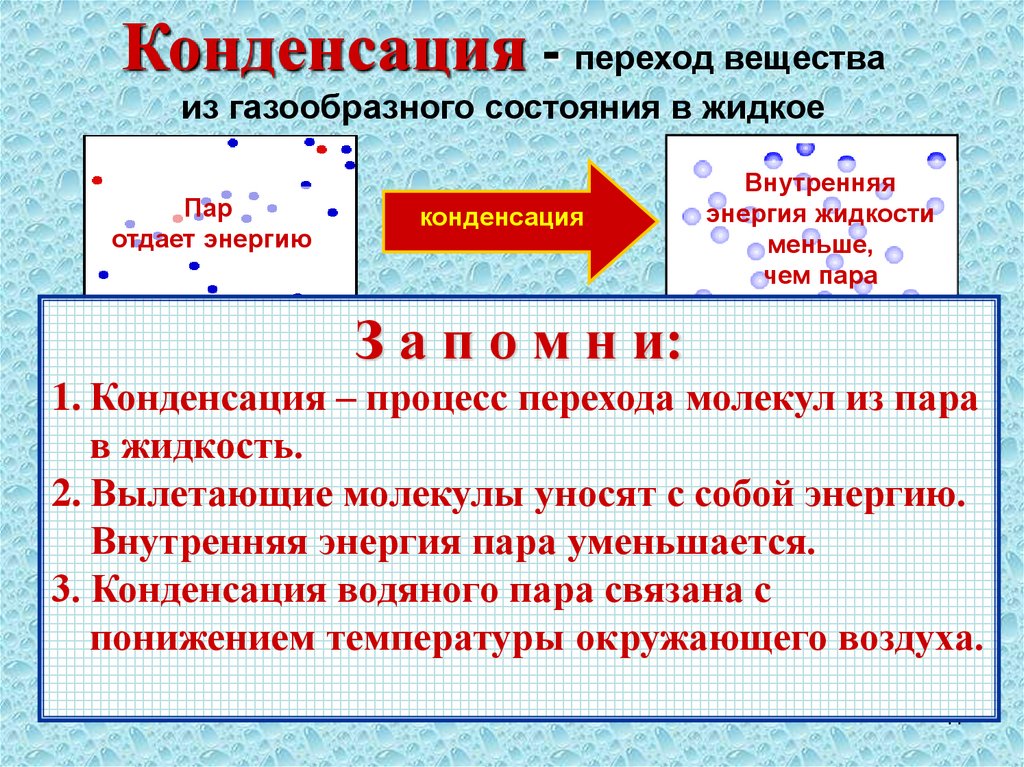
Конденсация - переход веществаиз газообразного состояния в жидкое
Пар
отдает энергию
конденсация
Внутренняя
энергия жидкости
меньше,
чем пара
З а п о м н и:
1. Как изменяется внутренняя энергия вещества при
1.конденсации?
Конденсация – процесс перехода молекул из пара
2. Как
изменяется характер движения молекул и их
в жидкость.
2.расположение?
Вылетающие молекулы уносят с собой энергию.
3. Как изменяется энергия молекул?
Внутренняя энергия пара уменьшается.
4. Изменяются ли молекулы вещества при конденсации?
3.Сравните
Конденсация
водяного
паратвердого
связанатела
с и жидкости
5.
внутреннюю
энергию
понижением температуры окружающего воздуха.
11
12. Удельная теплота парообразования L – количество теплоты, необходимое для того чтобы полностью превратить в пар 1 кг жидкости
Если идет процесс парообразования, то жидкоститребуется сообщить некоторое количество
теплоты, а если пар превращается в жидкость,
то количество теплоты выделяется.
Удельная теплота парообразования L –
количество теплоты, необходимое для того чтобы
полностью превратить в пар 1 кг жидкости
взятой при температуре кипения (стр.49).
Количество теплоты, необходимое для
парообразования и выделяющееся при конденсации,
определяется по формуле:
Q =+- L · m
12
13.
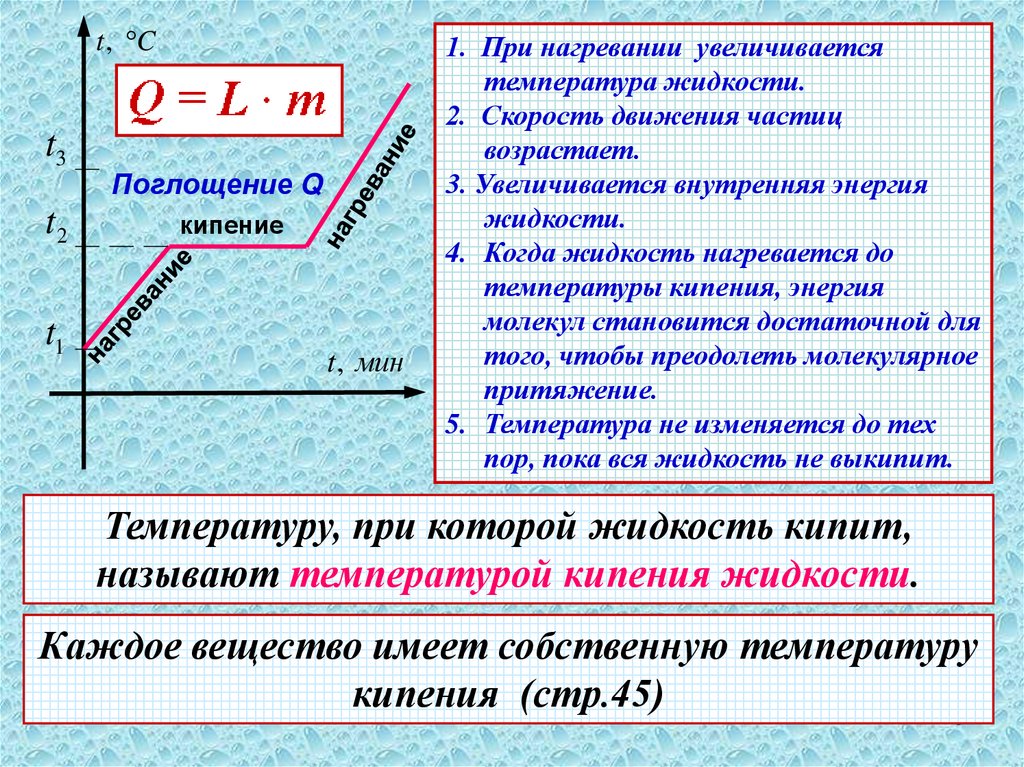
t , Ct3
t2
t1
Поглощение Q
кипение
t , мин
1. При нагревании увеличивается
температура жидкости.
2. Скорость движения частиц
возрастает.
3. Увеличивается внутренняя энергия
жидкости.
4. Когда жидкость нагревается до
температуры кипения, энергия
молекул становится достаточной для
того, чтобы преодолеть молекулярное
притяжение.
5. Температура не изменяется до тех
пор, пока вся жидкость не выкипит.
Температуру, при которой жидкость кипит,
называют температурой кипения жидкости.
Каждое вещество имеет собственную температуру
кипения (стр.45)
13
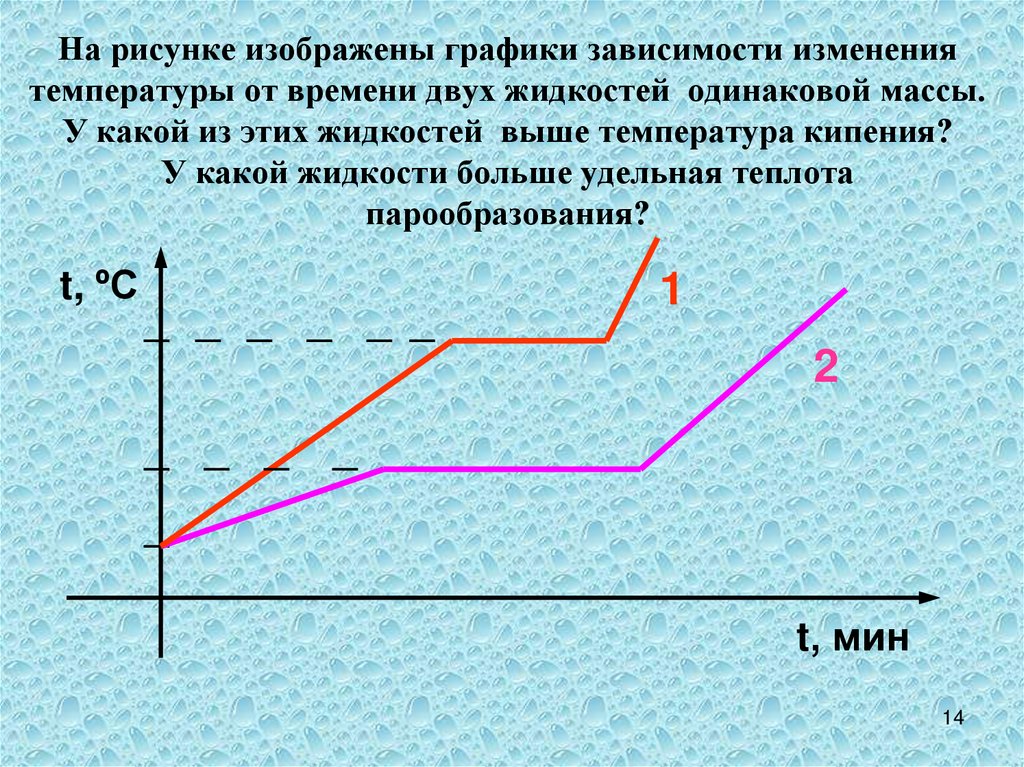
14. На рисунке изображены графики зависимости изменения температуры от времени двух жидкостей одинаковой массы. У какой из этих
жидкостей выше температура кипения?У какой жидкости больше удельная теплота
парообразования?
t, ºC
1
2
t, мин
14
15.
t , C1. При охлаждении уменьшается
температура пара, скорость
t3
движения его частиц, его
внутренняя энергия
2. Когда пар охлаждается до
Выделение Q
t2
температуры конденсации,
конденсация
энергия молекул уменьшается до
такой степени, что они
t1
сближаются на расстояние, на
котором действуют силы
молекулярного притяжения.
t кипения = t конденсации t , мин
Температуру, при которой вещество конденсируется,
называют температурой конденсации.
Количество теплоты, выделяющееся при
конденсации равно количеству теплоты,
поглощённому при кипении.
15
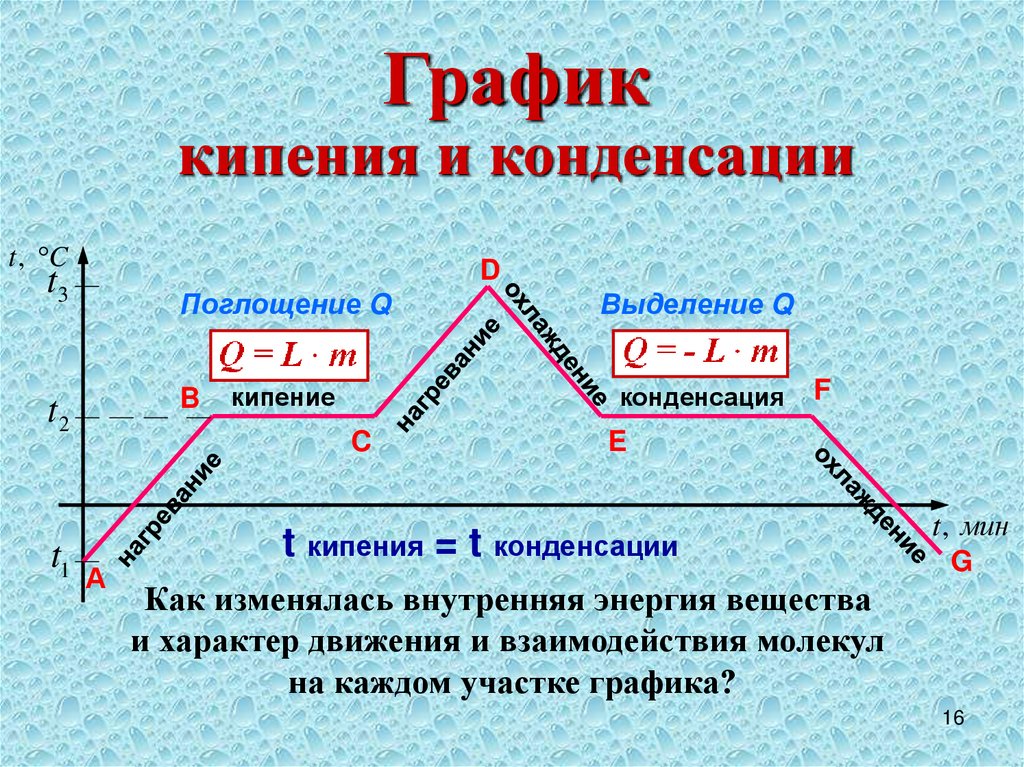
16.
Графиккипения и конденсации
t , C
D
t3
Выделение Q
кипение
конденсация
B
t2
t1
Поглощение Q
C
А
F
E
t кипения = t конденсации
t , мин
G
Как изменялась внутренняя энергия вещества
и характер движения и взаимодействия молекул
на каждом участке графика?
16
17. Домашнее задание
§ 16, 17, 18, 20, читать,отвечать на вопросы; упр.9
Спасибо за работу!
Желаю успехов!
17








 Физика
Физика








