Похожие презентации:
Закон термодинамики и его применение к изопроцессам
1.
ТЕРМОДИНАМИКА1 ЗАКОН ТЕРМОДИНАМИКИ И ЕГО ПРИМЕНЕНИЕ К ИЗОПРОЦЕССАМ
2.
Термодинамика – раздел физики,изучающий тела, находящиеся в состоянии
термодинамического равновесия и
явления, сопровождающие переходы
между этими состояниями.
В термодинамике изучаются
состояния и процессы, для описания
которых можно ввести понятие
температуры.
T [K] = t [ C] + 273.15
3.
Внутренняя энергия идеального газаВнутренняя энергия идеального газа — в идеальных газах внутренняя
энергия определяется как сумма кинетических энергий молекул.
Между молекулами идеального газа отсутствуют силы притяжения и
потенциальная энергия взаимодействия равна нулю.
[U]=[Дж]
U зависит от T, M, m
Внутренняя энергия идеального одноатомного
газа рассчитывается по формулам:
v - кол-во вещества [моль]
М - малярная масса [кг/моль]
m - масса вещества [кг]
V - объем [м^3]
R - универсальная газовая
постоянная [Дж/моль*к]
T - температура [К]
4.
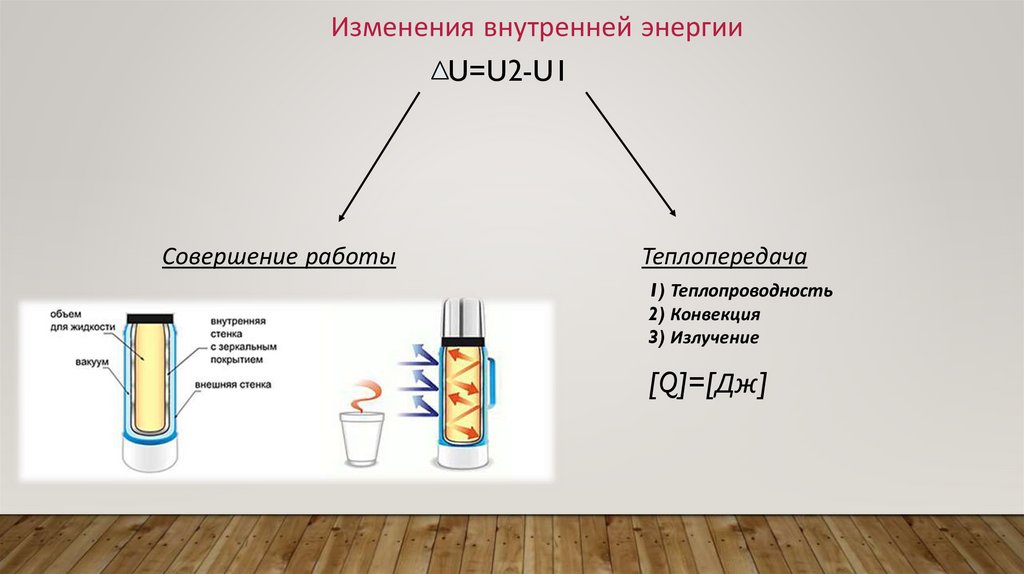
Изменения внутренней энергииU=U2-U1
Совершение работы
Теплопередача
1) Теплопроводность
2) Конвекция
3) Излучение
[Q]=[Дж]
5.
Работа в термодинамикеПри совершении работы в термодинамике меняется состояние макроскопических тел: их объем и
температура.
A’ - работа газа. Происходит расширение
за счет получения тепла.
A - работа над газом. Происходит
сжатие за счет отдачи тепла.
[A]=[Дж]
ΔU > 0 при ΔT > 0; ΔU < 0 при ΔT < 0;
A' > 0 при ΔV > 0; A' < 0 при ΔV < 0;
A > 0 при ΔV < 0; A < 0 при ΔV > 0;
Q > 0 при получении тепла; Q < 0 при потере тепла
A газа = -A над газом
A = P(V2 - V1) = P V = vR T
6.
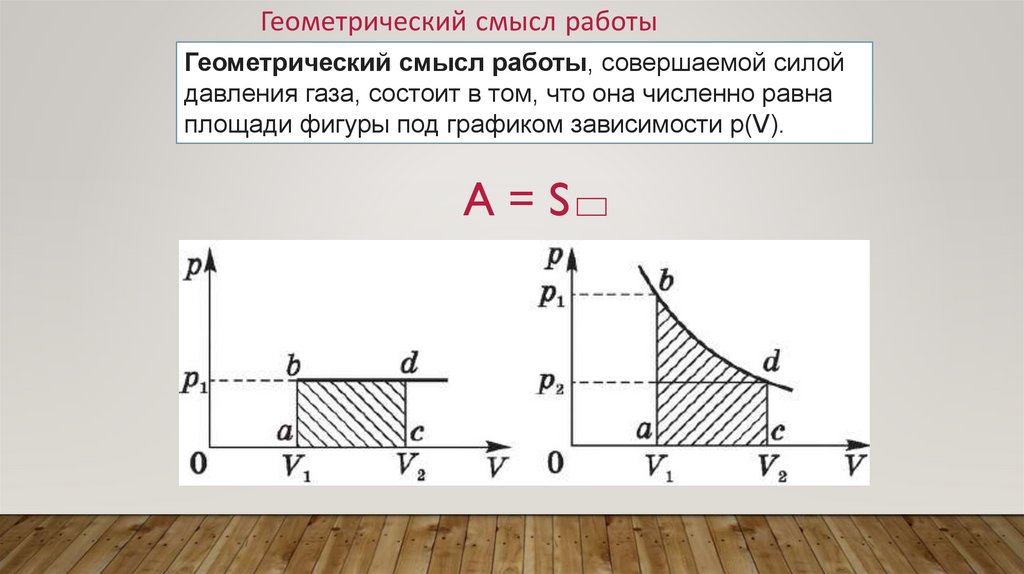
Геометрический смысл работыГеометрический смысл работы, совершаемой силой
давления газа, состоит в том, что она численно равна
площади фигуры под графиком зависимости p(V).
A=S
7.
I Закон термодинамикиВ изолированной термодинамической
системе сумма всех видов энергии является
величиной постоянной.
8.
Применение I закона термодинамики кизопроцессам
(В адиабатном процессе нет обмена тепла со средой)
9.
Задача 1На сколько изменяется внутренняя энергия
гелия массой 200 г при увеличении
температуры на 20 °С?
10.
Дано:Решение:
11.
Задача 2В двух цилиндрах под подвижным поршнем
находятся водород и кислород. Сравнить
работы, которые совершают эти газы при
изобарном нагревании, если их массы, а также
начальные и конечные температуры равны.
12.
Дано:Решение:
13.
Задача 3Для изобарного нагревания газа, количество
вещества которого 800 моль, на 500 К ему
сообщили количество теплоты 9,4 МДж.
Определить работу газа и приращение его
внутренней энергии.
14.
Дано:Решение:
15.
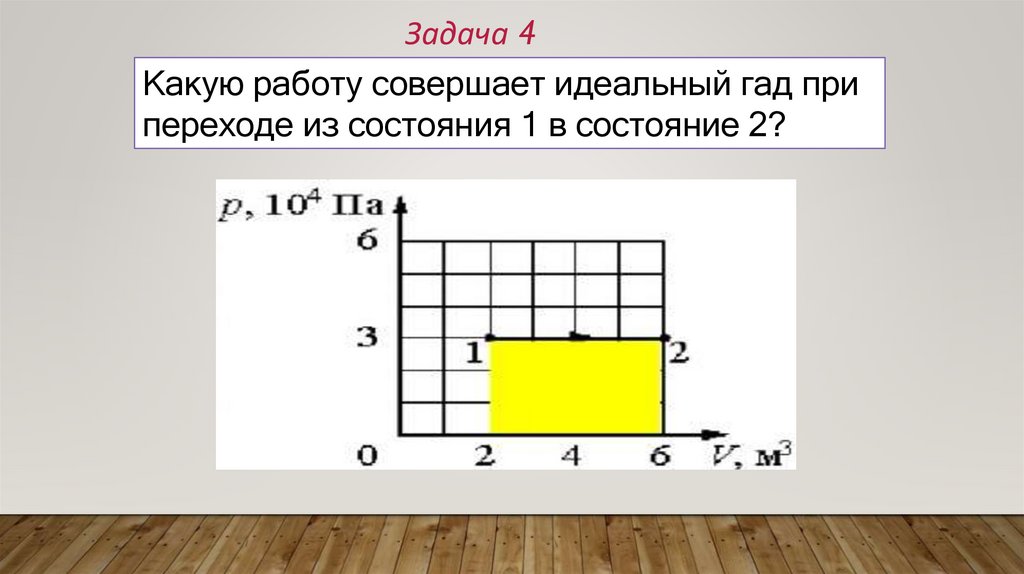
Задача 4Какую работу совершает идеальный гад при
переходе из состояния 1 в состояние 2?
16.
Решение:A=P(V2-V1)=3*10^4(6-2)=120кДж
17.
Задача 5Удельная теплоемкость азота, когда его нагревают при
постоянном давлении, равна 1,05 кДж/(кг • К), а при
постоянном объеме — 0,75 кДж/(кг⋅К). Почему эти величины
имеют разные значения? Какая совершается работа при
изобарном нагревании азота массой 1 кг на 1 К?
18.
Дано:Решение:















 Физика
Физика








