Похожие презентации:
Природные полимеры и перспективы их применения
1. ПРИРОДНЫЕ ПОЛИМЕРЫ и перспективы их применения
Уфимский государственныйнефтяной технический университет
д.т.н. Тептерева Галина Алексеевна
2.
ПРИРОДНЫЕ ПОЛИМЕРЫи перспективы их
применения
Уфимский государственный
нефтяной технический
университет, проф.
Кафедры ОАПХ , д.т.н.
Тептерева Галина
Алексеевна
3.
4.
История возникновения «Зеленойхимии»
Зеленая химия возникла после издания в США Акта о
предотвращении загрязнений, хотя к ранним предпосылкам
ее возникновения можно отнести движение, направленное
на ресурсо- и энергосбережение, которое было популярным
в СССР и других странах с момента развития
промышленности.
Основная цель «Зеленой химии»
Основная цель зеленой химии – поиск безопасных с точки
зрения химии и экологии способов деятельности общества
во всех аспектах – начиная от процессов производства и
способов использования энергоресурсов и до способов
выполнения нашей ежедневной домашней работы.
5. Основные направления развития «Зеленой химии» на современном этапе
Пути, по которым уже сейчас движетсязелёная химия, можно сгруппировать в три
большие направления:
1) новые пути синтеза (часто это реакции
с применением катализатора);
2) возобновляемые исходные реагенты
(то есть полученные не из нефти);
3) замена традиционных органических
растворителей.
6.
7. Немного о катализе
Традиционная органическая химия предполагаетмногостадийные процессы, в результате которых из исходных
веществ получаются продукты. Но схемы и механизмы реакций,
подходящие для лаборатории, совершенно не годятся для
крупнотоннажных процессов. Если на каждой стадии реакция
идёт с выходом, далеким от 100%, то при переносе на большой
масштаб вместе с нужным продуктом получаются огромные
количества ненужных веществ.
В цепочке реакций используют вспомогательные вещества,
часто после кислотной или щелочной нейтрализации образуются
неорганические соли (хлорид натрия, сульфат натрия, сульфат
аммония). Что касается потерь, то в многоступенчатых процессах
они бывают выше, чем конечный выход продукта. Эту проблему
химических и фармацевтических производств отчасти помогают
решить катализаторы, которые существенно уменьшают выход
8. Замена растворителей
Ещё одно направление зелёной химии — заменарастворителей в технологических процессах. Растворители
выполняют несколько функций: они играют роль транспорта
(разведение краски, удаление грязи) или помогают
смешивать компоненты. Также их используют для того,
чтобы доставить или убрать тепло, более эффективно
смешать реагенты или контролировать их реакционную
способность.
Абсолютное большинство растворителей, применяемых
сейчас, — это летучие органические вещества, производные
нефти. Следовательно, они во-первых, не бесконечны, вовторых, пожаро- и взрывоопасны, а в-третьих, вредны для
окружающей среды. Как от них избавиться?
9.
ВОЗМОЖНЫЕ РЕШЕНИЯПроведение химических процессов
вообще без растворителя;
можно использовать в качестве
растворителя воду, биоразлагающиеся
„зелёные“ растворители, ионные
жидкости (соли, плавящиеся при низких
температурах), сверхкритические
жидкости.
10. Новые технологии «Зеленой химии»
Обычные алкидные краски на основе нефтиобеспечивают получение долговечного
глянцевого покрытия. На них существует
большой спрос в архитектуре, промышленности
при получении изделий из металла
(сельскохозяйственных орудий, различных
конструкций). Но в технологии производства
этих красок применяются опасные органические
растворители. Сегодня разработаны технологии,
где в качестве растворителя применяют масло на
основе биологических продуктов – сахара и
растительного масла. Это позволяет получить
11.
Разработан каталитический способпроизводства бензина, дизельного или
реактивного топлива на основе возобновляемого
сырья – сахара, крахмала или целлюлозы растений.
В этом способе большую часть энергии,
требуемую для проведения процесса, получают
также из биомассы, требуется лишь
незначительная добавка энергии, полученной из
других источников.
Важным достоинством процесса является его
гибкость – целевой продукт можно изменять в
зависимости от потребностей рынка.
12.
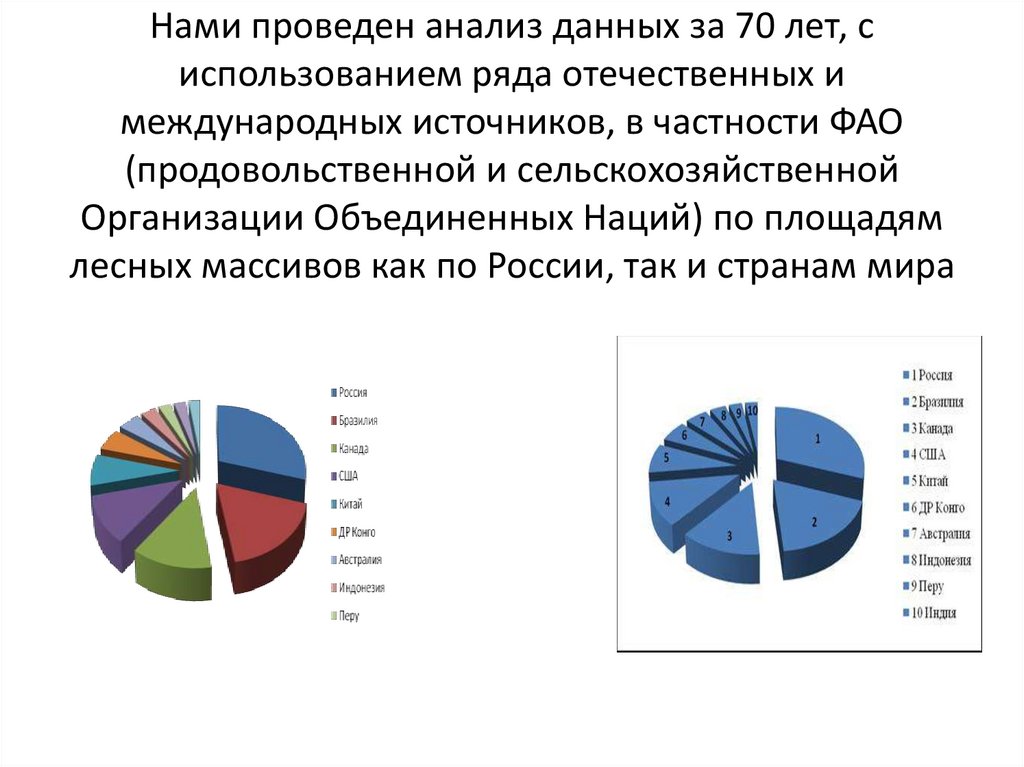
• Наиболее лесистымиявляются пять стран
мира:
• Республика Конго,
• Бразилия,
• Перу,
• Индонезия
• и Россия.
• Причем Россия не
является здесь лидером,
поскольку при
наибольшей площади
лесов, обладает и
наибольшей
территорией.
13.
Общая площадьлесов мира по
состоянию на
2018 год
составила 39 991
336,2 км², или
около 30,8% от
общей площади
суши в мире
• Однако, площадь лесов в
мире каждый год
уменьшается по мере роста
народонаселения и
увеличения спроса на
продовольствие и землю,
темпы чистых потерь леса
снизились более, чем
наполовину.
• в целом темпы чистой
потери общей площади,
занимаемой лесами,
замедлились в период
между 1990–2000 и 2010–
2015 более чем на
половину.
14. Нами проведен анализ данных за 70 лет, с использованием ряда отечественных и международных источников, в частности ФАО
(продовольственной и сельскохозяйственнойОрганизации Объединенных Наций) по площадям
лесных массивов как по России, так и странам мира
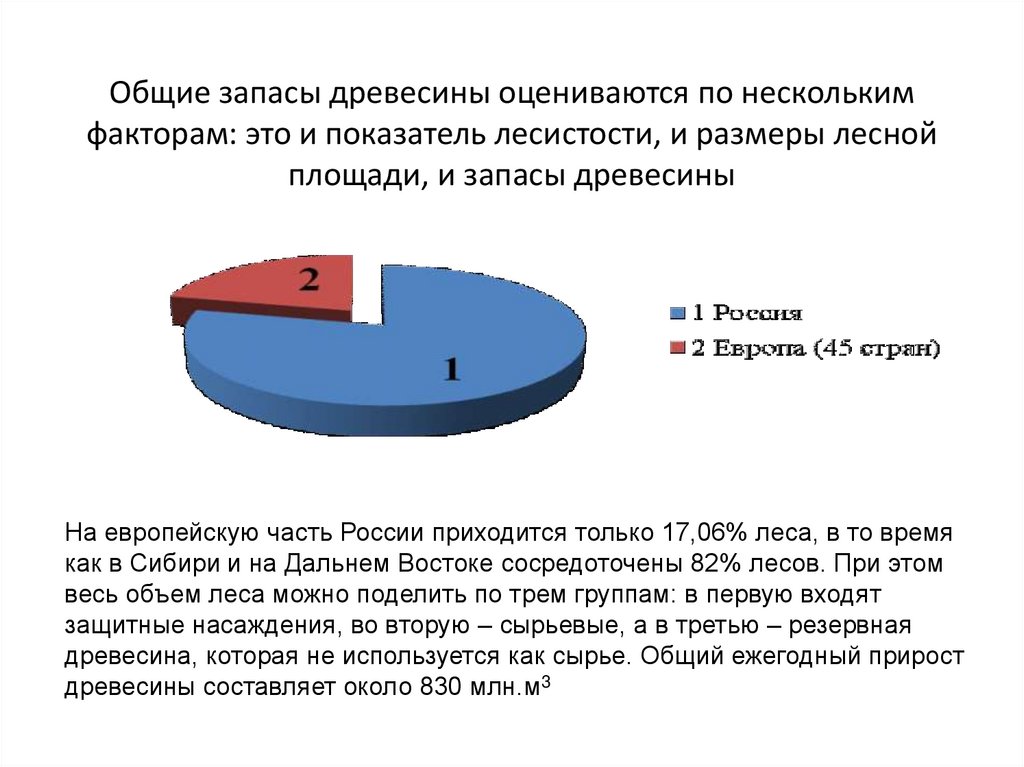
15. Общие запасы древесины оцениваются по нескольким факторам: это и показатель лесистости, и размеры лесной площади, и запасы
древесиныНа европейскую часть России приходится только 17,06% леса, в то время
как в Сибири и на Дальнем Востоке сосредоточены 82% лесов. При этом
весь объем леса можно поделить по трем группам: в первую входят
защитные насаждения, во вторую – сырьевые, а в третью – резервная
древесина, которая не используется как сырье. Общий ежегодный прирост
древесины составляет около 830 млн.м3
16.
.17. Древесина состоит из органической и неорганической части
– Органическая состоитиз углеводной или
полисахаридной
и
ароматической частей.
– Углеводная
часть
состоит
из
полисахаридов
различного строения и
полиуронидов.
– Полисахариды углеводной
части
можно
классифицировать
по
выполняемой функции и по
растворимости
компонентов.
– Основную
часть
полисахаридов относят к
структурообразующим
компонентам, участвующим
в построении клеточной
стенки, а водорастворимые
компоненты
относят
к
экстрактивным веществам
(водорастворимые
полисахариды
и
полиурониды).
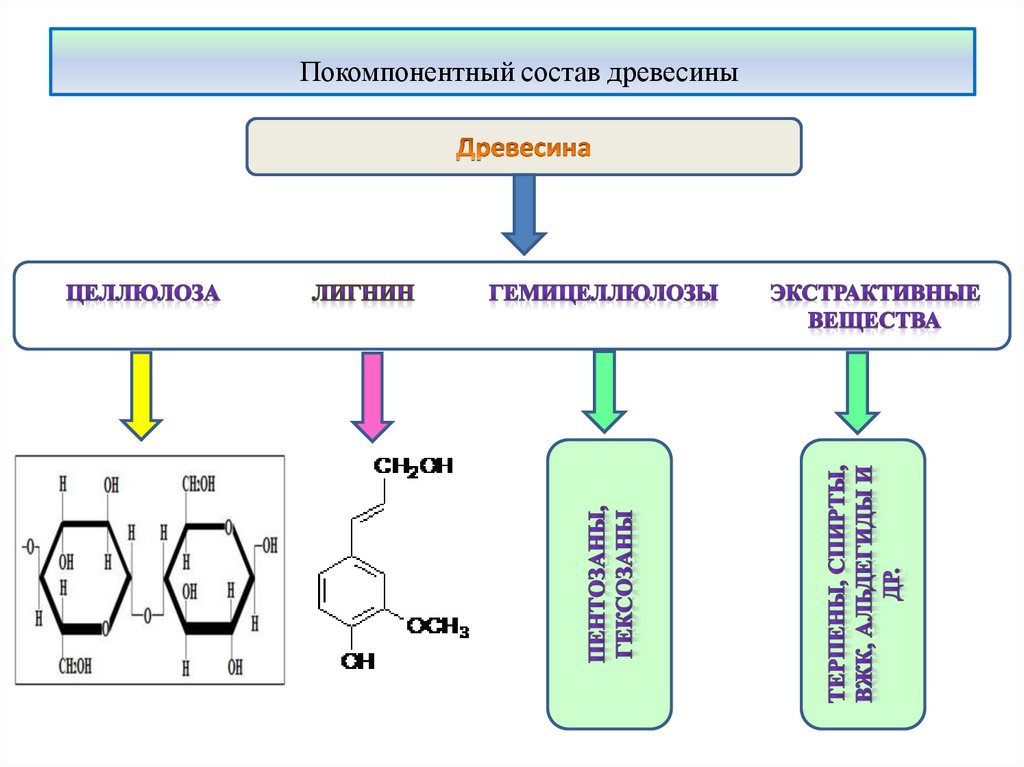
18. Покомпонентный состав древесины
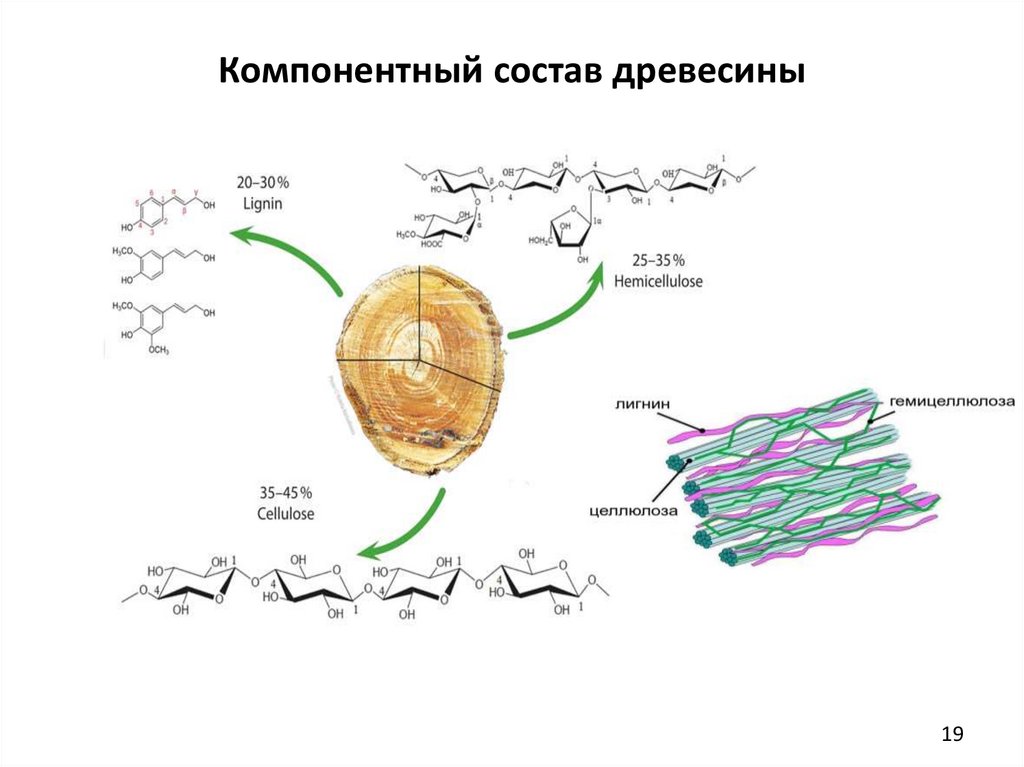
19. Компонентный состав древесины
1920.
21. Этапы изучения химии лигнина
1830-1879 г.г.А.Пайен,Э.Фреми - исследование элементного состава древесины
(открытие лигнина и целюлозы)
Ф.Тимман и Б.Мендельсон выделили из лигнина конифериловый
спирт; появление качественных реакций на лигнин (реакция
1880-1919г.г.
Визнера, реакция Е.Адлера); появление гипотезы П.Класона:
лигнин построен из фенилпропановых единиц , исходным
веществом является конифериловый спирт
Хегглундом и Холмбергом обоснована теория сульфитной
делигнификации
1920-1950г.г. К. Фрейденбергом , затем Ф.Браунсом предложены структурные
формулы лигнина.
С.М.Манской получен синтетический лигнин
Теория Флори-Штокмайера (гипотеза «гель-структуры»):
возможны взаимодействия между функциональными группами
1951-1990г.г.
разных макромолекул лигнина;
Создание отечественных буровых реагентов ФХЛС, КССБ,Окзил-М
Развитие направления применения лигнина как сырья для
1991-2019г.г.
21
нефтепромысловой химии
22. Исследование углеводного состава лигносульфонатов методом ТСХ
Нецеллюлозные полисахариды
Гексозан
ы
Маннаны
Галактаны
Глюканы
Крахмал
Пентозаны
Полиуронаны
Гидролиз
Арабинаны
Арабинаны
Ксиланы
Арабиноглюкуронксилан
D-манноза,
D-галактоза,
D-глюкоза,
L-арабиноза,
D-фруктоза
Полигалактуроновая
кислота
Полиглюкуроновая
кислота
Декарбоксилирование
Гидролиз
СО2
(включая СО2 из
глюкуроноксиланов)
D-ксилоза,
L-арабиноза,
D-глюкуроновая
4-О-метил-Dглюкуроновая кислоты
Соединени
е
Манноза
Ксилоза
Галактоза
Глюкоза
Арабиноза
Рамноза
а) L-ксилоза
Кислая сульфитная
варка
хвойных
лиственных
Сульфитная
(бисульфитна
я) варка
48
22
10
9
6
5
3
80
2
10
3
2
40
19
11
15
3
12
Нейтральносульфитная
(моносульфит
ная) варка
2
82
5
4
5
2
) L-рамноза
22
23. Основы классификации полимеров по происхождению
ПРИРОДНЫЕнеорганические
ХИМИЧЕСКИЕ
органические
искусственные
синтетические
поликонденсационные
полимеризационные
кварц
крахмал
вискоза
капрон
полиэтилен
графит
целлюлоза
ацетат
найлон
полиакриламид
силикаты
камедь
нитроцеллюлоза
лавсан
полистирол
корунд
каучук
фенолоформальдегид
полиакрилат
53%
Нефтегазовая отрасль
47%
Другие отрасли
Применение основных природных
полимеров (биополимеров) составляет
для нефтехимической отрасли 53%, для
остальных - пищевой,
фармацевтической, медицинской,
бумажной, строительной и др. - 47%
23
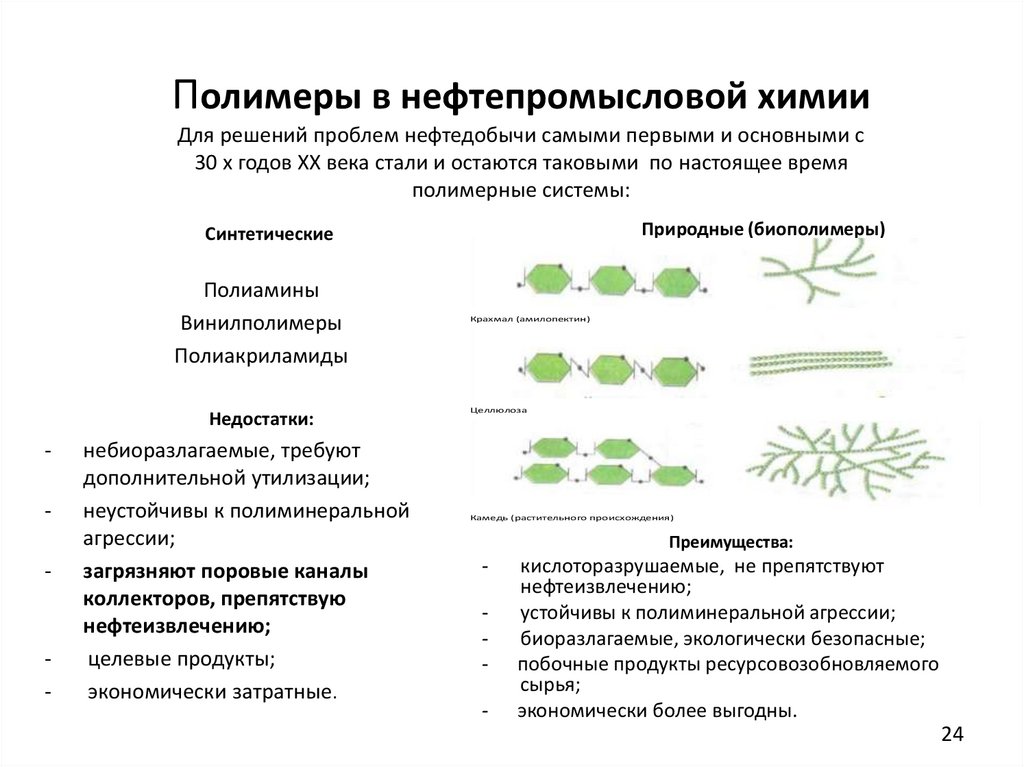
24. Полимеры в нефтепромысловой химии Для решений проблем нефтедобычи самыми первыми и основными с 30 х годов ХХ века стали и
остаются таковыми по настоящее времяполимерные системы:
Природные (биополимеры)
Синтетические
Полиамины
Винилполимеры
Полиакриламиды
Недостатки:
-
-
небиоразлагаемые, требуют
дополнительной утилизации;
неустойчивы к полиминеральной
агрессии;
загрязняют поровые каналы
коллекторов, препятствую
нефтеизвлечению;
целевые продукты;
экономически затратные.
Крахмал (амилопектин)
Целлюлоза
Камедь (растительного происхождения)
Преимущества:
-
кислоторазрушаемые, не препятствуют
нефтеизвлечению;
устойчивы к полиминеральной агрессии;
биоразлагаемые, экологически безопасные;
побочные продукты ресурсовозобновляемого
сырья;
экономически более выгодны.
24
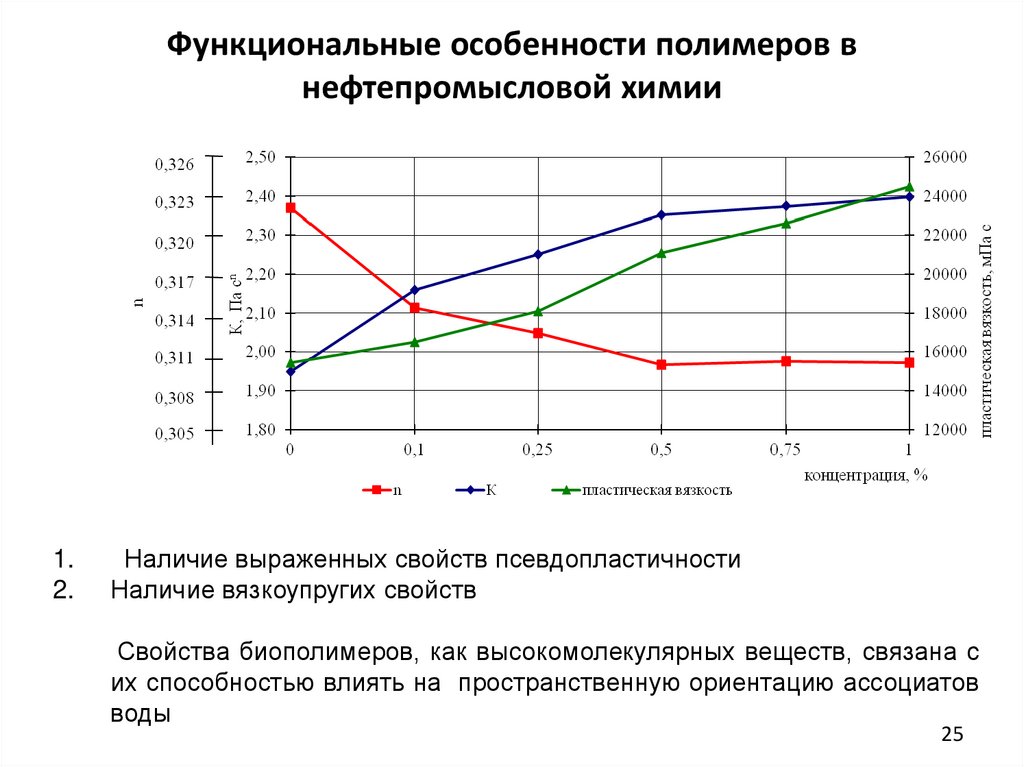
25. Функциональные особенности полимеров в нефтепромысловой химии
1.2.
Наличие выраженных свойств псевдопластичности
Наличие вязкоупругих свойств
Свойства биополимеров, как высокомолекулярных веществ, связана с
их способностью влиять на пространственную ориентацию ассоциатов
воды
25
26. Источники и технология получения некоторых основных биополимеров
ДревесинаЦеллюлоза
Камедь
Щепа
Древесина
Картофель, рис, пшеница,
кукуруза
Варка древесины
Этанол
Хлопок, конопля, лен
Промывка, сортировка, очистка
Крахмал
Целлюлоза
Хлопковый
линт
Биохимическая
переработка щелока
ЛСТ
Сжигание
Смеситель
Раствор щелочи
Варочный
котел
Промывочный
бак
Целлюлоза
Отбельная
башня
Туннельная
сушилка
Барабанная
мельница
26
27. Основная сырьевая база биополимеров
Россия – мировой лидер по лесным (древесным ресурсам (
)
)и
В промышленных целях используется не
более 30 % всех лесов. Во всем мире около
1,15 млрд га лесов используются в первую
очередь для производства древесной и
не древесной лесной продукции.
27
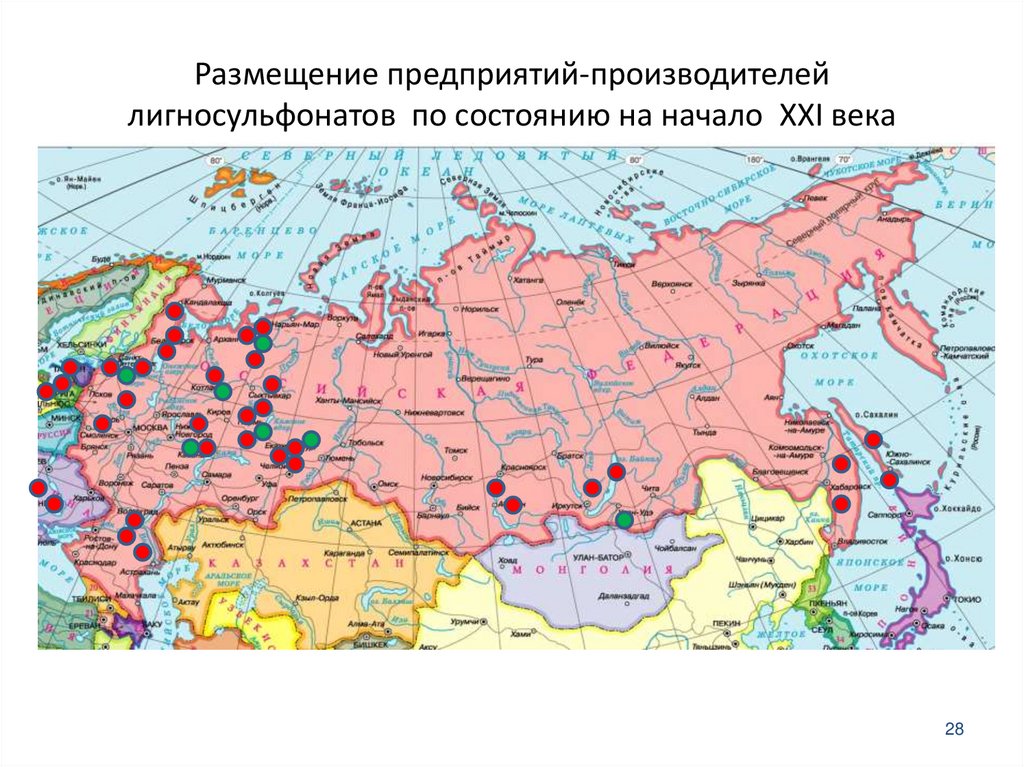
28. Размещение предприятий-производителей лигносульфонатов по состоянию на начало XXI века
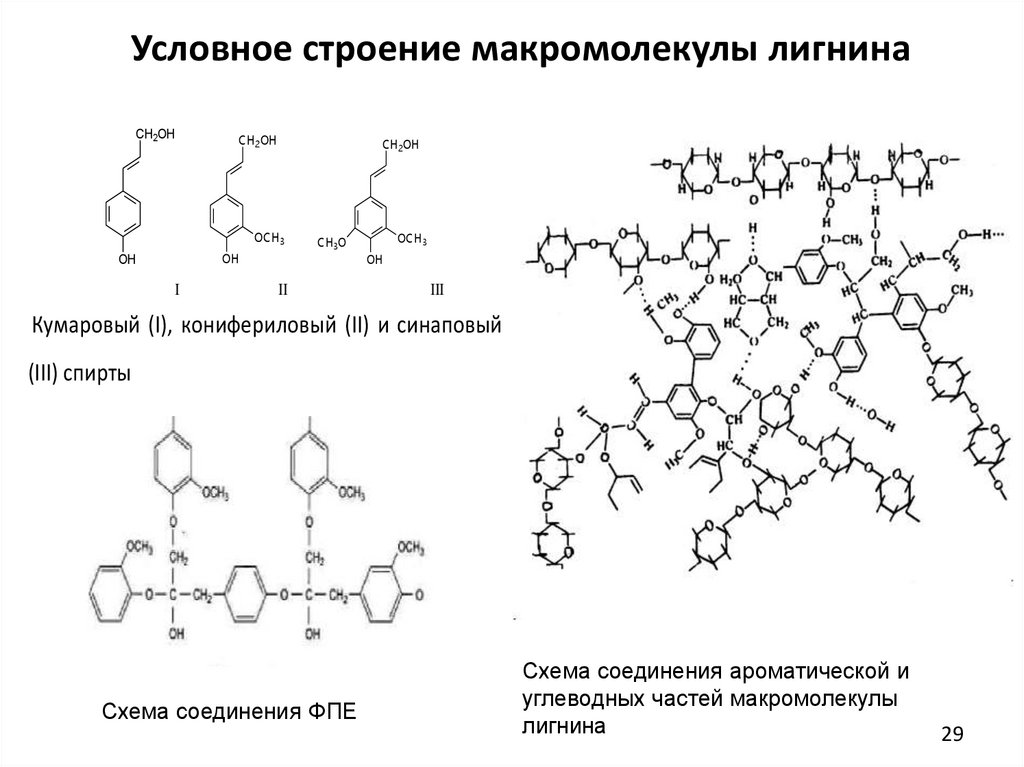
2829. Условное строение макромолекулы лигнина
CH2OHC H2OH
CH2OH
OC H3
OH
OH
I
CH3O
II
OCH3
OH
III
Кумаровый (I), конифериловый (II) и синаповый
(III) спирты
Схема соединения ФПЕ
Схема соединения ароматической и
углеводных частей макромолекулы
лигнина
29
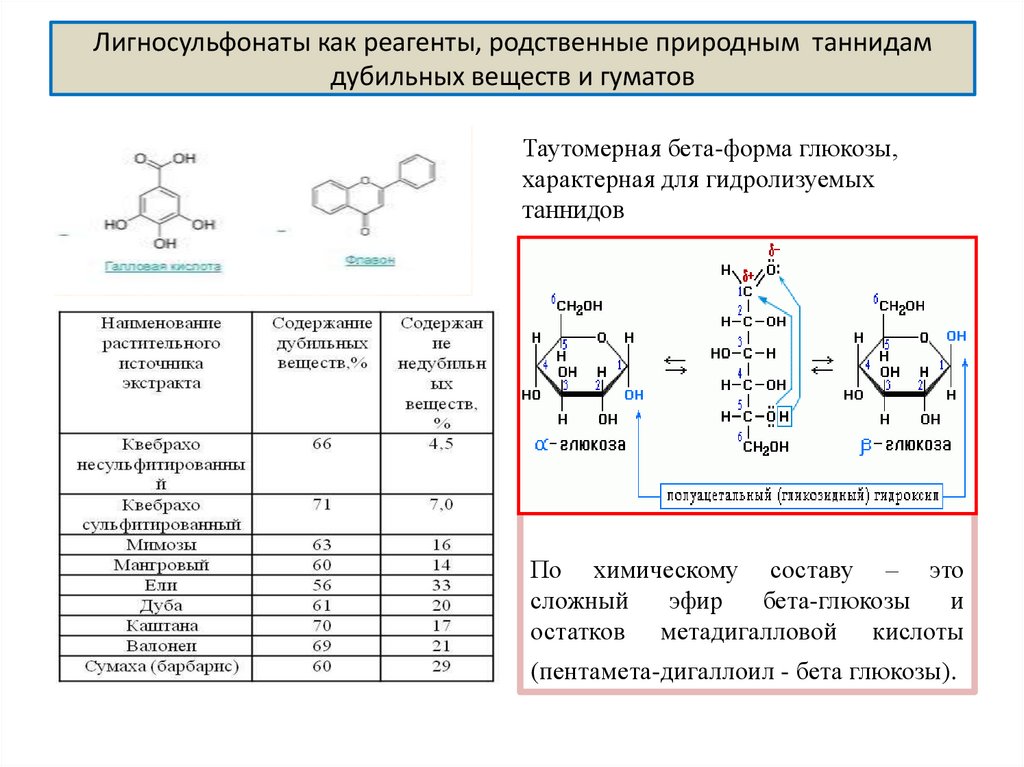
30. Лигносульфонаты как реагенты, родственные природным таннидам дубильных веществ и гуматов
Таутомерная бета-форма глюкозы,характерная для гидролизуемых
таннидов
По химическому составу – это
сложный
эфир
бета-глюкозы
и
остатков метадигалловой кислоты
(пентамета-дигаллоил - бета глюкозы).
31. Блок-схема получения лигносульфоната при различных способах делигнификации (варках)
Основной продукт целлюлозаПодготов
ка
древесно
го сырья
(окорка,
измельче
ние и др)
Сульфитная варка t0
135-1500С, 4-12 час.
Активный агент HSO3Отбор целевого
продукта 45-55%.
Нейтральносульфитная варка t0
160-1800С, 20-24 час.
Активный агент SO2Отбор целевого
продукта 80-85%.
Побочный продукт
– сульфитный
щелок (основное
вещество –
лигносульфонат)
Углеводная
составляющая
представлена, в
основном,
маннозой (48%)
Побочный продукт –
нейтральносульфитный щелок
(основное вещество –
лигносульфонат)
Углеводная
составляющая
представлена, в
основном,
ксилозой (82%)
Основной продукт целлюлозный
продукт
31
32.
Содержание кислых функциональных групп в расчете на одну фенилпропановую единицу (ФПЕ),%Сульфогруп Карбоксильны ОН-фенольные
е группы
группы
(-SO3H)
(-COOH)
Сырье-лигносульфонат
реагент1
1 СЩ
0,89
0,07
0, 28
Реагент 2
3
1,01
0,11
0,26
5 НСЩ
1,21
0,03
0,16
лст
7
1,19
0,07
Реагент на основе ЛСТ
объем титранта 0,5н
1 СЩ
1,65
0,18
0,42
3
1,62
0,18
0,33
содержание кислых групп, % [SO3H]= [V(LiOH) *
5 НСЩ
1,78
0,07
0,20
M (-SO3H) *C( LiOH )]/100
7
1,83
0,05
0,21
Дифференцированое определение содержания кислых групп методом кондуктометрического
титрования в водно-органической среде для растворов лигносульфонатов С = 2,5·10-4 М
Тип
№ щелока пы
ОН-С6Н5
-SO3H
-SO3H
-СОН
-СООН
ОН-С6Н5
32
Соотношение кислых групп в % представлено как
87 : 4 : 4 : 5 для нейтрального лигносульфоната
Соотношение кислых групп в % представлено как 30 :
10 : 20 : 40 для сульфитного лигносульфоната
33.
Сравнительная характеристика компонентного составасульфитного щелока - побочного продукта переработки
древесины
Показатель
Сульфитный ЛСТ
(технический)
Нейтрально-сульфитный ЛСТ
(технический)
Содержание лигносульфоната,
%
60
45
Содержание углеводов, %
масс.
Моносахариды, 8
Полисахариды, 16
Степень сульфирования
До 1 сульфогруппы на ФПЕ
0,3 атома S на ФПЕ
Содержание нерастворимых
веществ, %
0,5
10,2
рН раствора
4-5
7-7,4
43000-47000
4350-7500
Молекулярная масса, а.е.м.
Степень деструкции
полимерной сетки
Фрагментация сетки лигнина Нет деструкции сетки – нет лигнина
33
34.
Влияние способа делигнификациидревесины на компонентный
состав углеводной части
лигносульфоната
Разработанный способ
выделения полисахаридов
углеводной части
.
Подготовка
хроматографической
колонки
Заполнение колонки
гидролизованной в щелочной
Объединение
фракций по наличию
или отсутствию
характерных пиков
измерение оптической
плотности каждой
фракции
промывка колонки
с пробой ЛСТ
порциями элюата
автоматический
отбор фракций по
функции времени
Направление
пентозансодержащей фракции,
как сырья, на дальнейшую
переработку
Разработаны основы технологии использования
пентозансодержащей фракции нейтральных ЛСТ для
получения продуктов с антимикробными свойствами
34
35.
Достижения «зеленой химии»При производстве важных полимеров, например,
смазок, клеев и покрытий, требуется
использование опасных химикатов. За рубежом
разработан альтернативный процесс получения
полимеров «Радикальная полимеризация с
атомным переносом».
В процессе применяют экологически
безопасные химические вещества, например,
аскорбиновую кислоту (витамин С) в качестве
восстановителя, для процесса требуется меньшее
количество катализатора.
36.
Новые технологии «Зеленой химии»При производстве косметики и других средств
персонального ухода используют сложные эфиры. Обычно их
получают с помощью жестких химических методов, в
которых в качестве реагентов применяют сильные кислоты и
опасные растворители, и требуются значительные затраты
энергии. Фирма Eastman Chemical Company разработала новый
способ с применением иммобилизованных ферментов,
который позволяет избежать и избыточных затрат энергии, и
опасных реагентов – сильных кислот и органических
растворителей. Этот щадящий способ позволяет получать
сложные эфиры, которые невозможно было получить ранее, из
природного сырья.




























 Химия
Химия








