Korrekturen und Ergänzungen Stammdatenerfassung
1.
2.
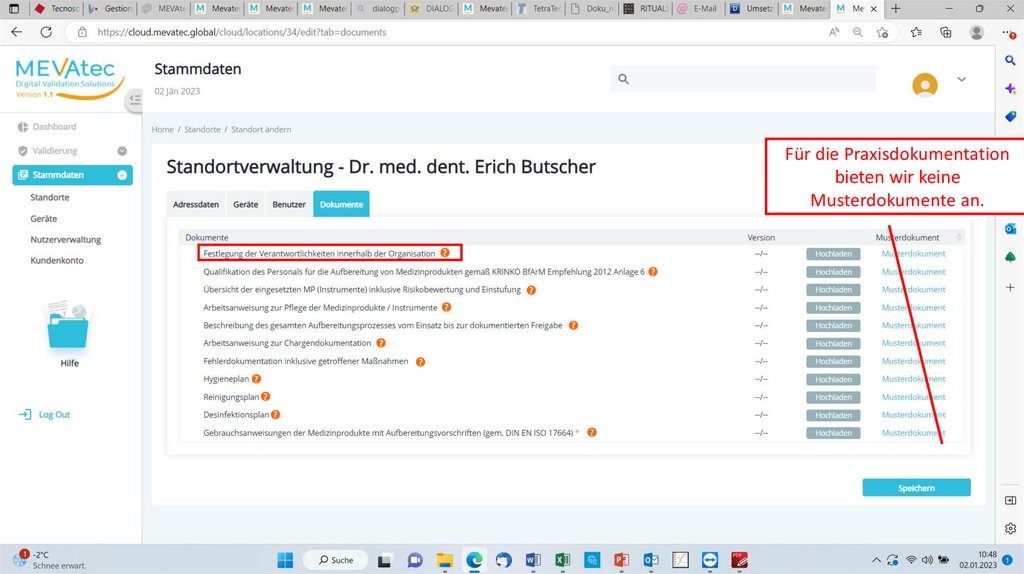
Erklärungen Dokumente Praxis3.
Für die Praxisdokumentationbieten wir keine
Musterdokumente an.
?
?
?
?
?
?
?
?
?
?
?
4.
??
?
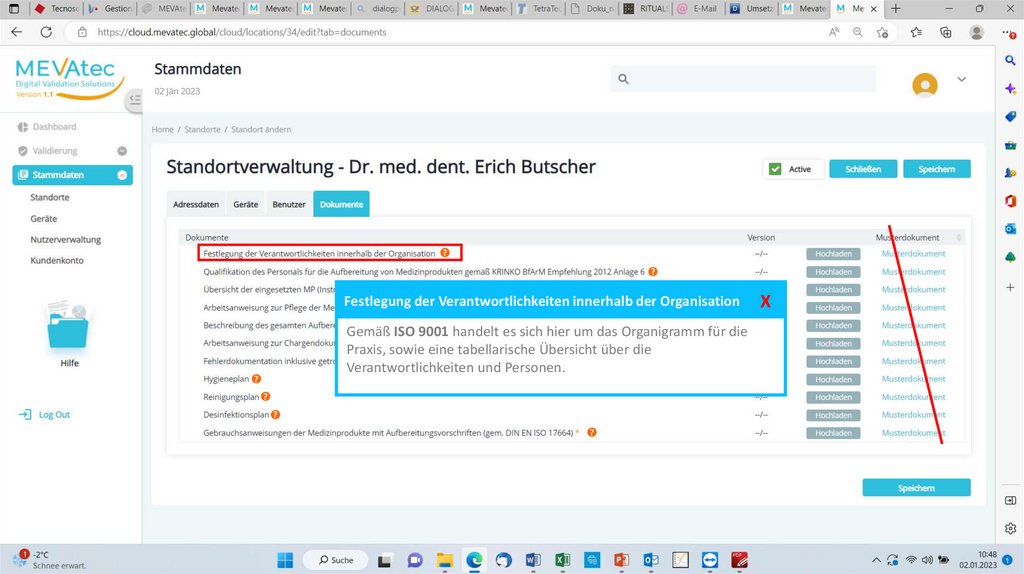
Festlegung der Verantwortlichkeiten
innerhalb der Organisation
?
Gemäß ISO 9001 handelt es sich hier ?um das Organigramm für die
?
Praxis, sowie eine tabellarische Übersicht über die
?
Verantwortlichkeiten
und Personen.
?
?
?
?
X
5.
??
?
?
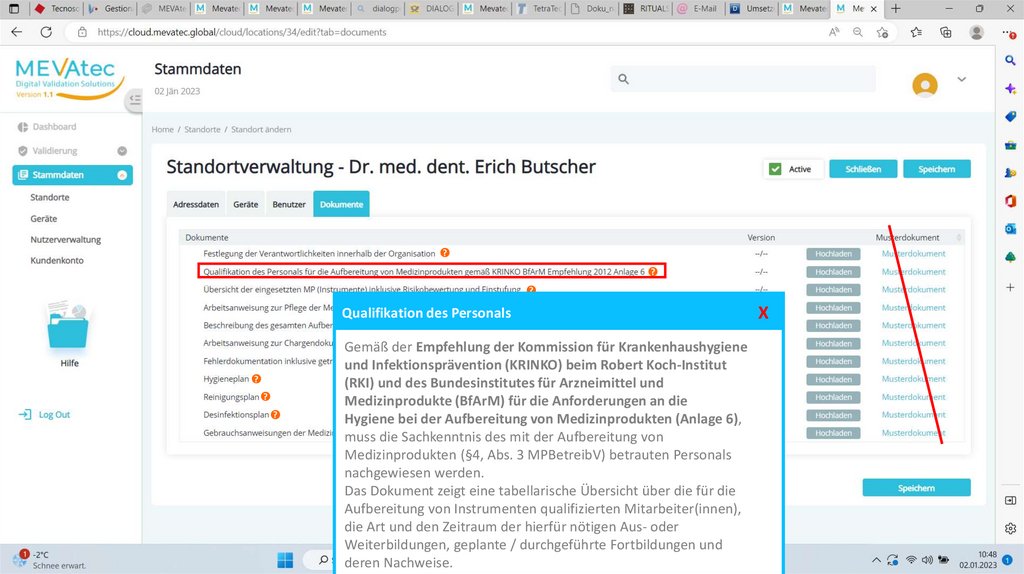
Qualifikation des Personals
?
?
?
?
?
Gemäß
der Empfehlung der Kommission für Krankenhaushygiene
?
und Infektionsprävention
(KRINKO) beim Robert Koch-Institut
(RKI) und des Bundesinstitutes für Arzneimittel und
Medizinprodukte (BfArM) für die Anforderungen an die
Hygiene bei der Aufbereitung von Medizinprodukten (Anlage 6),
?
muss die Sachkenntnis des mit der Aufbereitung
von
Medizinprodukten (§4, Abs. 3 MPBetreibV) betrauten Personals
nachgewiesen werden.
Das Dokument zeigt eine tabellarische Übersicht über die für die
Aufbereitung von Instrumenten qualifizierten Mitarbeiter(innen),
die Art und den Zeitraum der hierfür nötigen Aus- oder
Weiterbildungen, geplante / durchgeführte Fortbildungen und
deren Nachweise.
X
6.
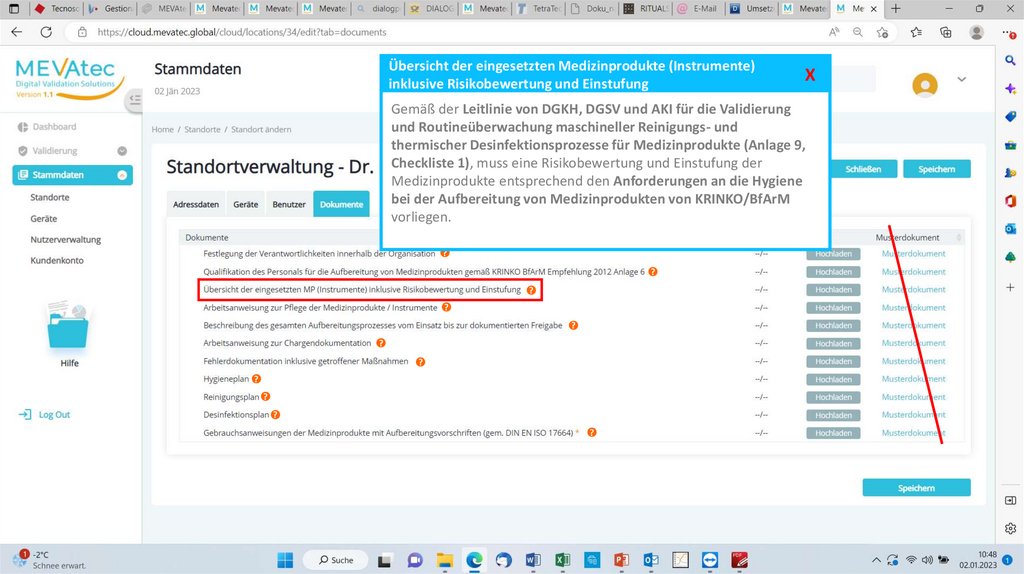
Übersicht der eingesetzten Medizinprodukte (Instrumente)inklusive Risikobewertung und Einstufung
X
Gemäß der Leitlinie von DGKH, DGSV und AKI für die Validierung
und Routineüberwachung maschineller Reinigungs- und
thermischer Desinfektionsprozesse für Medizinprodukte (Anlage 9,
Checkliste 1), muss eine Risikobewertung und Einstufung der
Medizinprodukte entsprechend den Anforderungen an die Hygiene
bei der Aufbereitung von Medizinprodukten von KRINKO/BfArM
vorliegen.
?
?
?
?
?
?
?
?
?
?
?
7.
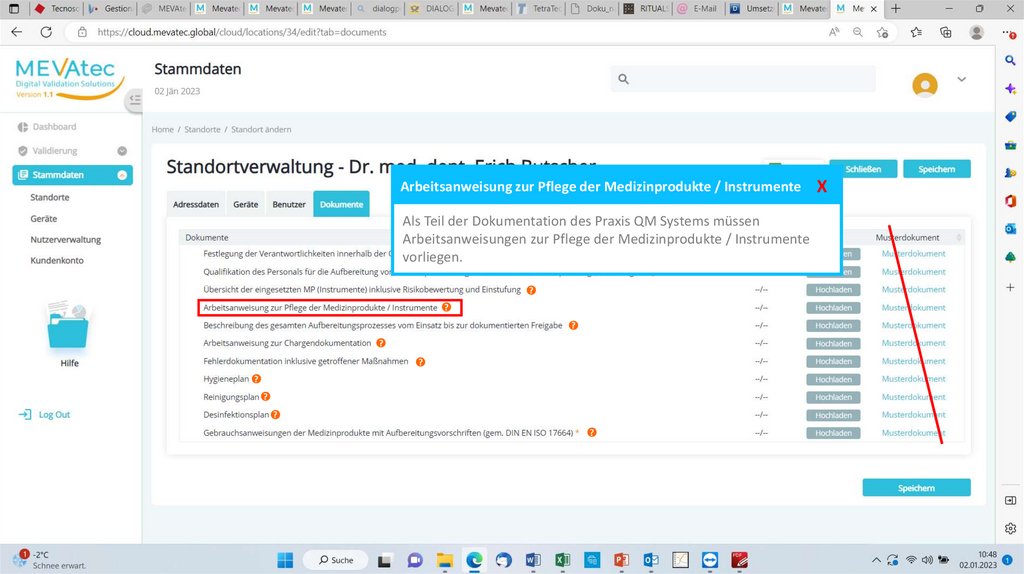
Arbeitsanweisung zur Pflege der Medizinprodukte / InstrumenteAls Teil der Dokumentation des Praxis QM Systems müssen
Arbeitsanweisungen zur Pflege der Medizinprodukte / Instrumente
?
vorliegen.
?
?
?
?
?
?
?
?
?
?
X
8.
??
?
?
?
?
?
?
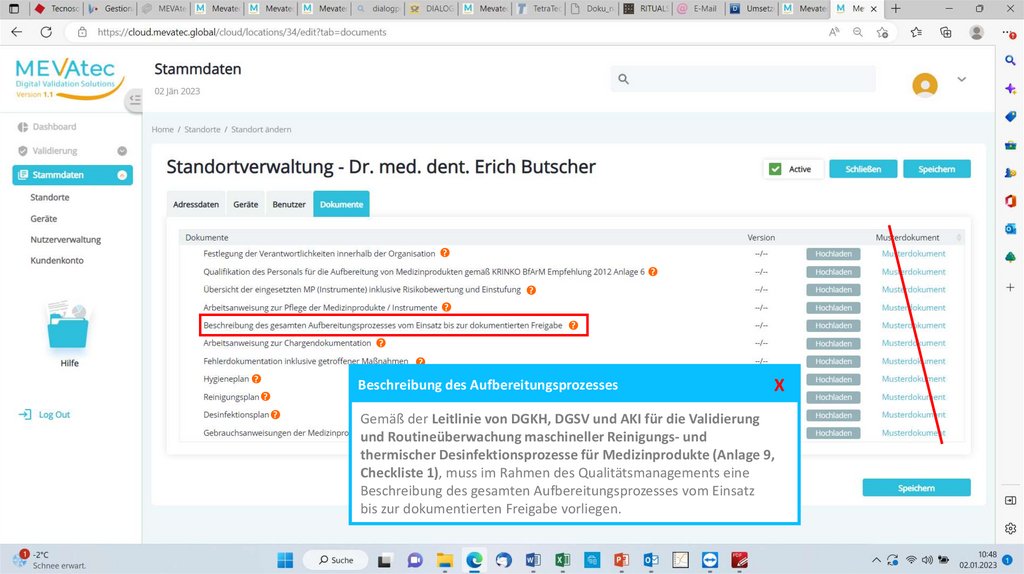
Beschreibung des Aufbereitungsprozesses
?
?
X
Gemäß der Leitlinie von DGKH, DGSV und AKI für die Validierung
?
und Routineüberwachung maschineller
Reinigungs- und
thermischer Desinfektionsprozesse für Medizinprodukte (Anlage 9,
Checkliste 1), muss im Rahmen des Qualitätsmanagements eine
Beschreibung des gesamten Aufbereitungsprozesses vom Einsatz
bis zur dokumentierten Freigabe vorliegen.
9.
??
?
?
?
?
?
?
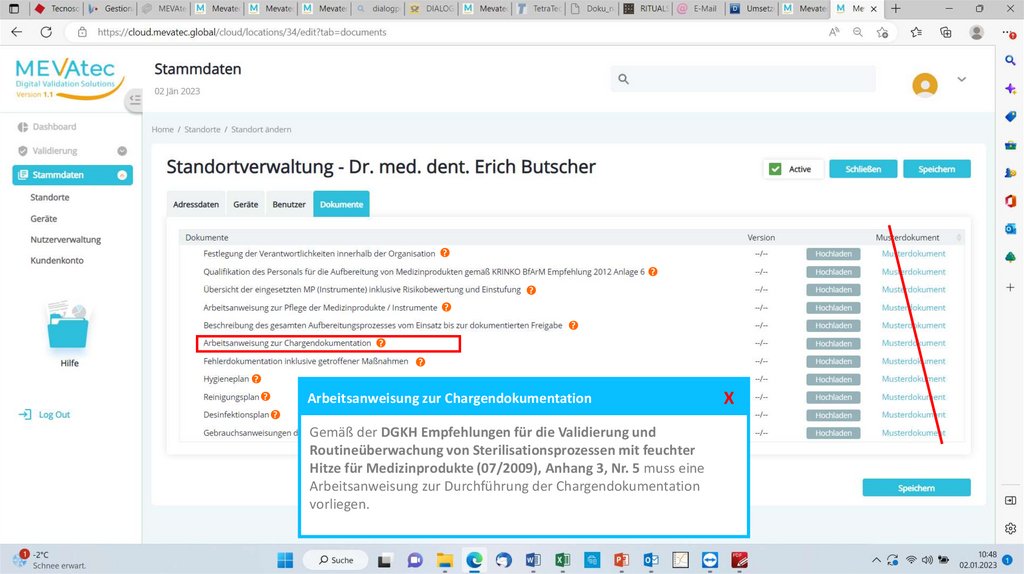
Arbeitsanweisung zur Chargendokumentation
?
?
?
Gemäß der DGKH Empfehlungen für die Validierung
und
Routineüberwachung von Sterilisationsprozessen mit feuchter
Hitze für Medizinprodukte (07/2009), Anhang 3, Nr. 5 muss eine
Arbeitsanweisung zur Durchführung der Chargendokumentation
vorliegen.
X
10.
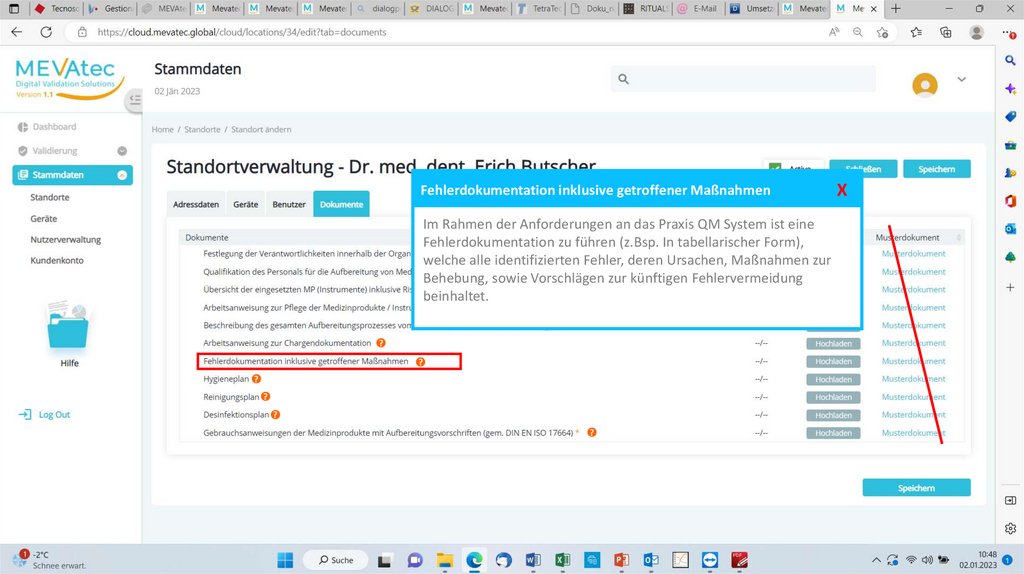
Fehlerdokumentation inklusive getroffener MaßnahmenIm Rahmen der Anforderungen an das Praxis QM System ist eine
Fehlerdokumentation zu führen (z.Bsp. In tabellarischer Form),
?
welche alle identifizierten Fehler, deren Ursachen, Maßnahmen zur
?
Behebung, sowie Vorschlägen zur künftigen Fehlervermeidung
?
beinhaltet.
?
?
?
?
?
?
?
?
X
11.
XHygieneplan
?
?
?
?
?
?
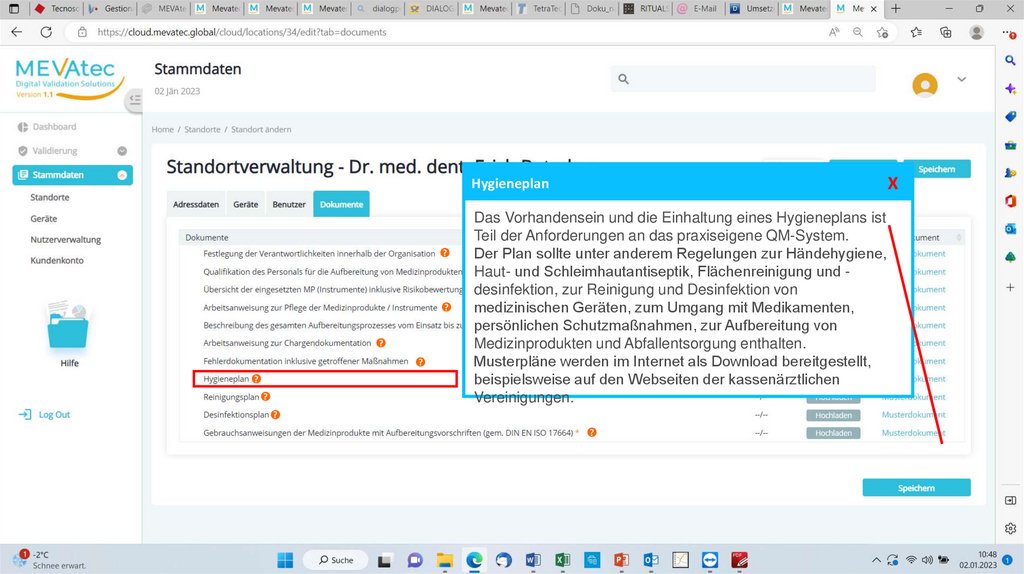
Das Vorhandensein und die Einhaltung eines Hygieneplans ist
Teil der Anforderungen an das praxiseigene QM-System.
Der Plan sollte unter anderem Regelungen zur Händehygiene,
?
Haut- und Schleimhautantiseptik,
Flächenreinigung und ?
desinfektion,
zur Reinigung und Desinfektion von
medizinischen Geräten, zum Umgang mit Medikamenten,
?
persönlichen Schutzmaßnahmen,
zur Aufbereitung von
Medizinprodukten und Abfallentsorgung enthalten.
Musterpläne werden im Internet als Download bereitgestellt,
beispielsweise auf den Webseiten der kassenärztlichen
Vereinigungen.
?
?
12.
XReinigungsplan
?
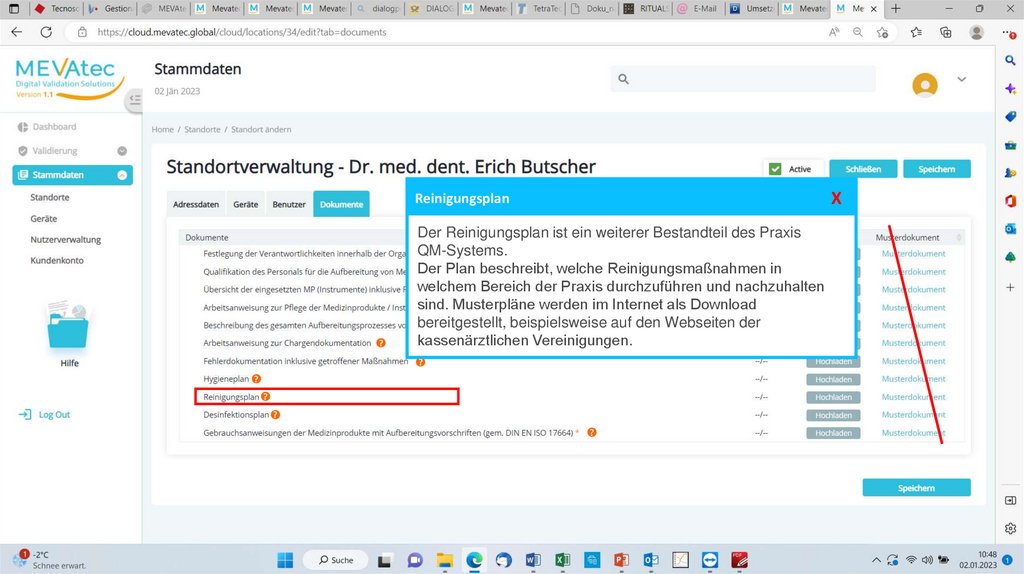
Der Reinigungsplan ist ein weiterer Bestandteil des Praxis
QM-Systems.
?
Der Plan beschreibt, welche Reinigungsmaßnahmen
in
?
welchem Bereich? der Praxis durchzuführen und nachzuhalten
sind.? Musterpläne werden im Internet als Download
bereitgestellt, beispielsweise
auf den Webseiten der
?
kassenärztlichen Vereinigungen.
?
?
?
?
?
13.
??
?
?
?
?
?
?
?
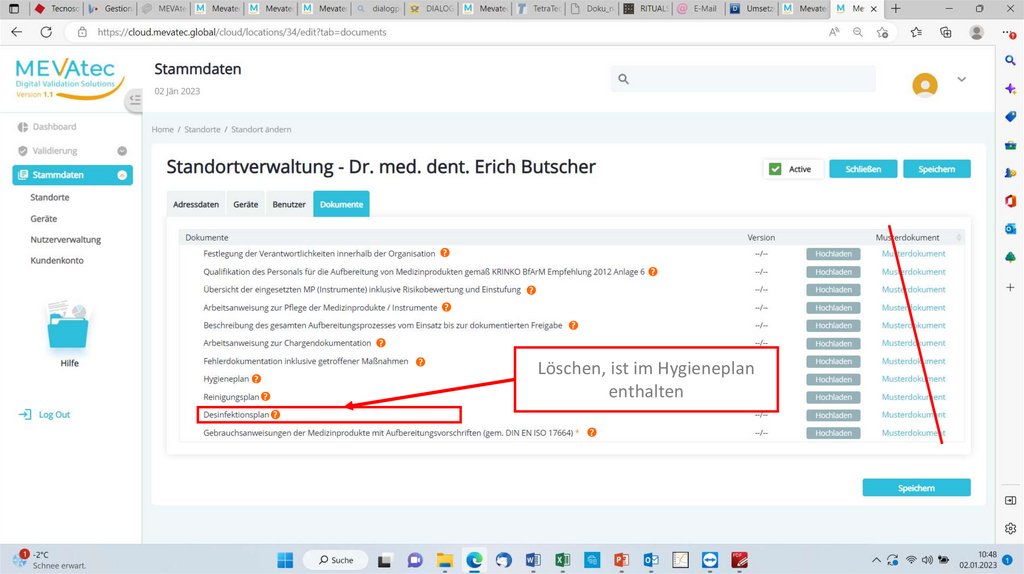
Löschen, ist im Hygieneplan
enthalten
?
?
14.
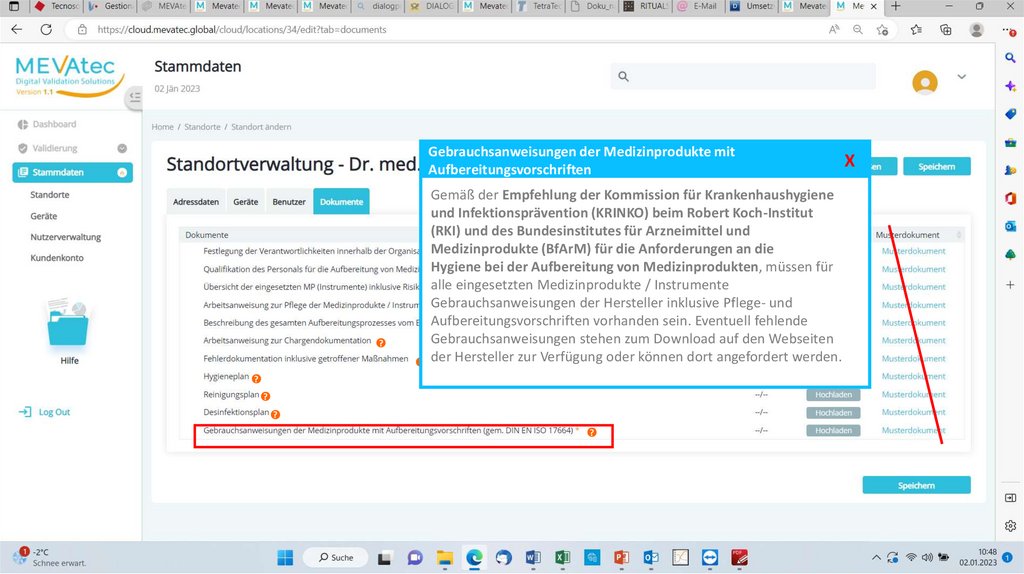
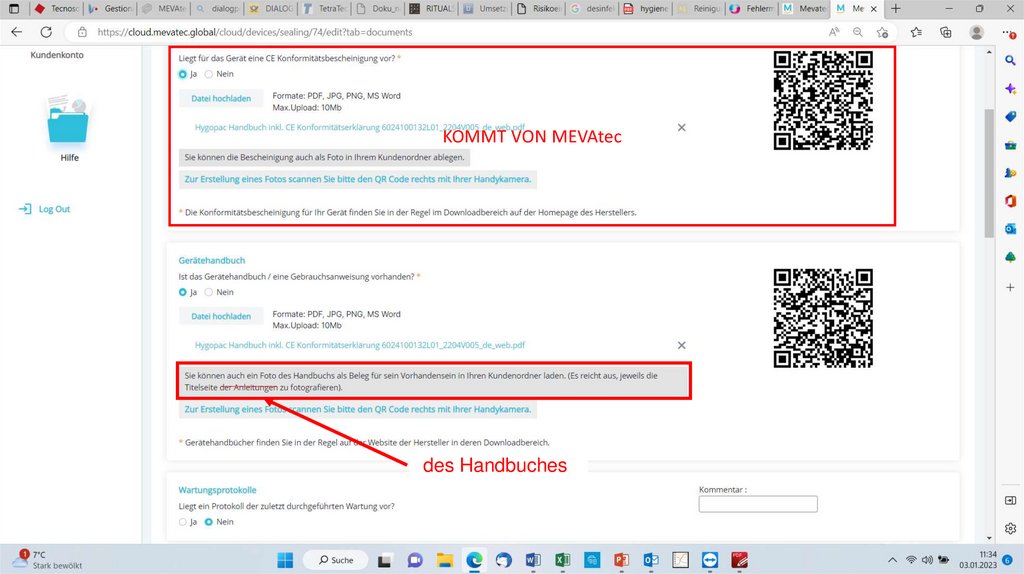
Gebrauchsanweisungen der Medizinprodukte mitAufbereitungsvorschriften
?
Gemäß der Empfehlung der Kommission für Krankenhaushygiene
und Infektionsprävention (KRINKO) beim Robert Koch-Institut
(RKI) und des Bundesinstitutes für Arzneimittel und
Medizinprodukte
(BfArM) für die Anforderungen an die
?
Hygiene bei der Aufbereitung von Medizinprodukten,
müssen für
?
alle eingesetzten? Medizinprodukte / Instrumente
Gebrauchsanweisungen
der Hersteller inklusive Pflege- und
?
Aufbereitungsvorschriften
vorhanden sein. Eventuell fehlende
?
Gebrauchsanweisungen stehen zum Download auf den Webseiten
? der Hersteller zur Verfügung oder können dort angefordert werden.
?
?
?
?
X
15.
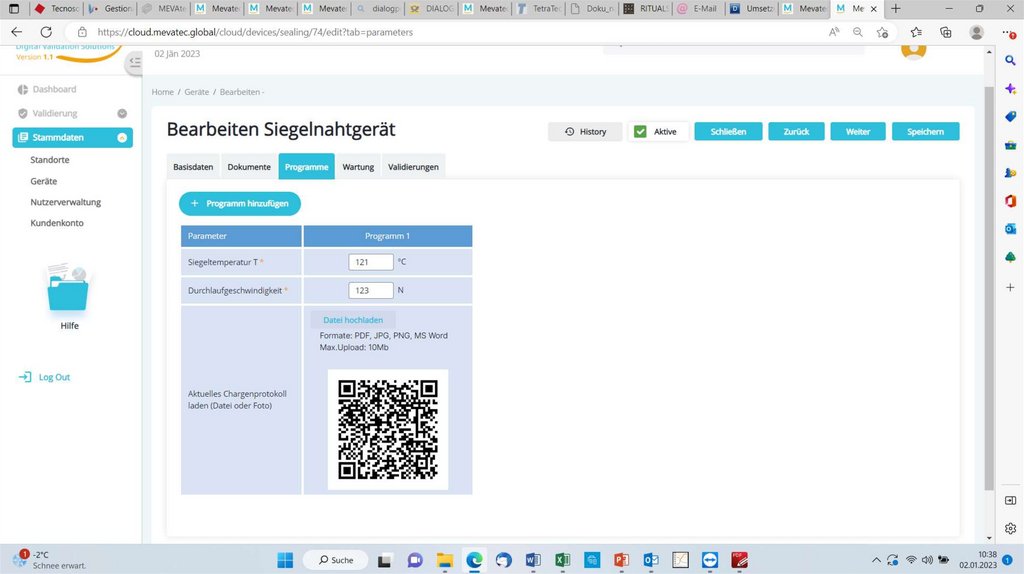
Erklärungen Dokumente Siegelnahtgerät16.
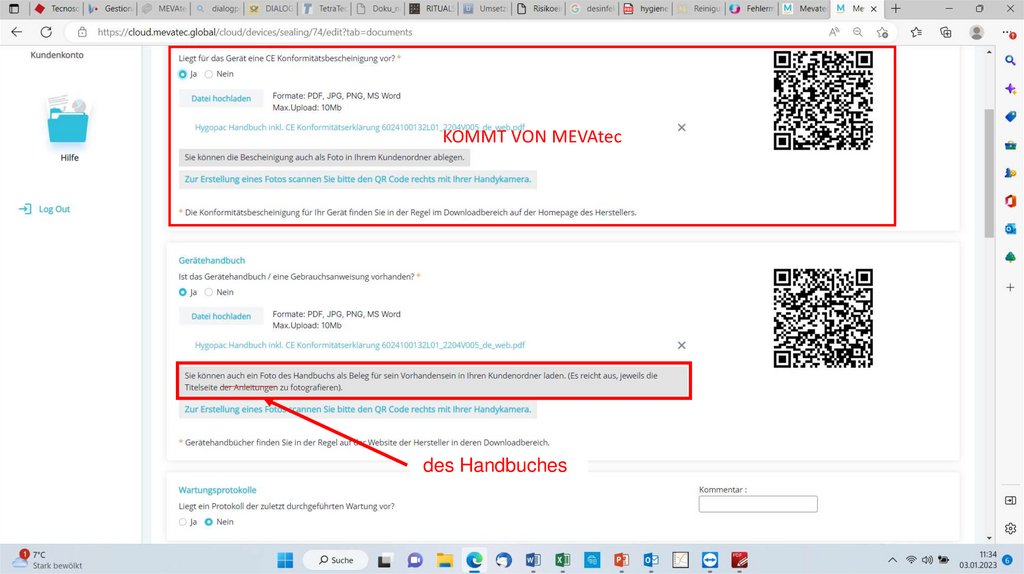
KOMMT VON MEVAtecdes Handbuches
17.
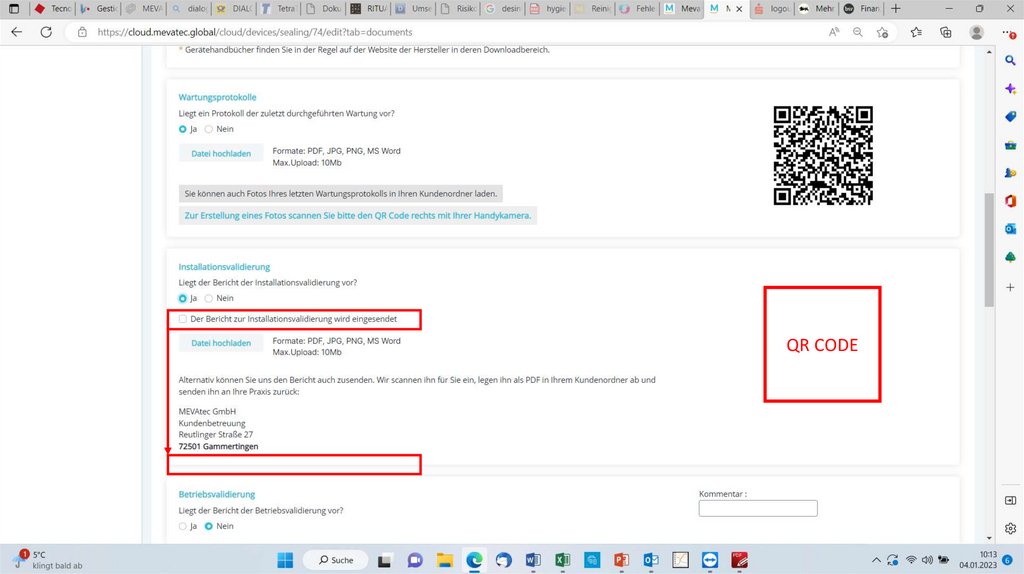
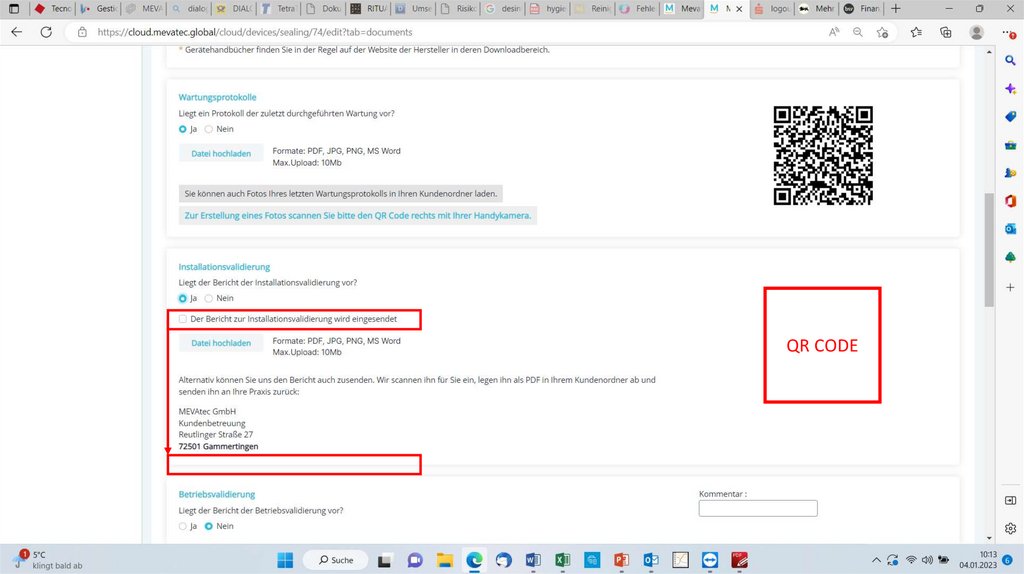
QR CODE18.
19.
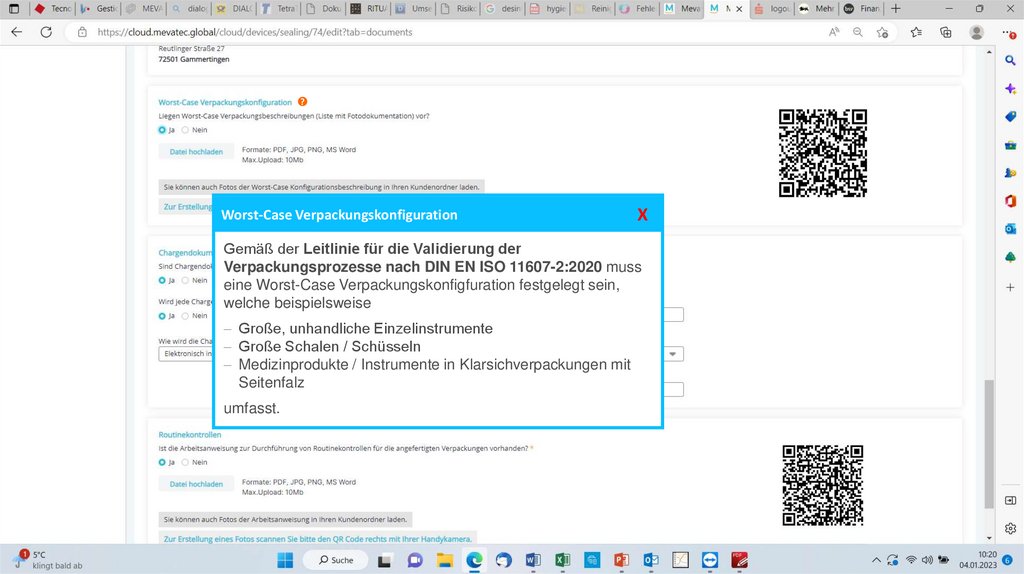
?Worst-Case Verpackungskonfiguration
X
Gemäß der Leitlinie für die Validierung der
Verpackungsprozesse nach DIN EN ISO 11607-2:2020 muss
eine Worst-Case Verpackungskonfigfuration festgelegt sein,
welche beispielsweise
Große, unhandliche Einzelinstrumente
Große Schalen / Schüsseln
Medizinprodukte / Instrumente in Klarsichverpackungen mit
Seitenfalz
umfasst.
20.
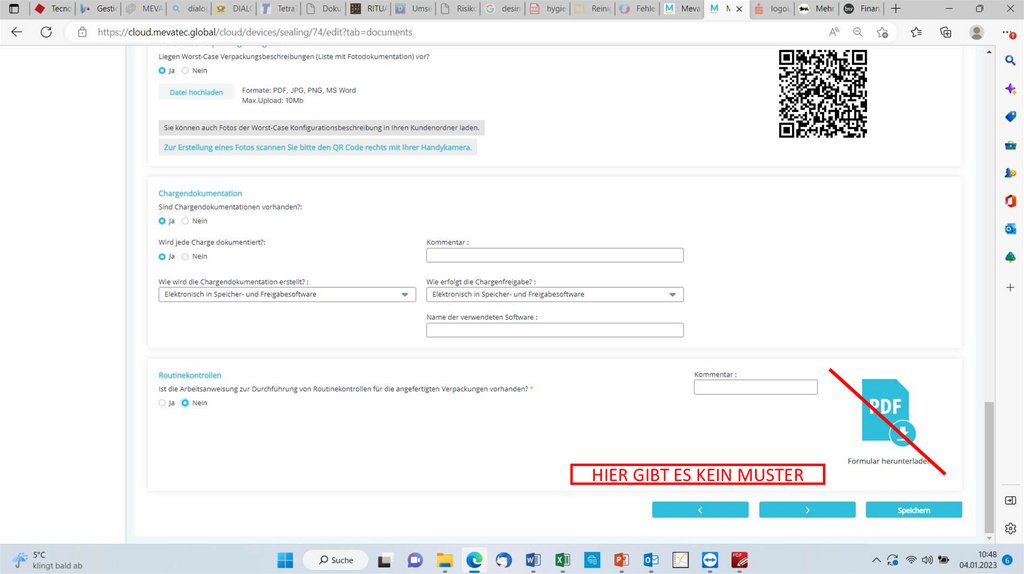
HIER GIBT ES KEIN MUSTER21.
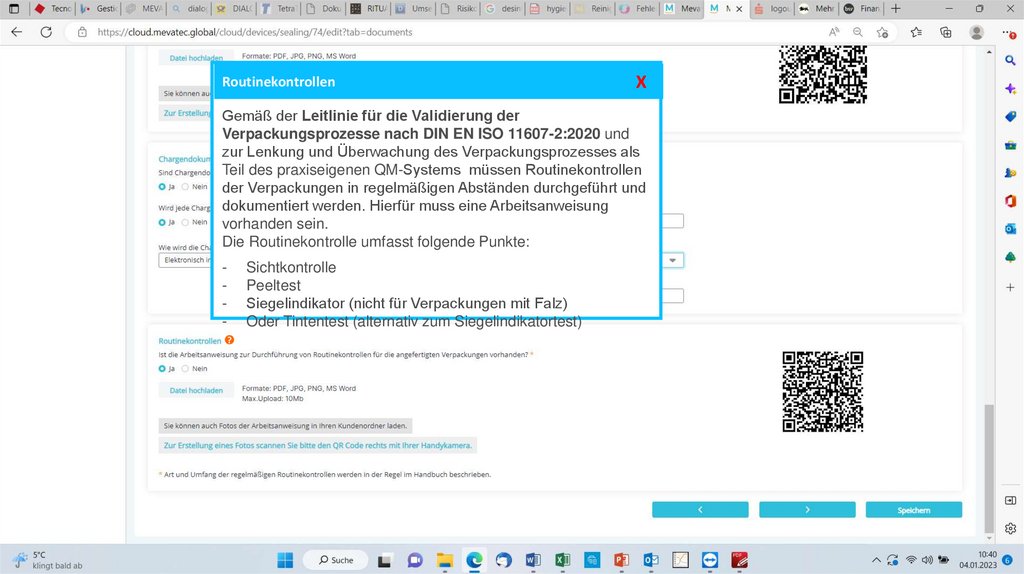
RoutinekontrollenX
Gemäß der Leitlinie für die Validierung der
Verpackungsprozesse nach DIN EN ISO 11607-2:2020 und
zur Lenkung und Überwachung des Verpackungsprozesses als
Teil des praxiseigenen QM-Systems müssen Routinekontrollen
der Verpackungen in regelmäßigen Abständen durchgeführt und
dokumentiert werden. Hierfür muss eine Arbeitsanweisung
vorhanden sein.
Die Routinekontrolle umfasst folgende Punkte:
-
Sichtkontrolle
Peeltest
Siegelindikator (nicht für Verpackungen mit Falz)
Oder Tintentest (alternativ zum Siegelindikatortest)
?
22.
Erklärungen Dokumente RDG23.
KOMMT VON MEVAtecdes Handbuches
24.
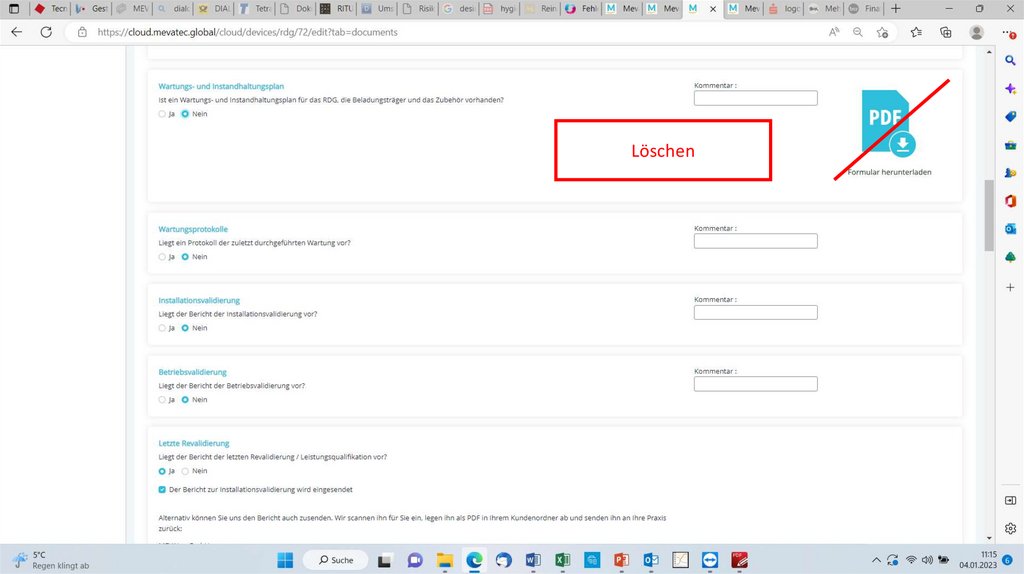
Löschen25.
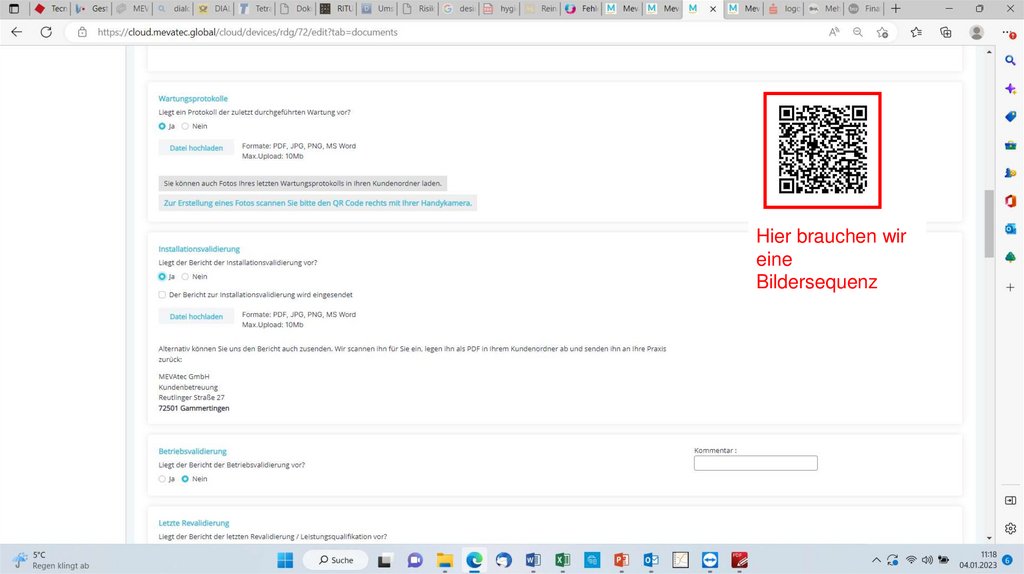
Hier brauchen wireine
Bildersequenz



 Программное обеспечение
Программное обеспечение