Похожие презентации:
Демонстрационный вариант экзаменационного билета
1.
ОМСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙУНИВЕРСИТЕТ
Кафедра химии
ХИМИЯ
КОНСУЛЬТАЦИЯ
Демонстрационный вариант
экзаменационного билета
Лектор: доктор биологических наук, профессор,
зав. кафедрой химии Ирина Петровна Степанова
2.
Общие положенияЭкзамен проводится в письменной форме.
На выполнение экзаменационной работы
отводится 2,0 астрономических часа (120
минут).
3.
Структура билетаБИЛЕТ СОСТОИТ ИЗ 2 ЧАСТЕЙ И
СОДЕРЖИТ 20 ЗАДАНИЙ.
Часть 1 включает 15 тестовых заданий. К
каждому заданию дается 4 варианта
ответов, из которых один правильный.
Десять заданий оценивается по 1 баллу,
пять заданий - по 2 балла.
Максимальное число баллов за часть 1 –
20 баллов.
4.
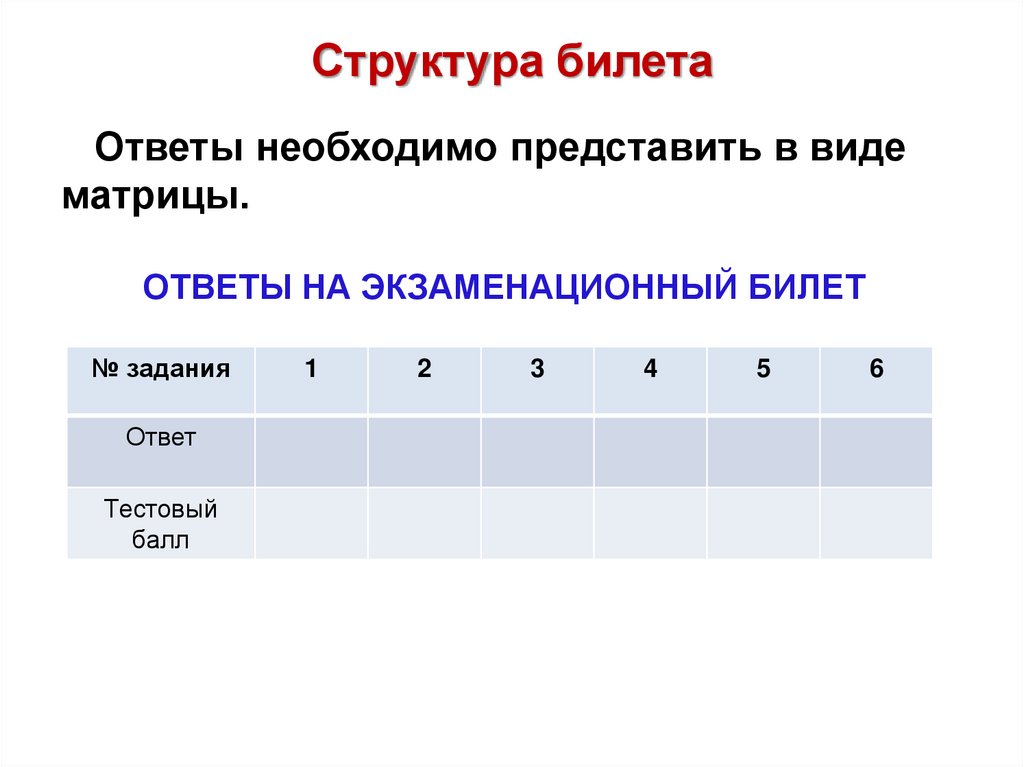
Структура билетаОтветы необходимо представить в виде
матрицы.
ОТВЕТЫ НА ЭКЗАМЕНАЦИОННЫЙ БИЛЕТ
№ задания
Ответ
Тестовый
балл
1
2
3
4
5
6
5.
Структура билетаЧасть 2, предусматривающая
развернутый письменный ответ, включает
5 расчетных задач. К каждой задаче дается
4 варианта ответов, из которых один
правильный.
Задачи 16 и 17 оцениваются в 4 балла,
задачи 17 и 18 – в 7 баллов, задача 20 – в
8 баллов.
Максимальное число баллов за часть 2 –
30 баллов.
6.
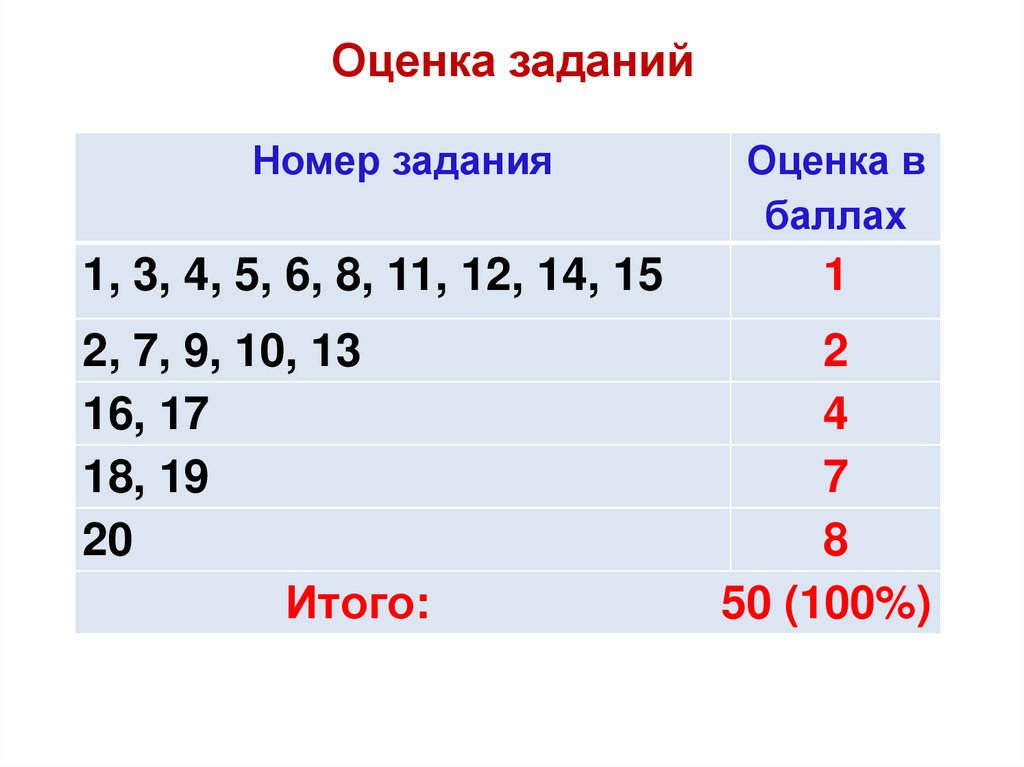
Оценка заданийНомер задания
1, 3, 4, 5, 6, 8, 11, 12, 14, 15
2, 7, 9, 10, 13
16, 17
18, 19
20
Итого:
Оценка в
баллах
1
2
4
7
8
50 (100%)
7.
Время выполнения заданийРекомендуемое время выполнения задания
в 1 балл – 1-2 минуты, в 2 балла – 3-4 минуты.
На выполнение тестовых заданий отводится
не более 40 минут!!!
Рекомендуемое время решения заданий 16 и
17 вместе с оформлением – 5-10 минут, задач
18 и 19 – 10-15 минут, задачи 20 – 15-20 минут.
8.
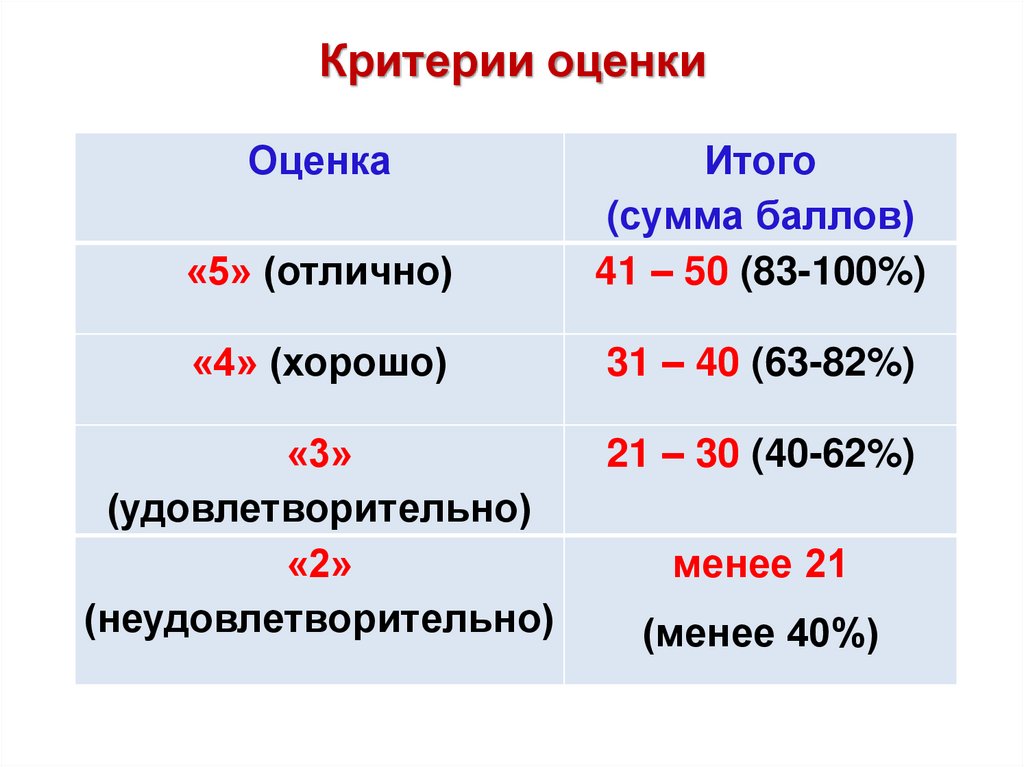
Критерии оценкиОценка
«5» (отлично)
Итого
(сумма баллов)
41 – 50 (83-100%)
«4» (хорошо)
31 – 40 (63-82%)
«3»
(удовлетворительно)
«2»
(неудовлетворительно)
21 – 30 (40-62%)
менее 21
(менее 40%)
9.
Общие положенияПри выполнении работы Вы можете
пользоваться:
• периодической системой химических
элементов Д.И. Менделеева;
• таблицей стандартных электродных
потенциалов металлов;
• таблицей растворимости солей, кислот и
оснований;
• калькулятором.
10.
Демонстрационныйбилет
11.
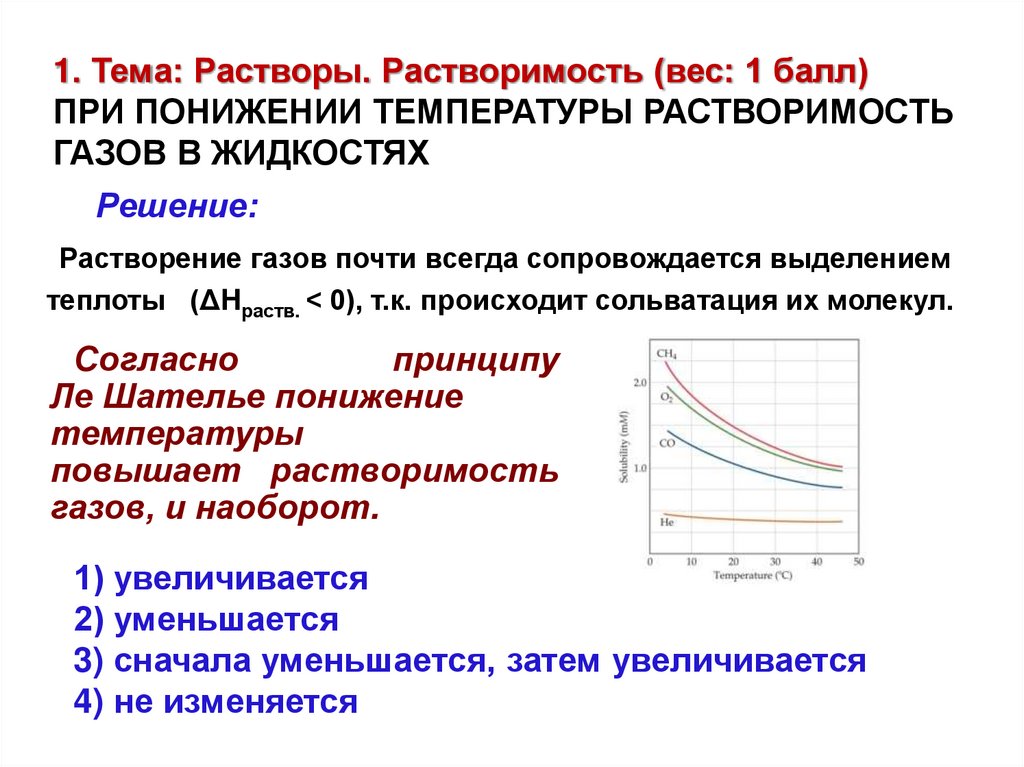
1. Тема: Растворы. Растворимость (вес: 1 балл)ПРИ ПОНИЖЕНИИ ТЕМПЕРАТУРЫ РАСТВОРИМОСТЬ
ГАЗОВ В ЖИДКОСТЯХ
Решение:
Растворение газов почти всегда сопровождается выделением
теплоты (ΔHраств. < 0), т.к. происходит сольватация их молекул.
Согласно
принципу
Ле Шателье понижение
температуры
повышает растворимость
газов, и наоборот.
1) увеличивается
2) уменьшается
3) сначала уменьшается, затем увеличивается
4) не изменяется
12.
2. Тема: Растворы. Способы выражения концентрациирастворов (вес: 2 балла)
ДЛЯ ПРИГОТОВЛЕНИЯ РАСТВОРА ИОДИДА КАЛИЯ
(Mr = 166), ИСПОЛЬЗУЕМОГО В МЕТОДЕ ИОДОМЕТРИИ,
8,3 г KI РАСТВОРИЛИ В МЕРНОЙ КОЛБЕ НА 500 мл.
РАССЧИТАЙТЕ МОЛЯРНУЮ КОНЦЕНТРАЦИЮ
ЭКВИВАЛЕНТА РАСТВОРА ИОДИДА КАЛИЯ.
Решение:
































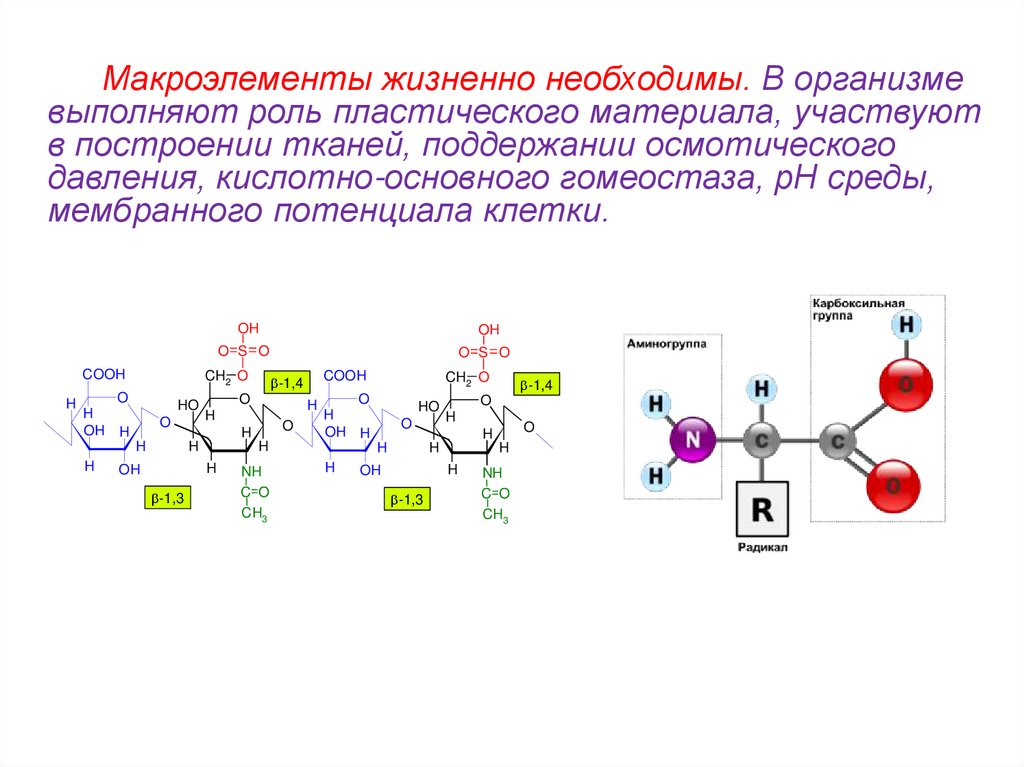












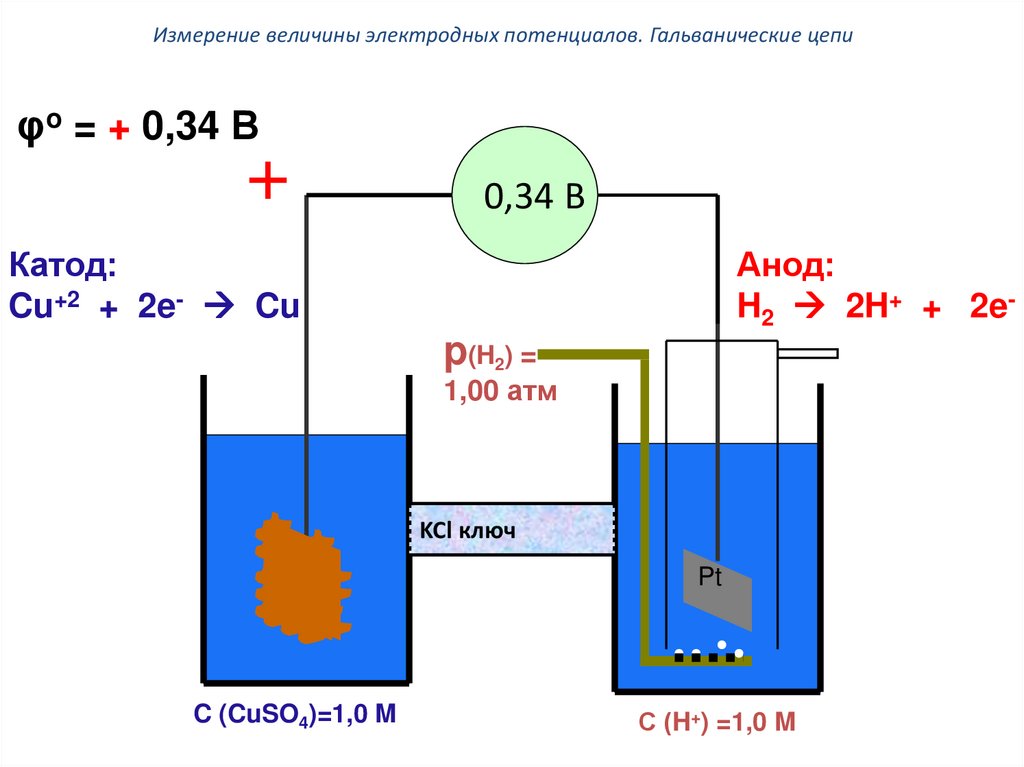






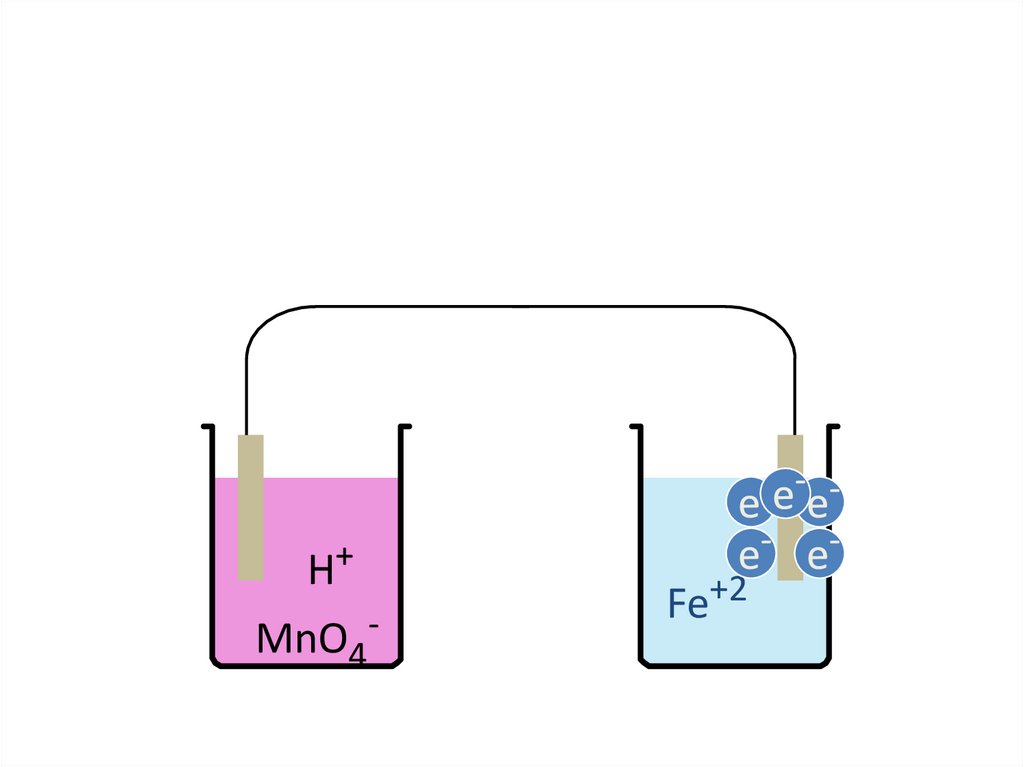
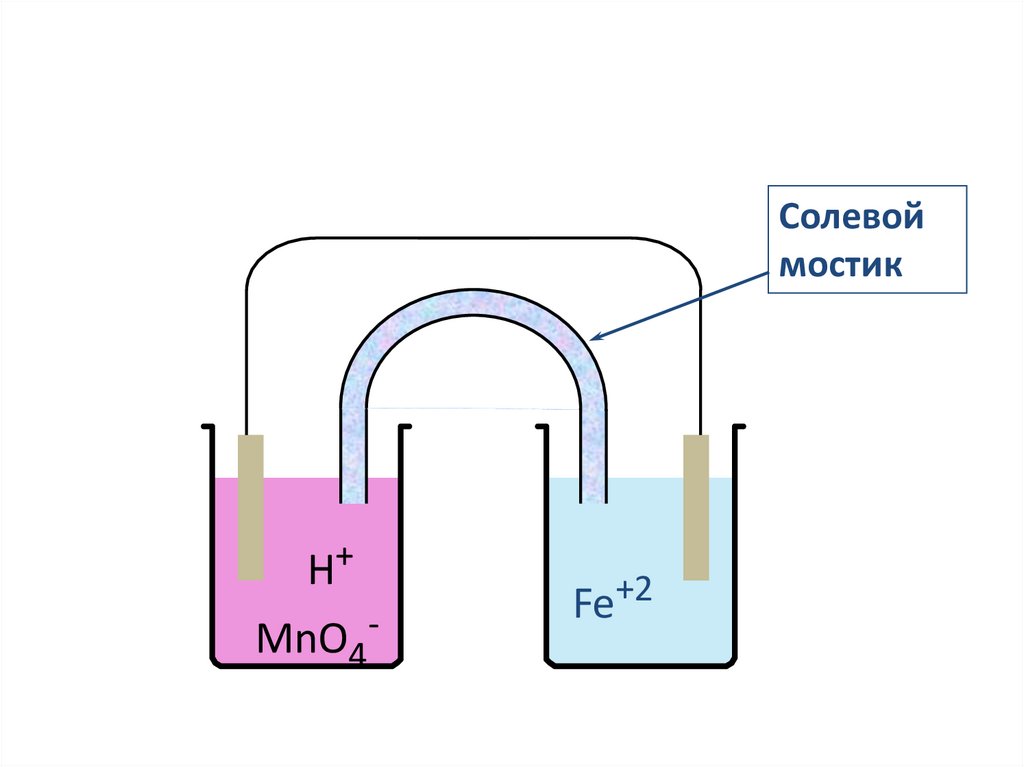

 Образование
Образование








