Похожие презентации:
Химические реакции в окружающей среде
1.
Химические реакции вокружающей среде.
Информационно – познавательное внеклассное
мероприятие из цикла
«Химия вокруг нас»
Подготовила учитель химии
МБОУ СОШ № 24
Волосатова И.В.
2.
Цель: сформировать у обучающихся убеждения вединстве и познаваемости мира, привить любовь к
химии, к профессии.
3.
Химия вокруг нас• Явления, при которых одни вещества
превращаются в другие, называют химическими
явлениями или химическими реакциями.
• Химические явления (реакции) могут протекать
- с выделением газа,
- образованием или растворением осадка,
- выделением или поглощением теплоты
- выделением света,
- изменением цвета и вкуса,
- появлением запаха.
4.
Химические реакции в природе. ГорениеС6Н10 О5 + 6 О2 = 6 СО2 + 5Н2 О + Q
• Процесс горения происходит
при участии кислорода,
который содержится в воздухе.
• Сгорая, древесина переходит в
газообразное состояние СО2
подобно тому, как вода при
нагревании превращается в пар,
образуется древесный уголь.
• Реакция сопровождается
выделением теплоты и света.
5.
Химические реакции в природе.Фотосинтез
6 СО2 + 6Н2 О = С6 Н 12 О6 + 6 О2
• Вследствие фотосинтеза
ежегодно из атмосферы
поглощается около
300 млрд. т углекислого
газа,
выделяется 200 млрд. т
кислорода и образуется
150 млрд. т органических
веществ.
6.
Химические реакции в природе. Грозы.Кислотные дожди.
N2 + О2 = 2 NО
t = 2000-2500˚С
2 NО + О2 = 2 NO2
(при избытке кислорода)
4 NO2 + 2H2O + О2 = 4 Н NO3
(во время дождя)
7.
Химические реакции в природе. Коррозия (ржавление )металлов.
• Слово коррозия
происходит от
латинского слова
corrodere, что означает
разъедать.
Коррозией называют
самопроизвольный
процесс разрушения
материалов и изделий
из них под химическим
воздействием
окружающей среды.
8.
Химические реакции в природе. Коррозия• Коррозии подвергаются
не только металлы, но и
камни ( известняки,
мрамор), полимеры,
древесина.
• В настоящее время
особое беспокойство
вызывают состояние
старинных зданий,
скульптур,
выполненных из камня,
которые разрушаются от
кислотных дождей.
9.
Коррозия4Fe + 3O2 = Fe2O3 • H2O
ржавчина
• Сущность процесса
коррозии сводится к
окислению металлов , т.е.
превращению металлов
в оксиды.
• В роли окислителя
выступают O2. Cl2, SO2 ,
CO2.
10.
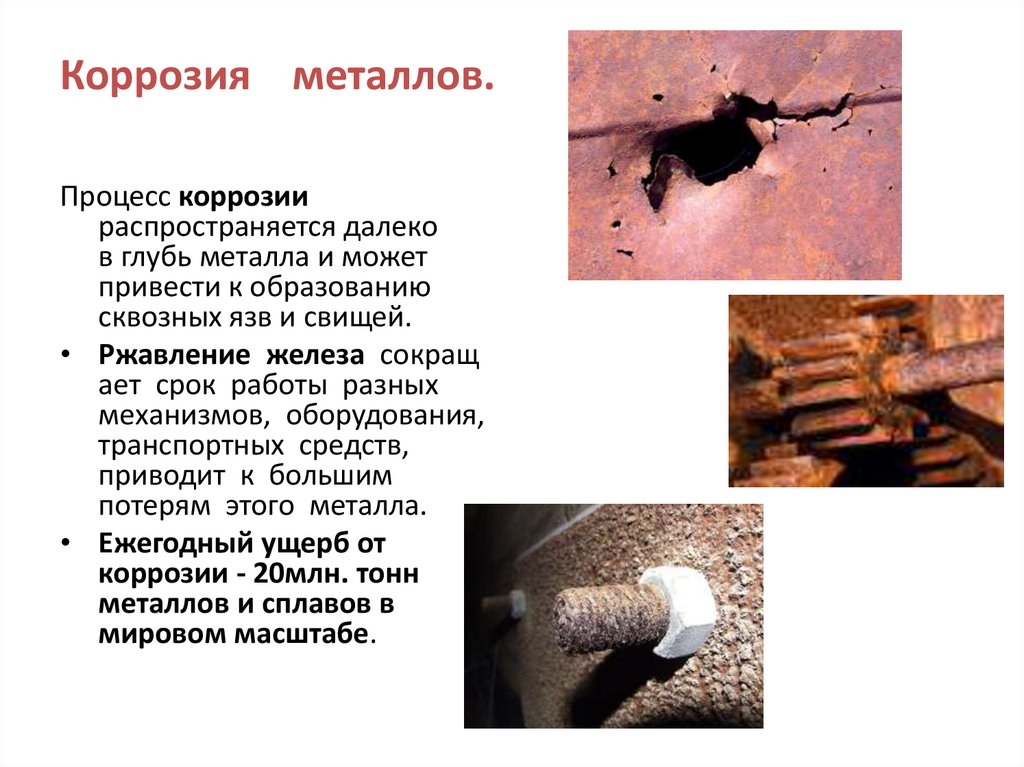
Коррозия металлов.Процесс коррозии
распространяется далеко
в глубь металла и может
привести к образованию
сквозных язв и свищей.
• Ржавление железа сокращ
ает срок работы разных
механизмов, оборудования,
транспортных средств,
приводит к большим
потерям этого металла.
• Ежегодный ущерб от
коррозии - 20млн. тонн
металлов и сплавов в
мировом масштабе.
11.
Химические реакции в природе. Коррозия(ржавление ) металлов
• Эйфелева башня - символ
Парижа неизлечимо
больна – она изготовлена
из обычной стали и
неотвратимо ржавеет и
разрушается, и только
постоянная химическая
обработка помогает
бороться с этим
смертельным недугом:
Эйфелеву башню красили
уже много раз отчего ее
масса 9000 т каждый
раз увеличивалась на 70
тонн










 Химия
Химия








