Похожие презентации:
Енергетичний стан поверхні. Сорбційні явища. Мезопористі матеріали
1. Лекція №8. Енергетичний стан поверхні. Сорбційні явища. Мезопористі матеріали
22.04.152.
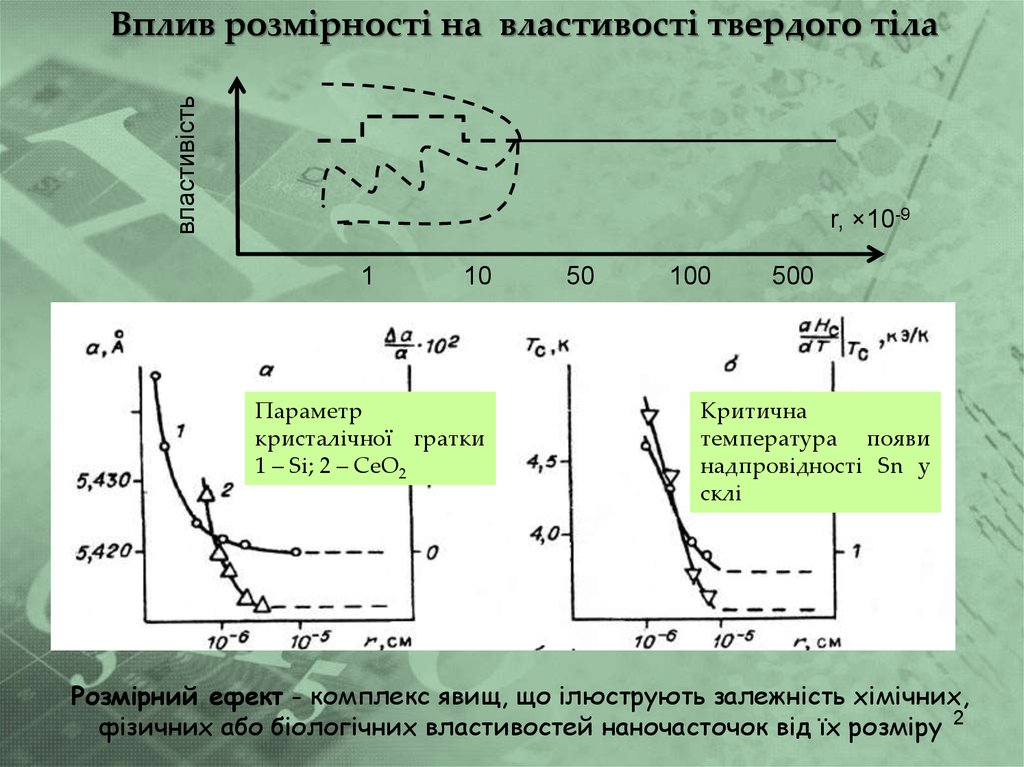
властивістьВплив розмірності на властивості твердого тіла
r, ×10-9
1
10
Параметр
кристалічної гратки
1 – Si; 2 – CeO2
50
100
500
Критична
температура появи
надпровідності Sn у
склі
Розмірний ефект - комплекс явищ, що ілюструють залежність хімічних,
фізичних або біологічних властивостей наночасточок від їх розміру 2
3. Поверхневі явища: роль межі поділу
Сферичначасточка
кубічна
часточка
3
D
R
6
D
R
3
Питома
поверхня
дисперсність
4. Принципи дослідження матеріалів
СкладБудова
дисперсність
Властивості
Термодинаміка поверхневих явищ
Метод
надлишкових
величин Гіббса
Метод шару
кінцевої
товщини
4
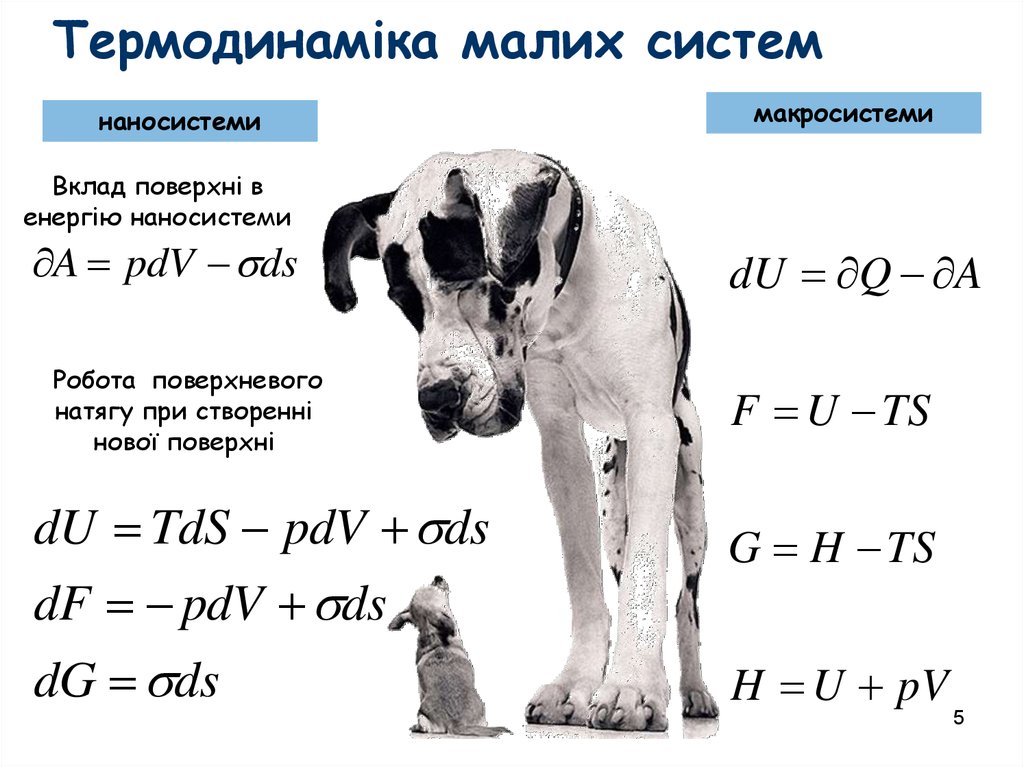
5. Термодинаміка малих систем
наносистемимакросистеми
Вклад поверхні в
енергію наносистеми
A pdV ds
Робота поверхневого
натягу при створенні
нової поверхні
dU Q A
F U TS
dU TdS pdV ds
dF pdV ds
G H TS
dG ds
H U pV
5
6. Другий закон термодинаміки для наносистем
Фактори ускладнення опису:-Вклад флуктуацій;
-Складнощі реалізації другого
закону термодинаміки
-Зникнення різниці між фазовими
переходами;
6
7. Фазові рівноваги
тискрідина
Тверде
тіло
температура
F F
1
2
F F F F
1
1
s
2
2
s
Сила поверхневого натягу: pout
2
d ( s) d (4 r ) 8 rdr
Внутрішній тиск:
4 r 2 pinner
4 r pout 4 r pinner 8 r
2
Рівняння Лапласа:
2
pinner pout p 2 / r
7
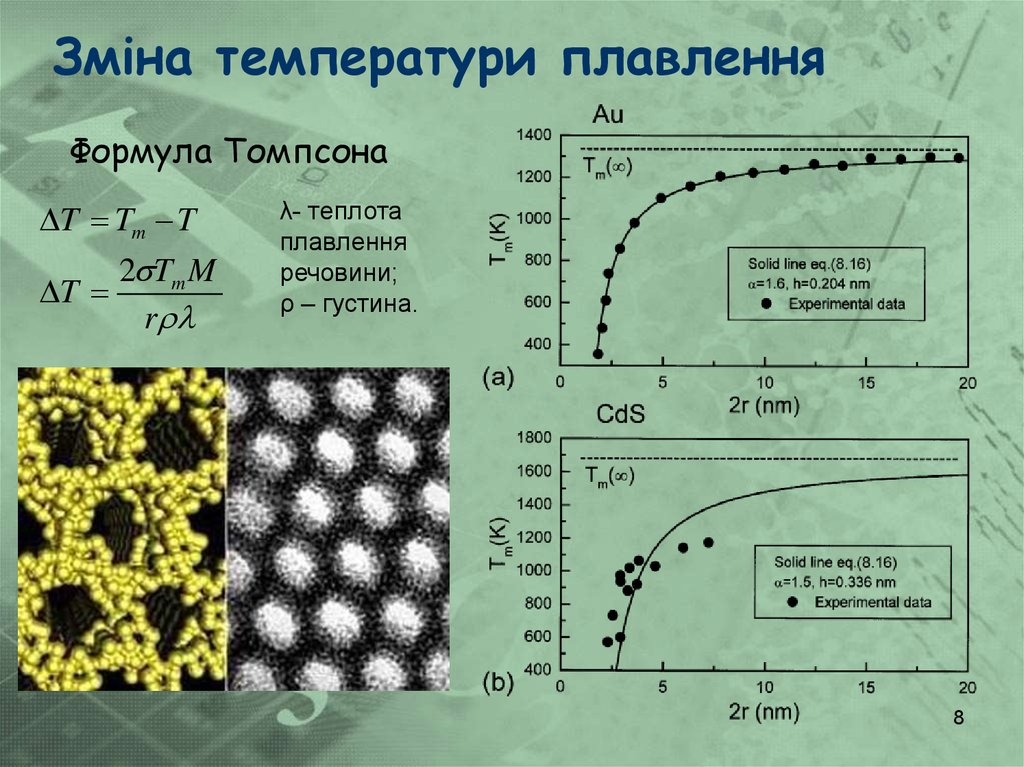
8. Зміна температури плавлення
Формула ТомпсонаT Tm T
2 Tm M
T
r
λ- теплота
плавлення
речовини;
ρ – густина.
8
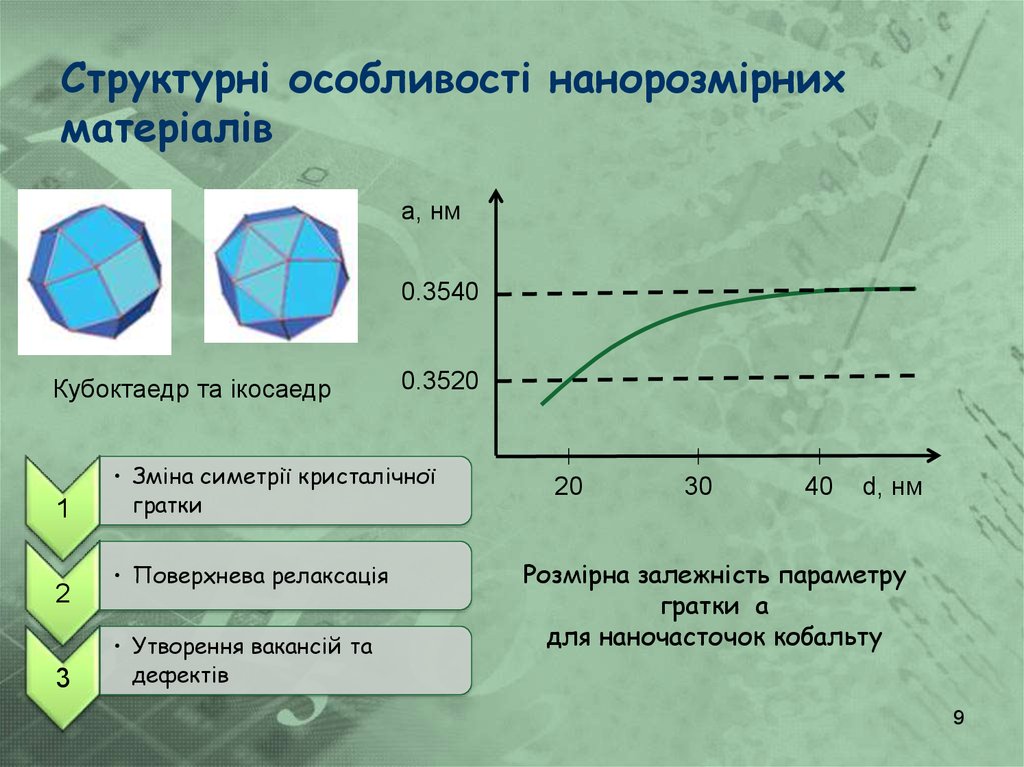
9. Структурні особливості нанорозмірних матеріалів
а, нм0.3540
Кубоктаедр та ікосаедр
1
2
3
0.3520
• Зміна симетрії кристалічної
гратки
• Поверхнева релаксація
• Утворення вакансій та
дефектів
20
30
40
d, нм
Розмірна залежність параметру
гратки а
для наночасточок кобальту
9
10. Вакансійний розмірний ефект
Концентрація вакансій:Еv = kTпл
Зміна концентрації вакансій від розміру
наночасточок золота при 300 К
10
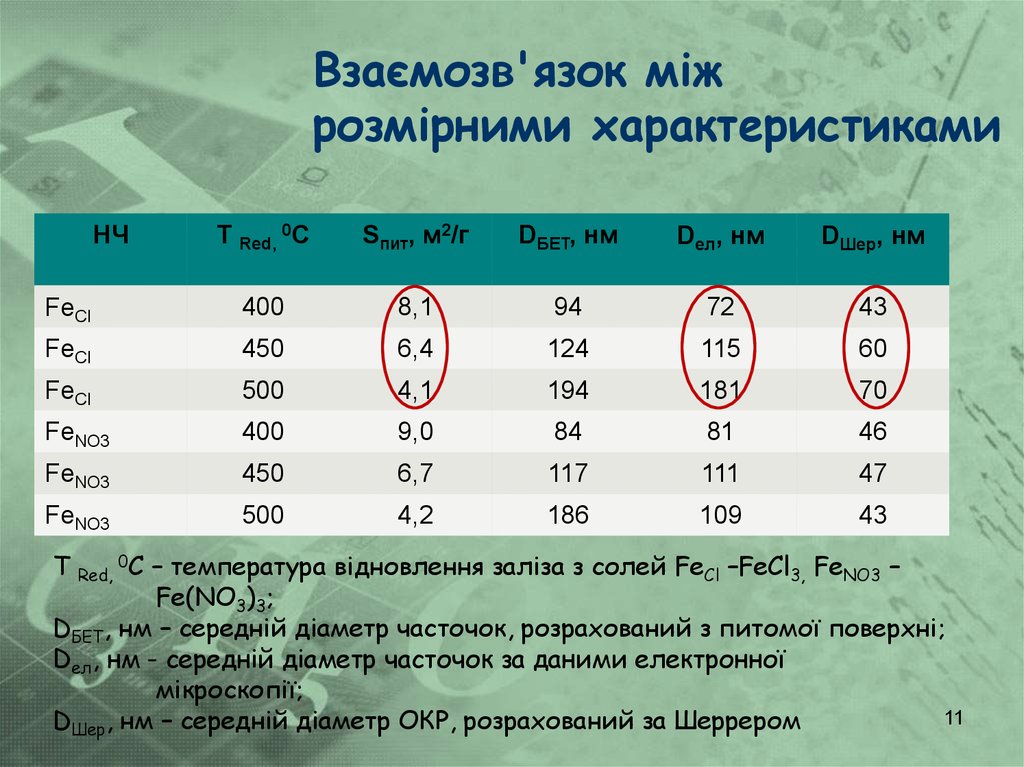
11. Взаємозв'язок між розмірними характеристиками
НЧТ Red, 0C
Sпит, м2/г
DБЕТ, нм
Dел, нм
DШер, нм
FeCl
400
8,1
94
72
43
FeCl
450
6,4
124
115
60
FeCl
500
4,1
194
181
70
FeNO3
400
9,0
84
81
46
FeNO3
450
6,7
117
111
47
FeNO3
500
4,2
186
109
43
Т
– температура відновлення заліза з солей FeCl –FeCl3, FeNO3 –
Fe(NO3)3;
DБЕТ, нм – cередній діаметр часточок, розрахований з питомої поверхні;
Dел, нм - cередній діаметр часточок за даними електронної
мікроскопії;
11
DШер, нм – середній діаметр ОКР, розрахований за Шеррером
Red,
0C
12.
концентрування речовини наповерхні розділу фаз
поглинання речовини, що
веде до її накопичення в
об’ємі іншої речовини
сукупна дія адсорбції і
абсорбції
адсорбція – зв’язування
молекул на межі розділу фаз за
рахунок “слабких” зв’язків
Оборотній
процес
Зменшення тиску або
концентрації адсорбату
- десорбція
адсорбція – адсорбція з
утворенням хімічних зв’язків.
Необоротній
процес
тиск або концентрація
впливають на десорбції
12
13.
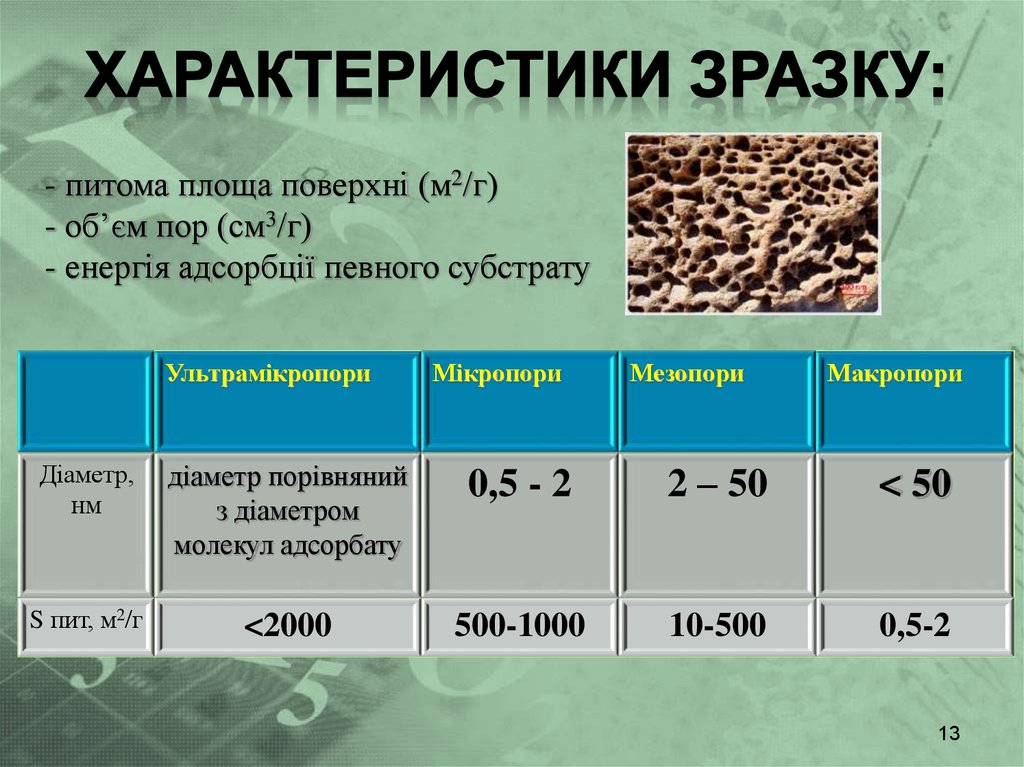
- питома площа поверхні (м2/г)- об’єм пор (см3/г)
- енергія адсорбції певного субстрату
Ультрамікропори
Мікропори
Мезопори
Макропори
Діаметр,
нм
діаметр порівняний
з діаметром
молекул адсорбату
0,5 - 2
2 – 50
< 50
S пит, м2/г
<2000
500-1000
10-500
0,5-2
13
14.
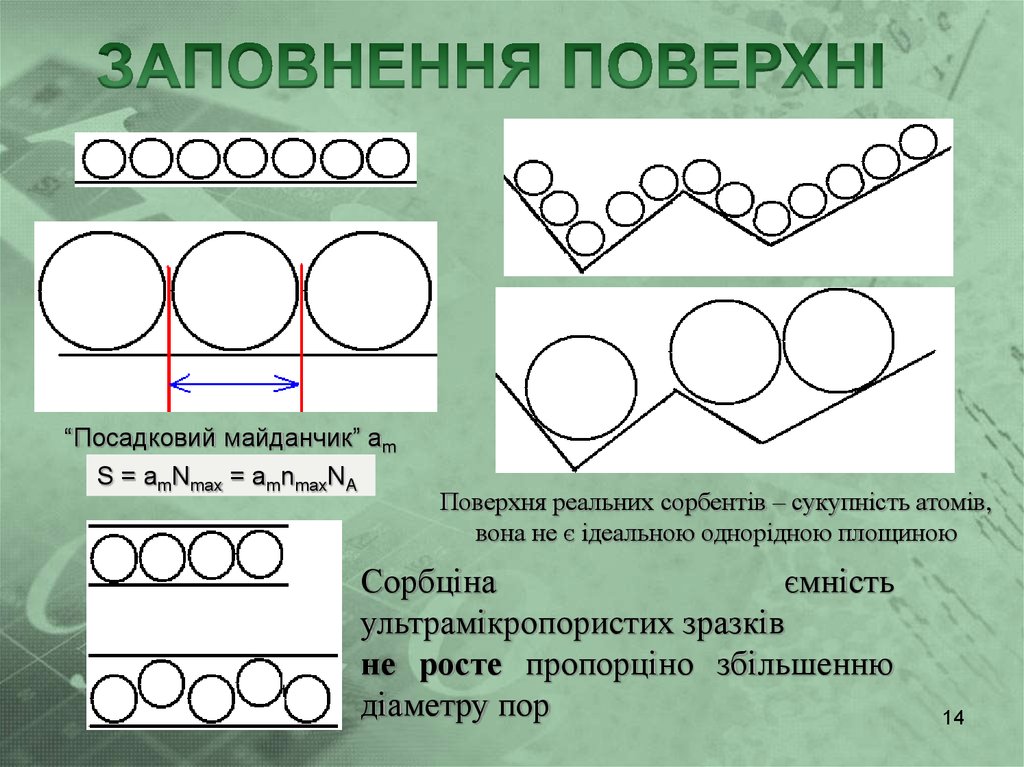
“Посадковий майданчик” amS = amNmax = amnmaxNA
Поверхня реальних сорбентів – сукупність атомів,
вона не є ідеальною однорідною площиною
Сорбціна
ємність
ультрамікропористих зразків
не росте пропорціно збільшенню
діаметру пор
14
15.
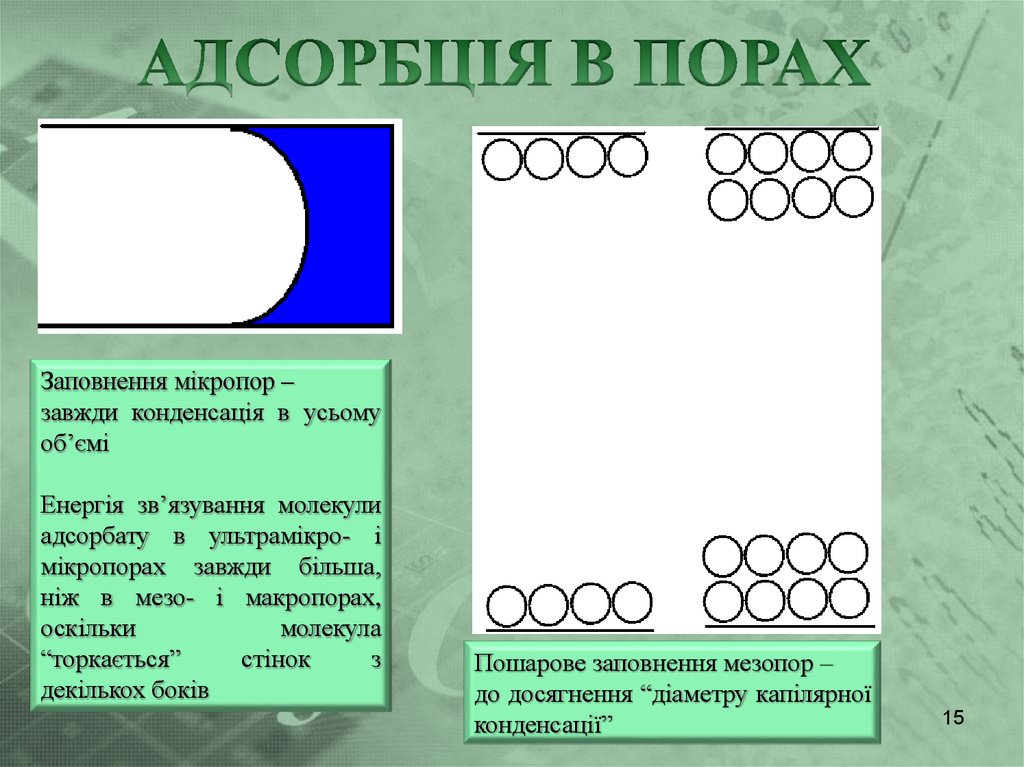
Заповнення мікропор –завжди конденсація в усьому
об’ємі
Енергія зв’язування молекули
адсорбату в ультрамікро- і
мікропорах завжди більша,
ніж в мезо- і макропорах,
оскільки
молекула
“торкається”
стінок
з
декількох боків
Пошарове заповнення мезопор –
до досягнення “діаметру капілярної
конденсації”
15
16.
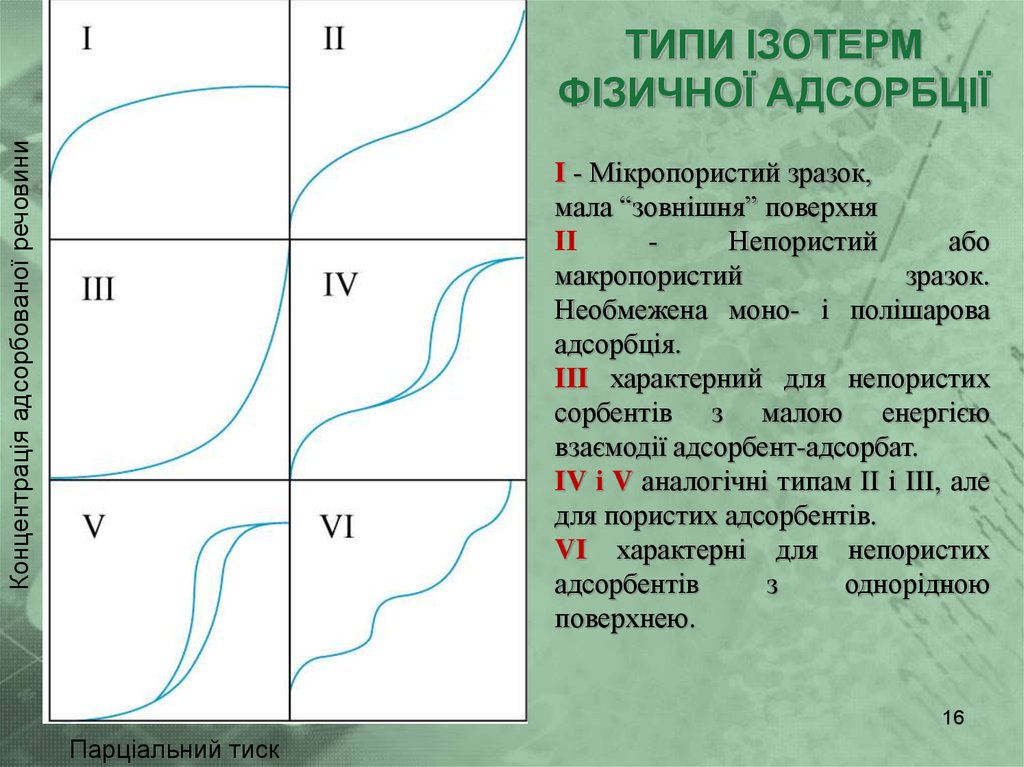
Концентрація адсорбованої речовиниТИПИ ІЗОТЕРМ
ФІЗИЧНОЇ АДСОРБЦІЇ
I - Мікропористий зразок,
мала “зовнішня” поверхня
II
Непористий
або
макропористий
зразок.
Необмежена моно- і полішарова
адсорбція.
III характерний для непористих
сорбентів з малою енергією
взаємодії адсорбент-адсорбат.
IV і V аналогічні типам II і III, але
для пористих адсорбентів.
VI характерні для непористих
адсорбентів
з
однорідною
поверхнею.
16
Парціальний тиск
17.
Модель - (а)з азотом (б);
вода на поверхні та в порі (в)
В суміші з етанолом (д)
17
18.
Матеріа Маса, гл
Pd
LaNi5
вугілля
0,223
1,058
0,742
графіт
НТ
0,898
0,121
Кількіст
ь H2, %
0,66
0,13
1,63
4,52
11,3?
Нанотрубки після
термічної десорбції
водню
18
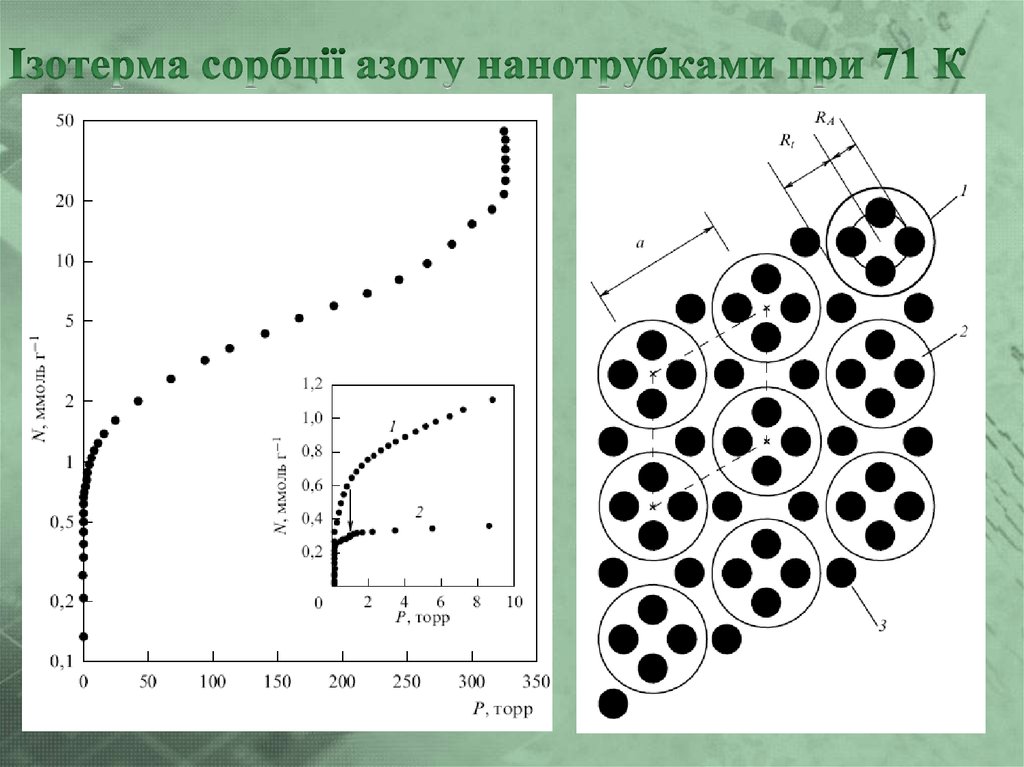
19. Ізотерма сорбції азоту нанотрубками при 71 К
1920. Сорбція водню вуглецевими матеріалами
МатеріалМаксимальна
ємність,
Т, K
мас.%
Тиск
водню,
МПа
8,25
5—10
4,2
Одностінні НТ
3,5
6,5—7
11—66
Графітове нановолокно
10—12
Графітове нановолокно + K 14
80
133
300
77—300
300
300
373
473—673
7,18
0,04
10—12
5—10
0,1
11
11
0,1
Графітове нановолокно + Li 20
473—673 0,1
20
21. Короткі нотатки:
Розвинута поверхня наносистем є однією з ключовихпричин виникнення розмірних ефектів.
Для
опису
термодинамічних
параметрів
розраховують
вклад
поверхневої
енергії
(поверхневого натягу). Для цього використовують
метод надлишкових величин Гіббса та метод шару
кінцевої товщини.
До
розмірних
ефектів
зумовлених
вкладом
поверхневих сил відносять зменшення температури
плавлення, зменшення параметрів кристалічної
гратки та зростання кількості приповерхневих
дефектів.
21
22. Література:
1.2.
3.
4.
5.
Родунер Э. Размерные эффекты в наноматериаллах. М.:
Техносфера – 2010 – 352с.
Рыжонков Д.И. Левина В.В., Дзидзигуги Э.Л., Наноматериаллы:
учебное пособие. М.: БИНОМ, - 2010 –с.106-237.
Л.В. Адамова. Процессы на поверхности раздела фаз.
Екатеринбург – 2007.
И. П. Суздалев, В. Н. Буравцев, Ю. В. Максимов, В. К. Имшенник,С.
В. Новичихин, В. В. Матвеев, А. С. Плачинда // Размерные
эффекты и межкластерные взаимодействия в наносистемах - Рос.
хим. ж. (Ж. Рос. хим. об-ва им. Д.И. Менделеева), 2001, т. XLV, №
3
Ю.С. Нечаев О природе, кинетике и предельных значениях
сорбции водорода углеродными наноструктурами // УФН – 2006 №6.
22












 Химия
Химия








