Похожие презентации:
Основи. Склад, назви, класифікація, використання
1.
ДЕВІЗ УРОКУ :НАВЧАЄМОСЯ НЕ ЗАРАДИ
ШКОЛИ, А ЗАДЛЯ ЖИТТЯ …
СЕНЕКА
(давньоримський філософ)
2. Тема: Основи: склад, назви, класифікація, використання
Мета уроку:вивчити склад основ,навчитися складати формули основ,
давати
назву
основам
за
їх
формулами,
зʼясувати
фізичні
властивості основ та їх використання.
3. Вправа “Третій зайвий”
.Вправа “Третій зайвий”
1. MgO, CO2, O2
2. SO2, SiO2, CuO
3. Al2O3, FeO, NO2
4. Na2O, SiO2, K2O
5. NO2, CO2, SO3 р
4. Вправа “Виправ помилку”
Al3O2, Fe2O,Ca2O, SO4,
MgO2, Na3O, BaO3
5. Загальна формула основ
nМе(ОН)n
Основи – це складні речовини, в
яких атоми металів з’єднані з
гідроксогрупою.
6. НАЗВИ ГІДРОКСИДІВ УТВОРЮЮТЬСЯ ТАК :
назва металу+ гідроксид
NaOH - натрій гідроксид
Якщо метал має змінну валентність :
назва металу + валентність металу + гідроксид
Fe(OH)3 ферум ( ІІІ ) гідроксид
7. СКЛАДІТЬ ФОРМУЛИ ГІДРОКСИДІВ:
алюміній гідроксиду,калій гідроксиду,
магній гідроксиду,
ферум (ІІІ) гідроксиду,
станум (ІІ) гідроксиду,
барій гідроксиду,
цинк гідроксиду,
плюмбум (ІІ) гідроксиду,
купрум (ІІ) гідроксиду.
8. Правильні відповіді
Al(OH)3 – алюміній гідроксидKOH –
калій гідроксид
Mg(OH)2 – магній гідроксид
Fe(OH)3 – ферум(ІІІ) гідроксид
Sn(OH)2 – станум (ІІ) гідроксид
Ba(OH)2 – барій гідроксид
Zn(OH)2 – цинк гідроксид
Pb(OH)2 – плюмбум (ІІ) гідроксид
Сu(OH)2 – купрум (ІІ) гідроксид
9. Фізичні властивості
ОСНОВИРозчинні -луги
Нерозчинні
-Тверді, білі, без запаху,
милкі на дотик
-.
-Тверді, різнокольорові,
без запаху, не милкі на
дотик
10. Будьте обережні!!! Потрапляння їдких лугів на шкіру призводить до опіків,
11.
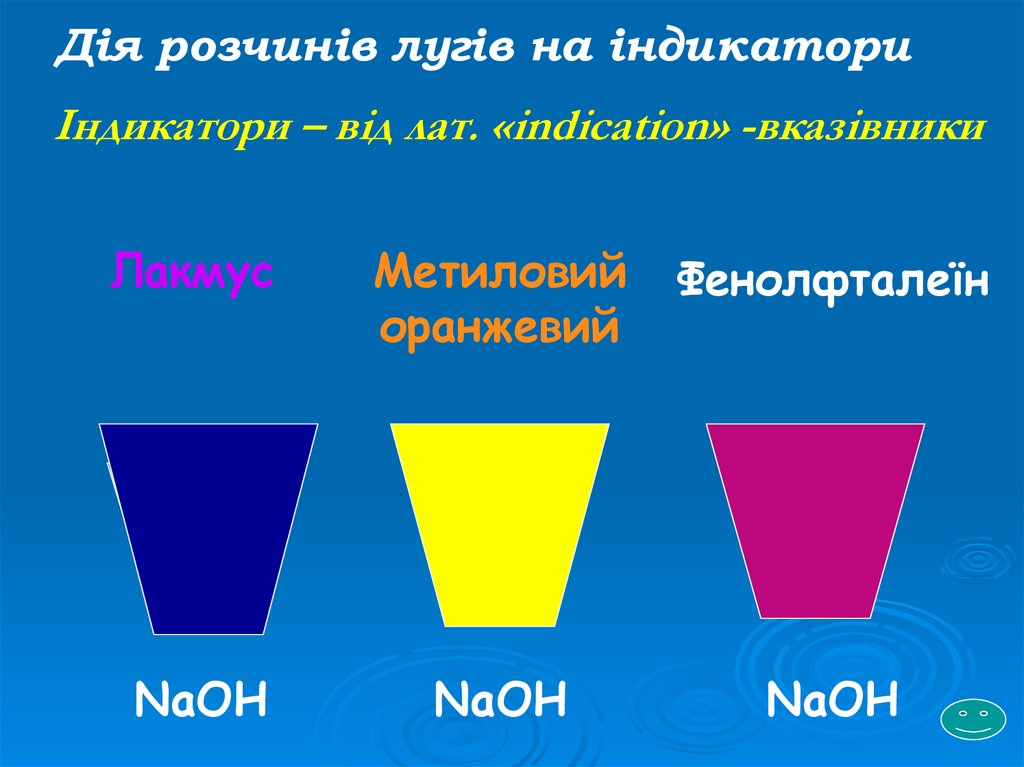
Дія розчинів лугів на індикаториІндикатори – від лат. «indication» -вказівники
Лакмус
Метиловий
оранжевий
Фенолфталеїн
NaОН
NaOH
NaOH
12. Здоровʼя – найбільше багатство
Широко хімія руки простягає,В усі сфери заглядає:
В медицину – раз,
В господарство – два,
В виробництво – три.
А ми продовжим працювати,
Щоб науку цю вивчати.
13. Використання основ:
Са(ОН)2Гашене вапно
Будівництво, цукрова
промисловість, зубні пасти,
побілка дерев.
14.
NаОНЇдкий натр
Виготовлення твердого
мила, паперу, ліків,
штучного волокна,
миючих засобів,
шкіряній
промисловості,
очищення нафти .
15.
КОН – їдке каліВиготовлення рідкого мила, електроліт.
16. LiOH –літій гідроксид
Гідроксид літію використовують для отримання солейлітію; як поглинач вуглекислого газу в протигазах,
підводних човнах і косміних кораблях.
Застосовується для наповнення лужних
акумуляторів, що збільшує срок їхньої дії,
використовується для виготовлення эмалі.
17. Mg(OH) 2
Гідроксид магнію застосовується в якості харчовоїдобавки, як добавка в миючі засоби, для отримання
оксиду магнію, рафінування цукру, в якості компоненту
зубних паст.
В медицині його використовують як лікарський
засіб для нейтралізації кислотності в шлунку.
18. Al(OH) 3
Використовується як компонент твердогореактивного палива, зубних паст, для
виробництва лакових фарб, обволікаючий та
адсорбуючий засіб у медицині
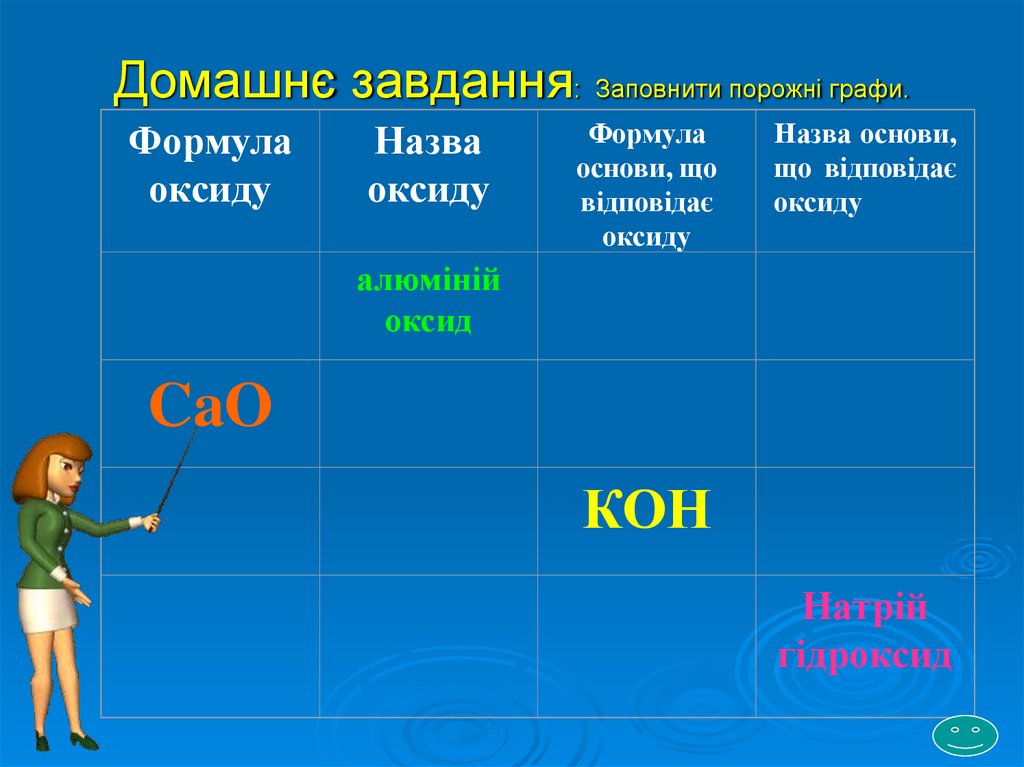
19. Домашнє завдання: Заповнити порожні графи.
Формулаоксиду
Назва
оксиду
Формула
основи, що
відповідає
оксиду
Назва основи,
що відповідає
оксиду
алюміній
оксид
CaO
КОН
Натрій
гідроксид


















 Химия
Химия








