Похожие презентации:
Углеводы
1.
2. Цели и задачи:
Повторить основные сведенья обуглеводах;
Познакомиться с наиболее ярким
представителем углеводов- глюкозой;
Отследить и установить причинно следственной связи: состав → строение →
свойства → применение → получение.
3. Установите соответствие «Класс вещества – функциональная группа»
Класс веществаФункциональная группа
1.
Многоатомные
спирты
А) Альдегидная
- COH
2. Альдегиды
Б) Карбоксильная
- COOH
3. Карбоновые
кислоты
В) Гидроксильные
- OH
4. ПРОВЕРЯЕМ «Класс вещества – функциональная группа»
Класс веществаФункциональная группа
1.
Многоатомные
спирты
В) Гидроксильные
- OH
2. Альдегиды
А) Альдегидная
- COH
3. Карбоновые
кислоты
Б) Карбоксильная
- COOH
5. Установите соответствие «Класс вещества –качественная реакция»
Название вещества /функциональная группа
Качественная реакция
1. Многоатомные
спирты
(гидроксильные)
А)
2. Альдегиды
(альдегидная)
Б)
3. Карбоновые
кислоты
(карбоксильная)
В)
Изменение окраски
метилового оранжевого.
С Cu(ОН)2, (ярко синее
окрашивание).
С Ag2O (Реакция «Серебряного
зеркала»);
С Cu(ОН)2, при нагревании
(морковный цвет).
6. ПРОВЕРЯЕМ «Класс вещества –качественная реакция»
Название вещества /функциональная группа
Качественная реакция
1. Многоатомные
спирты
(гидроксильные)
Б)
2. Альдегиды
(альдегидная)
В)
С Cu(ОН)2, (ярко синее
окрашивание).
С Ag2O (Реакция «Серебряного
зеркала»);
С Cu(ОН)2, при нагревании
(морковный цвет).
3. Карбоновые
кислоты
(карбоксильная)
А)
С металлами (выделение Н2);
Изменение окраски
индикатора.
7. ЧТО ОБЪЕДИНЯЕТ ЭТИ РАСТЕНИЯ
8. Установите соответствие «УГЛЕВОД – НАХОЖДЕНИЕ В ПРИРОДЕ»
А. Сахароза1
2
3
4
5
Б. Крахмал
В.
Целлюлоза
Г. Глюкоза
Д.
Фруктоза и
глюкоза
9. ПРОВЕРЯЕМ «УГЛЕВОД – НАХОЖДЕНИЕ В ПРИРОДЕ»
11
2
3
4
5
-Г. Глюкоза
-В.
Целлюлоза
3
-Б. Крахмал
2
4
-А. Сахароза
5
-Д. Фруктоза
и глюкоза
10. КЛАССИФИКАЦИЯ
По способности к гидролизу углеводыделятся на две группы:
1. Простые – моносахариды:
Триозы, тетрозы, пентозы
гексозы (ГЛЮКОЗА, фруктоза).
2. Сложные:
Дисахариды (сахароза).
Полисахариды (крахмал, целлюлоза)
11. ГЛЮКОЗА.
Молекулярный состав глюкозыС6Н12О6.
А как будет выглядеть
структурная формула?
УСТАНОВИМ ОСОБЕННОСТИ
СТРОЕНИЯ ГЛЮКОЗЫ?
12. ПРОГНОЗИРУЕМ:
В начале XIX века ученыеустановили формулу
глюкозы С6Н12О6.
Предположите химическое
строение глюкозы.
13.
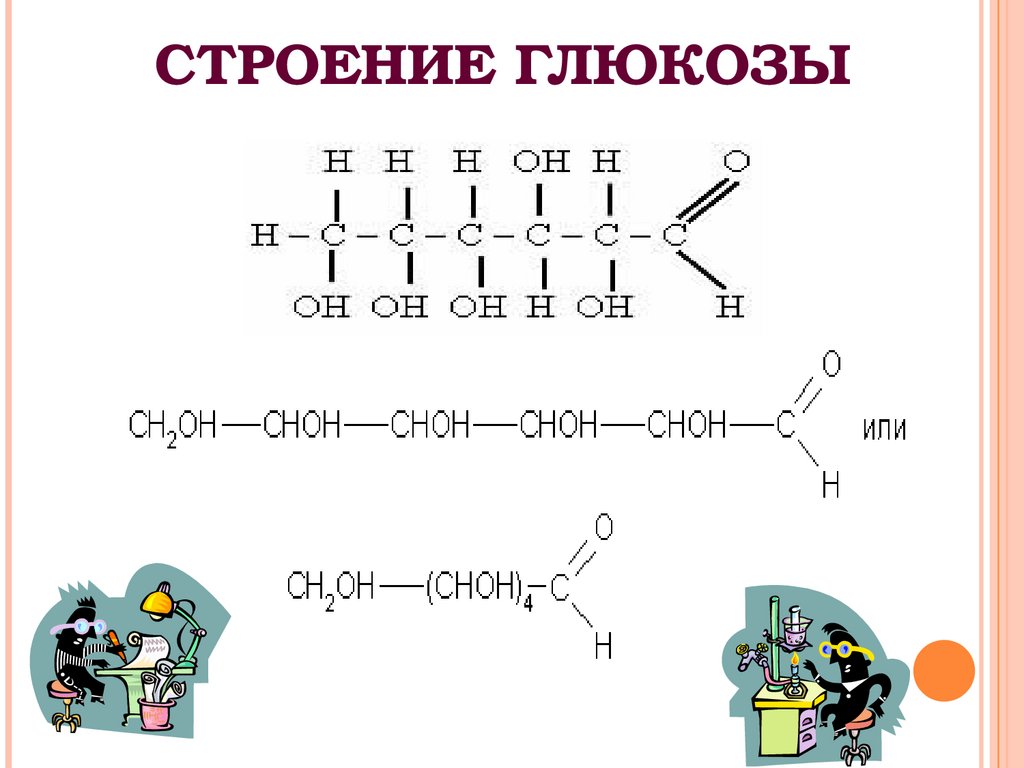
14. ГЛЮКОЗА.
Молекулярный состав глюкозыС6Н12О6.
Особенностью строения является
наличие:
альдегидной группы – СОН
(сходство с альдегидами);
пяти гидроксильных групп -ОН
(сходство с многоатомными
спиртами).
ГЛЮКОЗА – АЛЬДЕГИДОСПИРТ.
15. СТРОЕНИЕ ГЛЮКОЗЫ
16.
17. ХИМИЧЕСКИЕ СВОЙСТВА ГЛЮКОЗЫ
В связи с рассмотрением химических свойств глюкозыинтересно вспомнить эпизод из романа Валентина
Пикуля “Нечистая сила”, где идет речь о неудачной
попытке отравления Распутина в 1916 году.
“Лазоверт со скрипом натянул резиновые перчатки,
растер в порошок кристаллы цианистого калия…
Доктор щедро и густо насыщал внутренность
пирожных страшным ядом. …Распутин с неохотой
съел пирожное с ядом. Понравилось – потянулся за
вторым. Юсупов внутренне напрягся, готовый увидеть
перед собой труп. Но Распутин спокойно доедал восьмой
птифур…
Яд беспомощен! Гришка выпил и сожрал все, что
отравлено.
Герои Пикуля решили, что Григорий Распутин и
впрямь святой или заговоренный. Однако это не так.
18.
Распутина спасло то, что доктор незнал, что люди с давних времен при
опасности отравления цианидами
держали за щекой кусочек сахара. А
в 1915 году немецкие ученые Рупп и
Гольце обнаружили, что, как и
всякий альдегид, глюкоза
взаимодействует с цианидами и
циановодородом с образованием
нетоксичного циангидрин
19. РЕАКЦИИ ПО АЛЬДЕГИДНОЙ ГРУППЕ
1) Взаимодействие с аммиачнымраствором Ag2O (реакция серебренного
зеркала):
СН2ОН – (СНОН)4 – СОН + Ag2O →
→ СН2ОН – (СНОН)4 – СООН + +2Ag↓
2) Взаимодействие Cu(OH)2 (при нагревании):
СН2ОН – (СНОН)4 – СОН + 2Сu(ОН)2 →
→ СН2ОН – (СНОН)4 – СООН + Сu2О + 2Н2 О
20. РЕАКЦИИ ПО ГИДРОКСИЛЬНЫМ ГРУППАМ
Образование комплексныхсоединений синего цвета с
Сu(ОН)2 гидроксидом меди (II) –
качественная реакция на
гидроксильные группы
(многоатомные спирты).
21. РЕАКЦИИ БРОЖЕНИЯ ГЛЮКОЗЫ
а) спиртовое брожениеC6H12O6 2C2H5OH + 2CO2
б) молочнокислое брожение
C6H12O6 2CH3-CH(OH)-COOH
(молочная кислота)
22. ПОЛУЧЕНИЕ
Гидролиз крахмала(С6Н10O5)n + (n-1)H2O
nС6Н12O6
23. УСТАНОВИТЕ СООТВЕТСТВИЕ «Свойства глюкозы - применение»
1. Сладкий вкусА. При квашении
капусты, огурцов,
молока …
2. Окисление в
организме, с
выделением энергии
Б. В алкогольной
промышленности
3. Молочно – кислое
брожение
В. В кондитерской
промышленности
4. Спиртовое брожение
Г. В медицине
24. ПРОВЕРЯЕМ «Свойства глюкозы - применение»
1. Сладкий вкусВ. В кондитерской
промышленности
2. Окисление в
организме, с
выделением энергии
Г. В медицине
3. Молочно – кислое
брожение
А. При квашении
капусты, огурцов,
молока …
4. Спиртовое брожение
Б. В алкогольной
промышленности
25.
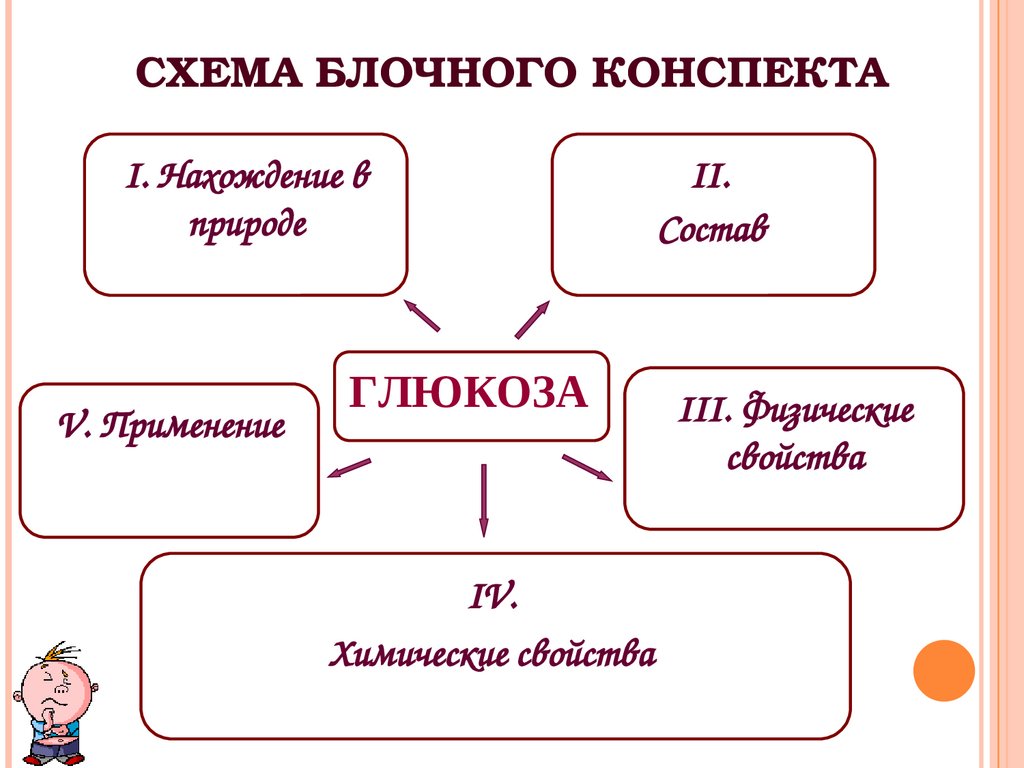
26. СХЕМА БЛОЧНОГО КОНСПЕКТА
I. Нахождение вприроде
V. Применение
ГЛЮКОЗА
IV.
Химические свойства
II.
Состав
III. Физические
свойства
27.
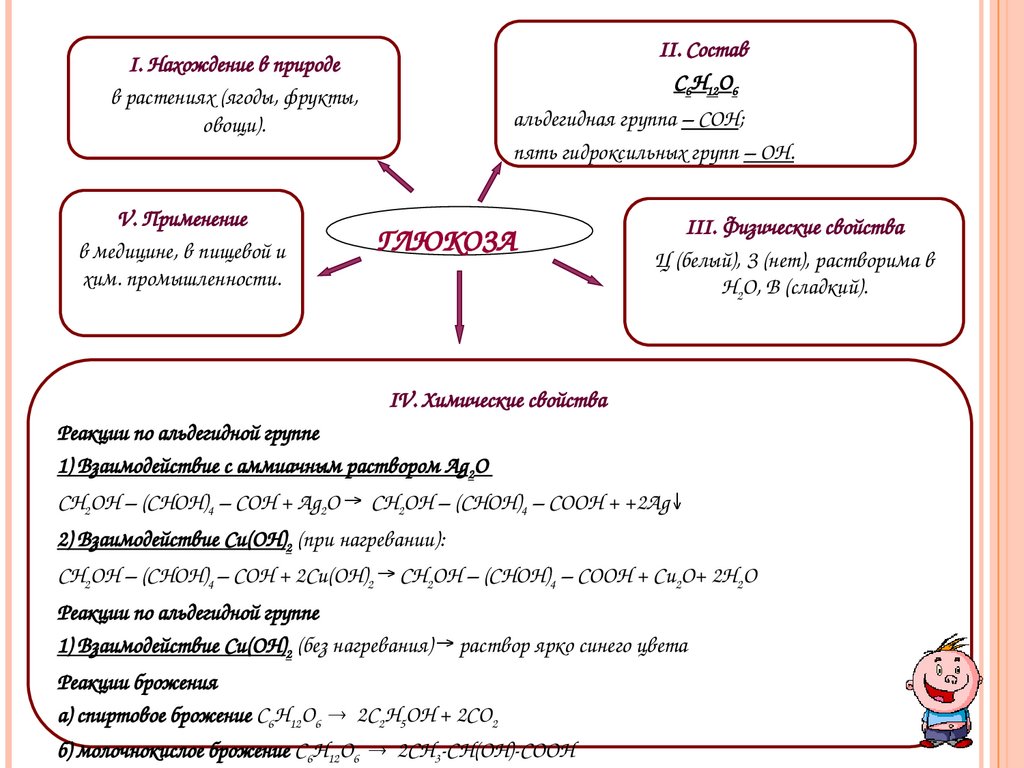
II. СоставС6Н12О6
I. Нахождение в природе
в растениях (ягоды, фрукты,
овощи).
V. Применение
в медицине, в пищевой и
хим. промышленности.
альдегидная группа – СОН;
пять гидроксильных групп – ОН.
ГЛЮКОЗА
III. Физические свойства
Ц (белый), З (нет), растворима в
Н2О, В (сладкий).
IV. Химические свойства
Реакции по альдегидной группе
1) Взаимодействие с аммиачным раствором Ag2O
СН2ОН – (СНОН)4 – СОН + Ag2O → СН2ОН – (СНОН)4 – СООН + +2Ag↓
2) Взаимодействие Cu(OH)2 (при нагревании):
СН2ОН – (СНОН)4 – СОН + 2Сu(ОН)2 → СН2ОН – (СНОН)4 – СООН + Сu2О+ 2Н2О
Реакции по альдегидной группе
1) Взаимодействие Cu(OH)2 (без нагревания) → раствор ярко синего цвета
Реакции брожения
а) спиртовое брожение C6H12O6 2C2H5OH + 2CO2
б) молочнокислое брожение C6H12O6 2CH3-CH(OH)-COOH
28. ТЕСТ «УГЛЕВОДЫ»
1. Глюкоза С6Н12О6 является:а) полисахаридом, б) дисахаридом, в)
моносахаридом.
2. Распознавание глюкозы осуществляется с
помощью:
а) йодной воды; б) раствора марганцовки, в)
аммиачного раствора оксида серебра.
3. Основными источниками углеводов являются :
а) нефть и каменный уголь; б) животные
организмы; в) растительные организмы.
4. В названных углеводов используют суффикс:
а) – овая; б) – оза; в) - аза; г) - ол
4. Как отличить растворы глюкозы и фруктозы:
а) йодной водой; б) нагреванием с раствором
оксида серебра; в) раствором хлорида железа
(III).
29. Проверяем тест
1. В, 2.В,3.В, 4. Б,5. Б30.
Я успел качественновыполнить работу!
Я молодчина!
Я хорошо подготовился к
уроку!
Я с работой не справился, в
следствии не качественной
подготовки к уроку.
На следующем уроке я буду
чувствовать себя так


























 Биология
Биология