Похожие презентации:
Молярная масса. Молярный объем газов
1.
МОЛЯРНАЯ МАССА.МОЛЯРНЫЙ ОБЪЕМ
ГАЗОВ.
2.
Молярная масса вещества –это величина, равная
отношению массы любой
порции этого вещества к его
химическому количеству.
3.
M=m/nm=M*n
n=m/M
4.
Ar =«безразмерная»
Mr = г/моль
5.
Если химическоеколичество газа увеличить,
то во столько же и возрастет
число его молекул.
6.
Отношение объема порции любого газа кего химическому количеству в этой же
порции всегда будет постоянной величиной.
Величина этого отношения будет одинакова
для любых порций любых газов, однако она
зависит от внешних условий. Эта постоянная
величина получила название молярный
объем газа и обозначается Vm.
V=n*Vm
n=V/Vm
Vm=V/n
7.
Установлено, что принормальных условиях
0
(температура 0 C и
давление 101325 Па или
101,325 кПа) Vm= 22,4
3
дм /моль.
8.
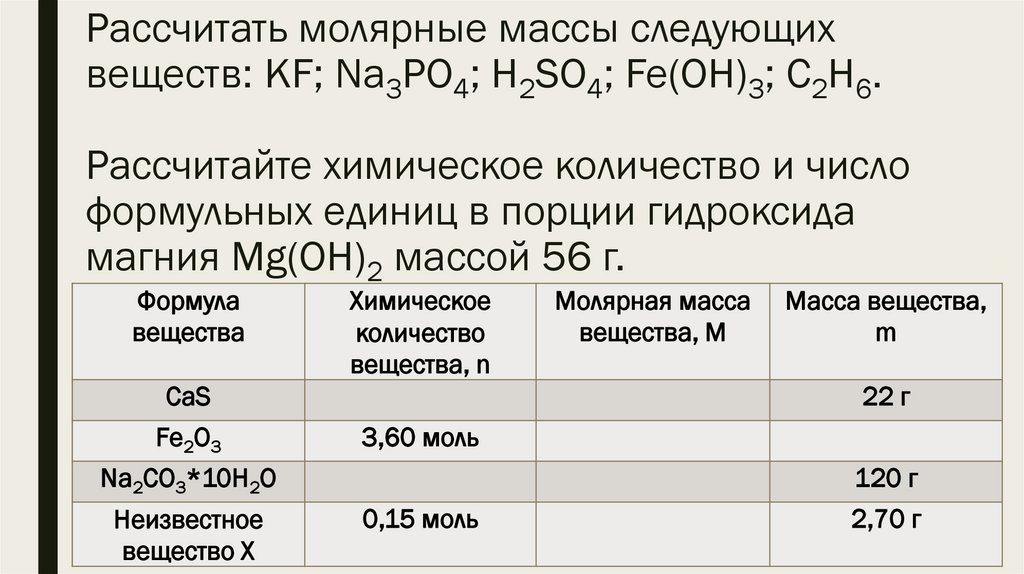
Рассчитать молярные массы следующихвеществ: KF; Na3PO4; H2SO4; Fe(OH)3; C2H6.
Рассчитайте химическое количество и число
формульных единиц в порции гидроксида
магния Mg(OH)2 массой 56 г.
Формула
вещества
Химическое
количество
вещества, n
CaS
Fe2O3
Масса вещества,
m
22 г
3,60 моль
Na2CO3*10H2O
Неизвестное
вещество Х
Молярная масса
вещества, M
120 г
0,15 моль
2,70 г
9.
Домашнее задание:Параграф 5 №2, №6
Формула
газообразного
вещества
NO2
Химическое
количество
вещества, n
2,6 моль
Объем
вещества, V
CH4
SO2
Масса
вещества, m
24 г
11,2 дм3


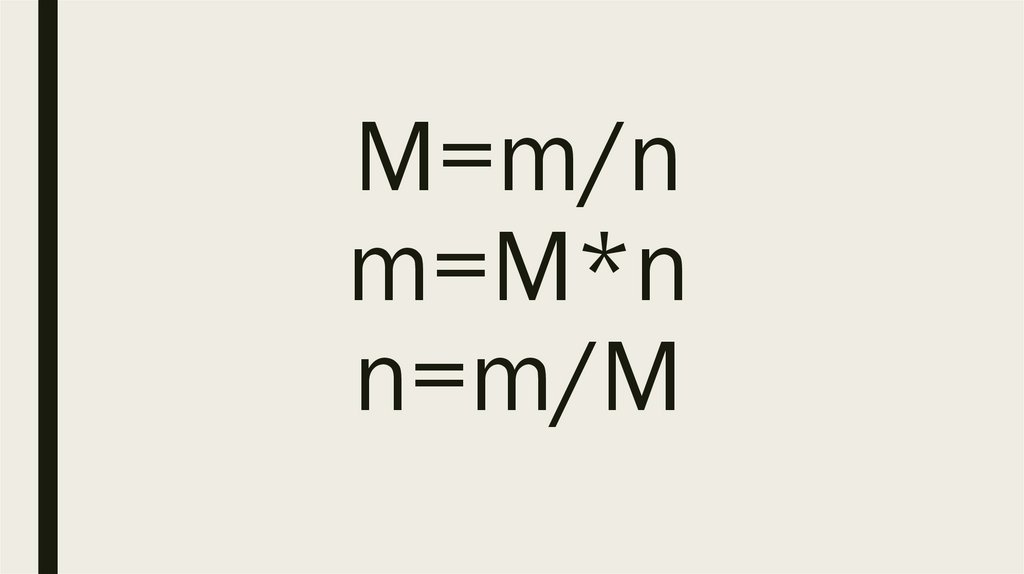






 Химия
Химия








