Похожие презентации:
Основания. Применение
1. ОСНОВАНИЯ
2. ПРИМЕНЕНИЕ
Моющиесредства
Краситель
Нашатырный
спирт
Сода
каустическая
3. Классификация оснований
Признакклассификации
Наличие кислорода
Кислотность
(число групп ОН- в составе или
число присоединяемых Н+)
Группа оснований
Пример
Кислородсодержащие
KOH, Sr(OH)2
Бескислородные
Аммиак NH3, амины
Однокислотные
NaOH, TlOH –
гидроксид таллия(I),
NH3, CH3 – NH2
Двухкислотные
Ca(OH)2, Mg(OH)2
Трехкислотные
La(OH)3, Tl(OH)3
Растворимые
NaOH, Вa(OH)2,
CH3 – NH2
Нерастворимые
Cr(OH)3, Mn(OH)3,
C6H5 NH2
Растворимость в воде
4. Классификация оснований
Признакклассификации
Степень
электролитической
диссоциации
Летучесть
Стабильность
Группа оснований
Пример
Сильные (α → 1)
LiOH - CsOH, Ca(OH)2
- Ca(OH)2, TlOH
Слабые (α → 0)
Нерастворимые
основания, NH3∙Н2О,
CH3NH2∙Н2О
Летучие
NH3, CH3 – NH2
Нелетучие
Щелочи,
нерастворимые
основания
Стабильные
NaOH, Вa(OH)2,
Нестабильные
NH3∙Н2О
5. Химические свойства растворимых оснований (щелочей)
ще
л
о
ч
и
6. Химические свойства нерастворимых оснований
Нерастворимыеоснования
7. Химические свойства бескислородных оснований
Бескислородныеоснования
8. Химические свойства оснований
ще
л
о
ч
и
Нерастворимые
основания
С кислотами
С кислотными оксидами
С кислотами
Общее свойство
основанийРазложение при t
С солями
взаимодействие с
кислотами
С кислотами
Бескислородные
основания
С водой
9.
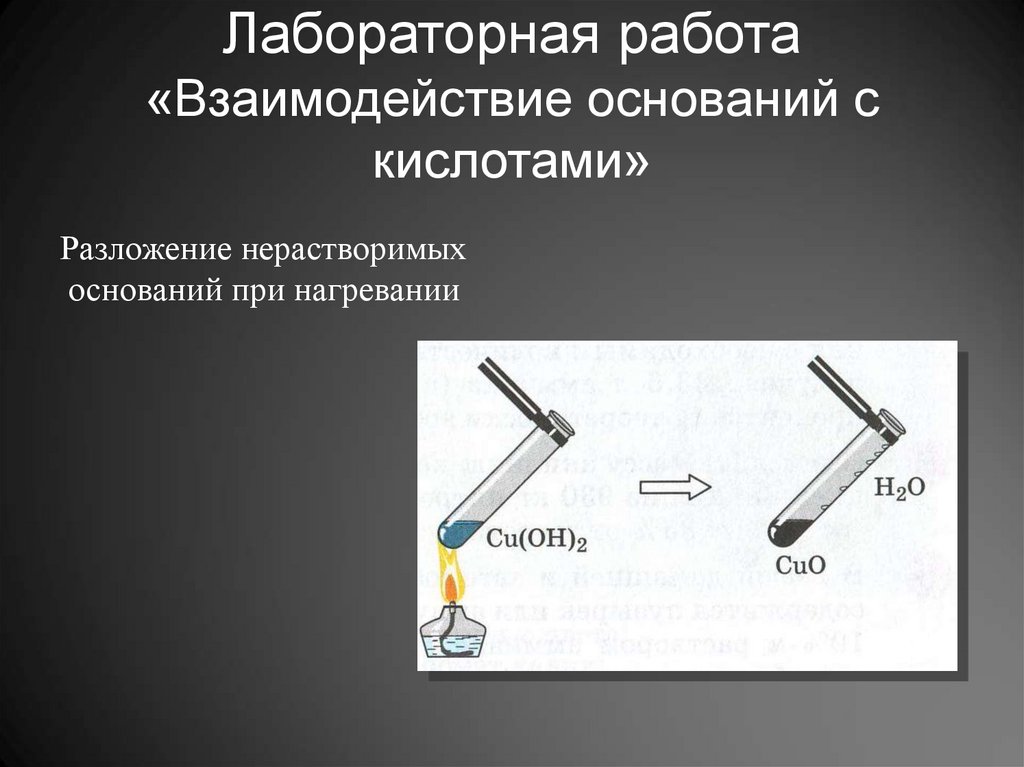
10. Лабораторная работа «Взаимодействие оснований с кислотами»
Разложение нерастворимыхоснований при нагревании
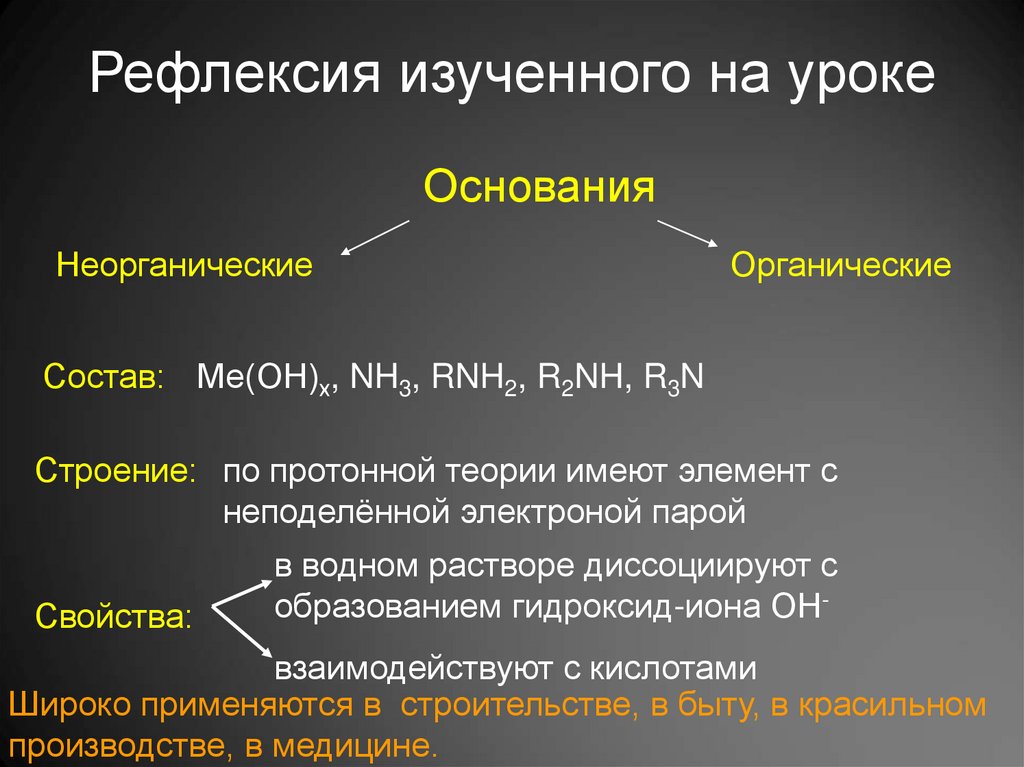
11. Рефлексия изученного на уроке
ОснованияНеорганические
Органические
Состав: Ме(ОН)х, NH3, RNH2, R2NH, R3N
Строение: по протонной теории имеют элемент с
неподелённой электроной парой
Свойства:
в водном растворе диссоциируют с
образованием гидроксид-иона ОН-
взаимодействуют с кислотами
Широко применяются в строительстве, в быту, в красильном
производстве, в медицине.








 Химия
Химия








