Похожие презентации:
Электрофорез как метод разделения
1.
Электрофорез какметод разделения
Хрусталева А.А.
2.
Электрохимические методыанализа
• — группа методов количественного химического анализа, основанные на
использовании электролиза.
• Разновидностями метода являются электрогравиметрический анализ
(электроанализ), внутренний электролиз, контактный обмен металлов
(цементация), полярографический анализ, кулонометрия и др.
• Электрогравиметрический анализ основан на взвешивании вещества,
выделяющемся на одном из электродов. Метод позволяет не только
проводить количественные определения меди, никеля, свинца и др., но и
разделять смеси веществ.
• Кроме того, к электрохимическим методам анализа относят методы,
основанные на измерении электропроводности (кондуктометрия) или
потенциала электрода (потенциометрия).
• Некоторые электрохимические методы применяются для нахождения
конечной точки титрования (амперометрическое
титрование, кондуктометрическое титрование, потенциометрическое
титрование, кулонометрическое титрование).
3.
Понятие об электрофорезеЭлектрофорез – один из наиболее распространенных методов
молекулярной биологии и биохимии, используемый для разделения
биологических полимерных молекул, таких как нуклеиновые кислоты
и белки, а также их фрагментов
Электрофорез впервые открыто профессорами Московского
университета П. И. Страховым и Ф. Ф. Рейссом в 1809 году.
Термин "электрофорез" состоит из двух частей – "электро" и "форез",
где "электро" означает электрический ток, а "форез" переводится с
греческого как перенос.
4.
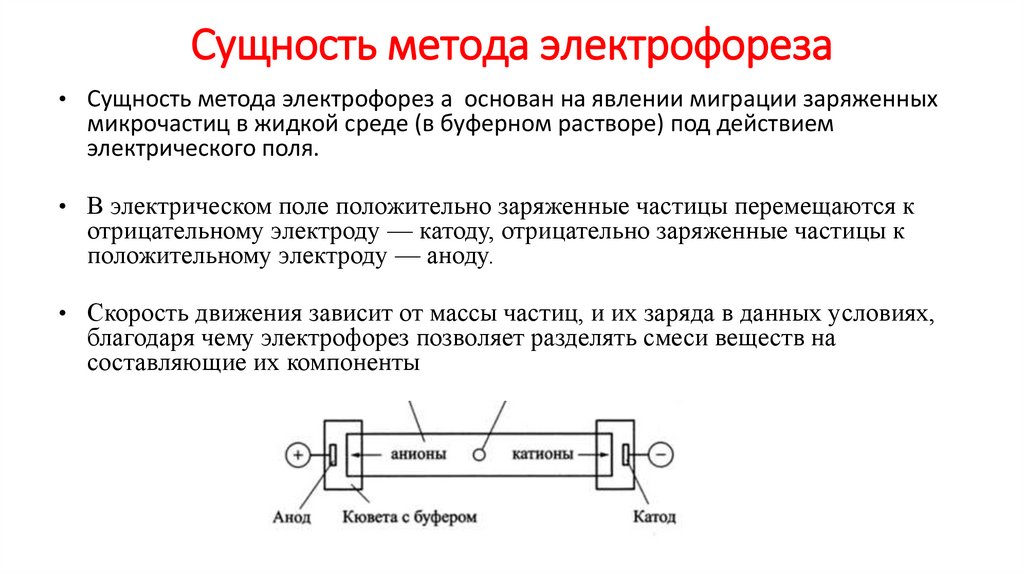
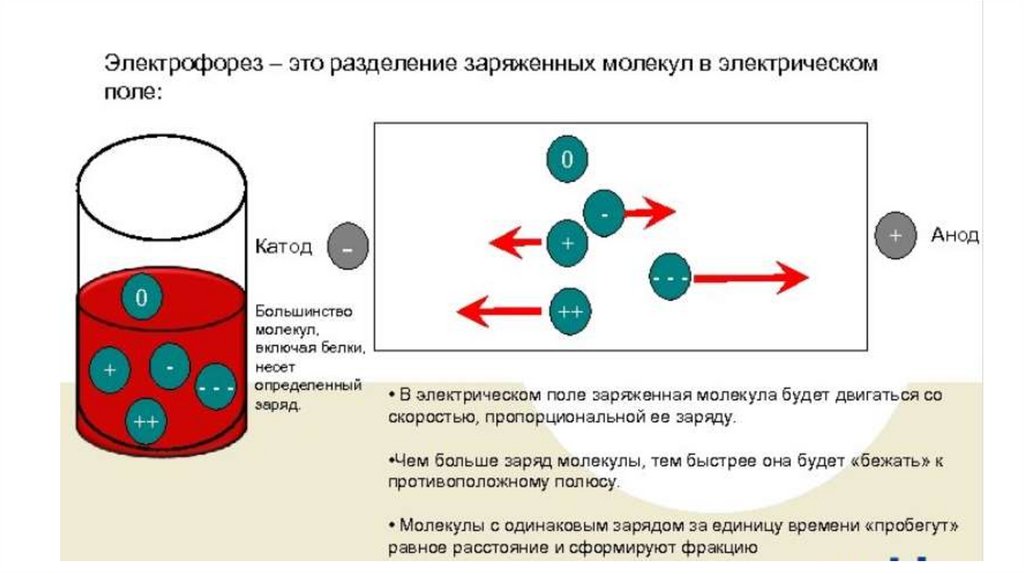
Сущность метода электрофореза• Сущность метода электрофорез а основан на явлении миграции заряженных
микрочастиц в жидкой среде (в буферном растворе) под действием
электрического поля.
• В электрическом поле положительно заряженные частицы перемещаются к
отрицательному электроду — катоду, отрицательно заряженные частицы к
положительному электроду — аноду.
• Скорость движения зависит от массы частиц, и их заряда в данных условиях,
благодаря чему электрофорез позволяет разделять смеси веществ на
составляющие их компоненты
5.
6.
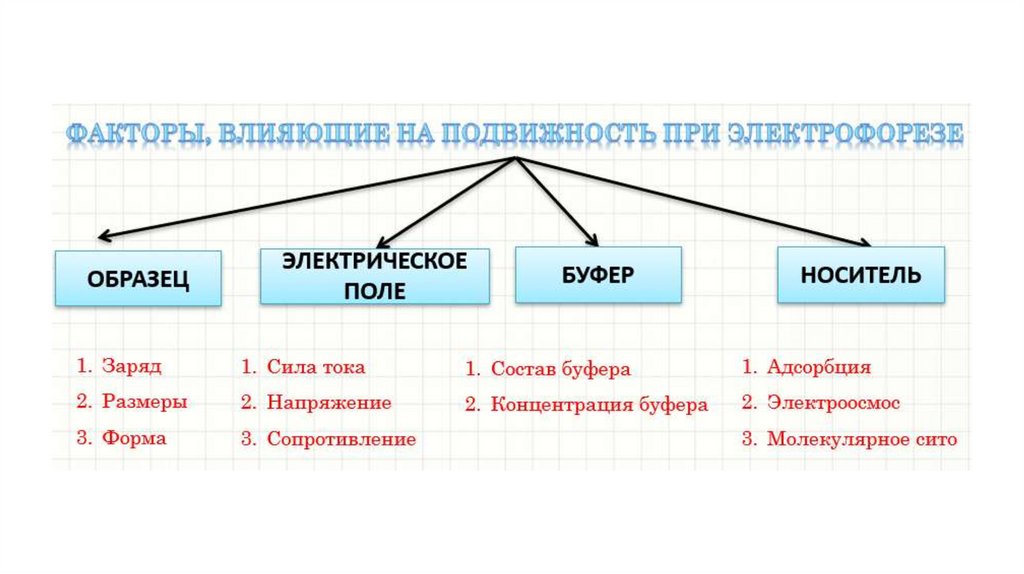
Принципы классификации электрофореза1.В зависимости от цели различают:
-Аналитический электрофорез – разделение смеси веществ с целью
их качественного и количественного анализа;
• -Препаративный электрофорез – разделение с последующим
выделением фракций для их участия в конкретных биохимических
процессах.
2.В зависимости от заряда источника тока различают:
• -катафорез — когда обрабатываемая поверхность имеет
отрицательный электрический заряд (то есть подключена к
отрицательному контакту источника тока) и
• -анафорез — когда заряд поверхности положительный.
7.
3.По степени денатурации разделяемых белковразличают:
нативный электрофорез и
электрофорез в денатурирующих условиях
В отличие от нативного электрофореза , электрофорез в
денатурирующих условиях предполагает применение химических
реагентов , разрушающих пространственную структуру
разделяемых белков..
8.
• 4. В зависимости от носителя электрофорез может быть:• без носителя,
• на фильтровальной бумаге,
• на пленках из ацетата из целлюлозы,
• в крахмальном геле,
• в агаровом и агарозном гелях,
• в полиакриламидном геле.
5.В зависимости от ориентации носителя (геля, бумаги, др.)
• вертикальным
• горизонтальным.
9.
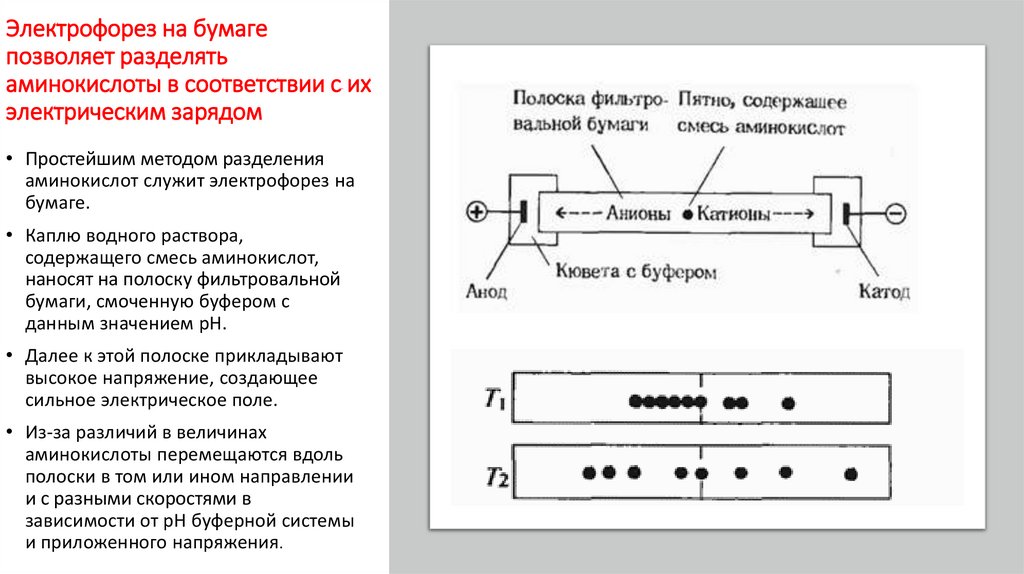
Электрофорез на бумагепозволяет разделять
аминокислоты в соответствии с их
электрическим зарядом
• Простейшим методом разделения
аминокислот служит электрофорез на
бумаге.
• Каплю водного раствора,
содержащего смесь аминокислот,
наносят на полоску фильтровальной
бумаги, смоченную буфером с
данным значением pH.
• Далее к этой полоске прикладывают
высокое напряжение, создающее
сильное электрическое поле.
• Из-за различий в величинах
аминокислоты перемещаются вдоль
полоски в том или ином направлении
и с разными скоростями в
зависимости от pH буферной системы
и приложенного напряжения.
10.
Разделение аминокислот методомэлектрофореза на бумаге.
• На полоску бумаги наносят каплю раствора, содержащего смесь аминокислот.
• Ей дают высохнуть, после чего эту полоску бумаги смачивают буфером с заданным
значением pH и помешают между охлаждающими пластинами.
• Концы полоски погружают в кюветы с электродами и включают высокое
напряжение.
• В возникающем при этом постоянном электрическом поле аминокислоты
разделяются в соответствии с их суммарным электрическим зарядом при выбранном
pH.
• Аминокислоты, которые при этом значении pH представляют собой катионы,
мигрируют к катоду (отрицательному полюсу), а аминокислоты, имеющие форму
анионов, перемещаются к аноду (положительному полюсу), как это показано на
схеме, изображающей электрофореграмму в момент времени .
• В конце процесса бумагу высушивают, опрыскивают нингидрином и нагревают, в
результате чего на бумаге проступают пятна, соответствующие расположению
различных аминокислот, которые можно идентифицировать путем сравнения их
положения с положением аутентичных аминокислот, используемых в качестве
«свидетелей».
11.
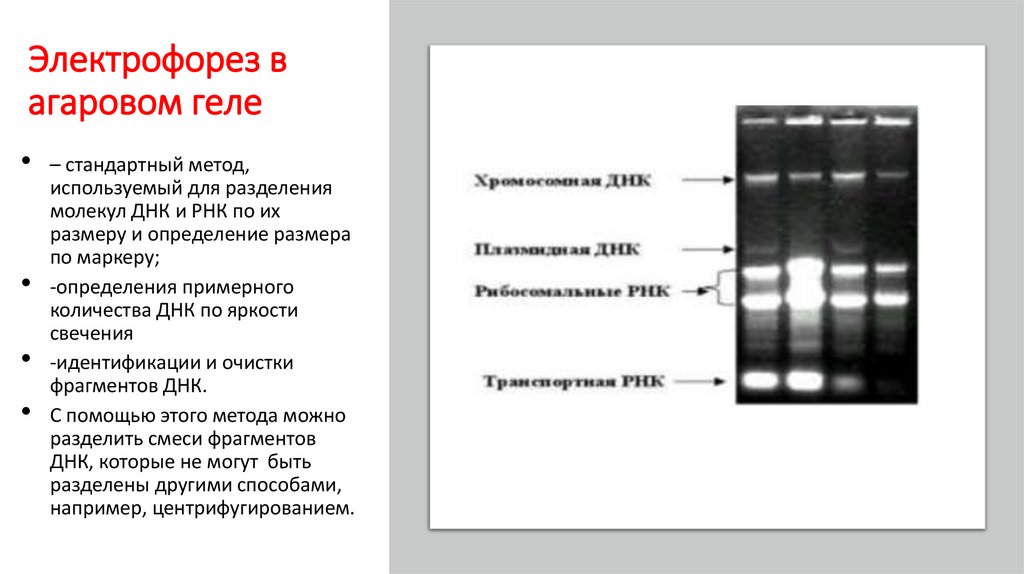
Электрофорез вагаровом геле
• – стандартный метод,
используемый для разделения
молекул ДНК и РНК по их
размеру и определение размера
по маркеру;
-определения примерного
количества ДНК по яркости
свечения
-идентификации и очистки
фрагментов ДНК.
С помощью этого метода можно
разделить смеси фрагментов
ДНК, которые не могут быть
разделены другими способами,
например, центрифугированием.
12.
Разделение фрагментов ДНК происходит из-за наличия у них заряда.Фосфатные остатки у нуклеотидов придают всей ДНК отрицательный заряд.
Это делает ее растворимой в воде и привлекает ее к положительному(+)
электроду.
Поэтому, если поместить ДНК в электрическое поле, то она будет двигаться
от минуса к плюсу. Чтобы ДНК не сильно бежала к плюсам, ее можно
перемещать в какой-нибудь вязкой среде. Для этого и нужен агарозный гель
(что-то очень похожее по консистенции на холодец или желе)
13.
Скорость миграции ДНК через агарозный гель при электрофорезе определяется
5 главными параметрами:
- размерами молекул ДНК. Фрагменты ДНК, имеющие наименьшие размеры
приближаются быстрее всего к + электроду, в то время как фрагменты более
большие остаются максимально близко к минусу;
- концентрацией агарозы. Увеличение концентрации агарозы в геле уменьшает
скорость миграции днк и позволяет разделять малые фрагменты днк;
- напряженности электрического поля. Чем больше напряжение тем быстрее
проходит форез но слишком сильное напряжение нагреет буфер а это недопустимо;
-конформации ДНК. Кольцевые плазмиды(неразрезанные рестриктазами)
двигаются с другой скоростью чем линейные или суперскрученные. ДНК, имеющие
одинаковую молекулярную массу, но разные конформации перемещаются в
электрическом поле с разными скоростями;
-состав оснований ДНК и температуры (слабо зависит). Обычно электрофорез
проводят при комнатной температуре.
Те же базовые принципы электрофореза могут использоваться для разделения РНК и
протеинов
14.
15.
16.
17.
18.
19.
20.
21.
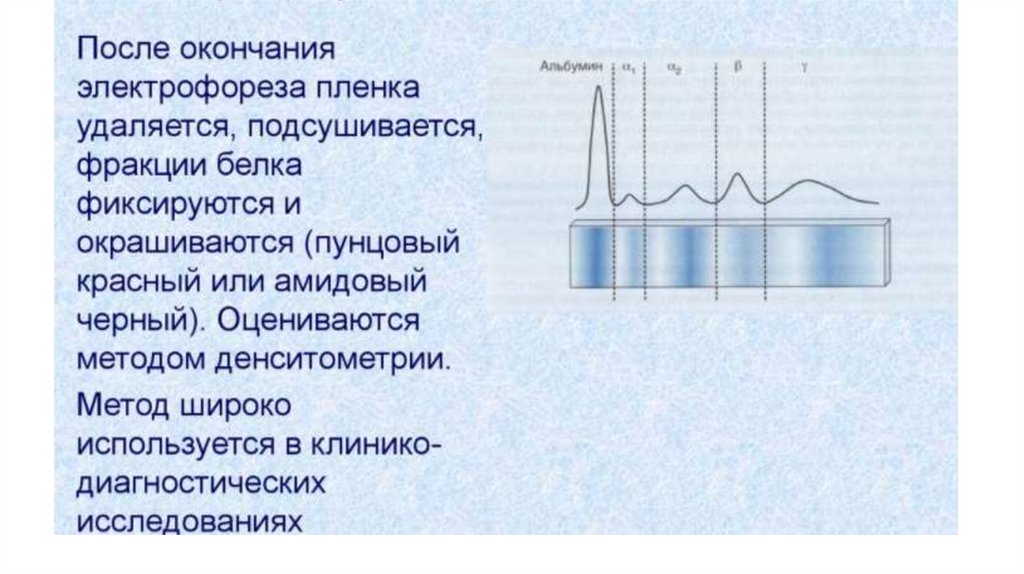
В фармации для определения чистоты лекарственныхпрепаратов используется тонкослойный электрофорез на
высокодисперсных адсорбентах или гель––электрофорез.
Для разделения антибиотиков, смеси лекарственных веществ в
лекарственных формах используется зональный свободный
электрофорез и электрофорез в поддерживающих средах.
Электрофорез на бумаге, агаровом или крахмальном геле
применяется для очистки, разделения и выделения
лекарственных веществ и биологически активных соединений.





















 Биология
Биология Химия
Химия








