Похожие презентации:
Дыхательная функция крови. Кислотно-основное состояние организма
1.
2.
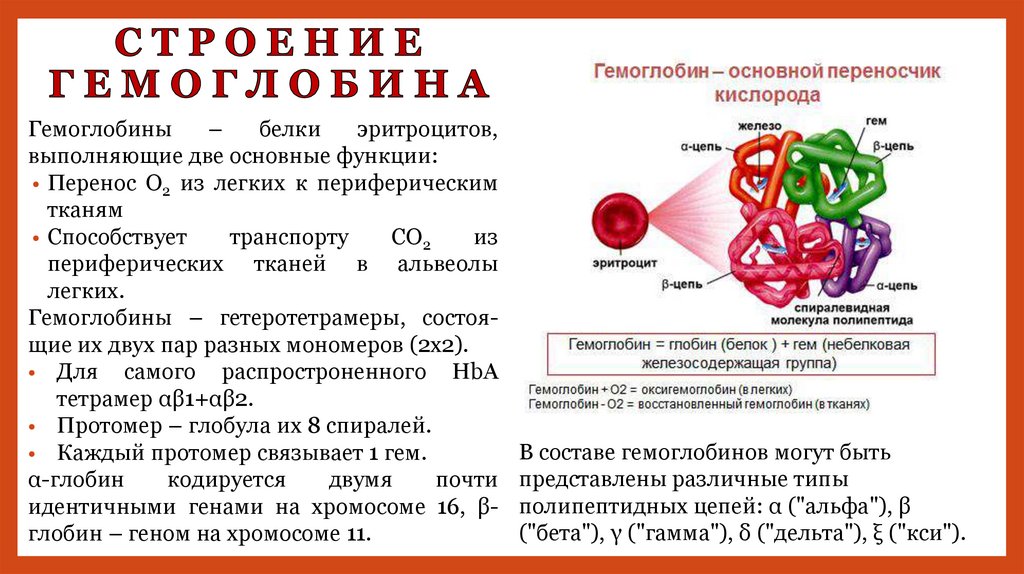
Гемоглобины–
белки
эритроцитов,
выполняющие две основные функции:
• Перенос О2 из легких к периферическим
тканям
• Способствует
транспорту
СО2
из
периферических тканей в альвеолы
легких.
Гемоглобины – гетеротетрамеры, состоящие их двух пар разных мономеров (2х2).
• Для самого распростроненного НbА
тетрамер αβ1+αβ2.
• Протомер – глобула их 8 спиралей.
• Каждый протомер связывает 1 гем.
α-глобин
кодируется
двумя
почти
идентичными генами на хромосоме 16, βглобин – геном на хромосоме 11.
В составе гемоглобинов могут быть
представлены различные типы
полипептидных цепей: α ("альфа"), β
("бета"), γ ("гамма"), δ ("дельта"), ξ ("кси").
3.
• Гем(железосодержащая часть) соединяется с белковой субъединицей через
остаток гистидина координационной связью железа, а также через гидрофобные
связи пиррольных колец и гидрофобных аминокислот.
• Гем располагается как бы в гидрофобном «кармане» своей цепи.
4.
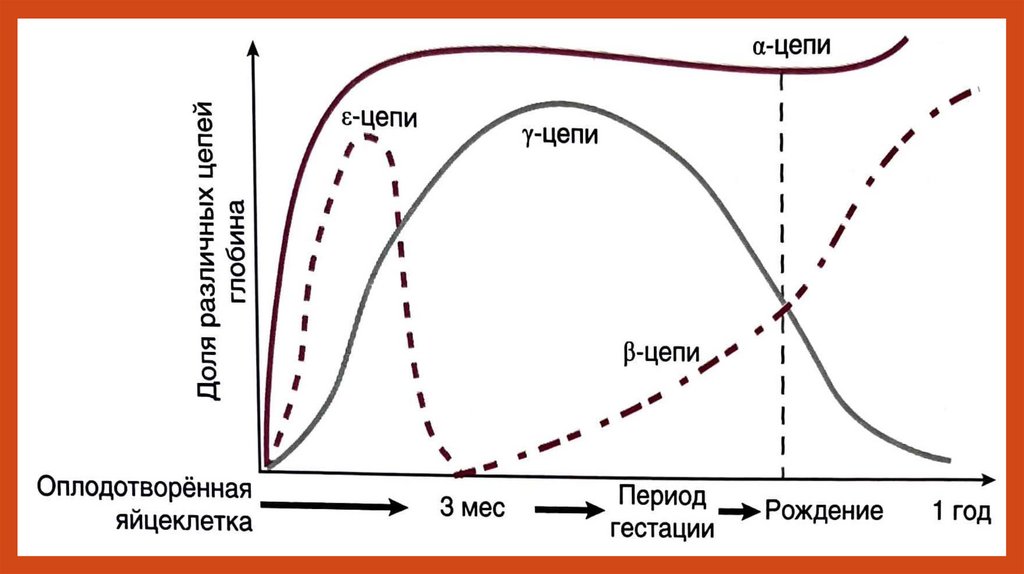
Существует несколько нормальных вариантов гемоглобина:• Говер 1 – примитивный гемоглобин, содержит 2ζ- и 2ε-цепи, первый гемоглобин
эмбриона.
• Говер 2 (HbР) – примитивный гемоглобин, содержит 2ξ- и 2ε-цепи, образуется на
7-12 неделях гестации.
• Портланд I и II – «минорные» эмбриональные гемоглобины (2ζ- и 2γ, 2ζ- и 2β).
• HbF – фетальный гемоглобин, содержит 2α- и 2γ-цепи, появляется после 12 недель
внутриутробного развития и является основным после с 3-го по 8-й месяц гемтации.
• HbA – основной гемоглобин взрослых, составляет >95% в популяции, содержит 2αи 2β-цепи.
• HbA2 – «минорный» гемоглобин взрослых, доля составляет <4% в популяции,
содержит 2α- и 2δ-цепи
• HbO2 – оксигемоглобин, образуется при связывании кислорода в легких, в
легочныхвенах его 94-98% от всего количества гемоглобина
• HbCO2 – карбогемоглобин, образуется при связывании углекислого газа в тканях, в
венозной крови составляет 15-20% от всего количества гемоглобина.
5.
– наследственные анемии, обусловленные нарушением синтеза какойлибо цепи гемоглобинаОбозначение
Типы
цепей
Патология
HbS
2α и 2βS
Серповидно-клеточная анемия. Замена в 6-м положении β-цепи
глутамата на валин.
HbС
2α и 2βС
Замена в 6-м положении β-цепи глутамата на лизин. Склонность к
гемолизу
HbЕ
2α и 2βЕ
Замена в 26-м положении β-цепи глутамата на валин. Склонность к
гемолитической анемии, риск β-талассемии.
HbJ
2αJ и 2β
Замена аланина в 120 положении α-цепи на глутамат.
HbD
2α и 2βD
Повышенный риск α-талассемии.
HbН
4β
Тетрамер β-цепей, α-талассемия.
Hb
Бартс
4γ
Тетрамер γ-цепей, α-талассемия. Обладает крайне высокой
связывающей способностью кислорода, вследствие чего не отдает
кислород тканям.
6.
- форма гемоглобина, включающая Fe3+ вместо Fe2+.Образуется под действием нитритов и нитратов, лекарственных препаратов
(сульфаниламидов), при недостаточности аскорбиновой кислоты. Не способен
связывать кислород. Для восстановления ионов железа в клинике используют
аскорбиновую кислоту и метиленовую синь.
- образуется при связывании гемоглобина с СО
(угарный газ) во вдыхаемом воздухе. Сродство СО к гемоглобину примерно в 200
раз выше, чем у кислорода. Карбоксигемоглобин не способен переносить кислород
к тканям организма. отравление СО может привести к летальному исходу.
– гемоглобин, который неферментно
связался с глюкозой. Его концентрация нарастает при хронической гипергликемии
и является хорошим скрининговым показателем патологического повышения
уровня глюкозы крови за последние 3 – 4 месяца длительный период времени. В
норме составляет < 5,7% общего гемоглобина, > 6,5% - сахарный диабет.
7.
протомеров гемоглобина реализуется как взаимовлияниесубъединиц друг на друга.
При присоединении первой молекулы кислорода к железу (за счет 6-й координационной связи) атом
железа втягивается в плоскость гема, кислород остается вне плоскости. Это вызывает перемещение
участка белковой цепи и изменение конформации первого протомера. Такой измененный протомер
влияет на другие субъединицы и облегчает связывание кислорода со второй субъединицей. Это меняет
конформацию второй субъединицы, облегчая присоединение последующих молекул кислорода и
изменение других протомеров. Четвертая молекула О2 присоединяется в 300 раз легче, чем первая.
8.
Кооперативность работы протомеров можно наблюдать и на кривой диссоциации. Кривая диссоциацияпоказывает насколько гемоглобин насыщен кислородом при определенном значении парциального
давления крови.
– изменение сродства гемоглобина к
кислороду при локальном изменении рН.
Происходит это в тканях с высоким уровнем
метаболизма.
Высокая
концентрация
СО2
превышает локальную концентрацию протонов,
понижая сродство гемоглобина к кислороду.
Кислород легче высвобождается в тканях.
При снижении рН (закислении среды) сродство
НЬ к О2 снижается и кривая смещается вправо.
При
повышении
рН
(защелачивании)
увеличивается сродство НЬ к О2 и кривая
смещается влево.
9.
При снижении температуры отдача О2 оксигемоглобином снижается (сродство повышается,кривая смещается влево), а при ее увеличении ускоряется этот процесс (сродство снижается,
кривая смещается вправо).
2,3-Дифосфоглицерат образуется в эритроцитах из 1,3-дифосфоглицерата, промежуточного
метаболита гликолиза. При снижении концентрации кислорода в эритроцитах повышается
содержание 2,3-ДФГ. Он располагается в центральной полости тетрамера дезоксигемоглобина
и связывается с β-цепями. Функция 2,3-ДФГ заключается в снижении сродства гемоглобина к
кислороду. Это имеет особенное значение при подъеме на высоту, при нехватке кислорода. В
этих условиях связывание кислорода с гемоглобином в легких не нарушается, так как
концентрация его относительно высока. Однако в тканях за счет 2,3-дифосфоглицерата отдача
кислорода возрастает в 2 раза.
10.
Каждую минуту от тканей к легким переноситсяпримерно 180 мл СО2.
• Часть СО2 переносится в физически растворенном
виде (12 – 15 мл), что составляет до 7% общего СО2.
• 3 – 10 % СО2 транспортируется в виде
карбогемоглобина.
• Большая часть СО2 (80%) транспортируется в
крови в виде бикарбонат-аниона НСО3- при
участии гемоглобина эритроцитов.
Оксигемоглобин по сравнению с Н2СО3 более сильная кислота и она связана с ионом К+ (КНbО2).
В периферической капиллярах большого круга кровообращения гемоглобин эритроцитов отдает
кислород тканям КHbО2 → О2 + КHb,
его способность связывать Н+ при этом увеличивается. Одновременно в эритроцит поступает СО2.
Под влиянием карбоангидразы СО2 взаимодействует с водой с образованием угольной кислоты
Н2СО3. Возникший за счет Н2СО3 избыток протонов связывается с гемоглобином, отдавшим
кислород, а накапливающиеся анионы НСО3- выходят из эритроцита в плазму:
КHb + Н2СО3 → К+ + НСО3- + НHb
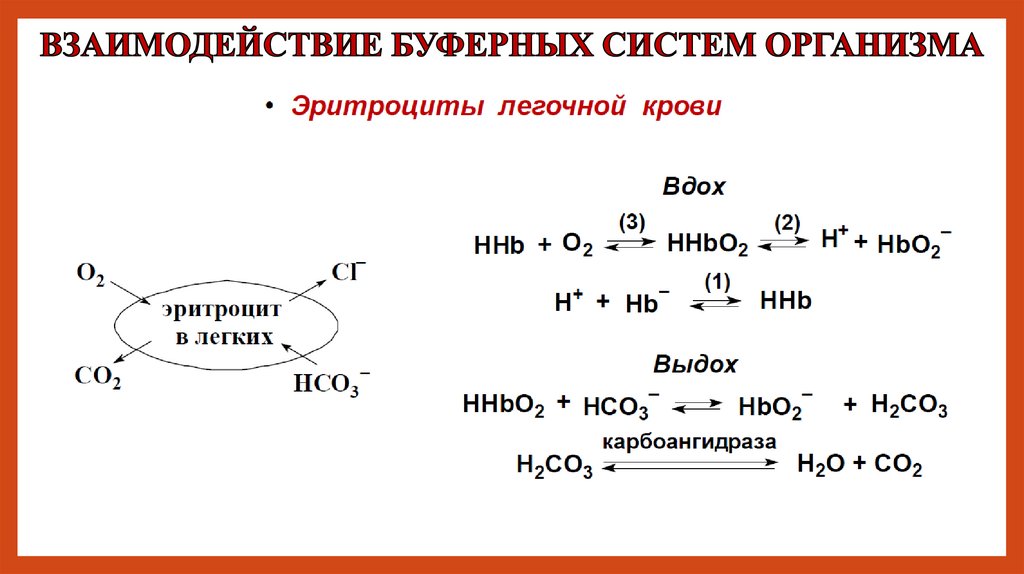
11.
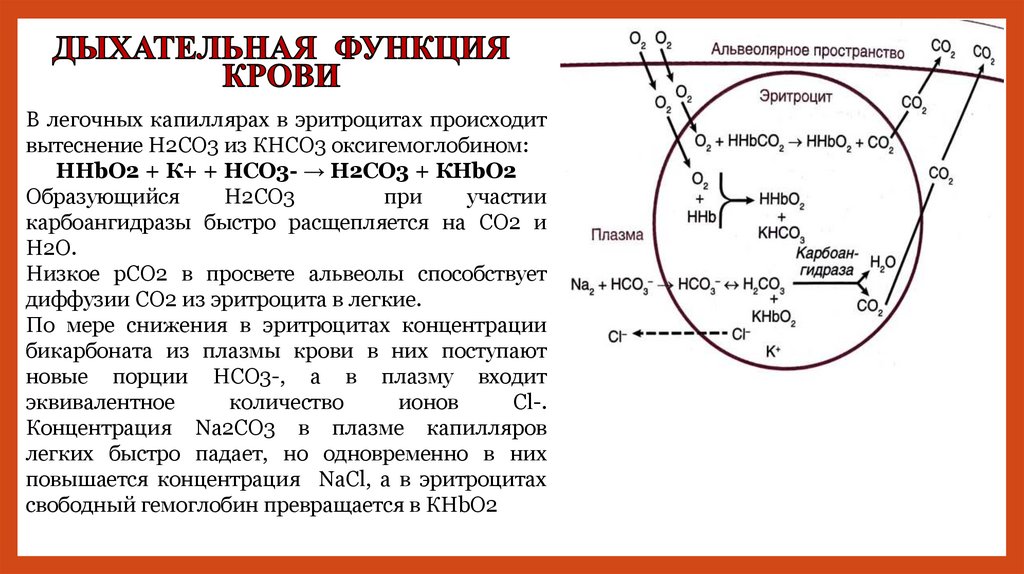
В легочных капиллярах в эритроцитах происходитвытеснение Н2СО3 из КНСО3 оксигемоглобином:
НHbО2 + К+ + НСО3- → Н2СО3 + КHbО2
Образующийся
Н2СО3
при
участии
карбоангидразы быстро расщепляется на СО2 и
Н2О.
Низкое рСО2 в просвете альвеолы способствует
диффузии СО2 из эритроцита в легкие.
По мере снижения в эритроцитах концентрации
бикарбоната из плазмы крови в них поступают
новые порции НСО3-, а в плазму входит
эквивалентное
количество
ионов
Сl-.
Концентрация Nа2СО3 в плазме капилляров
легких быстро падает, но одновременно в них
повышается концентрация NаСl, а в эритроцитах
свободный гемоглобин превращается в КНbО2
12.
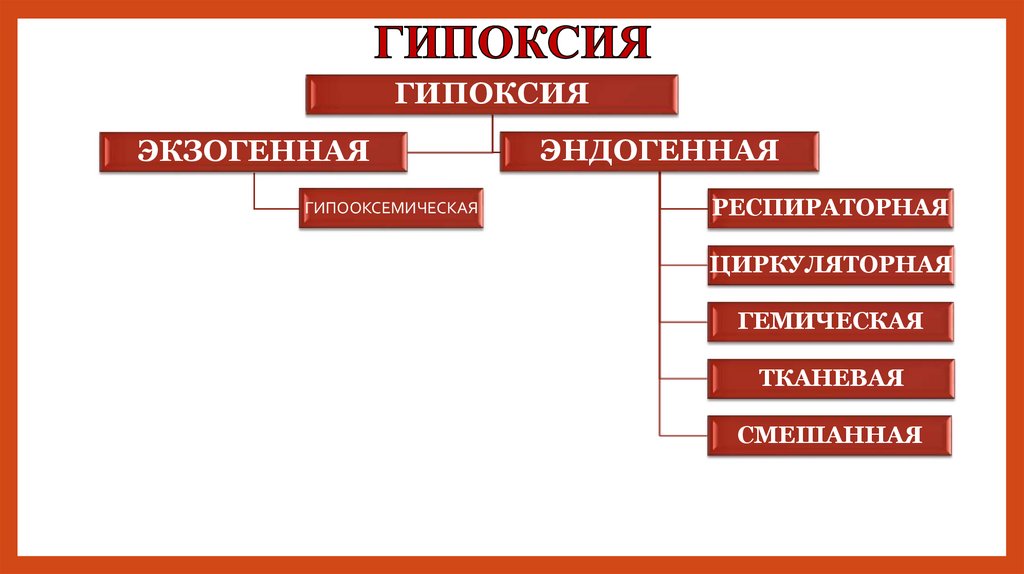
ГИПОКСИЯЭКЗОГЕННАЯ
ГИПООКСЕМИЧЕСКАЯ
ЭНДОГЕННАЯ
РЕСПИРАТОРНАЯ
ЦИРКУЛЯТОРНАЯ
ГЕМИЧЕСКАЯ
ТКАНЕВАЯ
СМЕШАННАЯ
13.
Гем является простетической группой гемоглобина,миоглобина, цитохромов, каталазы, пероксидазы.
Он синтезируется во всех клетках тела, но наиболее активно
синтез идет в печени и костном мозге.
Субстратами синтеза гема являются
В матриксе митохондрий из глицина и
сукцинил-КоА под действием пиридоксальзависимого
фермента
образуется 5аминолевулиновая
кислота,
которая
поступает
в
цитоплазму.
В
цитоплазме
фермент
катализирует реакцию
конденсации двух молекул 5-аминолевулиновой кислоты с
образованием
. Далее из четырех
молекул порфобилиногена последовательно образуются
промежуточные
метаболиты
,
последний из которых поступает в митохондрии и
превращается
в
.
Фермент
завершает образование гема, присоединяя
Fe2+ к протопорфирину IX
14.
Распад гема происходит в эндоплазматическом ретикулуме клеток эндотелиальной системы селезенки, костного мозга и печени при участии ферментов гемоксигеназной системы. В результате ряда превращений образуется непрямой (не дающий прямую реакцию с диазореактивом, так как связан с белком альбумином) – неконъюгированный билирубин. Билирубинплохо растворим в воде и транспортируется кро-вью в печень в комплексе с
альбумином. Билирубин поступает в гепатоциты с помощью белков-переносчиков лигандина и протеина Z. В печени билирубин конъюгирует с глюкуроновой кислотой под действием ферментов эндоплазматического ретикулума УДФ-глюкуронилтрансферазы I, катализирующей образование
билирубинмоноглюкуронида и УДФ-глюкуронилтрансферазы II, образующей билиру-биндиглюкуронид. В результате реакций конъюгации образуется прямой или конъюгированный, билирубин. По механизму активного транспорта прямой билирубин в составе желчи поступает в двенадцатиперстную кишку. В кишечнике ферментами микрофлоры он гидролизуется с образованием билирубина и глюкуроновой кислоты.Билирубин в
результате нескольких реакций восстановления превращается в бесцветные
тетрапирролы - уробилиногены. В результате окисления они превращаются в уробилин, который выводится из организма, являясь пигментом
кала уробилином (стеркобилином) (200-300 мг/сут). Небольшая часть
уробилиногенов всасывается в кишечнике, с кровью воротной вены транспортируется в печень, оттуда поступает в кровь, затем в почки и, окисляясь
в пигмент желтого цвета уробилин, удаляется с мочой(3-4 мг/ сут).
15.
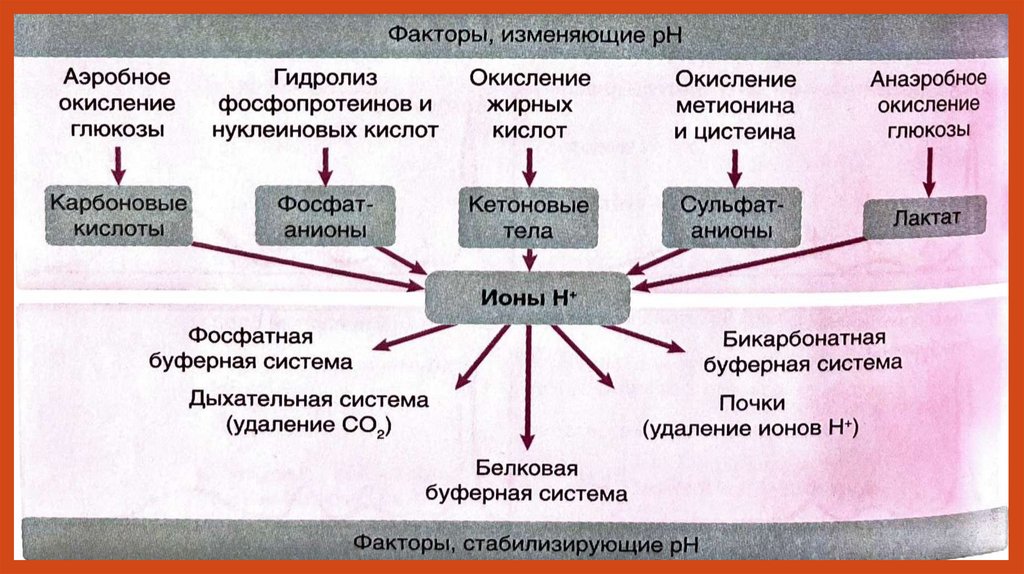
Кислотно-основное равновесие обеспечивается работой физиологических и физико-химическихпроцессов, составляющих функционально единую систему стабилизации концентрации ионов Н+.
Нормальные величины концентрации ионов Н+ около 40 нмоль/л, что в 106 раз меньше, чем
концентрация многих других веществ (глюкоза, липиды, минеральные вещества). Совместимые с
жизнью колебания концентрации ионов Н+ располагаются в пределах 16-160 нмоль/л.
рН – это отрицательный десятичный логарифм концентрации ионов водорода.
рН = - lg [ H+ ]
[ Н+ ] = [ ОН- ] = 10-7 – среда нейтральная – рН = 7
[ Н+ ] > 10-7 – среда кислая – рН < 7
[ Н+ ] < 10-7 – среда щелочная – рН > 7
рН внутренних сред организма (крови, лимфы, ликвора, желудочного сока, мочи) оказывает воздействие
на жизнедеятельность клеток, тканей, органов и организма в целом. Значение рН внутренних сред
характеризуется значительным постоянством и устойчивостью.
16.
• оптимальную функциональную активность белков плазмы крови имежклеточного пространства (ферменты, транспортные белки)
• Поддержание осмолярности биологических жидкостей
• растворимость неорганических и органических молекул
• неспецифическую защиту кожного эпителия
• отрицательный заряд наружной поверхности мембраны эритроцитов
• оптимальной активности ферментов мембран, цитоплазмы и
внутриклеточных органелл,
• формирования электро-химического градиента мембраны митохондрий на
должном уровне и достаточную наработку АТФ в клетке
Различные заболевания также сопровождаются изменением рН
биологических жидкостей. Знание этих закономерностей позволяет
прогнозирование нарушения КОС в организме и применять соответствующие
методы коррекции.
17.
18.
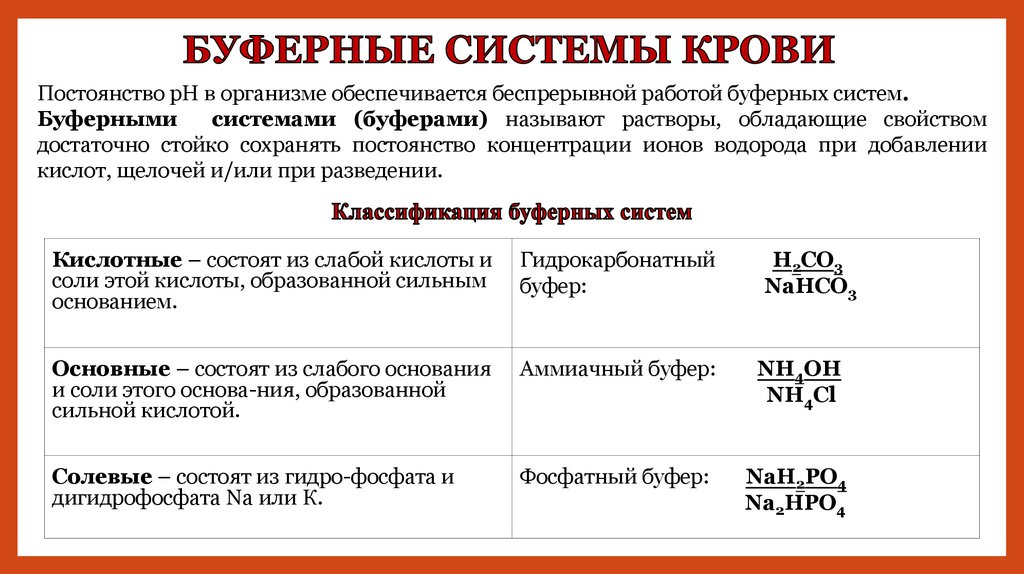
Постоянство рН в организме обеспечивается беспрерывной работой буферных систем.Буферными
системами (буферами) называют растворы, обладающие свойством
достаточно стойко сохранять постоянство концентрации ионов водорода при добавлении
кислот, щелочей и/или при разведении.
Кислотные – состоят из слабой кислоты и
соли этой кислоты, образованной сильным
основанием.
Гидрокарбонатный
буфер:
Н2СО3
NaHCO3
Основные – состоят из слабого основания
и соли этого основа-ния, образованной
сильной кислотой.
Аммиачный буфер:
NH4OH
NH4Cl
Солевые – состоят из гидро-фосфата и
дигидрофосфата Na или К.
Фосфатный буфер:
NaH2PO4
Na2HPO4
19.
Сыворотка крови7,35 – 7,45
Спинно-мозговая жидкость
7,35 – 7,45
Слюна
6,35 – 6,85
Желудочный сок
0,9 – 1,3
Моча
4,8 – 7,5
Слезная жидкость
7,2 – 7,4
Желчь в пузыре
5,4 – 6,9
20.
21.
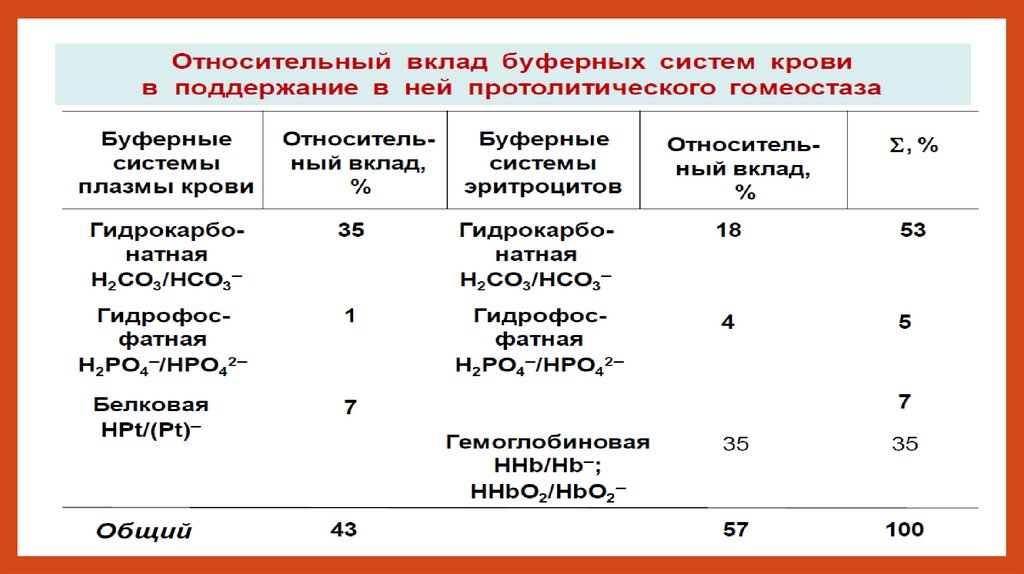
В плазме:В эритроцитах:
Na+ вне клетки
К+ внутри клетки
H2CO3
NaHCO3
гидрокарбонатный
Н2СО3
КНСО3
NaH2PO4
NA2HPO4
фосфатный
КН2РО4
К2НРО4
Pt – COOH
Pt - COONa
белковый
Органические кислоты
Na+ - соль
не характерен
Органические кислоты
К+ - соль
ННb
КНb
гемоглобиновый
ННbО2 оксигемоглобиновый
КНbО2
22.
Действует как в эритроцитах, так и во всех внеклеточных жидкостях. Это наиболее легко регулируемаявнеклеточная буферная система организма и потому наиболее значимаемая.
Состоит из слабой угольной кислоты Н2СО3 (образуется при взаимодействии СО2 с водой под действием
фермента карбоангидразы) и натриевой или калиевой соли, образованной этой кислотой и сильным
основанием.
H2CO3
NaHCO3-
или
H2CO3
КHCO3-
СО2 образуется в тканях в результате ферментного окисления углеводов, липидов, белков.
Соотношение гидрогенкарбонат-ионов и угольной кислоты в крови в норме 20:1.
Избыток гидрогенкарбонат-ионов обеспечивает так называемый щелочной резерв крови 25 – 30 ммоль/л
химически связанного углекислого газа.
Благодаря работе бикарбонатного буфера концентрация водородных ионов понижается
по двум причинам:
угольная кислота является очень слабой кислотой и плохо диссоциирует
в крови легких благодаря присутствию в эритроцитах фермента карбоангидразы, угольная кислота
быстро расщепляется с образованием CO2, удаляемого с выдыхаемым воздухом:
Н2СО3 ↔ Н2О + СО2↑
23.
Фосфатная буферная система составляет около 1-2% от всей буфернойемкости крови и
до 50% буферной емкости мочи. Она образована дигидрофосфатом
(NaH2PO4) и гидрофосфатом (Na2HPO4) натрия. Первое соединение
слабо диссоциирует и ведет себя как слабая кислота, второе обладает
щелочными свойствами. В норме отношение HРO42– к H2РO4– равно
4 : 1.
Основное значение фосфатный буфер имеет для регуляции pH
интерстициальной жидкости и мочи. В моче роль его состоит в
сбережении бикарбоната натрия за счет дополнительного иона
водорода (по сравнению с NaHCO3) в составе выводимого NaH2PO4:
Na2HPO4 + Н2СО3 ↔ NaH2PO4 + NaНСО3
Кислотно-основная реакция мочи зависит только от содержания
дигидрофосфата, т.к. бикарбонат натрия в почечных канальцах
реабсорбируется.
24.
При добавлении кислоты (+Н+)При добавлении основания (+ОН-)
NH3+-CH2-COOН
Идет присоединение протона к
отрицательно заряженной группе и
нейтрализация кислоты
NH2-CH2-COO- + Н2О
Идет присоединение ОН- к
положительно заряженной группе с
выделением воды
Белковая буферная система в плазме тесно взаимодействует с гидрокарбонатной БС и противодействует изменению
рН при возрастании СО2 в крови.
25.
26.
27.
28.
29.
30.
В почках активно протекают три процесса,связанных с ликвидацией кислых эквивалентов:
1. Реабсорбция бикарбонатных ионов HCO3–.
2. Ацидогенез – удаление ионов Н+ с
титруемыми кислотами (в основном в составе
дигидрофосфатов NaH2PO4).
3. Аммониегенез – удаление ионов Н+ в составе
ионов аммония NH4+.
В проксимальных канальцах ионы Na+
мигрируют в цитозоль эпителиальных клеток в
силу концентрационного градиента, который
создается на базолатеральной мембране при
работе фермента Na+/К+-АТФазы. В обмен на
ионы Na+ эпителиоциты канальцев активно
секретируют в канальцевую жидкость ионы
водорода.
31.
В процессе ацидогенеза в сутки с мочой выделяется 10-30 ммоль кислот, называемыхтитруемыми кислотами. Фосфаты, являясь одной из этих кислот, играют роль буферной
системы в моче. Роль ее состоит экскреции кислых эквивалентов без потерь бикарбонат-ионов
за счет дополнительного иона водорода в составе выводимого NaH2PO4 (по сравнению с
NaHCO3): Na2HPO4 + Н2СО3 ↔ NaH2PO4 + NaНСО3
После того как бикарбонат натрия в почечных
канальцах реабсорбируется, кислотность мочи
зависит только от связывания ионов Н+ с
HPO42– и содержания дигидрофосфата.
Хотя в крови соотношение HРO42– : H2РO4–
равно 4 : 1, в клубочковом фильтрате оно
меняется на 1 : 9. Происходит это из-за того, что
менее заряженный H2РO4– лучше фильтруется
в клубочках. Связывание ионов Н+ ионами
HРO42– на протяжении всего канальца приводит
к увеличению количества H2РO4–. В
дистальных канальцах соотношение может
достигать 1 : 50
32.
Наиболее активно идет в дистальных канальцах и собирательных трубочках. В этих сегментах секрецияионов Н+ происходит с участием Н+/Nа+-АТФазы апикальной мембране эпителиоцита. Ионы HCO3–
первичной мочи и секретируемые ионы Н+ образуют угольную кислоту Н2СО3. Карбоангидраза
катализирует распад угольной кислоты на СО2 и воду. В результате возникает градиент концентрации
углекислого газа между просветом канальцев и цитозолем и СО2 диффундирует в клетки.
Внутриклеточная карбоангидраза использует пришедший СО2 и образует угольную кислоту, которая
диссоциирует на ионы. НСО3– транспортируются в кровь, ионы Н+ – секретируются в мочу в обмен на
ионы Na+. Таким образом, объем реабсорбции НСО3– полностью соответствует секреции ионов Н+.
Глутамин и глутаминовая кислота, попадая в клетки
канальцев,
быстро
дезаминируются
ферментами
глутаминаза и глутаматдегидрогеназа с образованием
аммиака. Являясь гидрофобным соединением, аммиак
диффундирует в просвет канальца и акцептирует ионы Н+
с образованием аммонийного иона. Далее аммонийный
катион способен взаимодействовать с анионами Cl–,
SO42–, с органическими кислотами (лактат и другие) с
образованием аммонийных солей.
33.
Причины:1. Повышенное поступление кислых продуктов или недостаточность их удаления.
2. Изменение количества иона НСО3– в сторону увеличения или снижения.
3. Изменение концентрации компонентов буферных систем
Смещение КОС крови в сторону повышения концентрации ионов водорода (снижение рН до
7,0) и уменьшения резервной щелочности ― ацидоз. Смещение КОС крови в сторону
понижения концентрации ионов водорода (повышение рН до 7,8) и увеличения резервной
щелочности крови ―алкалоз.
34.
1. Повышение содержания кислот в крови• Кетоацидоз (при сахарном диабете, недостатке
углеводов в пище при достаточном потреблении
белков и жиров, при отравлении алкоголем)
• Лактоацидоз (при сепсисе, кровотечении, отеке
легких, сердечной недостаточности, при шоке,
повышении вязкости крови при остром
панкреатите, сахарном диабете, лейкемии,
хроническом алкоголизме).
2. Потеря бикарбонатов
• С кишечным, панкреатическим и билиарным
секретами
при
диареях
и
фистулах
кишечника
и
желчного
пузыря,
дренировании поджелудочной железы.
3. Недостаточное выведение ионов Н+ почками
(при ХПН или поражении канальцев).
Причинами являются нарушение вентиляции
легких, сопровождающиеся гиповентиляцией:
• Повреждения или заболевания легких
(пневмония, фиброз, отек легких)
• Все случаи механической асфиксии
• Повреждения или заболевания дыхательных
мышц (нехватка калия, боли после операции,
травмы, накопление жировых отложений)
• Угнетение дыхательного центра (опиаты,
барбитураты), неправильный режим ИВЛ
• Бронхиальная астма, эмфизема, бронхит.
При недостаточной вентиляции легких рСО2
способен достичь 140-150 мм рт.ст.
35.
1. Эндогенный синтез и повышеннаясекреция в кровь ионов НСО3–:
• обкладочными клетками желудка при
неукротимой рвоте, фистуле желудка,
кишечной непроходимости и тд.
1. Возбуждение дыхательного центра.
• изолированный ацидоз церебральной
жидкости, который является остаточным
явлением после компенсированного
ацидоза крови.
• субарахноидальное кровотечение, при
этом происходит стимуляция
дыхательного центра продуктами
гемолиза
• при циррозе печени и сепсисе происходит
стимуляция дыхательного центра
токсинами и циркулирующими
метаболитами.
2. Лихорадочные состояния.
3. Неправильный режим искусственной
вентиляции легких.






























 Биология
Биология








