Похожие презентации:
Дисперс системаларнинг коагуляцияси. Электролитлар таъсиридаги коагуляция. 10 - маъруза
1.
ТОШКЕНТ КИМЁ ТЕХНОЛОГИЯИНСТИТУТИ
«Ноорганик, аналитик, физикавий ва коллоид кимё
кафедраси»
Тузувчи:
Доцент – Х.С. Талипова
2.
10 - маърузаДИСПЕРС СИСТЕМАЛАРНИНГ КОАГУЛЯЦИЯСИ. Электролитлар таъсиридаги
коагуляция
РЕЖА:
•Гидрофоб золларнинг коагуляцияси.
•Коагуляция чегараси. Шульце-Гарди
қоидаси.
•Коагуляция тезлиги.
3.
TAYANCH SO‘Z VA IBORALARKoagulyatsiya
Ochiq koagulyatsiya
-dispers faza zarrachalarining yiriklashishi.
-koagulyatsiya sodir bo‘lganligini ko‘z bilan ko‘rish
mumkin bo‘lsa ochiq koagulyatsiya (loyqalanish,
rang o‘zgarishi, cho‘kma tushishi) deyiladi.
Yashirin koagulyatsiya
-koagulyatsiya sodir bo‘lishini ko‘z bilan ko‘rib
bo‘lmaydi.
Koagulyatsiyalovchi ion
Energetik barer
-bevosita koagulyatsiyani yuzaga keltiruvchi ion.
-zarrachalarning bir-biri bilan birikishi uchun yengish
kerak bo‘lgan itarilish kuchi.
Tez koagulyatsiya
-zarrachalar bir-biri bilan birinchi to‘qnashgandayoq
koagulyatsiyalanadi.
Sekin koagulyatsiya
-koagulyatsiya tezligi qo‘shilayotgan elektrolitning
konsentratsiyasiga bog‘liq bo‘ladi.
Koagulyatsiya chegarasi
(konsentratsiyasi)
-zolni koagulyatsiyalash uchun
elektrolitning eng kichik miqdori.
kerak
bo‘lgan
4.
Золларнинг коагуляциясиКоагуляция – қуюқланиш, ивиш деган маънони
билдиради.
Коллоид заррачаларни бир-бири билан бирикиб
йирикроқ агрегат ҳолатга ўтиши, яъни агрегатив
барқарорлигини
бузилиши,
сўнгра
кинетик
барқарорлигини йўқолиши – коагуляция дейилади.
Коагуляция турли омиллар туфайли вужудга
келади. Улардан– электролитлар таъсири, кескин иситиш ёки
кескин совутиш, электр токи таъсир эттириш, механик таъсир
кўрсатиш, юқори частотали тебраниш (масалан, ультратовуш),
ультрацентрифугада ажратиш, дисперс фазани концентрациясини
ошириш ва турли хил нурлар таъсир эттириш орқали
коагуляция чақириш мумкин.
5.
•Коагуляция тезлигиКоагуляция жараёни бошқа ҳар қандай
жараёнларга ўхшаб маълум вақт ичида
содир бўлади. Шунинг учун ҳам у кинетик
жараён ҳисобланади.
Коагуляция тезлиги коллоид система
заррачаларининг
броун
ҳаракатига,
уларнинг
ўзаро
таъсирига
(бошқача
айтганда,
заррачаларнинг
ўзаро
тортириш сфераси, радиуси катталигига
ва
диффузия
коэффициентига)
ва
электролитнинг
дастлабки
концентрациясига боғлиқ.
6.
Агар иккита заррача бир-бири билан бирмарта тўқнашгандаёқ ўзаро бирикиб, йирикроқ
заррача ҳосил қилса – тез коагуляция
дейилади. Унинг тезлиги броун ҳаракатининг
интенсивлигига боғлиқ, лекин қўшиладиган
коагуляцияловчи электролит концентрациясига боғлиқ эмас.
Коагуляция
тезлиги
қўшилаётган
электролит концентрациясига боғлиқ бўлса
– суст коагуляция дейилади.
7.
Электролитлар таъсиридаги коагуляцияКоагуляция жараёнини ҳар хил йўллар билан
тезлатиш мумкин.
• Коллоид
эритмаларга
(золга)
ҳар
хил
электролитлар қўшиб коагуляция жараёнини
тезлатиш мумкин.
• Коллоид эритмага бошқа коллоид қўшиб
коагуляцияни тезлатиш мумкин.
• Коллоид эритмани қиздириш йўли билан
коагуляция жараёнини тезлатиш мумкин.
Энг кучли коагуляция чақириш – электролитлар
таъсирида бўлади. Агар коллоид эритмага хар қандай
электролитдан етарли миқдорда қўшилса, коагуляция
содир бўлади.
8.
-Коагуляция содир бўлганлигини кўзбилан кўриш мумкин бўлса, очиқ коагуляция
(лойқаланиш, ранг ўзгариши, чўкма
тушиши);
-кўриш мумкин бўлмаса, яширин
коагуляция дейилади. Очиқ коагуляция
бўлиши учун электролит концентрацияси
коагуляция концентрацияси (коагуляция
чегараси)дан ортиқ бўлиши керак.
9.
Электролитнинг коагуляция концентрацияси(коагуляция чегараси) – 1л золни коагуляцияга
учратиш учун қўшилган электролитнинг ммоль
миқдори билан ифодаланади ва
эл. 1000
эл. зол
формула асосида ҳисоблаб топилади. Ёки
с n
a
1
b
2
1000
бунда
с - электролитнинг концентрацияси,
n - коагуляцияловчи ион валентлиги,
а - сувнинг миқдори,
b - электролитнинг миқдори.
10.
Коагуляция чегарасига тескари бўлган катталиккоагуляциялаш қобилияти дейилади.
1882 йилда Г.Шульце текширишлари бўйича
электролитнинг битта иони коагуляция чақиради
деган фикрни айтди. 1900 йилларда М.Гарди –
коагуляцияловчи ионнинг заряди заррача зарядига
қарама-қарши эканлигини аниқлади. Унга асосан
манфий зарядланган золни катион коагуляциялайди.
Мусбат зарядланган золда коагуляцияни анион
чақиради. Бу қонуниятлар Шульце-Гарди қоидасида ўз
ифодасини топган:
Коллоид
заррача
зарядига
қарама-қарши
зарядланган ион коагуляция чақиради. Унинг заряди
(яъни, ион валентлиги) қанча юқори бўлса,
коагуляциялаш қобилияти шунча кучли бўлади.
11.
ДЛФО назариясига кўра Шульце-Гардиқоидаси қуйидаги нисбат кўринишини олади:
эл
С :С
2
эл
:С
3
эл
1 1
1
1
1: 6 : 6 1:
:
2 3
64 729
ёки
Сэл : Сэл2 : Сэл3 729 : 64 : 1
Ионнинг коагуляция чақириш қобилияти
(фаоллиги) унинг валентлигига боғлиқ бўлиб,
валентликнинг
6
чи
даражасига
тескари
пропорционалдир.
12.
Бундан келиб чиқадики, агар бирор золникоагуляцияга учратмоқчи бўлсак,
1 валентли электролит оладиган бўлсак
ундан 1л эритмага 729 миллимол,
2 валентли электролит оладиган бўлсак
64 миллимол ва
3 валентли электролитдан 1 миллимол
керак бўлар экан.
13.
14.
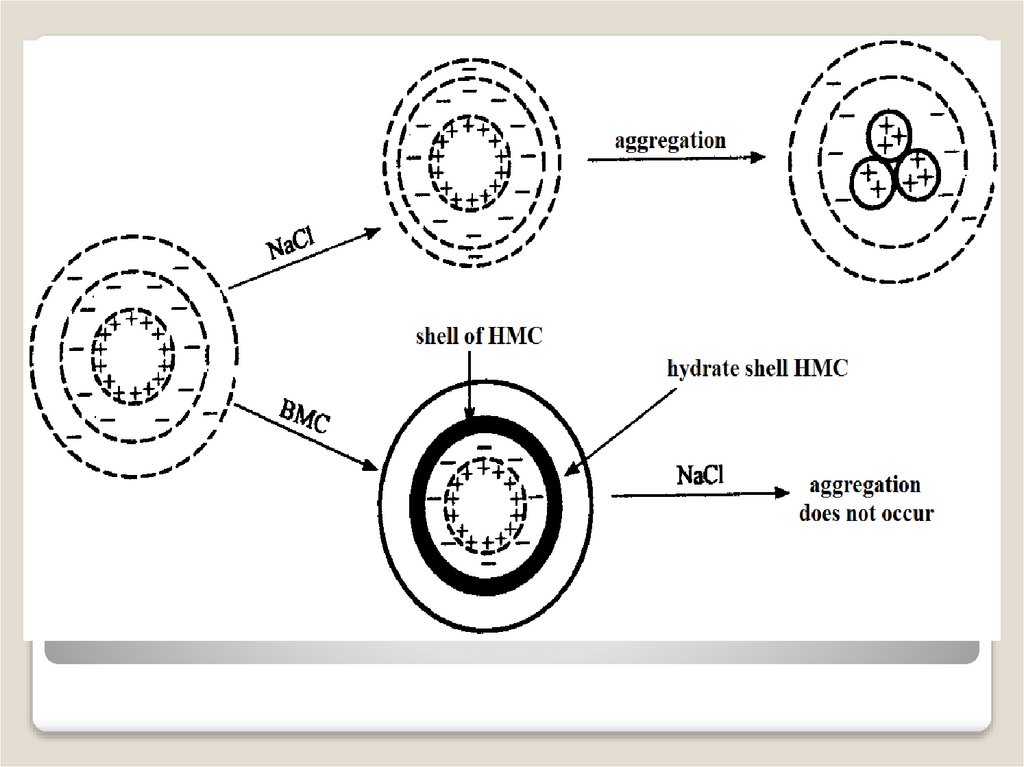
Электролитлар аралашмаси таъсиридагикоагуляция
Коллоид эритмаларга электролитлар аралашмаси қўшилганда
3 хил ҳол бўлиши мумкин:
•бир электролитнинг коагуляциялаш қобилияти иккинчи
электролитникига қўшилади. Бу ҳодиса – аддитивлик
дейилади.
1-биринчи электролит
C01 C02
2-иккинчи электролит
2
2
•бир электролитга иккинчи электролит қўшилса, биринчи
электролитнинг коагуляция таъсири кучаяди. Бу ҳодиса –
сенсибилизация (синеризм) дейилади. Бунда
C01
( ммоль / л)
2
- биринчи электролитдан қўшиш керак.
C02
( ммоль / л)
3
- иккинчи электролитдан қўшиш керак.
15.
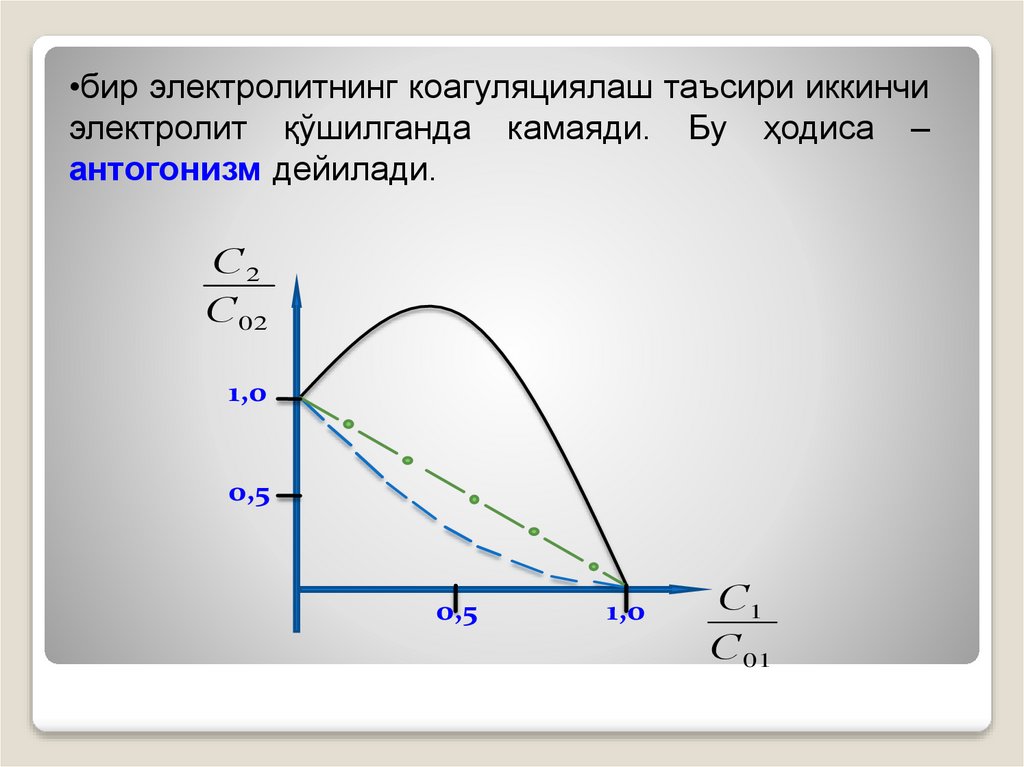
•бир электролитнинг коагуляциялаш таъсири иккинчиэлектролит қўшилганда камаяди. Бу ҳодиса –
антогонизм дейилади.
С2
С02
1,0
0,5
0,5
1,0
С1
С 01
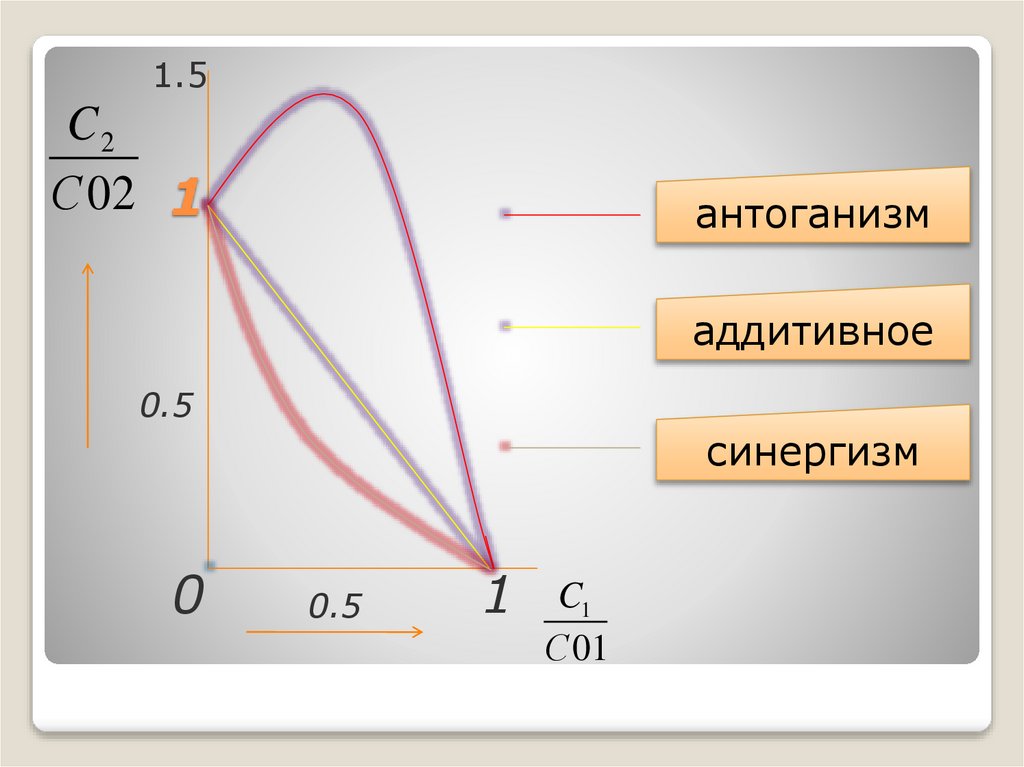
16. 1
1.5C2
С 02 1
антоганизм
аддитивное
0.5
синергизм
0
0.5
1
C1
С 01
17.
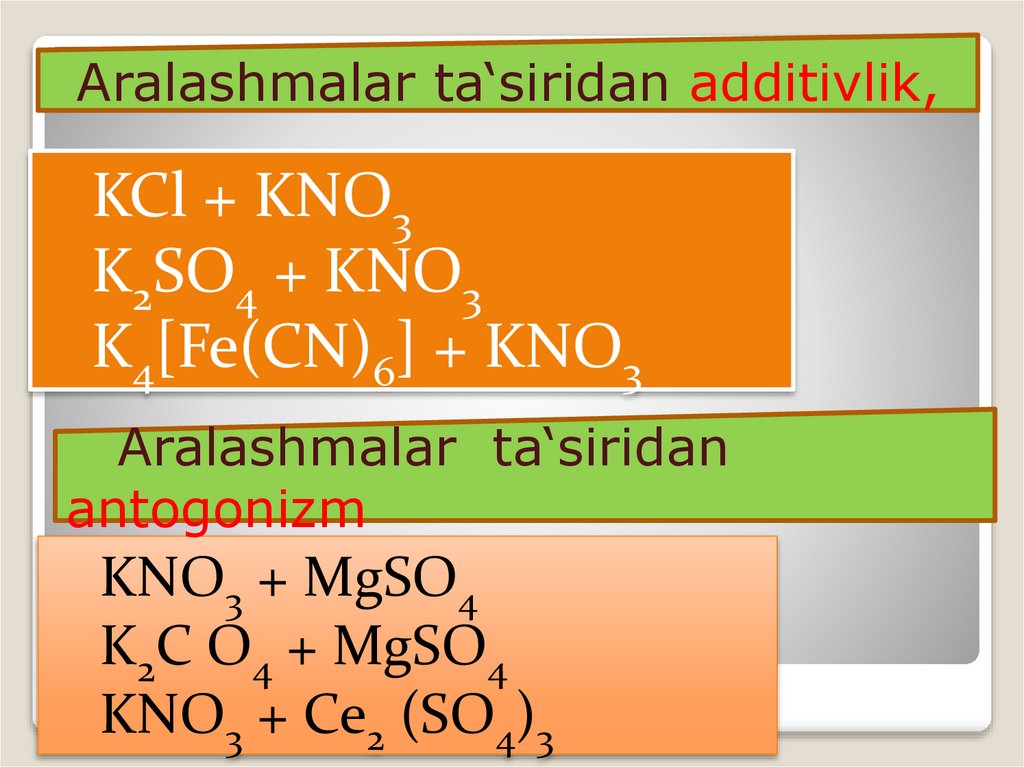
Aralashmalar ta‘siridan additivlik,KCl + KNO3
K2SO4 + KNO3
K4[Fe(CN)6] + KNO3
Aralashmalar ta‘siridan
antogonizm
KNO3 + MgSO4
K2C O4 + MgSO4
KNO3 + Ce2 (SO4)3
18.
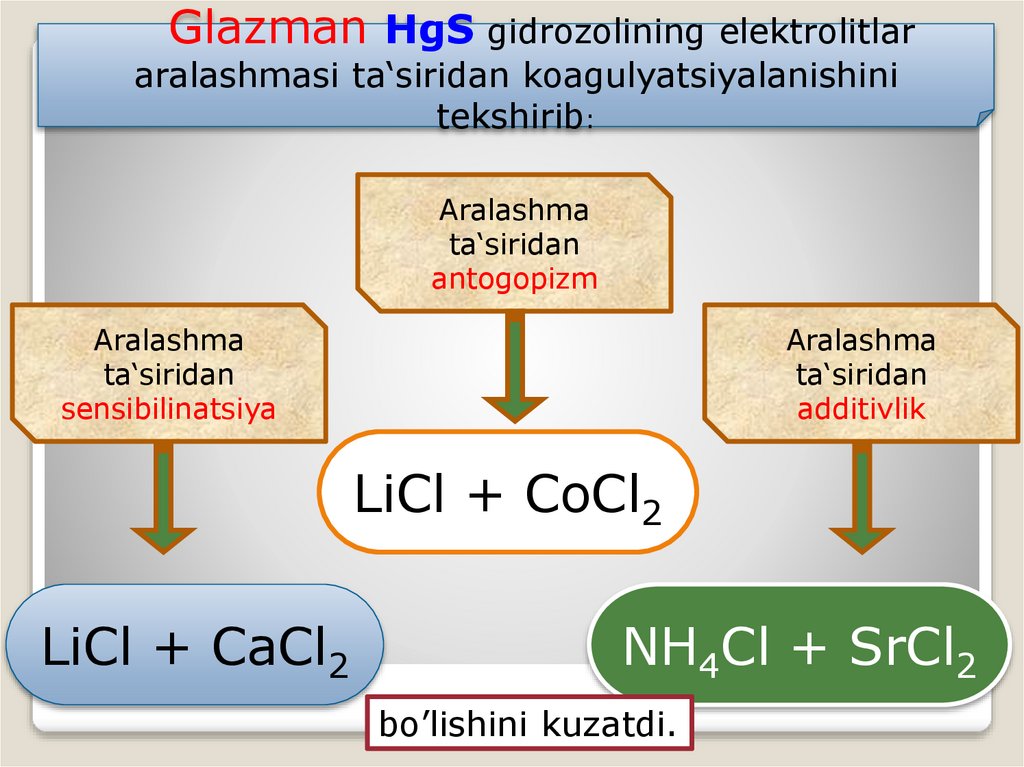
Glazman HgS gidrozolining elektrolitlararalashmasi ta‘siridan koagulyatsiyalanishini
tekshirib:
Aralashma
ta‘siridan
antogopizm
Aralashma
ta‘siridan
sensibilinatsiya
Aralashma
ta‘siridan
additivlik
LiCl + CоCl2
LiCl + CaCl2
NH4Cl + SrCl2
bo’lishini kuzatdi.
19.
Коагуляцияга оид ҳодисалар табиатда жуда кенгтарқалган ва уларнинг турмушда, ҳаётда аҳамияти
каттадир.
Масалан,
-қанд ишлаб чиқариш саноатида қанд лавлагининг
шарбатини
тозалашда
коагуляция
жараёнидан
кенг
фойдаланилади.
-сувдаги органик моддалар одатда манфий зарядли
бўлади. Сувга аввал хлор қўшилиб, сувдаги бактериялар
йўқотилгандан сўнг, унга оз миқдорда темир сульфат ёки
алюминий сульфат қўшилади. Бу тузлар гидролизланади.
Ҳосил бўлган гидроксидларнинг мусбат зарядли коллоидлари
сувдаги
органик
моддаларнинг
манфий
зарядли
коллоидларини коагуляциялайди. Натижада ҳосил бўлган
коагулянтлар чўкади ва сув тинади ва х.к.
20.
ETIBORINGIZUCHUN RAHMAT!!!















 Химия
Химия